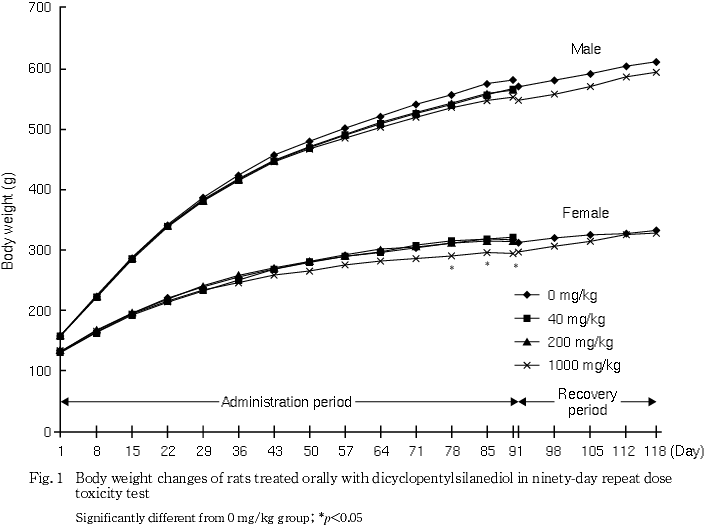
ジシクロペンチルシランジオールを0,40,200および1000 mg/kgの用量で雌雄のSD系ラットに90日間反復経口投与し,その毒性と回復性を検討した.
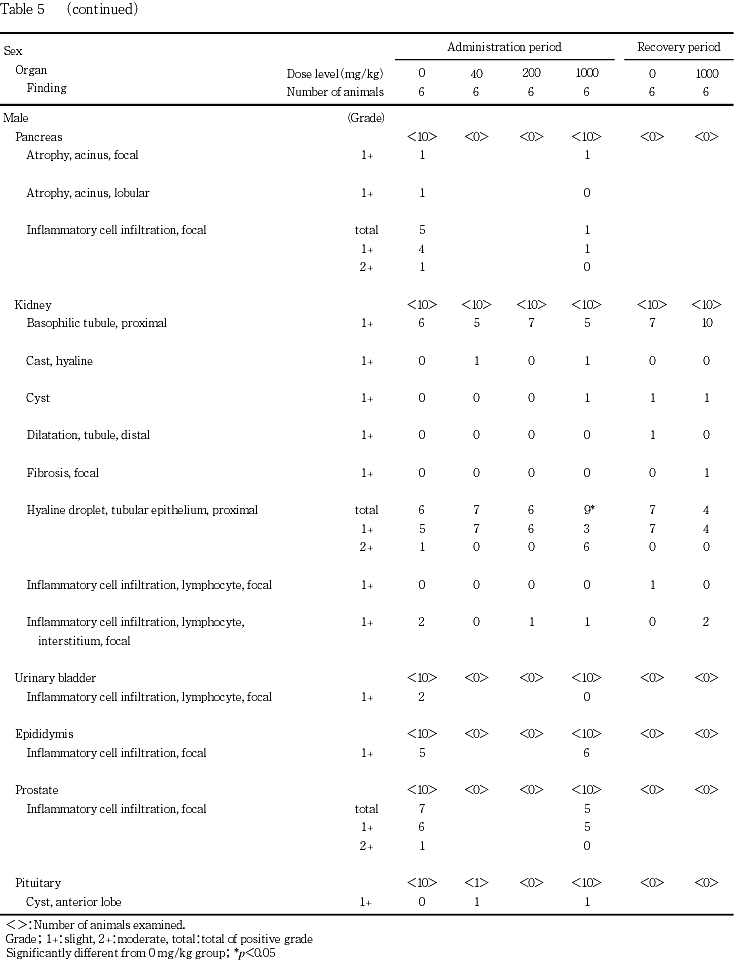
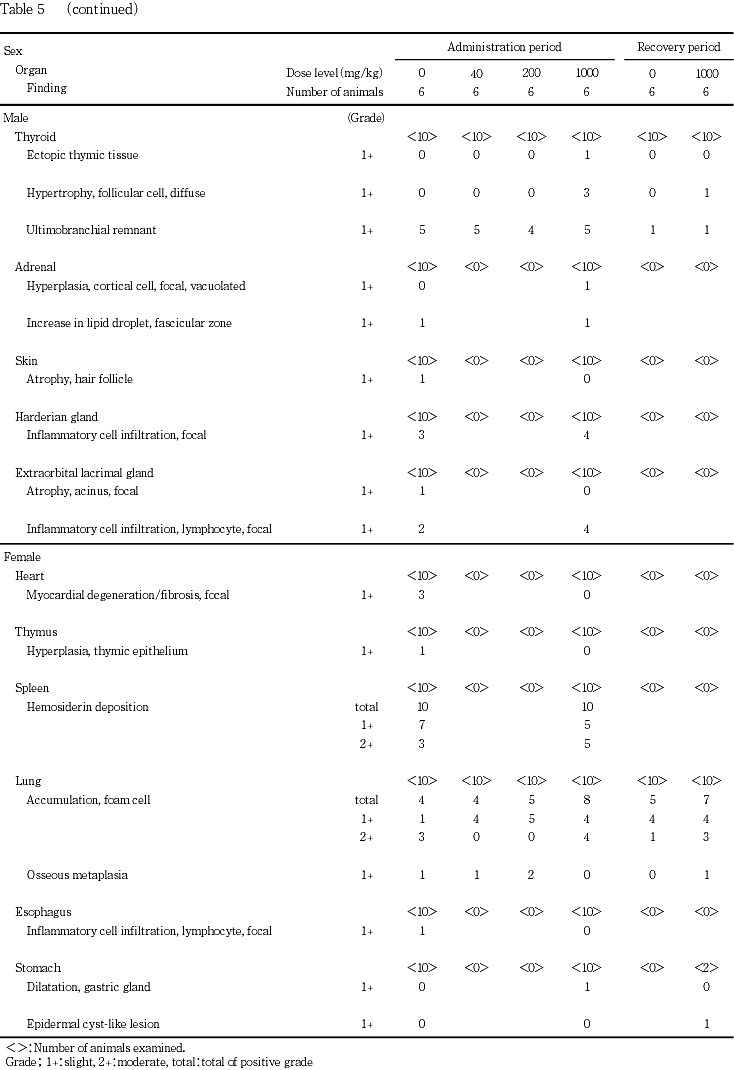
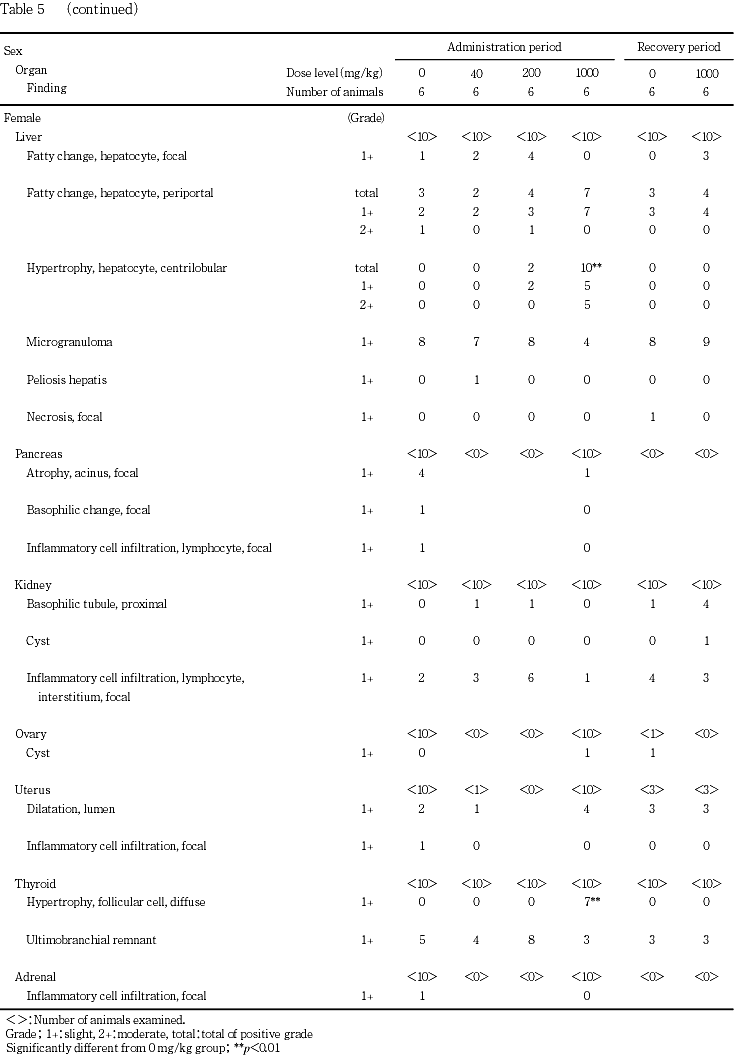
投与期間中に,一般状態において一過性の変化として歩行失調と流涎が200および1000 mg/kg群の雌雄に,自発運動の低下が1000 mg/kg群の雌雄に,それぞれ認められた.また,1000 mg/kg群の雌では自発運動の低下時に緩徐呼吸および側臥位を伴うものがみられた.体重の低値が1000 mg/kg群の雌で投与期間末期に認められた.投与期間終了時に,血液生化学検査において,総コレステロールの高値が200および1000 mg/kg群の雌に,トリグリセライドの低値が1000 mg/kg群の雄に,それぞれ認められた.器官重量において,肝臓絶対・相対重量の高値が1000 mg/kg群の雌に,肝臓相対重量の高値が200および1000 mg/kg群の雄に,腎臓相対重量の高値が1000 mg/kg群の雄に,それぞれ認められた.剖検において,肝臓の腫大と暗褐色化が1000 mg/kg群の雌に認められた.病理組織学検査において,肝臓の小葉中心性肝細胞肥大が200 mg/kg群の雌と1000 mg/kg群の雌雄に,甲状腺のびまん性の濾胞上皮細胞の肥大が1000 mg/kg群の雌雄に,腎臓の近位尿細管上皮の硝子滴発現の増強が1000 mg/kg群の雄に,それぞれ認められた.
回復期間終了時には,器官重量において,肝臓相対重量の高値が1000 mg/kg群の雌にみられたが,投与期間終了時に比べその程度は軽減した.病理組織学検査において,投与期間終了時にみられた変化の発現は例数が減少するかまたは消失し,回復性が認められた.
摂餌量測定,血液学検査,尿検査および眼科学検査の結果には,被験物質投与に起因すると考えられる変化は認められなかった.
以上,雌雄いずれも200および1000 mg/kg群で被験物質投与に起因すると考えられる変化が認められた.200 mg/kg群では,一般状態において雌雄に歩行失調および流涎,器官重量において雄に肝臓相対重量の高値,血液生化学検査において雌に総コレステロールの高値,病理組織学検査において雌に肝臓の肝細胞肥大がみられたことから,本試験条件下におけるジシクロペンチルシランジオールの無影響量(NOEL)は,雌雄いずれも40 mg/kg/dayと判断した.
検疫・馴化期間を含む全飼育期間を通して,温度22 ± 2 ℃,相対湿度55 ± 15 %,換気約12回/時(オールフレッシュエアー供給),照明12時間/日(7:00〜19:00)に自動調節した飼育室を使用した.動物を実験動物用床敷(ベータチップ,日本チャールス・リバー(株))を敷いたポリカーボネート製ケージに群分け前はケージあたり5匹以下(同性),群分け以降はケージあたり2匹(同性)収容し,飼育した.動物には,実験動物用固型飼料(MF,オリエンタル酵母工業(株))と,5 μmのフィルター濾過後,紫外線照射した水道水を自由に摂取させた.
 法),グルコース(GlcK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形;(株)日立製作所)により測定した.また,検査の結果からA/G比を算出した.
法),グルコース(GlcK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形;(株)日立製作所)により測定した.また,検査の結果からA/G比を算出した.
投与期間終了時解剖動物の対照群と1000 mg/kg群の雌雄全例の採材した全ての器官・組織,投与期間終了時に採取した40と200 mg/kg群および回復期間終了時解剖動物の雌雄全例の肺,肝臓,腎臓および甲状腺,ならびに対照群を含む全動物の肉眼的異常部位を常法に従ってヘマトキシリン・エオジン染色標本を作製し,鏡検した.
歩行失調は200 mg/kg群の雄2例,雌3例,1000 mg/kg群の雄12例,雌全例に投与後発現したが,翌日までに回復した.本変化は200と1000 mg/kg群の雌雄で投与開始日からみられ,投与期間が進むに従って発現例数は減少した.流涎は200 mg/kg群の雄3例,雌2例,1000 mg/kg群の雌雄全例に投与直後あるいは投与前に認められた.自発運動の低下は1000 mg/kg群の雄3例,雌2例に認められた.本変化は雄で第3週,雌で第6週以降のいずれも投与後に散発的にみられたが,翌日までに回復した.また,1000 mg/kg群の雌1例では,自発運動の低下時に緩徐呼吸あるいは側臥位を伴う例もあった.これらの変化は,回復期間中にはみられなかった.
この他,前肢の脱毛が対照群の雄3例および1000 mg/kg群の雌1例に,胸部の腫瘤が40 mg/kg群の雌1例にみられた.これらの変化については,その発現状況から被験物質投与とは関連のない変化と判断した.

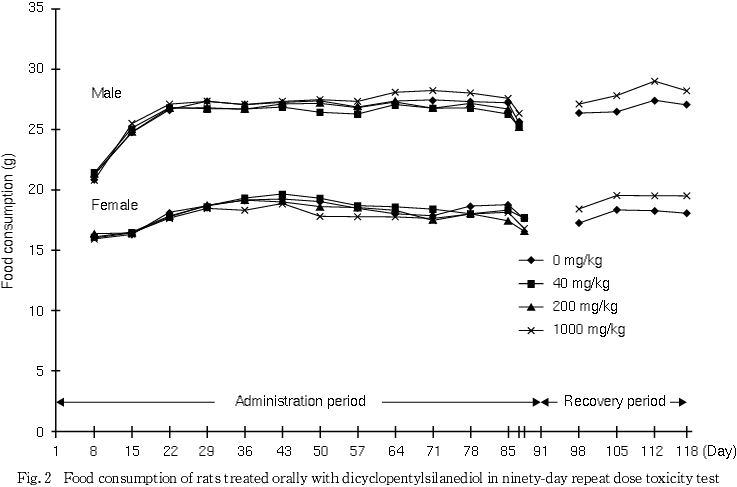
投与期間終了時の検査で,MCVおよびMCHの低値が200 mg/kg群の雄にみられた.しかし,これらは軽微な変化であり,1000 mg/kg群ではみられないことから,被験物質投与とは関連のない変化と判断した.
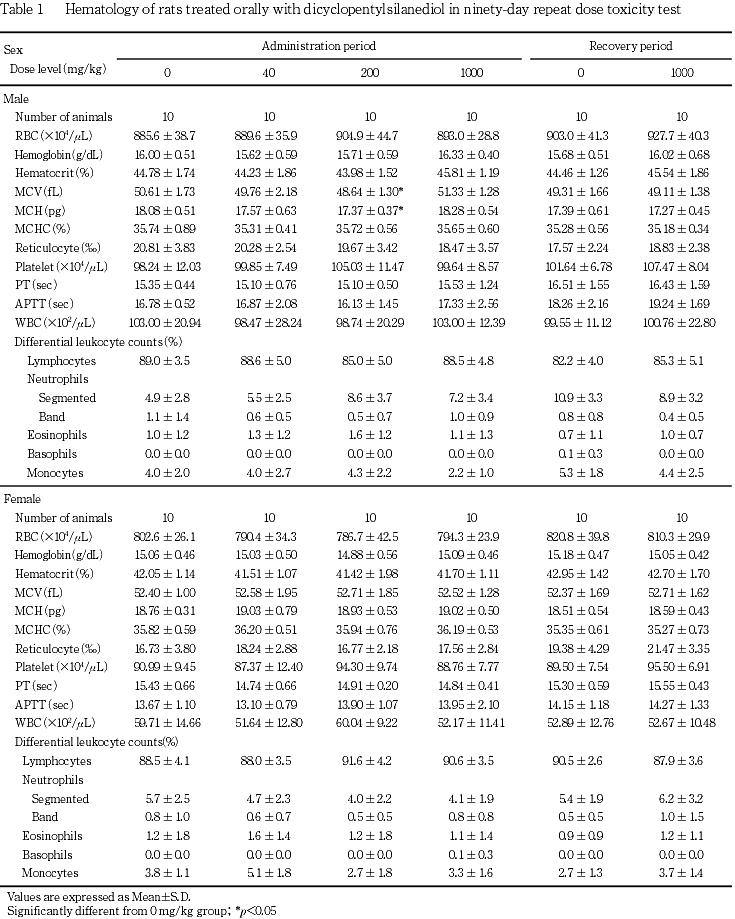
この他,回復期間終了時の検査で,尿素窒素の高値が1000 mg/kg群の雄に,カリウムの高値が1000 mg/kg群の雌に,それぞれみられた.しかし,これらは軽微な変化であり,投与期間終了時の検査ではみられないことから,被験物質投与とは関連のない変化と判断した.
pHの上昇が全被験物質投与群の雄でみられた.しかし,本変化は軽微な正常範囲内の変動であることから,被験物質投与とは関連のない変化と判断した.
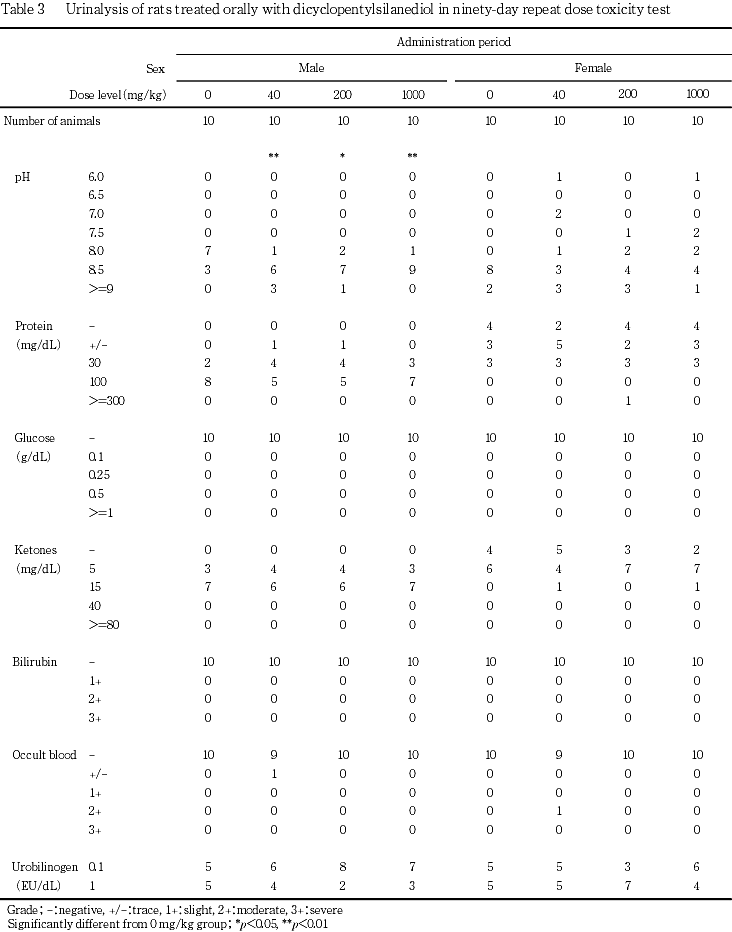
投与開始前および投与期間中の被験物質投与群では,偶発変化と思われる種々の変化が散見された.
この他,投与期間終了時の検査で,下垂体絶対・相対重量の高値が40 mg/kg群の雄に,下垂体相対重量の高値が200 mg/kg群の雄に,それぞれみられたが,これらは軽微な変化であり,1000 mg/kg群ではみられないことから,被験物質投与とは関連のない変化と判断した.
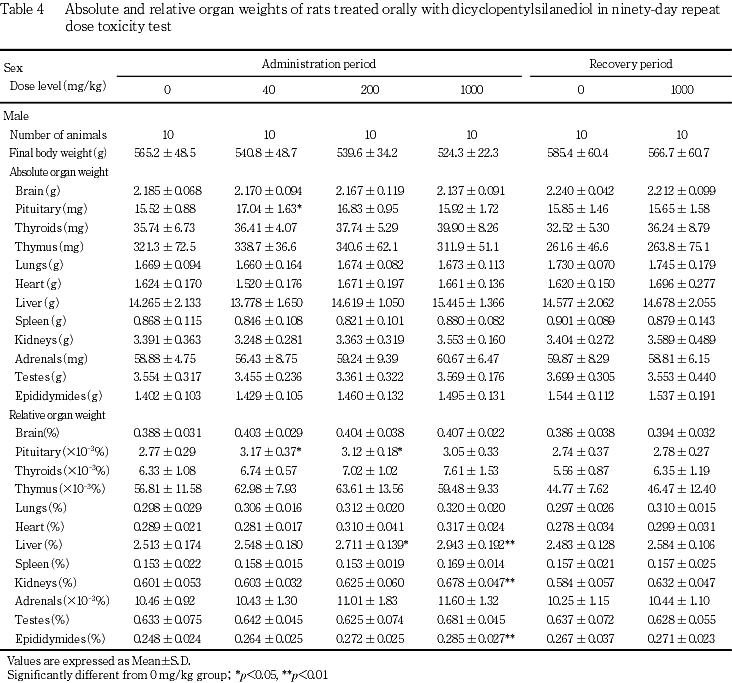
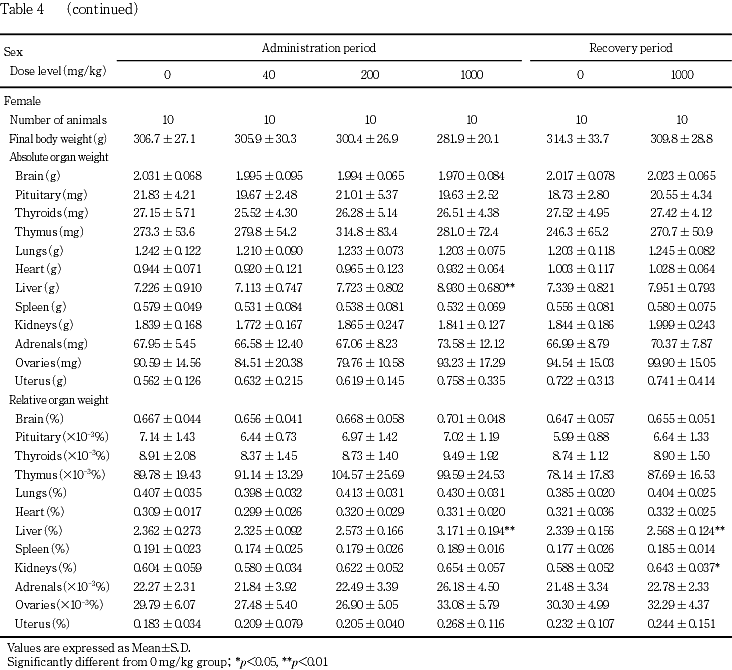
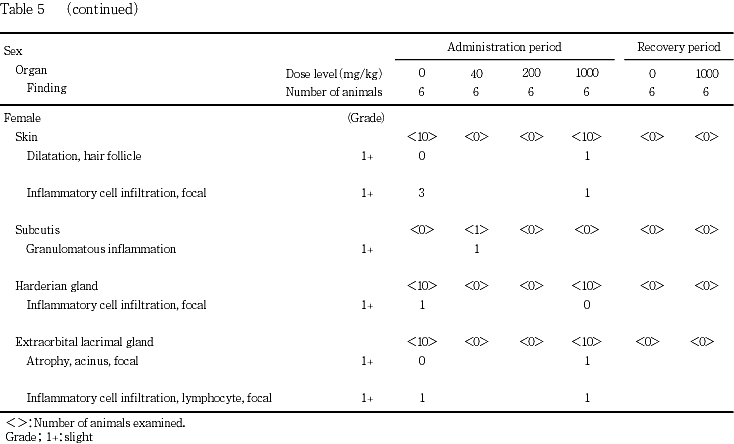
この他,投与期間終了時および回復期間終了時に被験物質投与群で,偶発変化と思われる種々の変化が散見された.
投与期間終了時の解剖動物で肺の泡沫細胞の集簇が全群の雌雄で比較的高頻度にみられたため,回復期間終了時に解剖動物の雌雄全例の肺についても検査したが,その発現状況から本変化は被験物質投与の影響ではないと判断した.また,回復期間終了時の検査で,腎臓相対重量の高値が1000 mg/kg群の雌にみられたため,回復期間終了時の解剖動物の雌の腎臓について検査したが,被験物質投与の影響と考えられる変化はみられなかった.
この他,投与期間終了時および回復期間終了時に被験物質投与群で,偶発変化と思われる種々の変化が散見された.
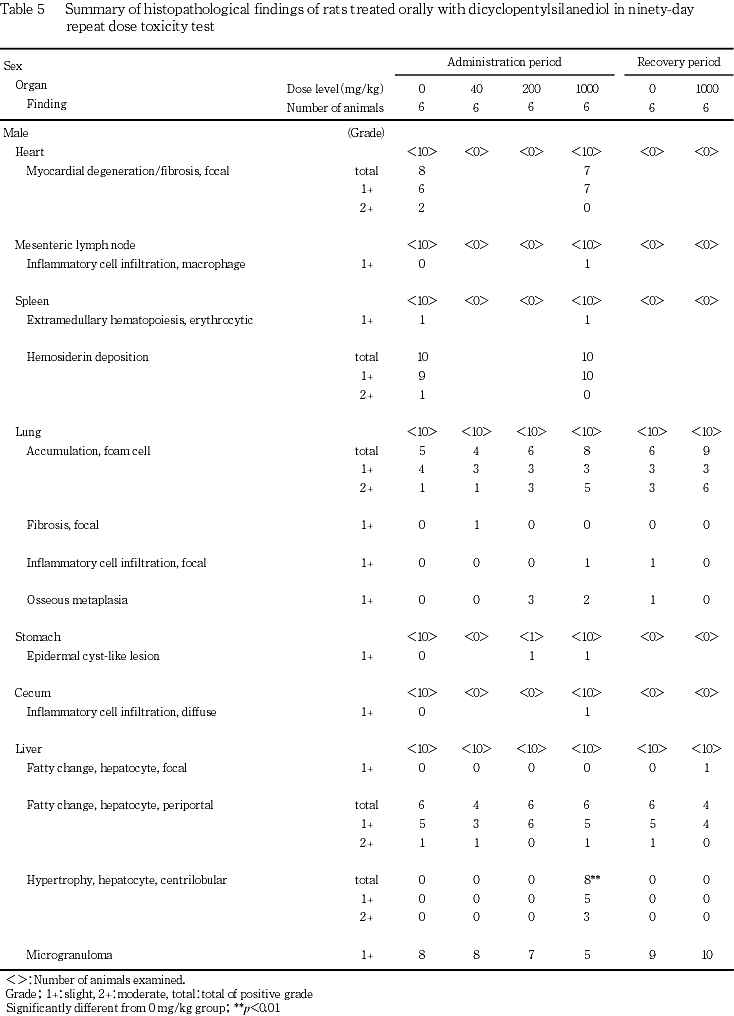
一般状態において,投与期間中に歩行失調と流涎が200および1000 mg/kg群の雌雄で,自発運動の低下が1000 mg/kg群の雌雄で,それぞれ認められた.また,1000 mg/kg群の雌では自発運動の低下時に緩徐呼吸および側臥位を伴うものがみられた.歩行失調については,投与後に一過性の中枢神経系障害が起こったためと考えられるが,病理組織学検査で中枢神経系の変化は認められなかった.また,投与期間が進むに従って本変化の発現例数は減少した.流涎については,主に投与後短時間に発現する一過性の変化であり,被験物質の直接的な口腔粘膜刺激による可能性が考えられるが,歩行失調がみられることから,中枢神経障害に起因する可能性も否定できない.自発運動の低下,緩徐呼吸および側臥位は投与後一過性の変化であった.これらの変化は投与の休止により消失した.
体重の低値が1000 mg/kg群の雌で投与期間末期(第78日から第90日)に認められた.回復期間中には,対照群の体重と差はみられなかった.
肝臓では,絶対・相対重量の高値が1000 mg/kg群の雌に,相対重量の高値が200および1000 mg/kg群の雄に,それぞれ認められた.剖検で暗褐色化と腫大が1000 mg/kg群の雌に,病理組織学検査で小葉中心性肝細胞肥大が200 mg/kg群の雌および1000 mg/kg群の雌雄に,それぞれ認められた.小葉中心性肝細胞肥大は,肝臓の薬物代謝酵素が誘導された場合の生体の適応反応として発現することが知られている1).回復期間終了時の検査では,相対重量の高値が1000 mg/kg群の雌にみられたが,投与期間終了時に比べその程度は軽減し,剖検および病理組織学検査では異常は消失して,これらの変化には回復性が認められた.
甲状腺では,濾胞上皮細胞の肥大が1000 mg/kg群の雌雄で認められた.本変化は,肝細胞肥大に伴ってしばしば引き起こされることが知られている2).回復期間終了時の解剖動物では,1000 mg/kg群の雄で本変化がみられたが,その発現例数は減少し,回復性が認められた.
腎臓では,病理組織学検査で近位尿細管上皮の硝子滴発現の増強が1000 mg/kg群の雄に認められた.雄ラットにおける特異的な変化として,各種の薬物や化学物質の投与により近位尿細管上皮の硝子滴発現の沈着が増強するα2uグロブリン腎症が知られている3, 4).本試験で認められた変化も雄のみの発現であったことからα2uグロブリン腎症に類似した変化と考えられる.また,1000 mg/kg群の雄では腎臓相対重量の高値もみられた.回復期間終了時の解剖動物では,これらの変化はみられず,回復性が認められた.
血液生化学検査において,総コレステロールの高値が200および1000 mg/kg群の雌に,トリグリセライドの低値が1000 mg/kg群の雄に,それぞれ認められた.これらの変化については,関連する変化が認められないことから,毒性学的意義の低い変化と思われる.これらの変化は回復期間終了時にはみられず,回復性が認められた.
この他,投与期間終了時の検査で,血液生化学検査においてA/G比の低値が1000 mg/kg群の雌で認められたが,総蛋白およびアルブミンに変動はみられないことから,毒性学的意義のない変化と判断した.また,器官重量において,精巣上体相対重量の高値が1000 mg/kg群の雄に,回復期間終了時の検査で,腎臓相対重量の高値が1000 mg/kg群の雌にみられた.しかし,病理組織学的には変化はみられず,絶対重量に変動はないことから,被験物質投与とは関連のない偶発変化と判断した.
摂餌量測定,血液学検査,尿検査および眼科学検査の結果には,被験物質投与に起因すると考えられる変化は認められなかった.
以上,雌雄いずれも200および1000 mg/kg群で被験物質投与に起因すると考えられる変化が認められた.200 mg/kg群では,一般状態において雌雄に歩行失調および流涎,器官重量において雄に肝臓相対重量の高値,血液生化学検査において雌に総コレステロールの高値,病理組織学検査において雌に肝臓の肝細胞肥大がみられたことから,本試験条件下におけるジシクロペンチルシランジオールの無影響量(NOEL)は,雌雄いずれも40 mg/kg/dayと判断した.
| 1) | P. Greaves, “Histopathology of preclinical toxicity studies,” eds by P. Greaves, Elsevier, Amsterdam, 1990, pp.393-441. |
| 2) | C. Gopinath, D. E. Prentice, and D. J. Lewis, “Atlas of experimental toxicological pathology,” eds by C. Gopinath, D. E. Prentice, and D. J. Lewis, MTP Press Limited, Lancaster, 1987, pp.104-121. |
| 3) | P. Greaves, “Histopathology of preclinical toxicity studies,” eds by P. Greaves, Elsevier, Amsterdam, 1990, pp.497-554. |
| 4) | J. A. Swenberg, B. Short, S. Borghoff, J. Strasser, and M. Charbonneau, Toxicol. Appl. Pharmacol., 97, 35(1989) |
| 連絡先 | |||
| 試験責任者: | 山下弘太郎 | ||
| 試験担当者: | 多田圭子,岡崎欣正,豊田直人 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-0255 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Kotaro Yamashita(Study director) Keiko Tada, Yoshimasa Okazaki, Naoto Toyota | |||
| Kashima Laboratory, Mitsubishi Chemical Safety Institute Ltd. | ||||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255, Japan. | ||||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |||