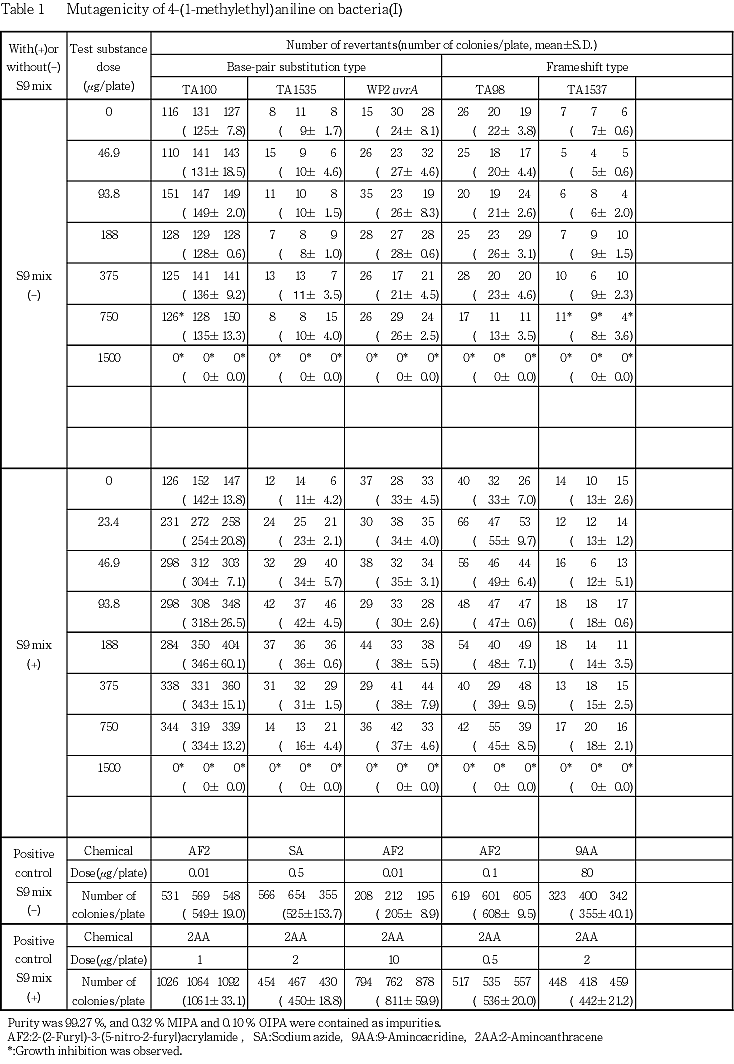
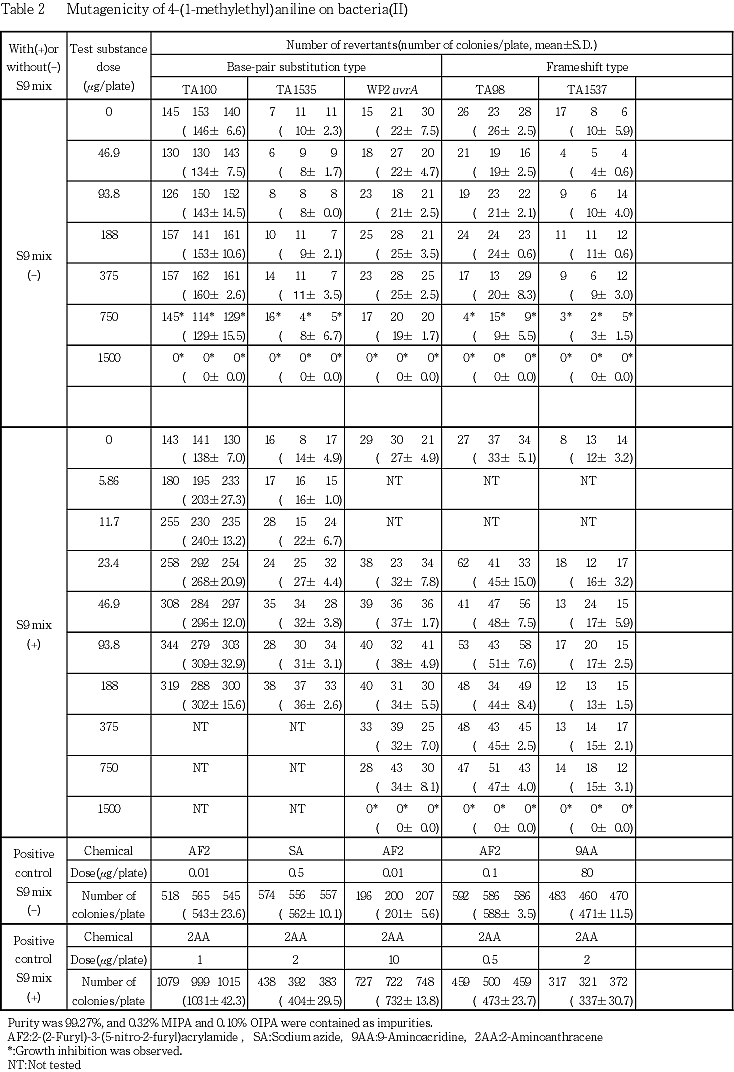
検定菌として,Salmonella typhimurium TA100,TA1535,TA98,TA1537 1)およびEscherichia coli WP2 uvrA 2)の5菌株を用い,S9 mix無添加および添加試験のいずれも,用量設定試験で抗菌性が認められたことから,本試験はS9 mix無添加試験では46.9〜1500 μg/plate,S9 mix添加試験では23.4〜1500 μg/plateの範囲で実施した.ただし,TA100とTA1535のS9 mix添加試験では,本試験Iで188または93.8 μg/plate以下の用量で復帰変異コロニー数の用量依存的な増加が認められたため,本試験IIでは5.86〜188 μg/plateの範囲で実施した.
その結果,2回の本試験とも,TA100とTA1535のS9 mix添加試験において,復帰変異コロニー数が溶媒対照値の2倍以上に増加し,用量依存性が認められた.
以上の結果から,4-(1-メチルエチル)アニリンは,用いた試験系において変異原性を有するもの(陽性)と判定した.
S. typhimuriumの4菌株は1975年10月31日にアメリカ合衆国,カリフォルニア大学のB. N. Ames博士から分与された.
E. coli WP2 uvrA株は1979年5月9日に国立遺伝学研究所の賀田恒夫博士から分与された.
検定菌は-80℃以下で凍結保存したものを用い,各菌株の特性確認は,凍結保存菌の調製時に,アミノ酸要求性,UV感受性,膜変異(rfa)およびアンピシリン耐性因子pKM 101(プラスミド)の有無について調べ,特性が維持されていることを確認した.
試験に際して,ニュートリエントブロスNo. 2(Oxoid Ltd.)を入れたL字型試験管に解凍した種菌を一定量接種し,37℃で10時間往復振とう培養したものを検定菌液とした.
分光光度計により660 nmの吸光度を測定し,検定菌液の増殖を確認した.
4-(1-メチルエチル)アニリンは,ジメチルスルホキシド(DMSO,ロット番号:TPJ5678,和光純薬工業(株))に溶解して最高用量の調製液を調製した後,同溶媒で所定の濃度に希釈して速やかに試験に用いた.
| AF2 | : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド(和光純薬工業(株)) |
| SA | : | アジ化ナトリウム(和光純薬工業(株)) |
| 9AA | : | 9-アミノアクリジン(Sigma Chem. Co.) |
| 2AA | : | 2-アミノアントラセン(和光純薬工業(株)) |
AF2,9AAおよび2AAはDMSOに,SAは超純水に溶解したものを-20℃で凍結保存し,解凍後,速やかに試験に用いた.
| (A) | バクトアガー(Difco Lab.) | 0.6 w/v% |
| 塩化ナトリウム | 0.5 w/v% | |
| (B)* | L-ヒスチジン | 0.5 mM |
| D-ビオチン | 0.5 mM |
| * | : | WP2 uvrA用には,0.5 mM L-トリプトファン水溶液を用いた. |
| 硫酸マグネシウム・7水和物 | 0.2 g |
| クエン酸・1水和物 | 2 g |
| リン酸水素二カリウム | 10 g |
| リン酸一アンモニウム | 1.92 g |
| 水酸化ナトリウム | 0.66 g |
| グルコース | 20 g |
| 大洋寒天(清水食品) | 15 g |
径90 mmのシャーレ1枚あたり30 mLを流して固めたものである.
| S9** | 0.1 mL |
| 塩化マグネシウム | 8 μmol |
| 塩化カリウム | 33 μmol |
| グルコース-6-リン酸 | 5 μmol |
| NADH | 4 μmol |
| NADPH | 4 μmol |
| ナトリウム-リン酸緩衝液(pH 7.4) | 100 μmol |
| ** | : | 7週齢のSprague-Dawley系雄ラットをフェノバルビタール(PB)および 5,6-ベンゾフラボン(BF)の併用投与で酵素誘導して作製されたS9(キッコーマン(株))を用いた. |
小試験管中に,被験物質調製液0.1 mL,リン酸緩衝液0.5 mL(S9 mix添加試験においてはS9 mix 0.5 mL),検定菌液0.1 mLを混合し,37℃で20分間プレインキュベーションしたのち,約45℃に保温したトップアガー2 mLを加えて混和し,合成培地平板上に流して固めた.また,対照群として被験物質調製液の代わりに使用溶媒,または数種の陽性対照物質溶液を用いた.各検定菌ごとに用いた陽性対照物質の名称および用量は各Table中に示した.同時に実施した試験については,溶媒および陽性対照群を共通とした.培養は37℃で48時間行い,生じた復帰変異コロニー数を目視またはコロニーアナライザーを用いて算定した.抗菌性の有無については,肉眼あるいは実体顕微鏡下で,寒天表面の菌叢の状態から判断した.用いた平板は用量設定試験においては,溶媒および陽性対照群では3枚ずつ,各用量については1枚ずつとした.また,本試験においては,両対照群および各用量につき,3枚ずつを用い,それぞれの平均値と標準偏差を求めた.用量設定試験は1回,本試験は2回実施し,結果の再現性を確認した.
したがって,本試験における最高用量は,S9 mix無添加試験および添加試験とも1500 μg/plate とした.
最高用量を1500 μg/plateとして,公比2で6〜7用量を設定して本試験Iを実施した(Table 1).その結果,TA100とTA1535のS9 mix添加試験では,それぞれ46.9〜750 μg/plateおよび23.4〜375 μg/plateの用量で溶媒対照値の2倍以上となる復帰変異コロニー数の増加が認められ,それぞれ188および93.8 μg/plateまで用量依存的に増加した.そこで,これらについては,本試験IIの実施に当たって,最高用量を188 μg/plateに下げて公比2で6用量を設定した(Table 2).その結果,両検定菌とも用量依存的な復帰変異コロニー数の増加が認められ,46.9 μg/plateで溶媒対照値の2倍に達した.
TA100とTA1535のS9 mix無添加試験およびその他の検定菌については,本試験Iと同一用量で本試験IIを実施した(Table 2).その結果,2回の試験とも溶媒対照値の2倍以上となる復帰変異コロニー数の増加は認められなかった.
以上の結果から,本被験物質はS9 mix添加条件下でTA100とTA1535に復帰変異を誘発するものと考えられる.当被験物質の最大比活性は,TA100のS9 mix添加試験における3454.2(本試験I,46.9 μg/plate)で,同一条件下における陽性対照物質2-アミノアントラセンの値(919000)の約270分の1であった.
以上の結果に基づき,4-(1-メチルエチル)アニリンは,用いた試験系において変異原性を有するもの(陽性)と判定した.
なお,本被験物質はチャイニーズ・ハムスター培養細胞を用いる染色体異常試験では陰性であった4).また,本被験物質の類縁化合物のアニリン5)およびm-トルイジン6)は,復帰変異試験で陰性の結果が得られている.

| 1) | D. M. Maron, B. N. Ames, Mutat. Res., 113, 173(1983). |
| 2) | S. Venitt, C. Crofton-Sleigh, "Evaluation of Short-Term Tests for Carcinogens," eds. by F. J. de Serres, J. Ashby, Elsevier, North-Holland, New York, 1981, pp. 351-360. |
| 3) | T. Matsushima, T. Sugimura, M. Nagao, T. Yahagi, A. Shirai, M. Sawamura, "Short-Term Test Systems for Detecting Carcinogens," eds. by K. H. Norpoth, R. C. Garner, Springer, Berlin, Heidelberg, New York, 1980, pp. 273-285. |
| 4) | 厚生省生活衛生局企画課生活化学安全対策室監修,"化学物質毒性試験報告,"Vol. 7,化学物質点検推進連絡協議会,東京,1999, p. 350. |
| 5) | 石館基監修,"微生物を用いる変異原性試験データ集,"エル・アイ・シー,東京,1991, pp. 27-28. |
| 6) | 厚生省生活衛生局企画課生活化学安全対策室監修,"化学物質毒性試験報告,"Vol. 2,化学物質点検推進連絡協議会,東京,1995, p. 79. |
| 連絡先 | |||
| 試験責任者: | 澁谷 徹 | ||
| 試験担当者: | 原 巧,川上久美子 | ||
| (財)食品薬品安全センター 秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Tohru Shibuya (Study Director) Takumi Hara, Kumiko Kawakami | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | FAX +81-463-82-9627 | |||