���η�̡�3�ݥ˥ȥ��٥ʥߥ��15 mg/kg/day�ʾ�����̤ϡ�5��7���֤�Ϣ³��Ϳ�ˤ�äƻ�ͺ��åȤ�磤μ��礢�뤤�ϰſ������褹ȿ����Ϳ����ȯ���̤Ǥ��ꡢ�����λ�Ǥ�ʬ�ڤ��뤤��Ӯ�鵡ǽ�˾㳲������ֲ�ǽ�����������줿���ޤ�50 mg/kg/day�ϡ���ͺ��åȤ��ν����ä��������뤤���ݱ��̤θ������褷�������ʬ������λ�1�㤬��˴�������Ȥ��顢�ܲ���ʪ��ǥ����åȤ��Ф���������̤�㴳ο�路���̤ȹͤ���줿���ʤ����ܲ���ʪ�ˤĤ��Ƥ�ͺ��åȤ��Ф��������������Τ��Ƥ��뤬���ܻ��ﲼ�ˤ����Ƥϡ�ͺ��åȤ�����ǽ�Ϥ��Ф������餫���������ʤ��ä����ޤ���50 mg/kg/day���ưʪ����Ϳ���Ƥ⤽�ν�������ȯ�顢��¸������ӷ��֤ˤϰ��ƶ���ڤܤ��ʤ��ä��������Τ��Ȥ��顢�ܻ��ﲼ�Ǥϡ�3�ݥ˥ȥ��٥ʥߥ�λ�ͺ��åȤ��Ф���ȿ����Ϳ�����˴ؤ���̵�ƶ��̤���ӻ��åȤ�����ǽ�Ϥ��Ф���̵�ƶ��̤�5 mg/kg��ͺ��åȤ�����ǽ�Ϥ��Ф���̵�ƶ��̤���Ӽ���������Ф���̵�ƶ��̤�50 mg/kg��Ƚ�Ǥ���롣
����OECD�ˤ���¸����ʪ���ΰ����������˷��������Ĵ�����Ȥΰ�ĤȤ���3�ݥ˥ȥ��٥ʥߥ�δʰ������������Ԥ����ܲ���ʪ��������ȯ�������ˤĤ��Ƹ�Ƥ�����ΤǤ��η�̤���𤹤롣
���︳ʪ����0.5%CMC-Na���ϱդ˷�����������������̤ˤ����Ƥ�1�����Ϳ���̤�5 ml/kg�ˤʤ�褦�˴��̤�Ĵ��������Ϳ���ΤȤ���Ĵ�������ž�ﲼ��̩���ݴɤ���Ĵ����7���������Ϳ������Ĵ��������︳ʪ���ϡ������������ݴɾ�ﲼ�Ǿ��ʤ��Ȥ�7���ְ���Ǥ��ꡢ�Ѱ�����ݻ����줿���ޤ������Ѥ�����Ϳ���Τδ���¬���̤ˤ�����Ϥʤ��ä���
��ưʪ�ϡ�����24��1����м���55��5%�����������15���֡�����12���֡ʸ���7�������7���ˤ�Ĵ�ᤵ�줿�Хꥢ�������ƥ�λ��鼼�ǡ���°�����־���������22��27��19 mm�����ܥ������ʳ��ˡˤ˸��̤˼��Ƥ��ƻ��餷���Ƿ�������CA-1�����ܥ��쥢�ʳ��ˡˤ���ӿ�ƻ���ͳ���ݼ褵������ǥ��18���ʸ����ưʪ�ˤϡ����饱�����ξ��˶�°�����Ĥ��ߤ������ߤȤ��ƥۥ磻�ȥե졼�������ܥ��㡼�륹����С��ʳ��ˡˤ�Ŭ�����뤷����
���뤷���������塢����Ӿ��ߤˤϻ�˻پ���褹��ǽ�����ͤ�������ʪ�κ��ߤϤʤ��ä���
�����̤���Ϳ���Τϡ�ͺ���Ф��Ƥϸ�����14���֤ȸ��۴���14���֤���Ӹ��۴��ֽ�λ��14���֤�Ϣ³42���֡��ޤ�������Ф��Ƥϸ�����14���֤ȸ��۴�����ʸ�����Ω�ޤ�;��Ĺ14���֡ˤʤ�Ӥ˸�����Ω��Ǥ�ǥ�����֤��̤���ʬ�ڸ��Ӯ��3���ޤ�����1��å��Ѱߴɤ��Ѥ��ƶ���Ū�˷и���Ϳ��������������Ϳ�ϡ���§�Ȥ��ư������δ֡��̾�13����16���ˤ˹Ԥ�����ưʪ����Ϳ���̤ϡ�ͺ�ʤ�Ӥ˸���������Ӹ��۴�����λ�ˤĤ��ƤϽ�1���¬���νŤ��Ȥˡ��ޤ���������Ω��λ�ˤĤ��Ƥ�ǥ��0�����νŤ��Ȥˤ��줾�컻�Ф�����
��˴��ϡ����������Ϳ���ˤ����Ƥ�ǧ����ʤ��ä������̾��֤˴ؤ��Ƥϡ�100 mg/kg��Ϳ�����������Ϳ10��14������Ϳ����������Ϳ0������Ϳ14����˶�����ˤ���ü����ɽ���������ߤ�줿��������¾�ˤϡ����������Ϳ���ˤ����Ƥ��︳ʪ������Ϳ�˵��������ȿ��ꤵ�����̾��֤��Ѳ���ǧ����ʤ��ä���
ii) �νŤ�����ݱ���
�νš��ν������̡��ݱ��̤Ȥ���оȷ����︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
iii) ˶���긫�����㤪���������ν���
磤μ��礢�뤤�ϰſ�������100 mg/kg��Ϳ����5�����㤪���50 mg/kg��Ϳ����5����4��ˤߤ�줿�ۤ������㤪���������Τΰ�̤���100 mg/kg��Ϳ����2�㤪���50 mg/kg��Ϳ����1��ˤߤ�줿�������������㤪���������Τν��̤ˤϡ��оȷ����︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
��˴��ϡ����������Ϳ���ˤ����Ƥ�ǧ����ʤ��ä������̾��֤˴ؤ��Ƥϡ�100 mg/kg��Ϳ�������㤪���50 mg/kg��Ϳ����5����4�����Ϳ10��18���δ֤���ü����ɽ���������ߤ�줿��
ii) �νŤ�����ݱ���
�νš��ν������̤ˤϤ������¬������ˤ����Ƥ��оȷ����︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä����ݱ��̤���100 mg/kg��Ϳ���ˤ�����ͭ�դ����ͤ�����
iii) ˶���긫
���︳ʪ����Ϳ���Ȥ⤹�٤Ƥλ��磤μ��礢�뤤�ϰſ�����ǧ���줿��
��ͺ�Ȥ⡢����ˤĤ��ƻ�����������ѻ�������
(2) �ν�
��ͺ�Ȥ⡢����ˤĤ����νŤ������潵1���ͺ����Ϳ0��7��14��21��28��35��41��������Ϳ0��7��14��21������Ϳ0������Ϳ�������ˡͤ���Ӳ�˶����¬�ꤷ�����ޤ���������Ω��Ǥϡ�ǥ��0��7��14��21����ʬ�ڤ�����Ǥϡ�ʬ�ڸ�1�����4����Ӯ��1�����4���ˤ��νŤ�¬�ꤷ����
(3) �ݱ���
��ͺ�Ȥ⡢����ˤĤ����ν�¬������Ʊ���˱½��̤�¬�ꤷ��¬�������鼡��¬�����ޤǤδ֤��ݱ��̤��ꤷ�������۴�������ݱ��̤�¬�ꤷ�ʤ��ä���������Ω��Ǥϡ�ǥ��0-7��7-14��14-20�������ʬ�ڤ�����Ǥϡ�Ӯ��1-4�����ݱ��̤�¬�ꤷ����
(4) ����
���ۤϡ���Ϳ14����15����Ϳ���ˤ�ͼ�������Ĺ2���֡�Ʊ�췲��λ�ͺ��1��1�ǽ���Ʊ�蘆���ƹԤä���������Ω�γ�ǧ�ϡ���ī��������뤤��絹�������Ҥ�¸�ߤ�Ĵ�٤뤳�Ȥˤ��Ԥ�����������ǧ���줿��ϡ���������ǥ��0���ȵ�������ͺ����ʬΥ�������̤˻��餷�������۷�̤��顢�Ʒ��ˤĤ��Ƹ���Ψ�Ρʸ���ưʪ����Ʊ��ưʪ���ˡ�100�ϡ��μ���Ψ��ǥ��ưʪ��������ưʪ���ˡ�100�Ϥ����Ʊ�ﳫ�������������ǧ���ޤǤ�����������ʤ���2���֤θ��۴�����˸������ʤ��ä���ͺ��̤����ͺ����ӻ�ˤϡ����۴��ֽ�λ������Ϳ28���������ˤ�˶��������
(5) ʬ�ھ���
�Ʒ��Ȥ������Ω��ϡ��������ʬ�ڤ�������ʬ�ھ��֤�ľ�ܴѻ��ϡ���ǽ�ʤ�ΤˤĤ��ƹԤä�����������ľ�ܴѻ��Ǥ��ʤ��ä����ΤˤĤ��Ƥ⡢ʬ�ڸ��ħ������ʬ�ں����ʬ���ٱ�ʤɤ�ʬ�ھ㳲��̵ͭ��Ƚ�Ǥ������̤˵�Ͽ������
(6) ʬ�����λ���
ʬ�ڤγ�ǧ�ϡ�����9����11���˸��ꤷ�����λ����Ӥ�ʬ�ڤ���λ���Ƥ��뤳�Ȥ��ǧ�������ΤˤĤ��ơ���������Ӯ��1��������������ʬ������Ӯ��0���ˤȵ��ꤷ��������11������ʬ�ڤ������ΤˤĤ��Ƥϡ�������Ӯ��1���Ȥ�����
ʬ�ڤ��ǧ��������ˤĤ���ǥ�����֡�ǥ��0����ʬ�����������ˤ��ꤷ�����ޤ����л�Ψ�Ρ������л������ǥ������ˡ�100�Ϥ����
(7) ˶��
a) ͺưʪ
̤����ͺ�ϸ��۴��ֽ�λ���ˡ�������Ωͺ�������42����Ϳ����������Ϳ42���ˤ˥����ƥ뿼��첼�����졦�व����˶���������ޤ�������ˤĤ������㤪���������Τ�Ŧ�Ф������̤�¬�ꤷ�������㤪���������Τϡ��֥���դ˸��ꤷ����¸����50 mg/kg��Ϳ��������оȷ�������ˤĤ��������ȿ���Ū������Ԥä���˶���ˤ����ư۾��ǧ��ﴱ��10%�ۥ�ޥ��˸��ꤷ����¸������
b) ��ưʪ
ʬ�ڤ������Ӯ��4���ˡ�����������ʬ�ڤ��ʤ����ǥ��25���������ˡ��ޤ���̤������ϸ��۴��ֽ�λ���ˤ��줾�쥨���ƥ뿼��첼�����졦�व����˶��������ǥ����ǥ�����̤�����Τ��������ˤ����Ƥ����㤪��ӻҵܤ�Ŧ�Ф����ҵܤˤĤ��Ƥ�Salewskiˡ3�ˤ���Ѥ����徲�����������徲�����ǧ����������ϥ֥���դ˸��ꤷ����¸�������θ���������ǥ�����ο���������ۤ���������������ǥ�Ǥ��ä����̤������ˤĤ��������ȿ���Ū������Ԥä���˶���ˤ����ư۾��ǧ��ﴱ����ӻҵܤ�10%�ۥ�ޥ��˸��ꤷ����¸������
Ӯ��1���˻���������¸���ܻ�˴���ˤ�Ĵ�١����λ���Ψ�Ρʻ��������徲�����ˡ�100�Ϥ���ӽ���Ψ�Ρʽл����������徲�����ˡ�100�Ϥ�������������̤�Ĵ�١���ɽ�۾��̵ͭ��ѻ�������
(2) ��˴�����λ���
��˴����������Ĵ�١�Ӯ��1������¸Ψ�Ρ����������������ˡ�100�Ϥ����Ӯ��4������¸Ψ�Ρ�Ӯ��4������������Ӯ��1�����������ˡ�100�Ϥ������˴����˶���������Ф����ʢ����δﴱ�������塢�����Ρ���˸��ꤷ����¸������
(3) ����
Ӯ��1�������4���˰�ʢñ�̤ǻ�ͺ�̤��νš�litter���̡ˤ�¬�ꤷ��[litter���̡�¬�����]���ʢ�ˤĤ��Ƶ���
(4) ˶��
Ӯ��4����������ƥ뿼��첼���व����˶�����������Ф����ʢ����δﴱ�ϡ���礷��Ŧ�Ф�����ʢ���Ȥ�10%�ۥ�ޥ��˸��ꤷ����¸���������������ϡ���ʢ���Ȥ˥����Ρ���˸��ꤷ����¸������
(5) ���ʴѻ�
50 mg/kg��Ϳ��������оȷ��ˤĤ���Ӯ��4����˶�������������㤪��Ӵѻ���ǽ�ʻ�˴����Dawsonˡ4�ˤˤ�����ɸ�ܤȤ������ʰ۾浪����Ѱۤ�̵ͭ��Ĵ�٤����ʤ�����˴���ˤĤ��Ƥϡ��оȷ��ˤϰ۾�ѰۤȤ�ˤߤ�줺50 mg/kg��Ϳ���ˤ����ƤΤ߹����Ѱۤ��ߤ�줿���Ȥ���ѻ����оݤ������˹��������٤Ƥδѻ���ǽ�ʻ�˴���ˤĤ��ƹ��ʴѻ���Ԥä���
 ˡ�ˤ���оȷ��ȳ��︳ʪ����Ϳ���Ȥδ֤�ʿ���ͤκ��θ����Ԥä���ʬ�������ͤǤʤ��ä����ϡ�Kruskal-Wallis�ν�̸����Ԥ������֤�ͭ������ǧ���줿�����оȷ��ȳ��︳ʪ����Ϳ���Ȥκ��ˤĤ���Dunnett�����뤤��Scheff
ˡ�ˤ���оȷ��ȳ��︳ʪ����Ϳ���Ȥδ֤�ʿ���ͤκ��θ����Ԥä���ʬ�������ͤǤʤ��ä����ϡ�Kruskal-Wallis�ν�̸����Ԥ������֤�ͭ������ǧ���줿�����оȷ��ȳ��︳ʪ����Ϳ���Ȥκ��ˤĤ���Dunnett�����뤤��Scheff ���θ����Ԥä���
���θ����Ԥä���
ͭ�տ��ϡ�5%�����1%�Ȥ�����
��˴��ϡ��оȷ���ޤत�������Ϳ���ˤ����Ƥ�ǧ����ʤ��ä���
(2) ���̾���
50 mg/kg��Ϳ����1��ˤ�������ü����ɽ������������Ϳ36����37����Ϳ���ˤ���˶�����ˤ�����ǧ���줿�����Τۤ��ˤϡ�5 mg/kg��Ϳ����1��ǡ�Ω�ӡ�����Ϥγ쿧���졢ʵ�ξ�γ��������Ϳ7������11����8���12����Ϳ���ˤˤ����ư��Ū�ˤߤ�줿����¾����Ϳ����������Ѳ���ǧ����ʤ��ä���
(3) �ν�
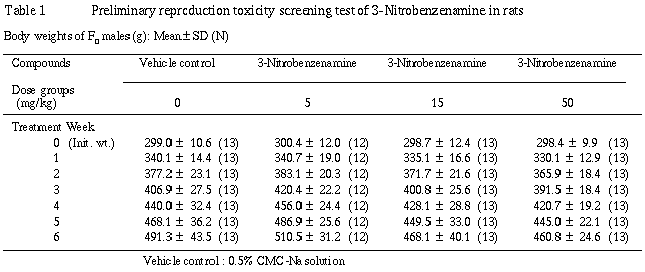
1) �νš�Table 1��
�������¬������ˤ����Ƥ��оȷ��ȳ��︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
2) ������
50 mg/kg��Ϳ���ˤ�������Ϳ���ϡ���Ϳ��1���������̤�ͭ�ա�p<0.05�ˤ����ͤ�����15 mg/kg��Ϳ���Ǥ���Ϳ��3��4���������̤�ͭ�ա�p<0.05�ˤ����ͤ����������̰�¸Ū���Ѳ��ǤϤʤ��ä���5 mg/kg��Ϳ���������̤ˤϤ������¬������ˤ����Ƥ��оȷ�����Ӥ���ͭ�պ���ǧ����ʤ��ä���
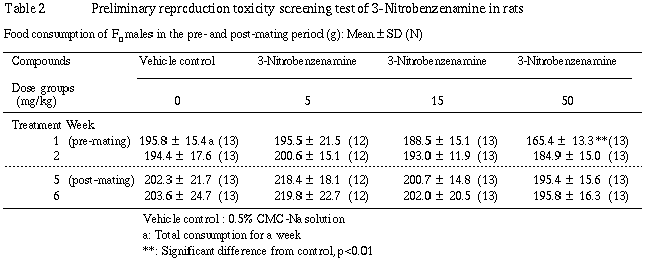
(4) �ݱ��̡�Table 2��
50 mg/kg��Ϳ���ˤ�������Ϳ��1�����ݱ��̤���ͭ�ա�p<0.05�ˤ����ͤ�����15 mg/kg�ʲ�����Ϳ�����ݱ��̤ˤϡ��︳ʪ������Ϳ�˵��������ȿ��ꤵ����Ѳ���ǧ����ʤ��ä���
(5) ˶���긫��Table 3��
50 mg/kg��Ϳ����13����3��˴Τμ��礪���50 mg/kg��Ϳ����13������ʤ�Ӥ�15 mg/kg��Ϳ����13����3���磤μ��礢�뤤�ϰſ������ߤ�줿�ۤ��ˤϡ��︳ʪ����Ϳ�˵�������ȿ��ꤵ����Ѳ��Ϥߤ��ʤ��ä���
(6) ���㤪���������ν���
���㤪���������Τν��̤ˤϡ��︳ʪ������Ϳ�˵��������ȿ��ꤵ����Ѳ���ǧ����ʤ��ä���
(7) ���㤪���������Τ������ȿ���Ū�긫
�оȷ���50 mg/kg��Ϳ��������ˤĤ��ƴѻ�������̡��︳ʪ���αƶ�������۾�긫�ϡ����������ˤ�ߤ��ʤ��ä���



50 mg/kg��Ϳ���ˤ�����1�㤬��ǥ��23���˻���2ɤ���ڽФ����ޤ�ʬ������ǻ�˴����������λ�˴ľ���ΰ��̾��֤��뤤��ʬ�ھ��֤ϴѻ��Ǥ��ʤ��ä�������ɽ�˰۾�Ϥߤ�줺���ޤ���˴�����ޤǤΰ��̾��֤ˤ�ʤ���Ѳ��Ϥߤ��ʤ��ä���˶���ˤ����Ƥϡ��������ֿ������٤�������Ѳ���Ʊ�ձ������ֿ���������ʪ��˳�����ò��ɡ�IJ��������ᤪ���磤ΰſ�����������Ǵ������礪�����।��ߤ�줿�������������Ǥ��ʤ��ä����ʤ�������β��ο�������徲���ϤȤ�˱�¦12����¦6�Ǥ��ꡢ˶���ˤ����Ʊ��ҵܳ����12ɤ�����ҵܳ����4ɤ�������ۻ����ǧ������
(2) ���̾���
50 mg/kg��Ϳ����1���ǥ�����֤θ�Ⱦ����ü����ɽ���������ߤ�줿¾�ˤϡ�������λ�ˤ��︳ʪ����Ϳ�˵��������ȿ��ꤵ����Ѳ��Ϥߤ��ʤ��ä���
(3) �νš�Table 4��
50 mg/kg��Ϳ�����νŤϡ���Ϳ���ϸ��Ӥ������ͤ˿�ܤ���������������������ǥ�������椪���ʬ�ڸ�Τ������¬������ˤ����Ƥ⡢����νŤ���������̤ˤϡ��оȷ��ȳ��︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
(4) �ݱ��̡�Table 5��
�������ˤ�����50 mg/kg��Ϳ������Ϳ��1�����ݱ��̤�ͭ�դ����ͤ�����ǥ�������椪���ʬ�ڸ���ݱ��̤ˤ��оȷ��ȳ��︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
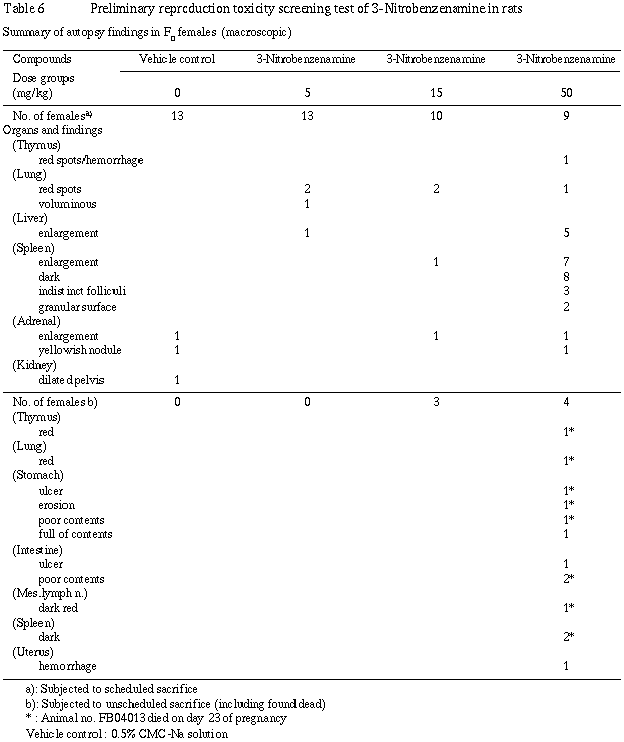
(5) ˶���긫��Table 6��
���λ����Ӯ��4����˶��������Ǥ�50 mg/kg��Ϳ����9����8�㤪���15 mg/kg��Ϳ����10����1�㡢��ǥ�����������˴�λ�ˤ����Ƥ�50 mg/kg��Ϳ����������˴��3����1���磤μ��礢�뤤�ϰſ������ߤ�줿���ޤ���Ӯ��4����˶��������ˤ�����50 mg/kg��Ϳ����9����5�㤪���5 mg/kg��Ϳ����13����1��˴Τμ��礬�ߤ�줿����Ʊ�ͤ��Ѳ���15 mg/kg��Ϳ���λ�Ǥ�ǧ����ʤ��ä������Τۤ��ˤϡ��︳ʪ����Ϳ�˵�������ȿ��ꤵ����Ѳ��Ϥߤ��ʤ��ä���
(6) ����������ȿ���Ū�긫
50 mg/kg��Ϳ���λ�˴��1�㡢������˴��3�㤪���15 mg/kg��Ϳ������ǥ��1�㡢������˴��2��ˤĤ��ƴѻ�������̡��︳ʪ���αƶ�������۾�긫�Ϥ��������ˤ�ߤ��ʤ��ä���


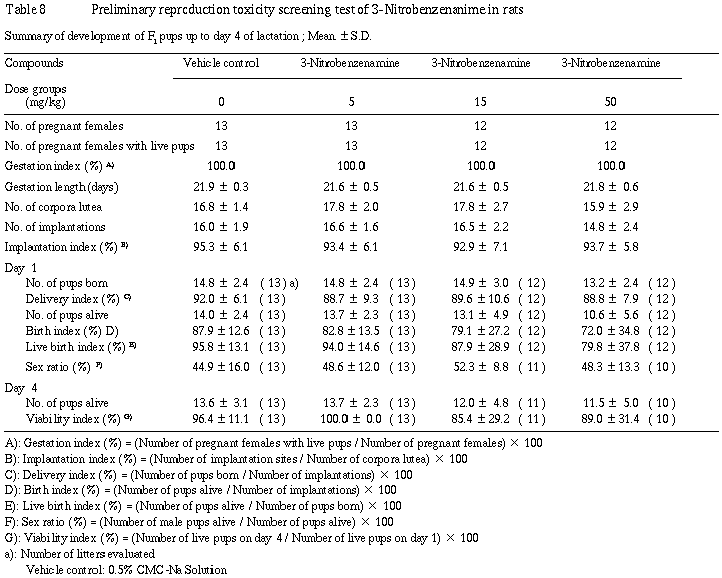

15�����50 mg/kg��Ϳ���Ǥϡ�Ӯ��1����������˴�����줾��1�����2��¸�ߤ������Ȥˤ�ꡢ���λ���Ψ����ӽ���Ψ�����ͤ�������ͭ�դ��Ѳ��ǤϤʤ��ä���Ӯ��1���λ�����������������¸Ψ�ʤ�Ӥ�Ӯ��4�����������������¸Ψ�ˤ��оȷ����︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
2) �νš�Table 9��
���������νŤˤϡ�Ӯ��1�����4���Τ�����ˤ����Ƥ��ͺ�Ȥ���оȷ����︳ʪ����Ϳ���Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
3) ˶���긫��Ӯ��4����
a. ��ɽ�긫
�оȷ��ν�����1��˺��ꤪ�������»���ߤ�줿¾�ˤϡ�������ν������ˤ����Ƥ⳰ɽ�۾�ϴѻ�����ʤ��ä����ʤ����������γ�ɽ�ѻ��ˤ����Ƥ�Ʊ�ͤν긫������줿�ۤ��ˤϰ۾��ǧ����ʤ��ä���
b. ��¡�긫
��¡�۾�ˤĤ��Ƥϡ�5 mg/kg��Ϳ���ν�����1��˲�����إ�˥������ޤ�����¡�ѰۤˤĤ��Ƥϡ��оȷ���1��˿�ⳳ�ĥ���ߤ�줿����15�����50 mg/kg��Ϳ���ν������ˤϡ���¡�۾�ѰۤȤ��ǧ����ʤ��ä���
c. ���ʽ긫
���ʰ۾�Ȥ��Ƥϡ�50 mg/kg��Ϳ����2��˶���ʬ�����硢�оȷ���1��ʳ�ɽ�۾���Ρˤ��硦���Ƿ�»��1���Ͼ����»��1��˶������Ρ��ǵݷ�»���ߤ�줿�������ѰۤˤĤ��Ƥϡ���Ͼ�������ǿ��Ѱۡ���Ͼ����50 mg/kg��Ϳ�����оȷ��ǡ���궻��ʬ��оȷ��ǡ�13Ͼ��û����50 mg/kg��Ϳ���Ǥ��줾����Ψ�˴ѻ����줿�������������ʰ۾浪����ѰۤȤ��ȯ�����٤ˤϡ��оȷ���50 mg/kg��Ϳ���Ȥδ֤�ͭ�պ���ǧ���줺���ޤ�������η��ΰ۾濫�뤤���Ѱۤ���50 mg/kg��Ϳ���ˤ��������ä��뷹����ǧ����ʤ��ä���
4) ��˴����˶���긫
�����ѰۤȤ��Ʒ�Ͼ��������٥뷿�������Τ���ӹ��ǿ��Ѱۤ����︳ʪ����Ϳ���˻������줿¾�ˤϡ����������Ϳ���λ�˴���ˤ����Ƥ⳰ɽ�۾��¡�۾��¡�Ѱۤ���ӹ��ʰ۾��ǧ����ʤ��ä���
Ϳ���ˤ����Ƥ⤽�ν�������ȯ����ȯ�餪�����¸�����Ѳ��Ϥߤ�줺�����ʤ��Ȥ�3�ݥ˥ȥ��٥ʥߥ��50 mg/kg�ʲ����̤ˤϼ���������Ф���ľ��Ū��������ǧ����ʤ��ä����ޤ����������η��֤ˤĤ��Ƥ⡢��˴����ޤ���︳ʪ����Ϳ�˵��������ȹͤ�����۾�Ϥߤ��ʤ��ä����Ȥ���Ŵ�����Ѥ�ǧ����ʤ��ä����ʤ����ܲ���ʪ�ˤĤ��Ƥ�ͺ��åȤ��Ф��������������Τ��Ƥ��ꡢͽ����ˤ����Ƥ�50 mg/kg��2���֤���Ϳ��5����1������㤪���������Τΰ�̤�ȯ�����������������ܻ�ˤ����Ƥϻ�ͺ��åȤθ�������Ӽ���ǽ�ϤˤϤʤ��ƶ��Ϥߤ�줺�����㤪���������Τ������ȿ���Ū�����ˤ����Ƥ�۾��ǧ����ʤ��ä������äơ�50 mg/kg�ϡ�����������ȯ���˴ؤ����׳��̤˶��ܤ����̤Ȥ�ͤ����롣�ܼ¸���ﲼ�Ǥϡ���ͺ��åȤ��Ф���ȿ����Ϳ�����˴ؤ���̵�ƶ��̤���ӻ��åȤ�����ǽ�Ϥ��Ф���̵�ƶ��̤�5mg/kg��ͺ��åȤ�����ǽ�Ϥ��Ф���̵�ƶ��̤���Ӽ���������Ф���̵�ƶ��̤�50 mg/kg��Ƚ�Ǥ���롣
| 1) | �������֡�¾, ���ܽ�, p. 147. |
| 2) | �Ϲ羼����¾������²�����˧��²�˥ȥ�����ʪ���Ѱ۸����ݹ��Ⱥ�������Ӥ��δ�Ϣʪ�������Ȱ�ء�29��34-54 (1987). |
| 3) | E. Salewski, Naunyn-Schmiedeberg's Arch. Exp.Pathol. Pharmakol. , 247, 367 (1964). |
| 4) | A. B. Dawson, Stain Technol. , 1, 123 (1926). |
| Ϣ���衧 | |||
| ���Ǥ�� | ��ë���� | ||
| �ʺ�˿������ʰ������������� | |||
| ��257 ������������� 729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence: | |||
| Mizutani, Masahiro | |||
| Hatano Research Institute, Food and Drug Safety Center | |||
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257, Japan | |||
| Tel 81-463-82-4751 | Fax 81-463-82-9627 | ||