テトラヒドロフルフリルアルコールのラットを用いる
経口投与簡易生殖毒性試験
Preliminary Reproduction Toxicity Screening Test of
Tetrahydrofurfuryl alcohol by Oral Administration in Rats
要約
テトラヒドロフルフリルアルコールは,溶剤,可塑剤,防かび剤,リジンの中間体,樹脂改質剤,塗料,ジヒドロピラン原料,合成医薬品中間体原料等に広く用いられている化学物質である.本物質の毒性について,ラット経口投与におけるLD50値は1.6〜3.2 g/kgで,皮膚や粘膜に対して刺激性を有する1)ことが知られている.また,ラットへの90日間混餌投与により精巣に対する毒性影響が認められている2)が,生殖発生毒性について詳細に検討した報告はみられない.
今回,テトラヒドロフルフリルアルコールについて,経口投与簡易生殖毒性試験を,SD系〔Crj:CD(SD)〕ラットを用い,0,15,50,150および500 mg/kg/day用量で実施した.動物は1群雌雄各12匹とし,被験物質は交配開始14日前から雄は47日間,雌は分娩後哺育4日(42〜52日間)まで投与した.
1. 反復投与毒性
150および500 mg/kg群で,雌雄に自発運動亢進あるいは亢進に続く自発運動低下並びに体重増加の抑制および摂餌量の減少が用量依存的に認められた.器官重量では,150 mg/kg群で雌に腎臓の相対重量の増加,500 mg/kg群で雄に胸腺,精巣および精巣上体の絶対重量および相対重量に共通した減少が認められた.剖検では,500 mg/kg群で雌雄に胸腺並びに雄に精巣および精巣上体の小型化の発現率の増加,また,150および500 mg/kg群で雌雄に脾臓の表面粗造および白色斑/域が認められ,一部の脾臓は周辺の器官・組織との癒着も認められた.病理組織学検査では,500 mg/kg群で雌雄に胸腺の萎縮,雄に精巣の精細管萎縮および間質細胞過形成,精巣上体の精巣上体管内精子減少および細胞崩壊物,また脾臓には150および500 mg/kg群の雌雄に被膜の炎症,500 mg/kg群の雌雄に髄外造血低減による赤脾髄の萎縮が認められた.
以上の結果から,テトラヒドロフルフリルアルコールのラットへの反復投与により主に胸腺,脾臓,精巣および精巣上体に対する毒性影響が認められ,無影響量は雌雄ともに50 mg/kg/dayと結論された.
2. 生殖発生毒性
親動物の生殖能に対して,雄親では,上述のように精巣および精巣上体に被験物質投与の影響が認められた.
雌親では,150 mg/kg群で性周期の延長傾向,妊娠期間の延長および出産率の低下が認められ,分娩後は哺育行動をとらない例が半数以上認められた.500 mg/kg群では,性周期の延長が認められ,全例で分娩が認められなかった.分娩の認められなかった例の子宮には,初期吸収胚が確認された.
児動物の発生に対しては,150 mg/kg群で総出産児数,分娩率,新生児数および出生率の顕著な減少が認められた.また,出生児は哺育0日の時点で半数以上が死亡し,哺育4日までの生存児は一腹からの4匹のみでいずれも低体重を示した.500 mg/kg群では,分娩は認められず,すべての母動物において剖検時に胚(胎芽)死亡が認められた.
以上の結果より,雄親動物の生殖能に対する無影響量は,150 mg/kg/day,雌親動物の生殖能および児動物の発生に対する無影響量はいずれも50 mg/kg/dayと結論された.
方法
1. 被験物質
テトラヒドロフルフリルアルコールは,水に可溶な無色透明の液体である.試験には,高圧化学工業(大阪)製造のもの(ロット番号2002-4,純度99.5 %,不純物として5-メチルテトラヒドロフルフリルアルコール0.34 %を含む)を入手し,冷暗所(4℃),密栓下で保管し,使用した.被験物質の投与液は,局方精製水〔共栄製薬 〕を溶媒として,所定の投与用量となる濃度の水溶液に調製し,使用時まで冷暗所(4 ℃)で密栓保管し,調製後7日間以内に使用した.被験物質の保管条件および投与形態での被験物質は安定であることを確認した.
〕を溶媒として,所定の投与用量となる濃度の水溶液に調製し,使用時まで冷暗所(4 ℃)で密栓保管し,調製後7日間以内に使用した.被験物質の保管条件および投与形態での被験物質は安定であることを確認した.
2. 供試動物および飼育条件
日本チャールス・リバーより搬入したSD系〔Crj:CD(SD)IGS〕ラットを13日間馴化・検疫飼育し,その間に雌については膣垢検査による性周期の確認も行い,異常の認められない動物を1群雌雄各12匹とし,10週齢(雄364〜431 g,雌208〜275 g)で試験に供した.ラットは温度21.9〜22.4℃,湿度49〜57 %,換気回数10回以上/時,照明12時間(午前7〜午後7時)に制御した飼育室で,金網ケージに個体別に収容し,固型飼料〔ラボMRストック,日本農産工業〕および水を自由に摂取させた.ただし,交尾確認後の雌は,巣作り材料〔ホワイトフレーク,日本チャールス・リバー〕を入れたポリカーボネート製ケージに収容した.
3. 投与量および投与方法
単回経口投与における致死量は,2000 mg/kg以上であった.5週齢のラットを用い,50,100,200,500および1000 mg/kg/dayで14日間反復経口投与した投与量設定試験においては,100 mg/kg群で,自発運動の亢進が認められたが,雌1匹のみの変化であった.200 mg/kg群では雌に自発運動の亢進並びに胸腺および下垂体の絶対および相対重量のいずれも低値が認められた.500 mg/kg群では雌雄に自発運動の亢進および低下,摂餌量の低値並びに盲腸の拡張,雄に立毛例および体重増加の抑制傾向,雌に胸腺および下垂体の絶対および相対重量のいずれも低値が認められた.1000 mg/kg群では,500 mg/kg群で認められた変化に加えて,雌に立毛例並びに胸腺の絶対および相対重量の低値が認められた.
また,0,10,150および600 mg/kg/dayで実施中であった本物質の28日間反復投与毒性試験においても,150 mg/kg群で雄に体重増加抑制傾向,600 mg/kg群で雌雄に自発運動の亢進および低下,雄に有意かつ,明らかな体重増加抑制および摂餌量の減少,雌に投与初期における体重増加抑制傾向および摂餌量の減少傾向が認められた.
以上のことから, 本試験における投与量は,500 mg/ kg/dayを最高用量とし,以下150,50および15 mg/kgの4用量を設定した.投与方法は,投与液量を体重100 g当たり0.5 mLとし,テフロン製胃ゾンデを装着した注射筒を用いて1日1回,交配開始14日前から雄は剖検前日までの47日間,雌は分娩後の哺育4日(42〜52日間)まで,経口投与した.対照群には,被験物質の溶媒として用いた局方精製水を同様に投与した.
4. 観察および検査
1) 親動物に関する項目
(1) 一般状態観察
投与期間中毎日,動物の生死,外観,行動等について観察した.
(2) 体重および摂餌量測定
体重の測定は, 投与開始日(投与開始直前)およびその後は7日間隔で行い,さらに最終投与日と屠殺日に測定した.ただし,雌の妊娠後は,妊娠0,7,14および20日と哺育0および4日に測定した.摂餌量は,体重測定日に合わせて翌日までの24時間の飼料消費量を測定した.雌の哺育4日の摂餌量は,前日からの24時間消費量を測定した.
(3) 性周期検査
雌について,馴化・検疫期間に引き続き,交尾が確認されるまで,Giemsa染色による膣垢塗抹標本を作製し,鏡検により性周期段階の判定を行った.平均性周期は,角化細胞のみが散在または集塊状にみられる発情後期 が回帰する日数の平均値とした.
が回帰する日数の平均値とした.
(4) 交配および分娩状態観察
投与15日の午後に,雄のケージに同一群内の雌を入れ(1対1),交尾が確認されるまで14日間を限度として連続同居させた.交尾の確認は毎朝一定時刻(9:30分頃)に行い,膣栓形成あるいは膣垢中に精子が確認された日を妊娠0日とした.分娩状態の観察も同じ時刻に行い,1腹ごとに分娩の終了が確認された日を哺育0日とした.交配および分娩の観察結果から,各群について交尾率〔(交尾成立動物数/同居動物数)×100〕,受胎率〔(受胎雌数/交尾成立雌数)×100〕および出産率〔(生児出産雌数/生存受胎雌数)×100〕ならびに分娩が確認された例について妊娠期間(妊娠0日から分娩が確認された日までの日数)を算定した.
(5) 病理学検査
雄は投与47日の翌日に,雌は計画殺動物では哺育5日に,15 mg/kg群で1匹認められた交尾しなかった雌については交配期間終了後24日に,150 mg/kg群で認められた12匹中8匹の全胎児死亡例は,全児死亡が確認された後4日以内に,また,分娩予定日を過ぎても分娩が認められなかった150 mg/kg群の2例および500 mg/kg群の全例は,分娩予定の4日後まで観察を続け翌日に,それぞれエーテル麻酔下で放血屠殺して剖検した.また,下垂体,胸腺および腎臓並びに雄の精巣,精巣上体を秤量(絶対重量)し,対体重比(相対重量)を算出した. 雌については,卵巣の黄体数および子宮の着床数を調べ,着床率〔(着床痕数/黄体数)×100〕を算定した.病理組織学検査は,採取した器官を10 %中性リン酸緩衝ホルマリン液(精巣および精巣上体のみブアン液)で固定後, 対照群および500 mg/kg群の下垂体,胸腺,精巣,精巣上体,卵巣および肉眼的に異常の認められた脾臓を検査した.脾臓については,投与開始時に完全無作為抽出法により選択した5匹および500 mg/kg群では肉眼的異常が認められた個体を含む12匹について検査した.その結果,精巣,精巣上体,胸腺および脾臓に投与に起因する変化が認められたので,15,50および150 mg/kg群では,これらの器官について検査した.検査対象動物については,投与開始時に完全無作為抽出法により選択した5匹とした.さらに,交尾が認められなかった対で交配後死亡した15 mg/kg群の雄の1匹については,精巣,精巣上体,下垂体,胸腺,脳,脊髄,胃,腸(パイヤー板を含む),副腎,脾臓,心臓,肝臓,腎臓,甲状腺(上皮小体を含む),気管,肺,膀胱,坐骨神経,骨髄およびリンパ節(頸部リンパ節,腸間膜リンパ節)を,その対の雌については卵巣,子宮および下垂体を検査した.15および150 mg/kg群で認められた非妊娠のつがいの雄は,精巣,精巣上体,前立腺,精嚢および下垂体を,雌は卵巣,子宮および下垂体を検査した.妊娠はしたものの分娩が認められなかった雌は,卵巣,子宮および下垂体を,さらに,分娩は認められたが哺育期間中に全児死亡が認められた雌については乳腺も検査した.検査は常法に従ってパラフィン切片を作製し,H-E染色を施して鏡検した.
2) 新生児に関する項目
(1) 産児数,性比および外表異常の観察
分娩完了の確認後,各腹の産児数(生産児と死亡児の合計)を調べ,分娩率〔(総出産児数/着床数)×100〕を算定した.また,肛門と生殖突起の長短により雌雄を判別し, 群ごとの性比を算出した.新生児については,口腔内を含む外表の異常を観察した.
(2) 一般状態観察
毎日一般状態および生死を確認し,出生率〔(出産確認時生児数/総出産児数)×100〕および新生児生存率〔(哺育4日生児数/出産確認時生児数)×100〕を求めた.
(3) 体重測定
新生児について哺育0日および4日に雌雄別に各腹ごとの総体重を測定し,1匹当たりの平均体重を算出した.
(4) 病理学検査
死亡例はその都度,生存例は哺育4日にエーテル麻酔下で放血死させ,胸腹部における主要器官を肉眼的に観察した.
5. 統計処理
パラメトリックデータは,Bartlettの分散検定を行い, 分散が一様な場合は一元配置の分散分析を行った.分散が一様でない場合およびノンパラメトリックデータは,Kruskal-Wallisの順位検定を行った.それらの結果,有意差を認めた場合,パラメトリック型またはノンパラメトリック型のDunnett法またはSheff 法(群の大きさが異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータは,生殖発生毒性に関するパラメータはχ2検定を,病理学的検査における異常例の出現率にはFisherの直接確率法を用いた.なお,新生児に関するデータは,1腹当たりの平均を1標本とした.
法(群の大きさが異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータは,生殖発生毒性に関するパラメータはχ2検定を,病理学的検査における異常例の出現率にはFisherの直接確率法を用いた.なお,新生児に関するデータは,1腹当たりの平均を1標本とした.
結果
1. 反復投与毒性
1) 一般状態および死亡
対照群並びに15および50 mg/kg群では,一般状態に変化は認められなかった.150 mg/kg群では,雌雄に投与後 5〜15分頃から軽度の自発運動の亢進が認められた.自発運動亢進に続いて,特に雄で,軽度の自発運動低下を呈するものが投与期間の前半に散見された.500 mg/kg群では,軽度の自発運動亢進およびそれに続く自発運動低下が投与期間を通じて認められるものが多く,雄は雌に比べて自発運動低下を示す頻度が多い傾向にあった.雌では妊娠後期において,500 mg/kg群の2匹に軽度の膣出血が認められた.15 mg/kg群で認められた交尾不成立の対の雄は,投与20日より中等度の自発運動低下が認められ,投与22日に死亡した.
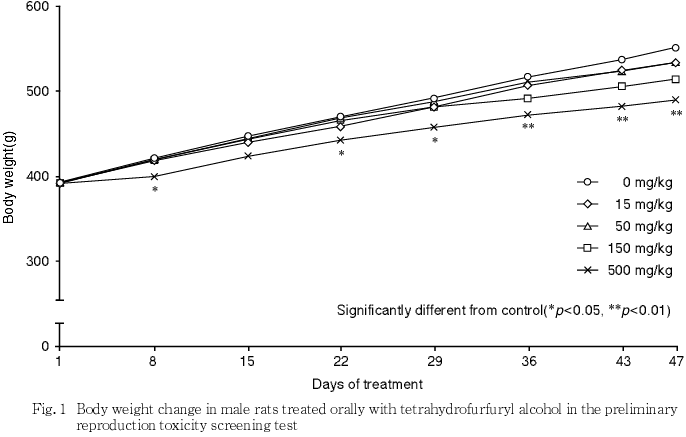
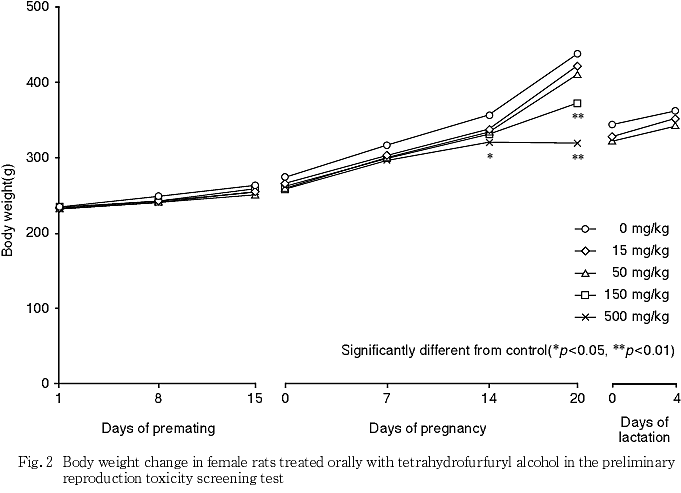
2) 体重(Fig.1,2)
15および50 mg/kg群では,雌雄ともに体重および体重増加量に対照群と比べて有意差は認められなかった.150 mg/kg群では,雄で投与36日以降,有意差はないものの体重増加の抑制傾向がみられ,投与期間中の体重増加量の有意な減少を認めた.雌では,妊娠20日の体重が対照群と比べ有意な低値を示し,妊娠期間中の体重増加量は有意に減少した.500 mg/kg群においては,雄で投与8日より有意な体重増加の抑制および投与期間中の体重増加量の有意な減少が認められた.雌では妊娠14日より有意な体重増加抑制および妊娠期間中の体重増加量の有意な減少が認められた.
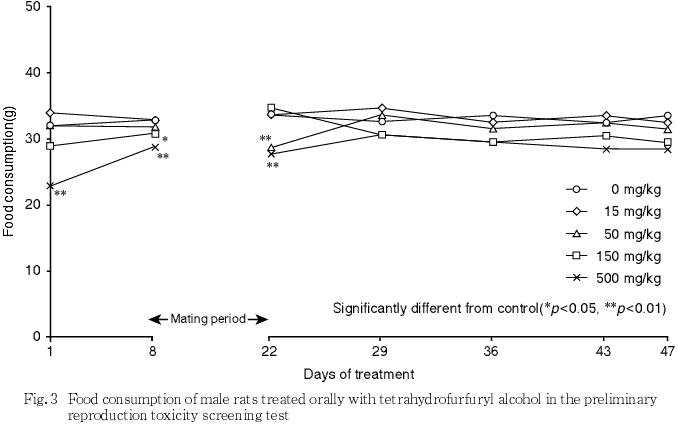
3) 摂餌量(Fig.3, 4)
15 mg/kg群では,雌雄ともに試験期間中を通して摂餌量に有意な変化は認められなかった.50 mg/kg群では,雄の投与22日の摂餌量にのみ対照群と比べて有意な減少が認められた.150 mg/kg群では,雄で投与8日,雌で妊娠14および20日の摂餌量に有意な減少が認められた.500 mg/kg群では,雄で投与1,8および22日,雌で投与1日,妊娠0,14および20日の摂餌量に有意な減少が認められた.

4) 剖検
計画屠殺の雄において,精巣および精巣上体の小型化が対照群で1匹,15 mg/kg群で1匹および150 mg/kg群で1匹に認められたのに対して,500 mg/kg群では10匹と,発現率の有意な増加が認められた.15および150 mg/kg群で精巣および精巣上体の小型化が認められた例は,いずれも妊娠を成立させなかった例であった.また,脾臓の表面粗造および白色斑/域が認められ,発現率は表面粗造が500 mg/kg群で6匹,白色斑/域が150 mg/kg群で1匹および500 mg/kg群で4匹で,500 mg/kg群の表面粗造および白色斑/域の発現率は有意なものであった.15 mg/kg群で交尾せず,その後死亡した雄では,肺の暗赤色化,心臓の灰白点,脾臓および胸腺の小型化が認められた.
計画屠殺の雌において,胸腺の小型化が対照群の1匹および50 mg/kg群の1匹,胸腺の赤色斑が 15 mg/kg群の1匹に認められた以外,変化は認められなかった.15 mg/kg群の1匹の交配不成立例,15 mg/kg群の1匹および150 mg/kg群の1匹の妊娠不成立例では,変化は認められなかった.150 mg/kg群の分娩後全児死亡の8匹では,胸腺の萎縮が1匹,脾臓の表面粗造が2匹に認められた.150 mg/kg群の2匹および500 mg/kg群の12匹の全胎児死亡例では,150 mg/kg群の1匹の子宮に米粒大あるいはそれより小さな初期吸収胚および胎児のミイラ変性が認められ,500 mg/kg群を含むその他の全例の子宮には初期吸収胚が確認された.また,500 mg/kg群では胸腺の小型化が5匹に認められた.また,脾臓の表面粗造が11匹および白色斑/域が5匹に認められ,うち2匹は周辺脂肪組織あるいは膵臓との癒着を伴っていた.脾臓の表面粗造および白色斑/域の発現率には有意差が認められた.
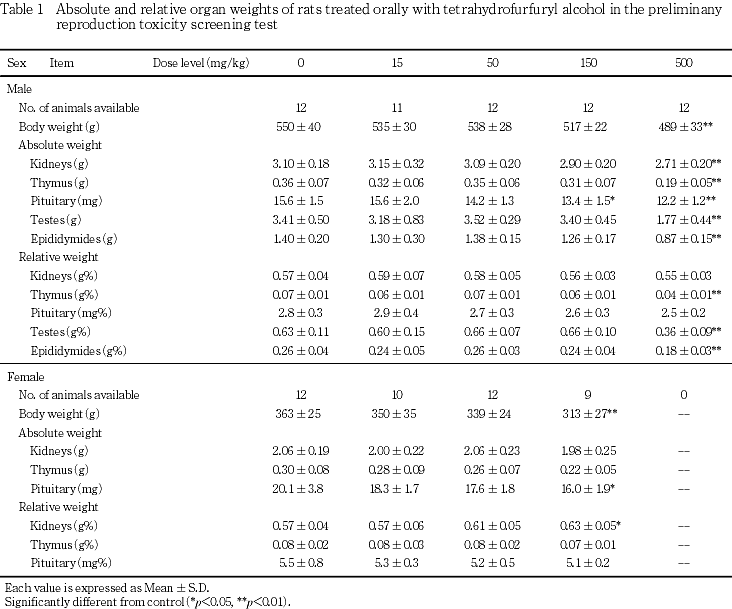
5) 器官重量(Table 1)
15および50 mg/kg群では,最終体重および秤量器官の重量に有意な変化は認められなかった.150 mg/kg群では,最終体重は雄で減少傾向,雌で有意な減少が認められ,雌雄の下垂体の絶対重量に有意な減少が認められたが,相対重量には有意な変化は認められなかった.雌の腎臓は絶対重量でやや減少する傾向にあり,相対重量では有意な増加を示した.500 mg/kg群では,雄で最終体重の有意な減少が認められ,雄の胸腺,精巣および精巣上体は,絶対および相対重量に共通して有意な減少を示した.腎臓および下垂体の絶対重量にも有意な低下が認められたが,相対重量には有意な変化は認められなかった.
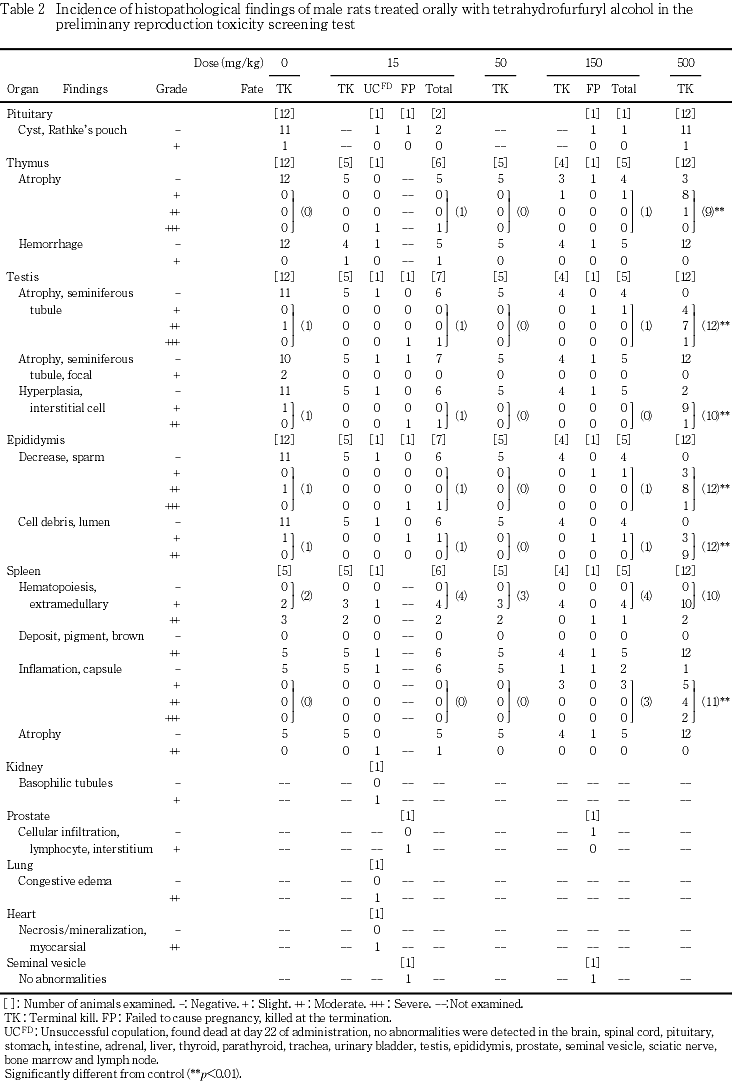
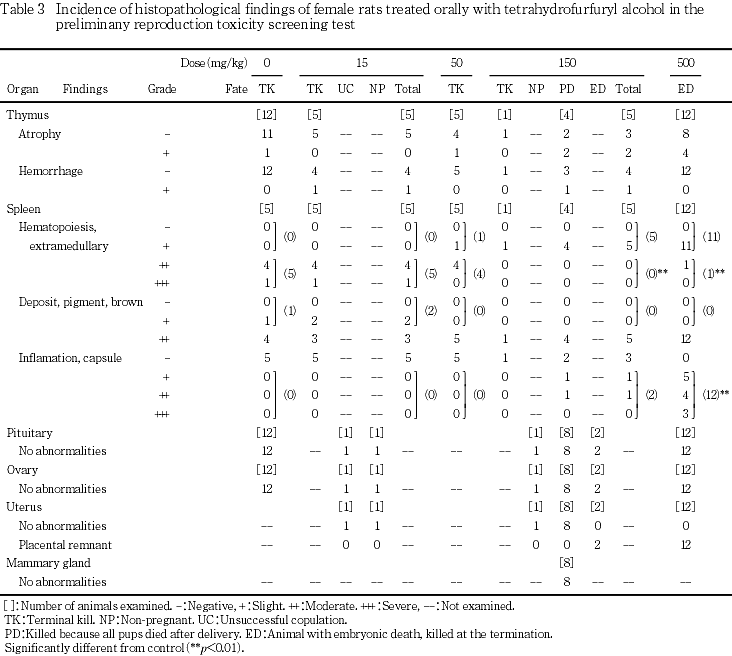
6) 病理組織学検査(Tables 2,3)
被験物質の投与に起因する変化が,精巣,精巣上体,胸腺および脾臓に認められた.
(1) 生殖器系以外の器官
胸腺の萎縮は対照群においても雌の1匹に認められたが,150 mg/kg群の雌および500 mg/kg群での雄雌では発現率の増加傾向がみられ,500 mg/kg の雄の発現率には有意差が認められた.脾臓において,150および500 mg/kg群の雄雌の赤脾髄の髄外造血の程度は低下傾向にあり,150および500 mg/kg群の雌では有意差が認められ,赤脾髄の萎縮が示唆された.また,脾臓に被膜の細胞浸潤/線維化等の炎症が 150 mg/kg群の雄の5匹中3匹および雌の5匹中2匹,500 mg/kg群の雄の12匹中11匹および雌の12匹中12匹に認められた.15 mg/kg群で認められた死亡例では,心臓の心筋壊死・鉱質沈着,肺のうっ血性水腫,胸腺および脾臓の萎縮,腎臓の好塩基性尿細管が認められ,心臓の心筋壊死・鉱質沈着および肺のうっ血性水腫が主な死因と推定された.以上の変化に加えて,被験物質の投与とは無関係に下垂体のラトケ嚢,胸腺の出血,脾臓の褐色色素沈着が認められた.分娩後全児死亡の雌の乳腺に,変化は認められなかった.
(2) 生殖器系器官
妊娠の成立した雄において,精巣の精細管萎縮が500 mg/kg群の12匹全例に認められ,10匹では間質細胞の過形成を伴っていた.これらの例では精細管内精子形成の低減が認められ,変化の強い部位ではセルトリ細胞を残して生殖細胞は消失していた.精細管萎縮は対照群の3匹(限局性変化の2匹を含む)にも認められ,1匹は間質細胞の過形成を伴っていた.対照群の例を含むこれら精細管萎縮の認められた動物の精巣上体には,精巣上体管内精子の減少および細胞崩壊物が認められた.妊娠の成立しなかった15 mg/kg群の1匹および150 mg/kg群の1匹にも,精巣の精細管萎縮および間質細胞の過形成並びに精巣上体の精巣上体管腔内精子の減少および細胞崩壊物が認められ,150 mg/kg群の例では,さらに前立腺の間質細胞浸潤も認められた.
雌において,全胎児死亡の150 mg/kg群の2匹および500 mg/kg群の12匹全例に,子宮の胎盤遺残が確認された.卵巣には変化が認められなかった.
2. 生殖発生毒性
1) 親動物に及ぼす影響(Table 4)
(1) 性周期検査
群分け時から交配前までにおいて,対照群では,概ね4日の性周期を示したが,6日および5日を示す動物が1匹ずつ認められたため,平均性周期は4.3日であった.これに対し,15および50 mg/kg群では,概ね4日周期を示し,平均性周期はそれぞれ4.0および4.1日であった.150 mg/kg 以上の群では,対照群と比べて性周期の延長傾向が認められ,5日以上の性周期を示す個体が150 mg/kg群で4匹,500 mg/kg群では7匹認められ,150 mg/kg群では4.5日の平均性周期を示し,500 mg/kg群では平均性周期は4.8日と対照群と比べて有意に長かった.また,150 mg/kg 以上の群では,発情後期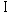 期像が2日ないし3日連続して認められる個体が散見された.
期像が2日ないし3日連続して認められる個体が散見された.
(2) 交尾率および受胎率
交尾は15 mg/kg群の1対を除いて全例に成立し,成立に要する期間にも,対照群と被験物質投与各群との間に有意な差は認められなかった.15 mg/kg群の交尾不成立のつがいの雄は,投与22日に死亡し,その後,交尾が確認された別の雄と交配を続けたが,交尾は認められなかった.受胎率は,15および150 mg/kg群で1例ずつの不妊例が認められたが,対照群と被験物質投与各群との間に有意差は認められなかった.
(3) 黄体数,着床数および着床率
被験物質投与各群の黄体数,着床数および着床率は,対照群と比べて有意差は認められなかった.
(4) 出産率および妊娠期間
出産率は,対照群,15および50 mg/kg群ではいずれも100 %であったが,150 mg/kg群では,36.4 %と有意に低下した.500 mg/kg群では,分娩は1例も認められなかった.妊娠期間については,15および50 mg/kg群では,対照群との間に有意差は認められなかった.150 mg/kg群では,妊娠期間の有意な延長が認められた.
(5) 分娩および哺育状態
対照群,15および50 mg/kg群では,分娩および哺育状態に異常は認められなかった.150 mg/kg群では,11匹中9匹に分娩が認められたが,そのうちの5匹については,夕方に分娩開始が確認されたものの,哺育行動はとらず,翌朝には全ての児が死亡または食殺された.他の4匹には哺育行動は認められたものの,ミルクスポットは小さかった.

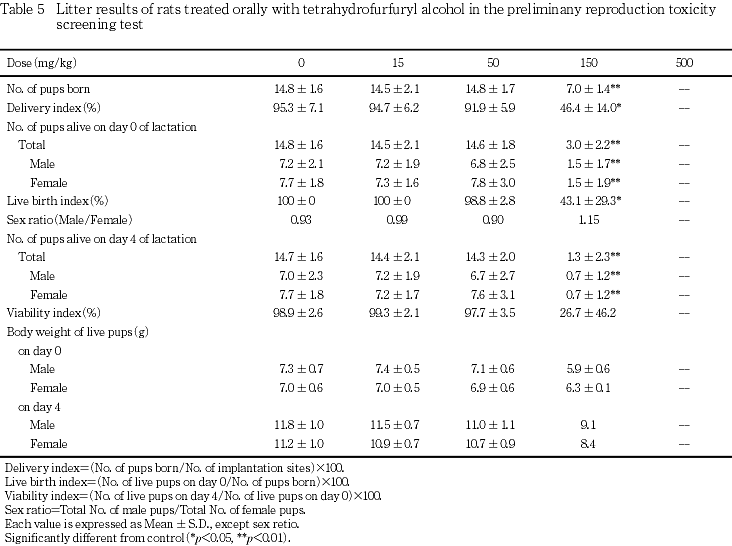
2) 新生児に及ぼす影響(Table 5)
(1) 生存性および体重
15および50 mg/kg群の1腹当たりの総出産児数,分娩率,新生児数,出生率,性比,哺育0日の体重並びに哺育4日の生存率および体重には,いずれも対照群と比べて有意差は認められず,新生児の一般状態にも異常は認められなかった.150 mg/kg群では,出産確認時に生存児を有する母動物は4匹で,1腹当たりの総出産児数,分娩率,新生児数および出生率は有意に減少した.出生児は,哺育0日に半数以上が死亡し,哺育4日までの生存児は1腹からの4匹のみであり,いずれも低体重を示した.500 mg/kg群では,分娩が認められず,新生児は得られなかった.
(2) 形態
150 mg/kg群で全身性浮腫が4腹から得られた出生児の28匹中1匹に認められた他は,いずれの群においても外表および内臓異常を有する児動物は認められなかった.内臓変異については,胸腺の頸部残留が各群に認められ,50 mg/kg群で,やや高い発現率(8.4 %)を示したものの,対照群(3.2 %)と比べて有意差は認められなかった.また,左臍動脈遺残が対照群(1.2 %)と 50 mg/kg群(2.2 %)でみられたが,その発現に有意差は認められなかった.
考察および結論
1. 反復投与毒性
投与後,自発運動亢進あるいは亢進に続く自発運動低下が150 mg/kg 以上の群の雌雄に認められ,自発運動低下は用量の増加に伴い現れやすい傾向にあった.本被験物質の基本骨格であるテトラヒドロフランには麻酔作用が報告3)されているが,これらの症状から,本被験物質も中枢神経系に対して軽度な影響を有する可能性が示唆される.また,150 mg/kg 以上の群で,雌雄に体重増加の抑制および摂餌量の減少が用量依存的に認められた.なお,50 mg/kg群の雄で投与22日の摂餌量が対照群と比べて低値を示したが,投与の経過に伴う変化傾向は認められず,体重に対する影響も伴っていないことから,被験物質の投与とは無関係な偶発的所見と判断された.
器官重量では,150 mg/kg群で雌に腎臓の相対重量増加,500 mg/kg群で雄に胸腺,精巣および精巣上体の絶対重量および相対重量の減少が認められた.剖検では,500 mg/kg群で雌雄に胸腺並びに雄に精巣および精巣上体の小型化の発現率の増加,また,150および500 mg/kg群で雌雄に脾臓の表面粗造および白色斑/域が認められ,一部の脾臓は周辺の器官・組織との癒着も認められた.
病理組織学検査では,500 mg/kg群で雌雄に胸腺の萎縮,雄に精巣の精細管萎縮および間質細胞過形成,精巣上体の精巣上体管内精子減少および細胞崩壊物,また,脾臓には150および500 mg/kg群の雌雄に被膜の炎症,500 mg/kg群の雌雄に髄外造血低減による赤脾髄の萎縮が認められた.
これらの雌雄の胸腺および脾臓並びに雄の精巣の病理組織学的変化,雌の病理組織学的変化を伴わない腎臓重量の変化は,本被験物質のラットを用いた28日間反復投与毒性においても認められており4),本試験においてもこれら器官に対する毒性影響が確認された.
投与後22日に死亡した15 mg/kgの雄については,心臓の心筋壊死・鉱質沈殿および肺のうっ血性水腫が主な死因と推定されたが,高用量群を含む他の動物にこのような死亡例はなく,被験物質投与とは関連のない偶発的なものと考えられる.また,計画屠殺の雌において,胸腺の小型化が対照群の1匹および50 mg/kg群の1匹,赤色斑が15 mg/kg の1匹に認められたが,これらはいずれも自然発生的な変化と判断される.
以上の結果から,親動物への反復投与における無影響量は,雄雌ともに50 mg/kg/dayと判断された.
2. 生殖発生毒性
親動物に対して,雄親では500 mg/kg群で精巣および精巣上体の小型化および重量減少が認められた.病理組織学検査では,精巣の間質細胞の過形成を伴う精細管萎縮および精巣上体の精巣上体管腔内の精子減少および細胞崩壊物が認められた.
本被験物質をラットへ90日間混餌投与した試験において,精巣に対する毒性影響が報告されており2),本試験においても明らかな精巣毒性が確認された.このような精巣毒性が認められたにもかかわらず,受胎に対する影響が認められなかったのは,投与開始が交配前2週間からであり,交配時点では精子が残存していたものと推察され,卵子と受精することができたものと判断された.
雌では,150 mg/kg 以上の群で性周期の延長傾向および発情後期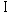 期像の延長傾向が認められ,被験物質による性周期への影響が疑われた.交尾,排卵,受精および着床の過程においては,毒性影響を示唆する変化は認められなかった.しかしながら,その後の妊娠継続に対しては,150 mg/kg群で,妊娠期間の延長および出産率の低下が認められ,500 mg/kg群では,分娩は1例も認められなかった.また,150 mg/kg群で分娩した動物においても哺育行動をとらない例が半数以上認められた.下垂体,卵巣,子宮および乳腺の組織学検査においては,特に被験物質による影響は認められなかったことから,母動物への一般毒性学的影響による二次的影響の可能性が考えられる.
期像の延長傾向が認められ,被験物質による性周期への影響が疑われた.交尾,排卵,受精および着床の過程においては,毒性影響を示唆する変化は認められなかった.しかしながら,その後の妊娠継続に対しては,150 mg/kg群で,妊娠期間の延長および出産率の低下が認められ,500 mg/kg群では,分娩は1例も認められなかった.また,150 mg/kg群で分娩した動物においても哺育行動をとらない例が半数以上認められた.下垂体,卵巣,子宮および乳腺の組織学検査においては,特に被験物質による影響は認められなかったことから,母動物への一般毒性学的影響による二次的影響の可能性が考えられる.
妊娠の不成立が15および500 mg/kg群に各1対認められ,これらの対の雄では,精巣の精細管萎縮および精巣上体の精巣上体管内精子の減少が認められ,これが妊娠不成立の原因であると推察された.しかしながら,妊娠不成立例の発現率には用量依存性は認められず,被験物質の投与とは無関係な所見と判断された.
また,15 mg/kg群で認められた交尾不成立例について,雌は順調な性周期を示し,剖検および組織学所見にも異常は認められなかった.交配ペアの雄の1匹は死亡例であり,心臓および肺に病理学的変化を伴って死亡していることから,これらの異常が交尾不成立と関連するものと思われた.その後に交配を継続した別の雄は,前述の精巣および精巣上体に変化が認められたものであったが,交尾経験を有する個体であり,交尾不成立の原因は不明であった.
児動物に対しては,150 mg/kg 以上の群で着床後の胚(胎芽)発育および生存性に顕著な毒性影響が認められ,150 mg/kg群では,出産確認時に生存児を有する母動物は4匹のみで,総出産児数,分娩率,新生児数および出生率は顕著に減少した.また,出生児は哺育0日の時点で半数以上が死亡し,哺育4日までの生存児は1腹からの4匹のみでいずれも低体重を示した.500 mg/kg群では,分娩は認められず,すべての母動物において剖検時に胚(胎芽)死亡が認められ,いずれも妊娠初期吸収胚と判断された.150 mg/kg群における未分娩例においても初期吸収胚または後期吸収胚が認められた.
150 mg/kg 以上の群の母動物は,妊娠中期から後期に体重および摂餌量の減少が認められており,母動物に毒性影響が認められた用量で本被験物質は発生毒性を有するものと判断され,妊娠初期から中期に胚致死作用を及ぼすものと考えられた.
出生児の形態への影響については,150 mg/kg群では,発生毒性が顕著であったため,検査例数が少なく,評価は困難であった.15および50 mg/kg群では対照群と同様,少数例の内臓変異がみられたが,いずれも自然発生的に認められる5)もので,発現率に有意差は認められず,催奇形性を示唆する変化ではないと判断された.
以上の結果から,雄親動物の生殖能に対する無影響量は150 mg/kg/day,雌親動物の生殖能および児動物の発生に対する無影響量は50 mg/kg/day と判断された.
文献
| 1) | Richardson ML, Gangolliet S:“The Dictionary of Substances and their Effects”, Vol. 7, The royal society of chemistry, England(1994)pp. 353-354. |
| 2) | TSCA Section 8, (e)Data, 8EHQ-1091-1381 A, -0692-1381B,and -0992-1381C(1992). |
| 3) | IUCLID(International Uniform Chemical Information Data Base) Data Sheet, EU(1995). |
| 4) | 伊藤義彦ら:テトラヒドロフルフリルアルコールのラットを用いる28日間反復投与毒性試験.化学物質毒性試験報告,11:162-174(2004). |
| 5) | Morita H,et al.:Spontaneous malformations in laboratory animals, Frequency of external, internal and skeletal malformations in rats, rabbits and mice. Cong Anom, 27:147-206(1987). |
| 連絡先 |
| 試験責任者: | 野田 篤 |
| 試験担当者: | 山口真樹子,伊藤雅也,杉本忠美,
昆 尚美,下平裕二,藤波志保,
伊藤義彦 |
| (財)畜産生物科学安全研究所 |
| 〒229-1132 神奈川県相模原市橋本台3-7-11 |
| Tel 042-762-2775 | Fax 042-762-7979 | |
| Correspondence |
| Authors: | Atushi Noda(Study director)
Makiko Yamaguchi, Masaya Ito,
Tadami Sugimoto, Naomi Kon,
Yuji Shimodaira, Shiho Fuzinami,
Yoshihiko Ito |
| Research Institute for Animal Science in Biochemistry and Toxicology |
| 3-7-11 Hashimotodai, Sagamihara-shi,Kanagawa, 229-1132, Japan |
| Tel +81-42-762-2775 | Fax +81-42-762-7979 | |

 〕を溶媒として,所定の投与用量となる濃度の水溶液に調製し,使用時まで冷暗所(4 ℃)で密栓保管し,調製後7日間以内に使用した.被験物質の保管条件および投与形態での被験物質は安定であることを確認した.
〕を溶媒として,所定の投与用量となる濃度の水溶液に調製し,使用時まで冷暗所(4 ℃)で密栓保管し,調製後7日間以内に使用した.被験物質の保管条件および投与形態での被験物質は安定であることを確認した.
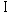 が回帰する日数の平均値とした.
が回帰する日数の平均値とした.
 法(群の大きさが異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータは,生殖発生毒性に関するパラメータはχ2検定を,病理学的検査における異常例の出現率にはFisherの直接確率法を用いた.なお,新生児に関するデータは,1腹当たりの平均を1標本とした.
法(群の大きさが異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータは,生殖発生毒性に関するパラメータはχ2検定を,病理学的検査における異常例の出現率にはFisherの直接確率法を用いた.なお,新生児に関するデータは,1腹当たりの平均を1標本とした.







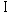 期像が2日ないし3日連続して認められる個体が散見された.
期像が2日ないし3日連続して認められる個体が散見された.


 期像の延長傾向が認められ,被験物質による性周期への影響が疑われた.交尾,排卵,受精および着床の過程においては,毒性影響を示唆する変化は認められなかった.しかしながら,その後の妊娠継続に対しては,150 mg/kg群で,妊娠期間の延長および出産率の低下が認められ,500 mg/kg群では,分娩は1例も認められなかった.また,150 mg/kg群で分娩した動物においても哺育行動をとらない例が半数以上認められた.下垂体,卵巣,子宮および乳腺の組織学検査においては,特に被験物質による影響は認められなかったことから,母動物への一般毒性学的影響による二次的影響の可能性が考えられる.
期像の延長傾向が認められ,被験物質による性周期への影響が疑われた.交尾,排卵,受精および着床の過程においては,毒性影響を示唆する変化は認められなかった.しかしながら,その後の妊娠継続に対しては,150 mg/kg群で,妊娠期間の延長および出産率の低下が認められ,500 mg/kg群では,分娩は1例も認められなかった.また,150 mg/kg群で分娩した動物においても哺育行動をとらない例が半数以上認められた.下垂体,卵巣,子宮および乳腺の組織学検査においては,特に被験物質による影響は認められなかったことから,母動物への一般毒性学的影響による二次的影響の可能性が考えられる.