120 mg/kg群の雄4/5例および雌5/5例,60 mg/kg群の雄1/5例および雌3/5例が投与後30〜45分に死亡した.一般状態では,散瞳,自発運動の低下,緩徐呼吸,振戦および腹臥位が認められた.病理学検査では,肉眼的に腺胃粘膜に軽度の暗赤色点,組織学的に腺胃粘膜固有層の軽度の出血が認められた.
生存例では,120 mg/kg群の雄1例で死亡例と同様の症状が認められた.60 mg/kg群では,雄で散瞳,自発運動の低下,緩徐呼吸および振戦がみられ,雌で散瞳および自発運動の低下が認められた.30 mg/kg群の雄では散瞳がみられ,雌では散瞳,自発運動の低下,緩徐呼吸および振戦が認められた.これらの変化は投与後1日にはすべて消失していた.体重では,60 mg/kg群の雌雄および30 mg/kg群の雌で低値傾向を示した.病理学検査では,全例で何ら変化は認められなかった.
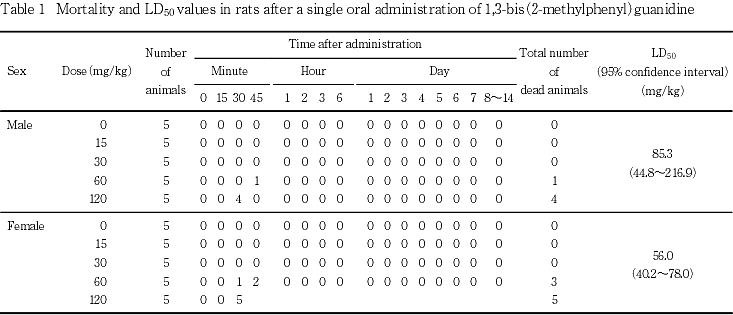
以上の結果から,1,3-ビス(2-メチルフェニル)グアニジンのLD50値(95 %信頼限界)は雄が85.3 mg/kg (44.8〜216.9 mg/kg),雌が56.0 mg/kg(40.2〜78.0 mg/kg)であった.
動物は,温度24 ± 2℃,湿度55 ± 10 %,照明12時間(午前7時〜午後7時)および換気回数13〜15回/時に設定したバリアーシステム飼育室で床敷(ホワイトフレーク,日本チャールスリバー)を入れたポリカーボネイト製ケージに1ケージ当たり2〜3匹ずつ収容して飼育した.飼料は高圧蒸気滅菌処理した固型飼料(CRF-1,オリエンタル酵母工業)を,飲水は次亜塩素酸ナトリウムを添加(約2 ppm)した井戸水を給水瓶によりそれぞれ自由に摂取させた.
投与経路は,経口とし,約18時間絶食させた動物に胃管を用いて1回強制投与した.投与容量は10 mL/kgとし,各動物の投与液量は投与日の体重を基に算出した.対照群には同容量の媒体を投与した.

生存例では,120 mg/kg群の雄1例で投与後15分より死亡例と同様の症状がみられ,投与後6時間まで認められたが,投与後1日にはすべて消失しており,その後は何ら変化は認められなかった.60 mg/kg群では,雄で投与後15分より投与後2時間まで散瞳,自発運動の低下,緩徐呼吸および振戦がみられ,雌では投与後15分より投与後1時間まで散瞳および自発運動の低下が認められた.30 mg/kg群では,雄で投与後45分より投与後1時間に散瞳がみられ,雌では投与後30分より投与後2時間まで散瞳,自発運動の低下,緩徐呼吸および振戦が認められた.15 mg/kg群および対照群の雌雄では,観察期間を通して何ら変化は認められなかった.
120 mg/kg群の雄4/5例および雌5/5例,60 mg/kg群の雄1/5例および雌3/5例が投与後30〜45分に死亡した.
死亡例では,雌雄ともに,一般状態の観察で散瞳,自発運動の低下,緩徐呼吸,振戦および腹臥位が認められた.病理学検査では,60および120 mg/kg群の雌で肉眼的に腺胃粘膜に軽度の暗赤色点,組織学的に腺胃粘膜固有層の軽度の出血が認められた.この変化は出血のみの変化で,粘膜上皮の変性や壊死を伴わないものの被験物質にわずかな刺激性があるものと考えられた.また,120 mg/kg群の雄で肉眼的に肺に軽度の暗赤色化,組織学的に軽度のうっ血が認められたが,程度が弱く,出現頻度が低いこと,かつ死亡例でしばしば認められる変化であることから,被験物質投与に起因した変化ではないと考えられた.
生存例では,120 mg/kg群の雄1例で死亡例と同様の症状がみられ,投与後6時間まで観察されたが,投与後1日にはすべて消失しており,その後は何ら変化は認められなかった. 60 mg/kg群では,雄で散瞳,自発運動の低下,緩徐呼吸および振戦がみられ,雌で散瞳および自発運動の低下が認められた.30 mg/kg群では,雄で散瞳がみられ,雌で散瞳,自発運動の低下,緩徐呼吸および振戦が認められた.また,60 mg/kgの雄および30 mg/kgの雌で投与後1日に,60 mg/kg群の雌では観察期間を通して,体重が低値傾向を示した.
以上のことから,LD50値(95 %信頼限界)は雄が85.3 mg/kg(44.8〜216.9 mg/kg),雌が56.0 mg/kg(40.2〜78.0 mg/kg)であった.
| 連絡先 | |||
| 試験責任者: | 本田久美子 | ||
| 試験担当者: | 榎嶋輝彦,浜村政夫,大西幹雄, 和泉宏幸,鍬先恵美子 | ||
| (株)パナファ−ム・ラボラトリ−ズ安全性研究部 | |||
| 〒869-0425 熊本県宇土市栗崎町1285 | |||
| Tel 0964-23-5111 | Fax 0964-23-2282 | ||
| Correspondence | ||||
| Authors: | Kumiko Honda(Study Director) Teruhiko Enoshima, Masao Hamamura, Mikio Oonishi, Hiroyuki Izumi, Emiko Kuwasaki | |||
| Safety Assessment Laboratory, Panapharm Laboratories Co., Ltd. | ||||
| 1285 Kurisaki-machi, Uto-shi, Kumamoto,869-0425, Japan | ||||
| Tel +81-964-23-5111 | Fax +81-964-23-2282 | |||