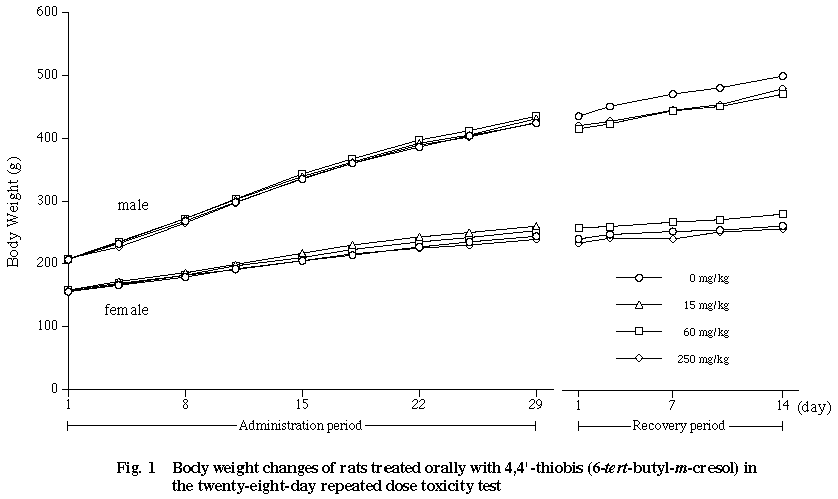
被験物質投与に起因する一般状態の変化はみられず,体重への影響もみられなかった.
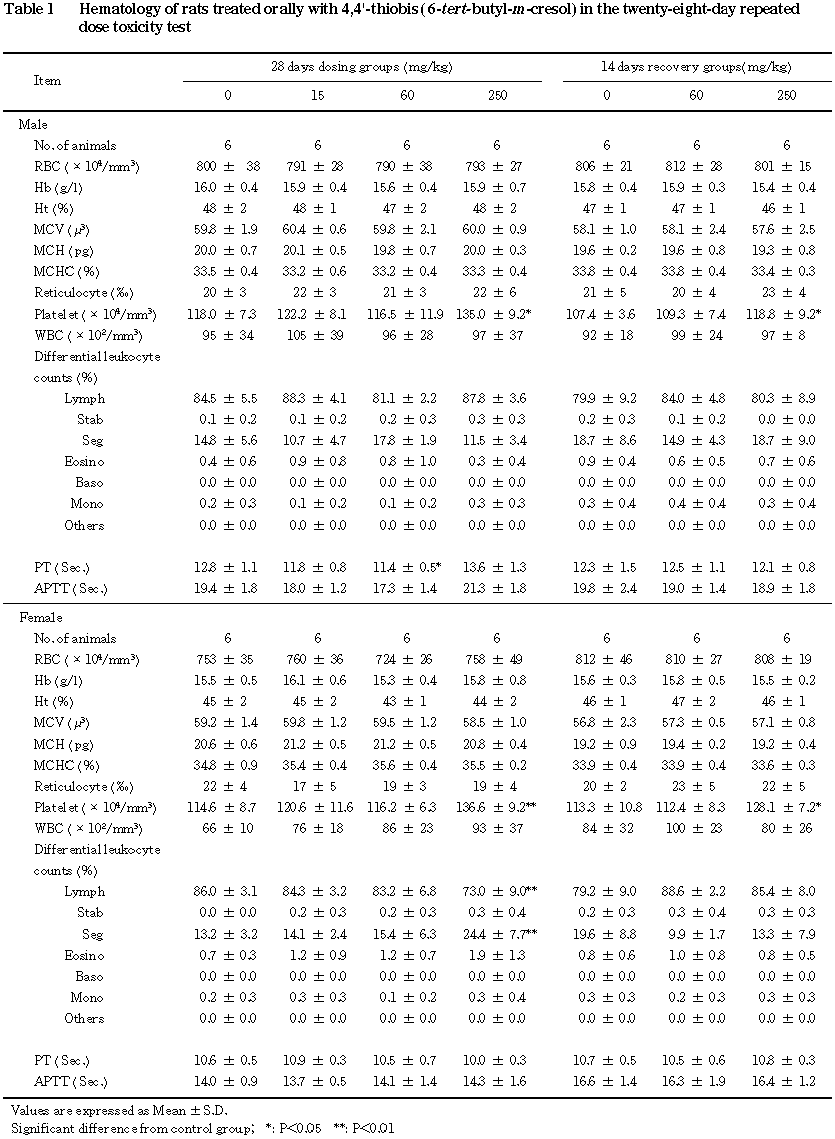
摂餌量では,投与開始初期に一時的な減少が 250 mg/kg群の雌雄でみられたが,雄ではその後対照群をやや上回って推移した.60 mg/kg群の雄の摂餌量も対照群をやや上回って推移した.尿検査では,pHの低下が60 mg/kg群の雌と250 mg/kg群の雌雄に,尿蛋白およびケトン体の増加が60および250 mg/kg群の雌に,血液学検査では,血小板数の増加が250 mg/kg群の雌雄に,分葉核好中球比率の増加およびリンパ球比率の減少が250 mg/kg群の雌に,血液生化学検査では,無機リンの増加が60 mg/kg以上の投与群の雌に,総コレステロールの増加が250 mg/kg群の雌雄に,リン脂質および尿素窒素の増加と血糖値の低下が250 mg/kg群の雌にみられた.
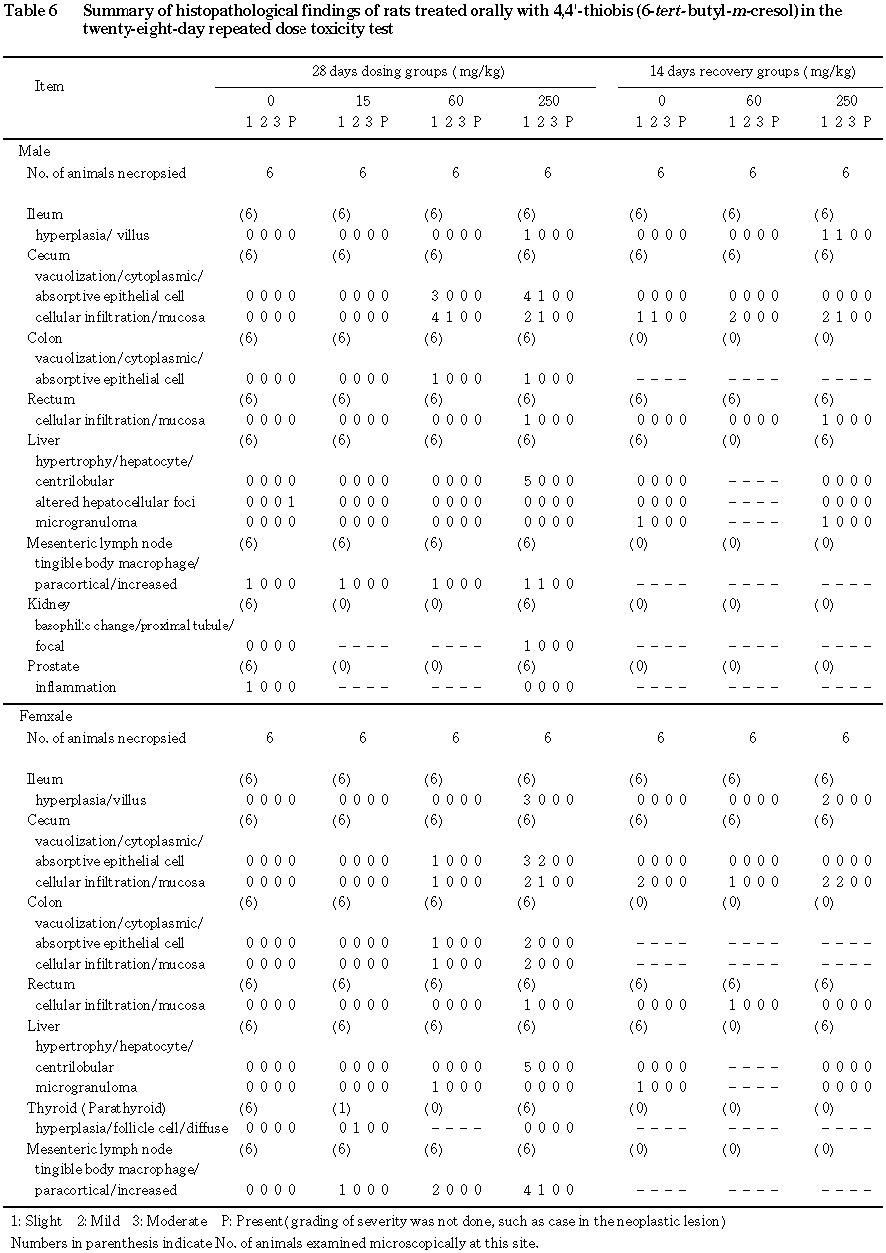
病理学検査では, 250 mg/kg群の雌雄に肝臓重量の増加,肉眼的な小腸壁の肥厚と盲腸の拡張がみられた.組織学的には,肝臓で小葉中心帯肝細胞の肥大と回腸における腸絨毛の過形成が250 mg/kg群の雌雄に,盲腸と結腸で吸収上皮細胞の空胞化が60 mg/kg以上の投与群の雌雄に,また,盲腸粘膜の細胞浸潤が60 mg/kg以上の投与群の雌雄に,結腸粘膜の細胞浸潤が60 mg/kg以上の投与群の雌にみられた.さらに,腸間膜リンパ節では,傍皮質領域における“tingible body macrophage”が250 mg/kg群の雌に多くみられた.回復群においては,回腸以外のほとんどの変化は消失した.
以上の結果から,本試験条件下における 4,4'-チオビス(6-tert-ブチル-m-クレゾール)の無影響量は雌雄とも15 mg/kg/dayと考えられた.
投与容量が 5 ml/kg体重となるよう,5%アラビアゴム水溶液に懸濁して0.3,1.2および5%(w/v)懸濁液を調製した.0.1〜5%(w/v)懸濁液は,室温で1日間および冷蔵(約4℃)・暗所(褐色ガラス瓶)で8日間まで安定であったことから,最大1週間分を一括して調製し,1日分ずつ褐色ガラス瓶に分注して冷蔵庫(約4℃)に保存した.また,投与開始前および投与終了週の2回,投与に使用する各濃度液について当施設で測定した結果,いずれも濃度は適正でかつ均一であった.
動物は,群分け当日の体重に基づいて層別化し,各群平均体重がほぼ均等となるよう,コンピュータを用いて各群に割り付けた.
動物は,温度 23±3℃,相対湿度50±20%,換気回数1時間当たり11〜13回,照明1日12時間の飼育室で,金属製網ケージに1匹ずつ収容し,固型飼料(放射線滅菌CRF-1,オリエンタル酵母工業(株))および飲料水(水道水)を自由に摂取させ飼育した.
被験液の投与容量は 5 ml/kg体重とし,金属製胃ゾンデを用いて1日1回28日間強制経口投与した.対照群には溶媒(5%アラビアゴム水溶液)を同様に投与した.投与液量は最新の体重を基準に算出した.回復期間は14日間とした.
 法),ナトリウム,カリウムおよび塩素(イオン選択電極法),カルシウム(OCPC法),無機リン(モリブデン酸法),総蛋白質(Biuret法),アルブミン(BCG法)およびA/G比(総蛋白質およびアルブミンから算出)を測定した.また,ヘパリンを加えた容器に採血し,遠心分離(3000 rpm,10分間)により得られた血漿を用いてGOT,GPT,LDH(UV-rate法),γ-GTP(γ-グルタミル-3-カルボキシ-4-ニトロアニリド法)およびChE(DTNB法)(以上いずれも自動分析装置Monarch,Instrumentation Laboratory)を測定した.
法),ナトリウム,カリウムおよび塩素(イオン選択電極法),カルシウム(OCPC法),無機リン(モリブデン酸法),総蛋白質(Biuret法),アルブミン(BCG法)およびA/G比(総蛋白質およびアルブミンから算出)を測定した.また,ヘパリンを加えた容器に採血し,遠心分離(3000 rpm,10分間)により得られた血漿を用いてGOT,GPT,LDH(UV-rate法),γ-GTP(γ-グルタミル-3-カルボキシ-4-ニトロアニリド法)およびChE(DTNB法)(以上いずれも自動分析装置Monarch,Instrumentation Laboratory)を測定した.
脳,胸腺,心臓,肺 (気管支を含む),肝臓,脾臓,腎臓,副腎,精巣,卵巣
脳 *,脊髄*,坐骨神経*,胸大動脈,心臓*,気管*,肺(気管支を含む)*,舌,食道,胃*,十二指腸*,空腸*,回腸*,盲腸*,結腸*,直腸*,唾液腺(顎下腺・舌下腺),肝臓*,膵臓*,下垂体*,甲状腺(上皮小体を含む)*,副腎*,胸腺*,脾臓*,腸間膜リンパ節*,頸部リンパ節*,腎臓*,膀胱*,精巣*,精巣上体*,精嚢,前立腺*,卵巣*,子宮*,腟*,乳腺,皮膚,眼球*,ハーダー腺,骨及び骨髄(胸骨・大腿骨)*,大腿筋,肉眼的異常部位*
 法(各群の例数が異なるとき)を用いて対照群と各投与群との平均値の差の検定を行った.分散が均一でない場合には,Kruskal-Wallisの順位検定を行い,有意であればDunnett型(各群の例数が等しいとき)またはScheff
法(各群の例数が異なるとき)を用いて対照群と各投与群との平均値の差の検定を行った.分散が均一でない場合には,Kruskal-Wallisの順位検定を行い,有意であればDunnett型(各群の例数が等しいとき)またはScheff 型(各群の例数が異なるとき)を用いて対照群と各投与群との平均順位の差の検定を行った.検定はいずれも両側で,有意水準は5および1%とした1).
型(各群の例数が異なるとき)を用いて対照群と各投与群との平均順位の差の検定を行った.検定はいずれも両側で,有意水準は5および1%とした1).

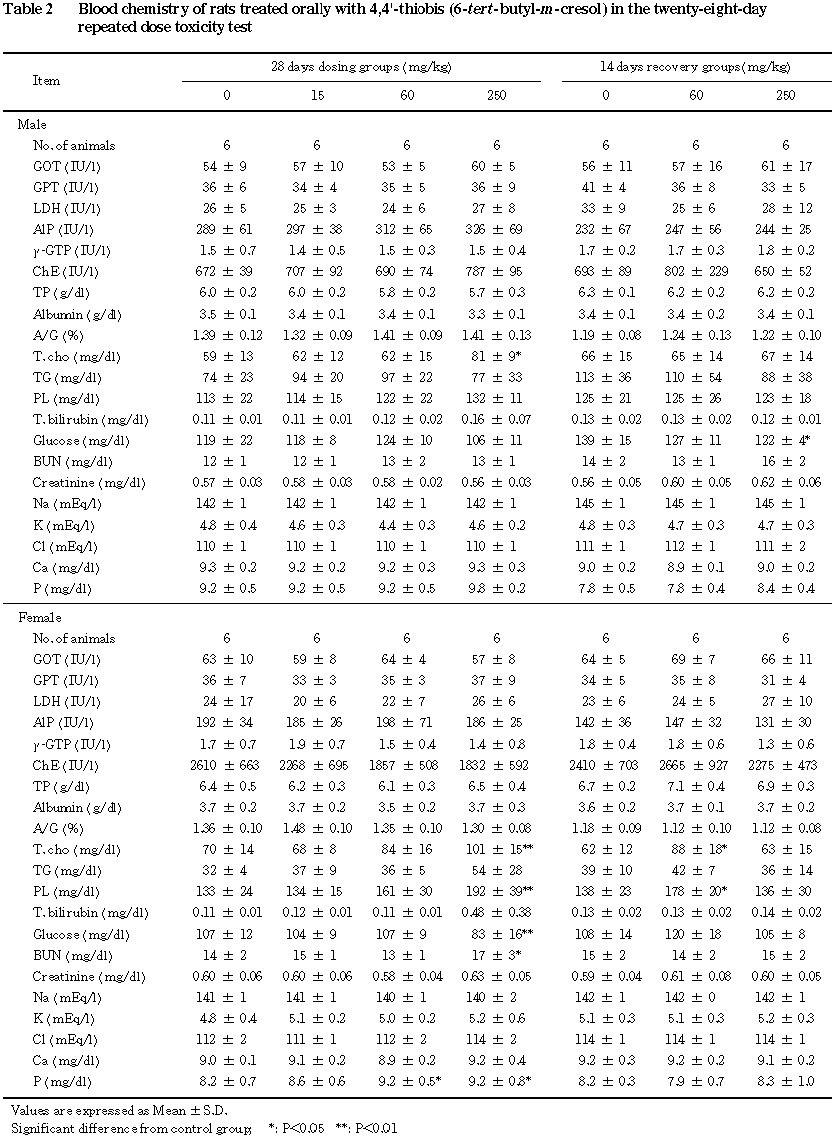


他に,脳の絶対重量の有意な増加が雌の 60 mg/kg群にみられたが,用量と関連した変化ではなかった.
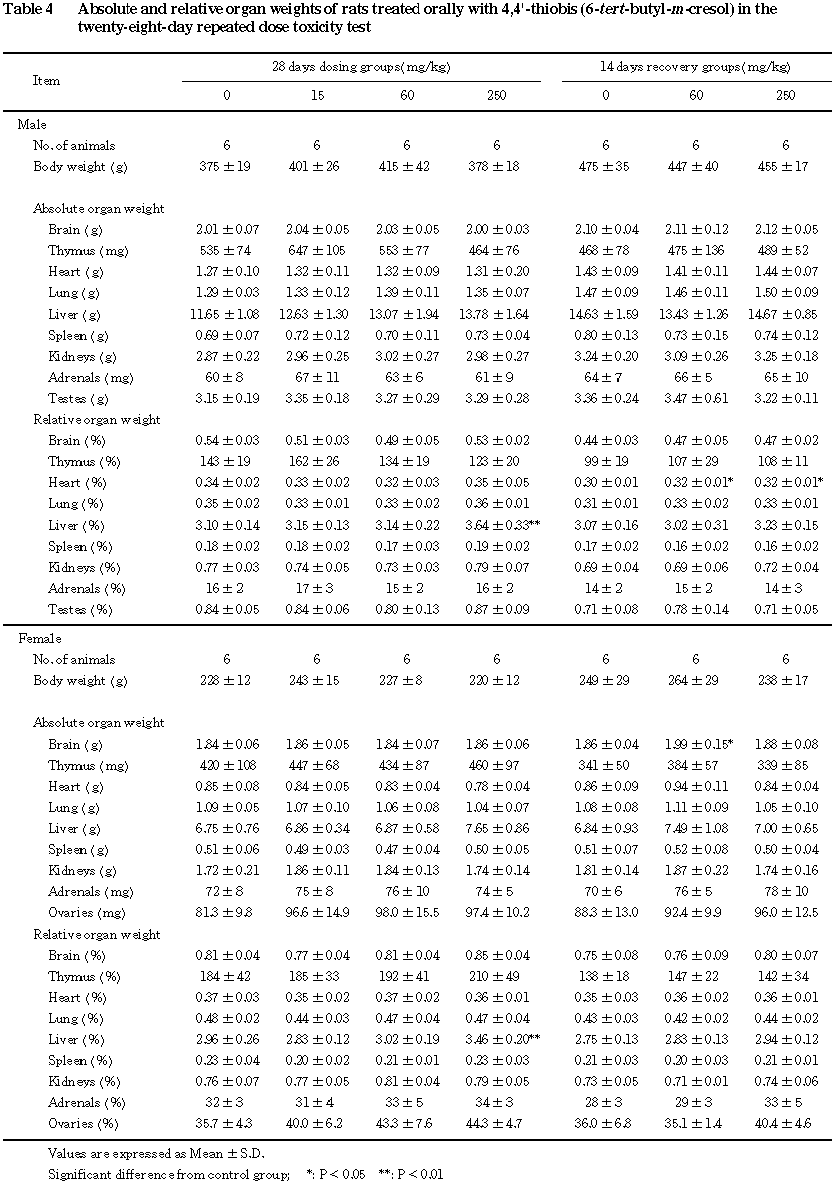

回腸:腸絨毛のごく軽度な過形成が 250 mg/kg群の雄1例と雌3例にみられた.本所見は,腸絨毛の丈の高さの増大として観察され,組織構築の変化あるいは炎症反応は認められなかった.
盲腸:吸収上皮細胞のごく軽度から軽度な空胞化が 60 mg/kg群の雄3例と雌1例,250 mg/kg群の雌雄各5例にみられた.また,粘膜におけるごく軽度から軽度な細胞浸潤が60 mg/kg群の雄5例と雌1例,250 mg/kg群の雌雄各3例にみられたが,吸収上皮細胞の空胞化を示す個体と細胞浸潤を示す個体とは必ずしも一致していなかった.
結腸:吸収上皮細胞のごく軽度な空胞化が 60 mg/kg群の雌雄各1例,250 mg/kg群の雄1例と雌2例にみられた.また,粘膜におけるごく軽度な細胞浸潤が雌の60および250 mg/kg群でそれぞれ1および2例にみられた.
直腸:粘膜におけるごく軽度な細胞浸潤が 250 mg/kg群の雌雄各1例にみられた.
肝臓:小葉中心帯肝細胞のごく軽度な肥大が 250 mg/kg群の雌雄各5例にみられた.
腸間膜リンパ節:傍皮質領域において,核崩壊物を容れたマクロファージ“ tingible body macrophage”の出現が,対照群で雄1例(ごく軽度),15 mg/kg群で雌雄各1例(いずれもごく軽度),60 mg/kg群で雄1例と雌2例(いずれもごく軽度)にみられたのに対し,250 mg/kg群では雄で2例(1例がごく軽度,残る1例が軽度)と雌で5例(4例がごく軽度,残る1例が軽度)にみられ,250 mg/kg群の雌で例数がやや多かった.
上記以外の所見は出現状況とその病理学的性状からいずれも偶発所見と判断した.
盲腸:吸収上皮細胞の変化は認められなかった.なお,粘膜におけるごく軽度から軽度な細胞浸潤が対照群で雌雄各 2例,60 mg/kg群で雄2例と雌1例,250 mg/kg群で雄3例と雌4例にみられた.
直腸:粘膜におけるごく軽度な細胞浸潤が 60 mg/kg群の雌1例,250 mg/kg群の雄1例にみられた.
肝臓:肝細胞の肥大は認められなかった.なお,ごく軽度な微小肉芽腫が対照群の雌雄各 1例,250 mg/kg群の雄1例にみられた.
十二指腸,空腸,結腸および腸間膜リンパ節には異常所見は認められなかった.
摂餌量では, 250 mg/kg群の雌雄で投与開始4日に減少を示したが,雄ではその後対照群をやや上回った.60 mg/kg群でも雄の摂餌量は対照群をやや上回った.これらの投与群の体重は,対照群とほぼ同様であったことから,食餌効率は低下しているものと考えられ,後述の腸管に対する障害がその要因と推察される.
尿検査では, 60 mg/kg以上の投与群で尿pHの低下,尿蛋白およびケトン体の増加が主として雌にみられた.同時に,血液生化学検査において,雌で尿素窒素や無機リンの増加がみられたことから,尿蛋白の増加は本被験物質の腎臓に対する影響と考えられるが,腎臓では組織学的変化は認められなかった.また,250 mg/kg群の雌の血糖値は低下していたことから,尿中ケトン体の増加は,血糖値の低下に伴い,エネルギー源としての脂質要求が増大したためと推察される.
血液学検査では,血小板数の増加,リンパ球比率の減少と分葉核好中球比率の増加が 250 mg/kg群の主として雌にみられた.250 mg/kg群の雌におけるリンパ球および分葉核好中球の実数を,白血球数とその分画比率から求めると,リンパ球数は対照群平均値の約20%増,分葉核好中球数は対照群平均値の約160%増であったことから,本試験における白血球分画比率の変化は,分葉核好中球の実質的な増加に起因し,大腸粘膜での細胞浸潤との関連性が示唆される.
血液生化学検査では,既に述べた血糖,尿素窒素および無機リンの変動のほか,総コレステロールとリン脂質の増加が 250 mg/kg群にみられ,脂質代謝への影響も示唆された.
病理学検査では,小腸,大腸,腸間膜リンパ節および肝臓に変化がみられた.小腸では,肉眼的な壁の肥厚が 250 mg/kg群にみられ,組織学的には,回腸で腸絨毛の過形成がみられた.既に述べた如く,60 mg/kg以上の投与群では食餌効率の低下が示唆されたが,小腸における形態学的変化は,消化・吸収能の低下に対する適応的な生体反応と考えられる.また,大腸では,肉眼的な盲腸の拡張が250 mg/kg群にみられ,組織学的には盲腸および結腸で吸収上皮細胞の空胞化および粘膜の細胞浸潤が60 mg/kg以上の投与群にみられ,大腸に対する障害性が示唆された.ただし,吸収上皮細胞の変化を示す個体と細胞浸潤を示す個体とは必ずしも一致せず,両者の関連性は明らかでなかった.腸間膜リンパ節では,傍皮質領域における“tingible body macrophage”が250 mg/kg群にやや多くみられた.この変化は,頸部リンパ節や胸腺,脾臓など他のリンパ器官では認められなかったことから,腸管障害と関連した所見であり,リンパ系器官に対する直接的な作用ではないと考えられる.なお,投与終了時剖検例のうち,250 mg/kg群の雌雄各1例に,直腸粘膜の細胞浸潤がみられたが発現例数が少なく,また,この種の動物では背景的に観察されることから,被験物質投与との関連性はないと判断された.
肝臓では, 250 mg/kg群で重量が増加し,組織学的には小葉中心帯肝細胞の肥大が認められた.血液生化学検査では,GOTやGPTの上昇など肝機能障害を示す所見はみられなかったことから,肝臓の組織所見は,薬物代謝酵素の誘導を示唆するもの2)と推察される.
回復群においては,被験物質投与に関連すると考えられる変化のうち, 250 mg/kg群の尿pHの低下,尿蛋白の増加,血小板数の増加および回腸における腸絨毛の過形成を除く所見は認められず,概ね可逆性の変化と考えられた.
以上の如く, 4,4'-チオビス(6-tert-ブチル-m-クレゾール)をラットに28日間反復投与した結果,主な変化が60 mg/kg以上の投与群の大腸に,さらに250 mg/kg群では小腸および肝臓にみられ,本被験物質の主な標的器官は腸管と肝臓と考えられた.一方,15 mg/kg群では変化は認められなかった.これらの結果から,本試験条件下における4,4'-チオビス(6-tert-ブチル-m-クレゾール)の無影響量は雌雄とも15 mg/kg/dayと考えられた.
| 1) | S. C. Gad and C. S. Weil, "Principles and Methods of Toxicology," 2, ed. by A. Wallace Hayes, Raven Press, Ltd., New York, 1989, pp. 435-483. |
| 2) | J. R. Glaister. "毒性病理学の基礎," 高橋道人監訳, ソフトサイエンス社, 東京, 1992, pp.85-98. |
| 連絡先 | |||
| 試験責任者: | 岡崎修三 | ||
| 試験担当者: | 榎並倫宣,中村英明,畠山和久,田村一利,沼田弘明,勝亦倶慶 | ||
| (株)ボゾリサーチセンター 御殿場研究所 | |||
| 〒412 静岡県御殿場市かまど1284 | |||
| Tel. 0550-82-2000 | Fax. 0550-82-2379 | ||
| 連絡先 | |||
| Authors: | Shuzo Okazaki(Study director) Tomonori Enami, Hideaki Nakamura, Kazuhisa Hatayama, Kazutoshi Tamura, Hiroaki Numata, Tomoyoshi Katsumata | ||
| Gotemba Laboratory, Bozo Research Center Inc. | |||
| 1284, Kamado, Gotemba-shi, Shizuoka, 412, Japan | |||
| Tel.+81-550-82-2000 | Fax.+81-550-82-2379 | ||