エチルメチルケトキシムのラットを用いる
28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of
Ethyl methyl ketoxime in Rats
要約
塗料の皮張り防止剤,シリコン樹脂の硬化剤およびウレタンのブロッキング剤として使用されるエチルメチルケトキシムの
4,20および100 mg/kg/dayをCrj:CD(SD系)雌雄ラットに28日間経口反復投与し,その毒性並びに投与終了後14日間の回復性を検討した.
血液学検査では,網状赤血球率の上昇が雌雄の
20 mg/kg以上の群に,血小板数の増加が雌の20 mg/kg以上の群に,赤血球数,ヘマトクリット値および血色素量の減少が雄の100 mg/kg群および雌の20 mg/kg以上の群に,平均赤血球容積,平均赤血球ヘモグロビン量および白血球数の増加が雌雄の100 mg/kg群に認められた.血液生化学検査では,カリウムの増加が雌雄の100 mg/kg群に,A/G比およびアルブミン分画の上昇,α1-グロブリン分画の低下,総ビリルビンおよび総コレステロールの増加が雌の100 mg/kg群に認められた.器官重量では,脾臓重量の増加および脾臓の体重重量比の上昇が雄の100 mg/kg群および雌の20 mg/kg以上の群に,肺の体重重量比の上昇が雄の100 mg/kg群に,心臓の体重重量比の上昇が雌の100 mg/kg群に認められた.剖検では,脾臓の腫大が雄の20 mg/kg以上の群および雌の100 mg/kg群に認められた.病理組織学検査では,肝臓にヘモジデリン貪食を伴うクッパー細胞の肥大が雄の100 mg/kg群および雌の20 mg/kg以上の群,髄外造血が雌雄の100 mg/kg群,腎臓に尿細管上皮のリポフスチン様物質の沈着が雌雄の100 mg/kg群,脾臓にうっ血,髄外造血の亢進およびヘモジデリン顆粒の増加が雌雄の20 mg/kg以上の群に認められた.
上述の変化はその多くが
14日間の回復期間終了時には消失あるいは軽減した.
以上のことから,雌雄の
20 mg/kg以上の群に網状赤血球率の上昇および脾臓に対する影響等が認められたことから,本試験におけるエチルメチルケトキシム投与による無影響量は,雌雄ともに4 mg/kg/dayであると考えられた.
方法
1. 被験物質
エチルメチルケトキシムは水溶性
(水溶解度:25℃で114 g/l)の無色透明液体である.本試験では宇部興産(株)より提供されたロット番号40930(純度99.0%以上)のものを使用した.なお,被験物質は,納品後3カ月間の品質が保証されており,冷暗所(2〜8℃設定)に保存した.
投与には,用時に次の
3濃度に調製したものを用いた.すなわち,被験物質を1%の濃度となるように精製水(日本薬局方,ヤクハン製薬(株))に溶解して調製し,その1%調製液を0.2%および0.04%の濃度となるように精製水で希釈して調製した.なお,各濃度の調製液は規定の濃度であることが確認されている.
2. 試験動物および飼育条件
生後
3週齢のCrj:CD(SD系)SPFラット雌雄を日本チャールス・リバー(株)より受け入れ,11日間の検疫・馴化飼育を行い,異常がなく順調な発育を示した動物を試験に用いた.
動物は,温度
23±3℃,湿度55±10%,換気回数10〜15回/時および照明12時間/日に設定したバリアシステムの飼育室で,ブラケット式金属製金網床ケージに群分け前は5匹以内,群分け後は1匹を収容して飼育した.飼料は固型飼料 (CRF-1,オリエンタル酵母工業(株)),飲料水は水道水(札幌市水道水)をそれぞれ自由に摂取させた.
3. 試験群の設定
試験群は,エチルメチルケトキシムの
100,300および1000 mg/kg/dayを設定した14日間反復経口投与毒性試験の成績を参考に設定した.すなわち,100 mg/kg群で赤血球数の低値,平均赤血球容積および平均赤血球ヘモグロビン濃度の高値,脾臓の腫大および脾臓重量の高値などが認められたことから,高用量は確実に赤血球および脾臓への影響が予想される100 mg/kg/dayとし,以下公比5で20および4 mg/kg/dayを設定した.さらに,精製水を投与する対照を加えて計4群とした.
動物数は,対照群で雌雄各
14匹,4および20 mg/kg群で雌雄各7匹,100 mg/kg群で雌雄各14匹とし,そのうち回復性試験のために対照群および100 mg/kg群の雌雄各7匹をあてた.群分けは,馴化期間の最終日に体重別層化無作為抽出法により行った.
4. 投与方法
投与は胃ゾンデを用いた強制経口投与とし,
1日1回連続28回行った.回復性試験の日数は14日間とした.投与容量は,体重1kg当たり10 mlとして投与日に最も近い日に測定した体重に基づいて算出した.投与は5週齢から開始し,投与開始時の平均体重(体重範囲)は雄で164.6 g(152〜176 g) ,雌で138.3 g(122〜159 g)であった.
5. 観察,測定および検査項目
1) 一般状態観察
投与期間および回復期間中,全例について
1日1回以上の頻度で観察した.
2) 体重および摂餌量測定
全例について,体重を投与
1日(投与前),投与2,7,14,21および28日(投与終了日),回復1,2,7および14日並びに剖検日に測定した.摂餌量測定は剖検日を除いて体重測定と同じ日に測定した.また,投与1から28日の体重増加量および体重増加率を算出した.
3) 尿検査
投与期間の最終週
(投与23〜24日)および回復期間の最終週(回復12〜13日)に全例を代謝ケージに収容して非絶食下で採尿を行った.約3時間の蓄尿についてpH,蛋白,糖,ケトン体,ウロビリノーゲン,ビリルビン,潜血反応(以上,試験紙マルティスティックス;バイエル・三共),色調(肉眼観察)および沈渣(鏡検)を検査し,21時間蓄尿について尿量(容量),比重(アタゴ製屈折計ユリコン),ナトリウム,カリウム(以上,炎光法:コーニング480型炎光光度計)およびクロール(電量滴定法:平沼CL-6M型クロライドカウンター),カルシウム(OCPC法),無機リン(フィスケ・サバロー法)(以上,日立7150形自動分析装置)を測定した.
4) 血液学検査
剖検時に全例について約
16時間絶食させた後,エーテル麻酔下で大腿静脈より採血し,EDTA・2Kで処理した血液を用いて赤血球数,平均赤血球容積,血小板数,白血球数(以上,電気抵抗法),血色素量(シアンメトヘモグロビン法)(以上,コールターカウンターT660型),ヘマトクリット値(赤血球数,平均赤血球容積より算出),平均赤血球ヘモグロビン量(赤血球数,血色素量より算出),平均赤血球ヘモグロビン濃度(ヘマトクリット値,血色素量より算出),網状赤血球率(Brecher法)および白血球型別百分率(鏡検)を測定した.また,無処理血液を用いて,凝固時間(流体粘度変化による空気圧測定法:グライナー社製マイクロコアグロメータ)を測定した.さらに,腹部大動脈より採血しクエン酸ナトリウムで処理した後,3000 rpmで10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法) および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,AMELUNG KC-10A バクスターKK)を測定した.
5) 骨髄検査
剖検時に全例について,左大腿骨から骨髄を採取秤量後,希釈液
[培養液 (RPMI-1640リキッド,日水製薬(株)) とラット血清を1:1で混合し,混合液2 mlに対し抗凝固剤 (アングロット,日本商事(株)) 1滴を添加] 1 ml中に入れ,22Gあるいは25G針付シリンジで吸引・射出を繰り返して細胞を分散させた.分散させた後,200メッシュナイロンガーゼでろ過し,ろ液(浮遊液)中の有核細胞数を測定(電気抵抗法,コールターカウンターT660型)して,骨髄1 mg中の有核細胞数を算出した.その後,ろ液を1000 rpmで5分間遠心し,沈渣から塗抹標本を作製し,メイ・ギムザ染色を施した後,対照群と100 mg/kg群の雌雄全例について顕微鏡下で500個の細胞を検査した.
6) 血液生化学検査
血液学検査に引き続いて,全例について腹部大動脈より採血し,
3000 rpmで10分間遠心分離して得られた血清を用いてGOT,GPT(以上,IFCC法),γ-GTP (包接L-γ-グルタミル-p-ニトロアニリド基質法),アルカリフォスファターゼ(ベッセィ・ローリー法),乳酸脱水素酵素(ロブレスキー・ラ・デュー法),血糖(ヘキソキナーゼ法),総コレステロール(以上,酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(ヤッフェ法),カルシウム(OCPC法),無機リン(フィスケ・サバロー法),総蛋白(ビウレット法),アルブミン(BCG法),クレアチンフォスフォキナーゼ (GSCC法)(以上,日立7150形自動分析装置),ナトリウム,カリウム(以上,炎光法:コーニング480型炎光光度計),クロール(電量滴定法:平沼CL-6M型クロライドカウンター),A/G比(総蛋白,アルブミンより算出)および蛋白分画(セルロースアセテート膜電気泳動法)を測定した.
7) 剖検および器官重量測定
投与期間および回復期間終了の翌日に全例について,体外表部を観察し,エーテル麻酔下で採血後放血致死させ剖検した.また,脳,下垂体,甲状腺,肺,心臓,肝臓,腎臓,脾臓,副腎,胸腺,精巣および卵巣の重量を測定するとともに,器官体重重量比を算出した.
8) 病理組織学検査
全例について肝臓,腎臓,脾臓,心臓,肺,脳
(大脳・小脳),下垂体,副腎,甲状腺,上皮小体,胸腺,腸間膜リンパ節,膵臓,舌,下顎リンパ節,顎下腺,舌下腺,耳下腺,乳腺,皮膚,胸骨および大腿骨(骨髄を含む),脊髄(頸部),骨格筋(外側広筋),胸部大動脈,喉頭,気管,気管支,食道,胃(前胃・腺胃),十二指腸,空腸,回腸,盲腸,結腸,直腸,膀胱,精巣,精巣上体,精嚢(凝固腺を含む),前立腺,卵巣,子宮,腟および坐骨神経を10%中性緩衝ホルマリン液,眼球およびハーダー腺をデビッドソン液で固定し,常法に従いパラフィン切片を作製し,ヘマトキシリン・エオジン染色あるいは特殊染色 [鉄(ベルリン青)染色およびシュモール反応] 標本を作製し,病理組織学検査を行った.
6. 統計処理
Bartlettの等分散検定の後,一元配置分散分析法あるいはKruskal-Wallis法により解析し,有意な場合,Dunnettの検定法あるいはMann-WhitneyのU-検定法により対照群とエチルメチルケトキシム投与各群との比較を行った.なお,尿検査の定性的項目についてはKruskal-Wallis法およびMann-WhitneyのU-検定法を用いて解析し,対照群との検定については危険率5%以下を統計学的に有意とした.
結果
1. 一般状態
投与期間および回復期間のいずれにおいても,雌雄ともに異常は認められなかった.
2. 体重(Table 1)
投与期間および回復期間のいずれにおいても,雌雄ともに対照群と比較して有意差は認められなかった.

3. 摂餌量
投与期間では,雌雄ともに対照群と比較して有意差は認められなかった.
回復期間では,雌の
100 mg/kg群で摂餌量の減少が回復1日に認められた.
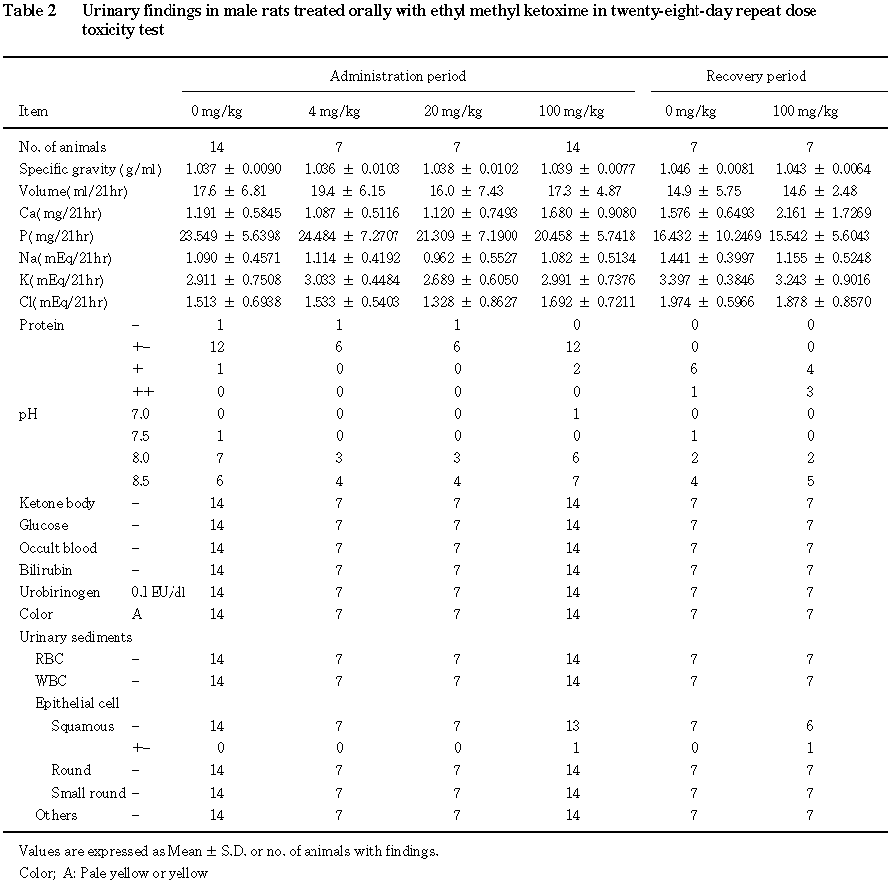
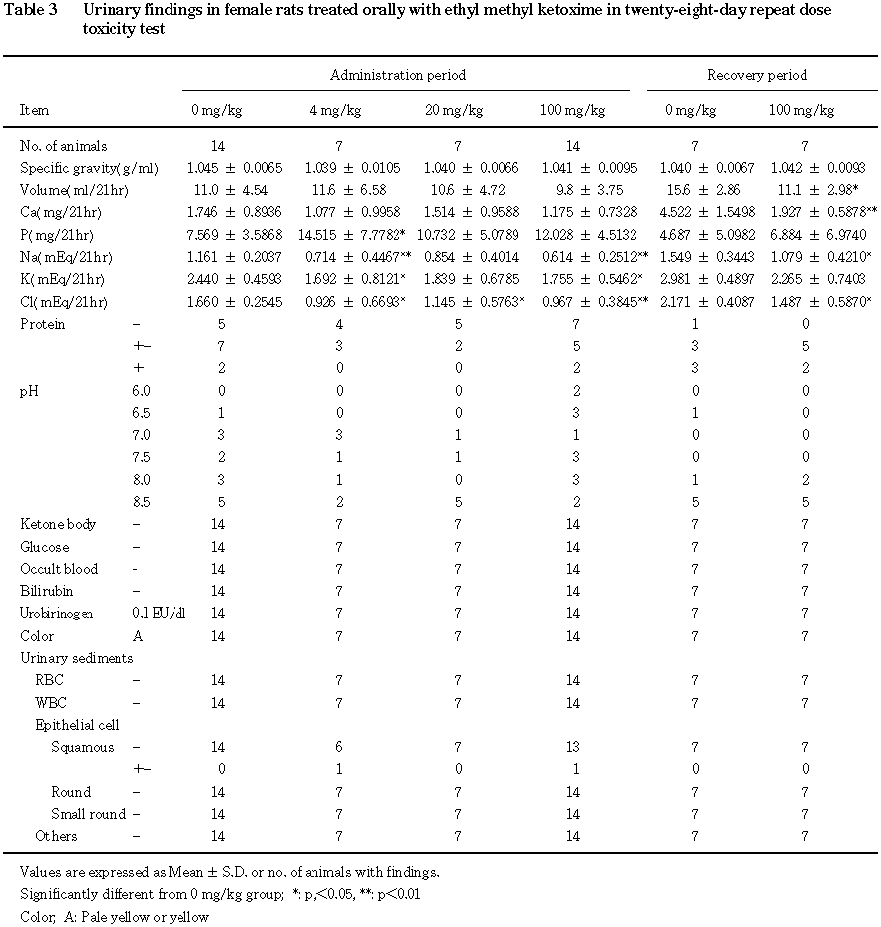
4.尿検査(Table 2,3)
投与期間最終週には,雌では,
4 mg/kg群でナトリウム,カリウムおよびクロールの減少,20 mg/kg群でクロールの減少,100 mg/kg群でナトリウム,カリウムおよびクロールの減少が認められた.その他,エチルメチルケトキシム投与による異常は認められなかった.
回復期間最終週には,雌の
100 mg/kg群で尿量,ナトリウム,クロールおよびカルシウムの減少が認められた.
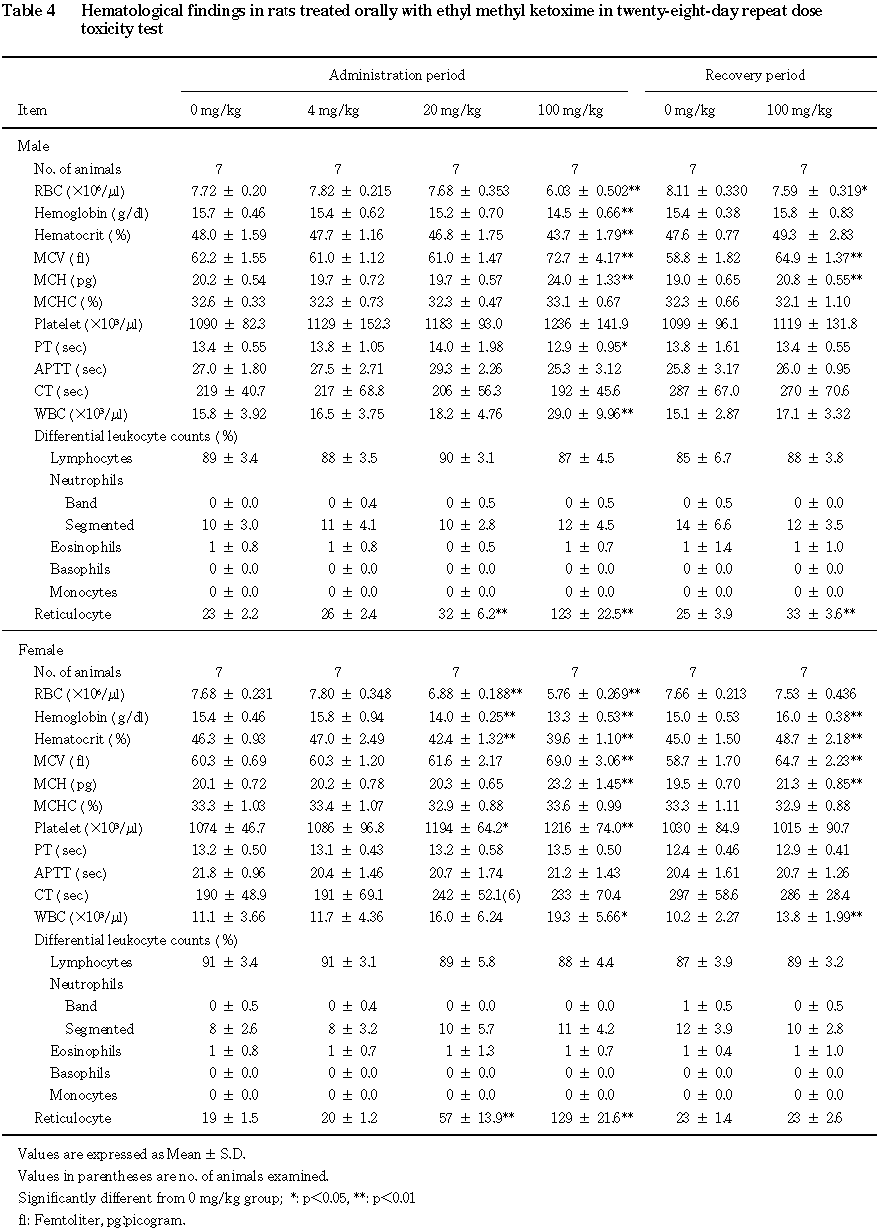
5.血液学検査(Table 4)
投与期間終了時には,雄では,
20 mg/kg以上の群で網状赤血球率の上昇,100 mg/kg群で赤血球数,ヘマトクリット値および血色素量の減少,平均赤血球容積,平均赤血球ヘモグロビン量および白血球数の増加が認められた.雌では,20 mg/kg以上の群で赤血球数,ヘマトクリット値および血色素量の減少,血小板数の増加,網状赤血球率の上昇,100 mg/kg群で平均赤血球容積,平均赤血球ヘモグロビン量および白血球数の増加が認められた.その他,雄の100 mg/kg群でプロトロンビン時間の短縮が認められた.
回復期間終了時には,雄の
100 mg/kg群で赤血球数の減少,平均赤血球容積,平均赤血球ヘモグロビン量および網状赤血球率の上昇が認められた.雌では,100 mg/kg群でヘマトクリット値,血色素量および白血球数の増加,平均赤血球容積および平均赤血球ヘモグロビン量の上昇が認められた.
6. 骨髄検査
投与期間終了時および回復期間終了時のいずれにおいても,雌雄ともに対照群と比較して有意差は認められなかった.
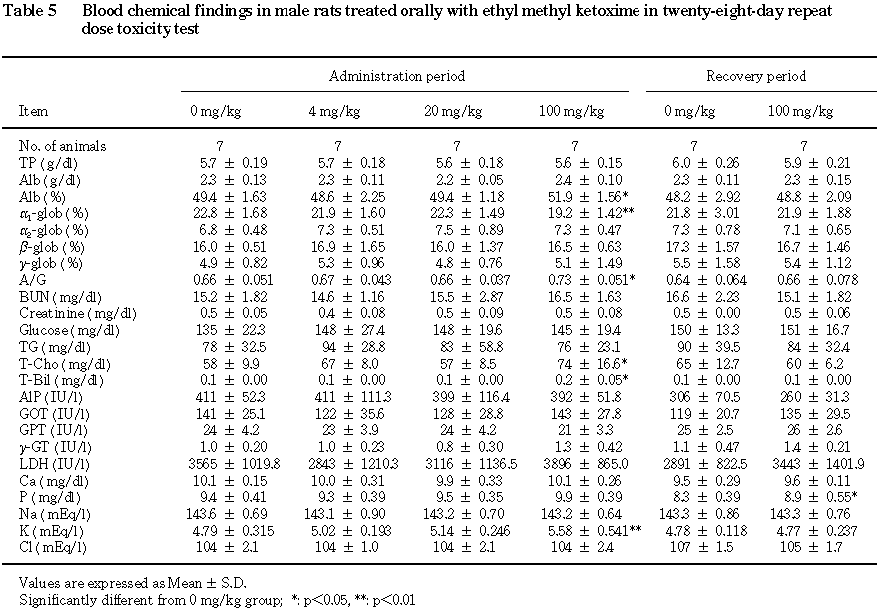
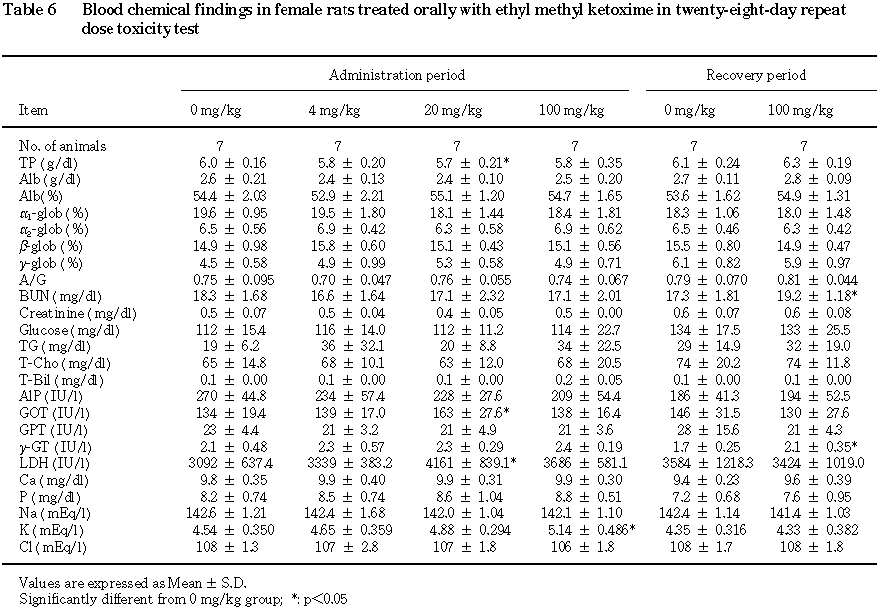
7. 血液生化学検査(Table 5,6)
投与期間終了時には,雄の
100 mg/kg群でA/G比およびアルブミン分画の上昇,α1-グロブリン分画の低下,総ビリルビン,総コレステロールおよびカリウムの増加が,雌の100 mg/kg群でカリウムの増加が認められた.その他,エチルメチルケトキシム投与による異常は認められなかった.
回復期間終了時には,雄の
100 mg/kg群で無機リンの増加が,雌の100 mg/kg群でγ-GTPおよび尿素窒素の増加が認められた.
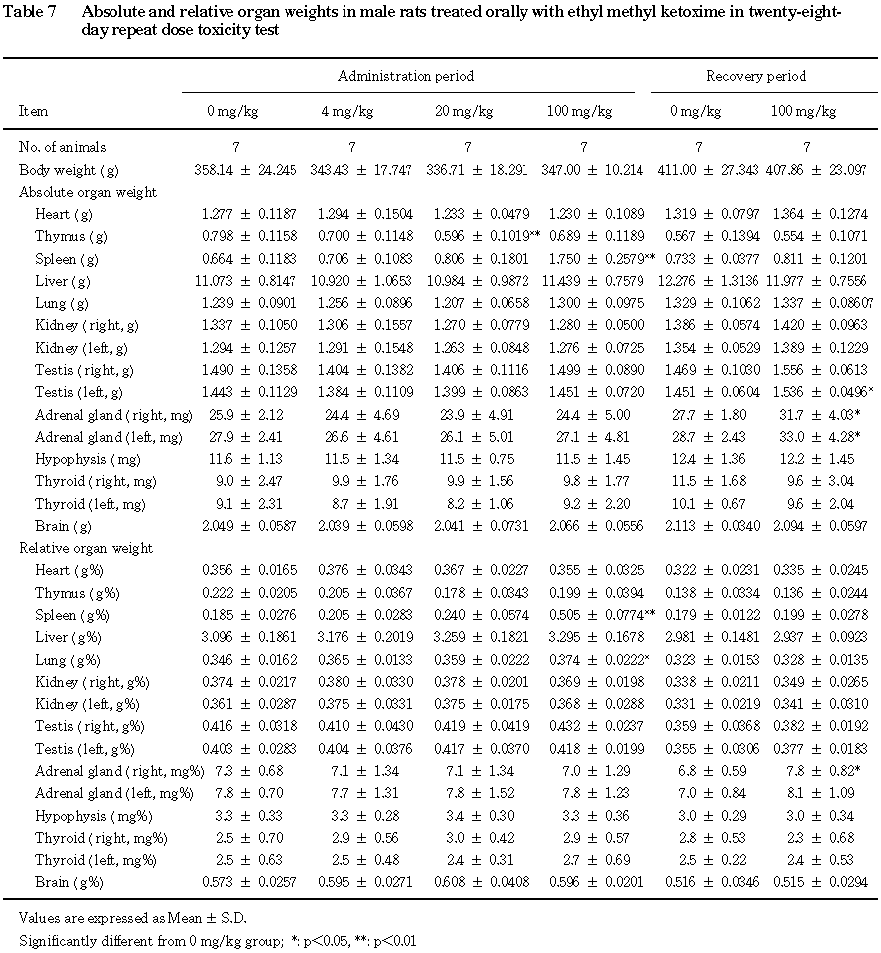
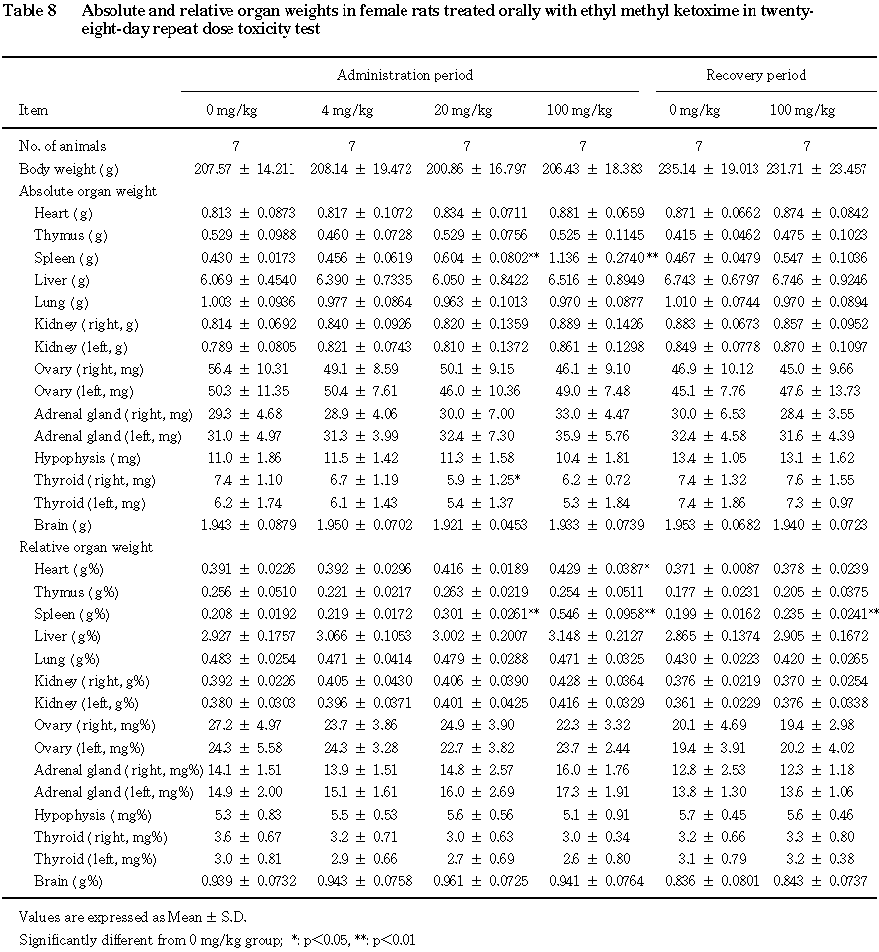
8.器官重量(Table 7,8)
投与期間終了時には,雄の
100 mg/kg群で脾臓重量の増加,脾臓および肺の体重重量比の上昇が認められた.雌では,20 mg/kg以上の群で脾臓重量の増加,脾臓の体重重量比の上昇,100 mg/kg群で心臓の体重重量比の上昇が認められた.その他,エチルメチルケトキシム投与による異常は認められなかった.
回復期間終了時には,雄の
100 mg/kg群で,脾臓の重量および体重重量比に有意差は認められなかったが,副腎重量の増加,副腎の体重重量比の上昇が認められた.雌では,100 mg/kg群で脾臓の体重重量比の上昇が認められた.その他,雄の100 mg/kg群で精巣重量の増加が認められた.
9. 剖検
投与期間終了時には,脾臓の腫大が
4 mg/kg群の雄1例,20 mg/kg群の雄3例,100 mg/kg群の雌雄全例に認められた.
回復期間終了時には,エチルメチルケトキシム投与による異常は認められなかった.
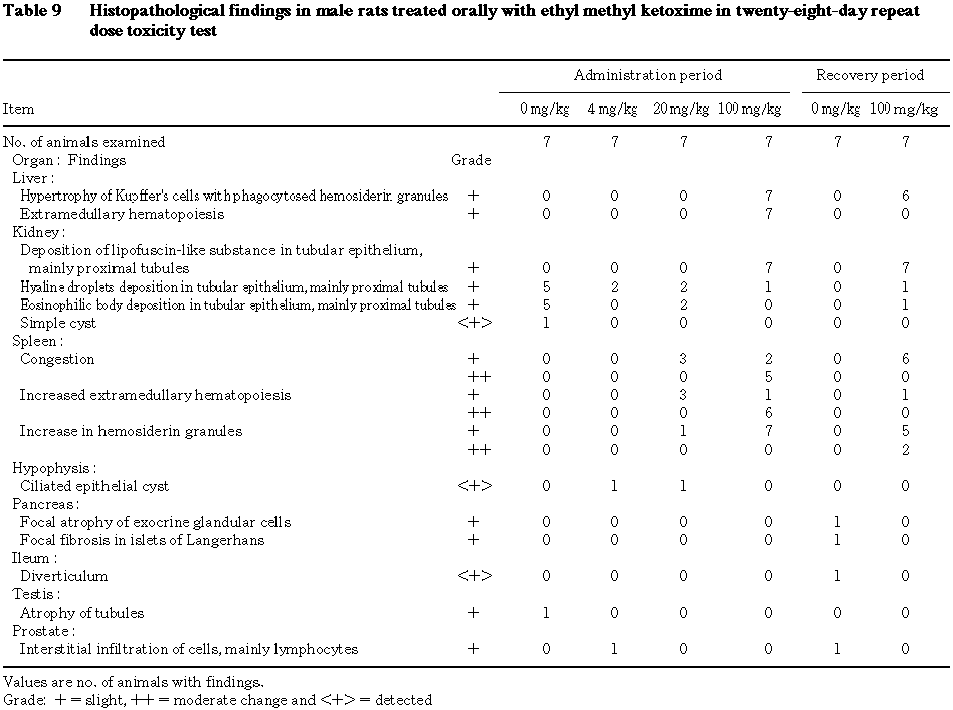
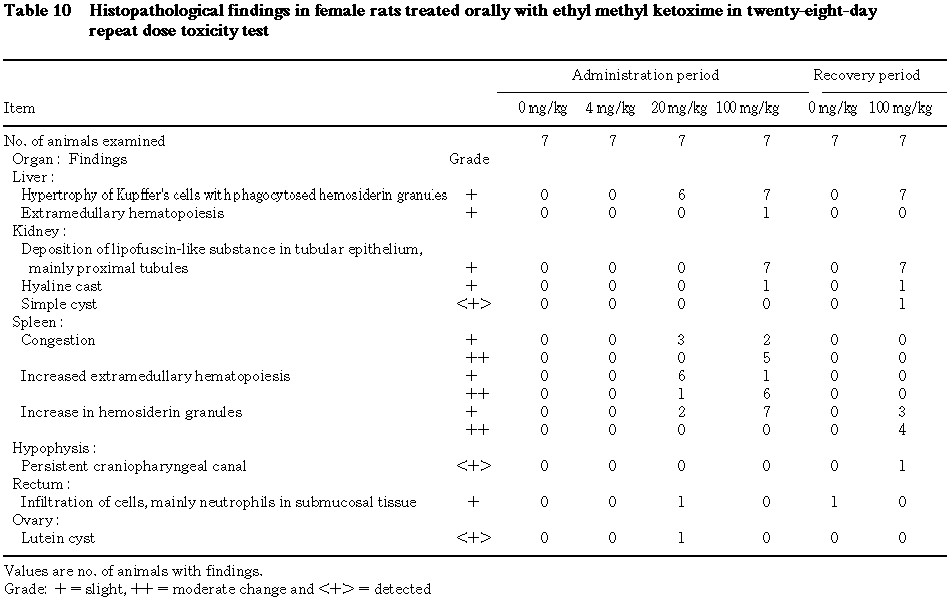
10. 病理組織学検査(Table 9,10)
投与期間終了時には,肝臓では,ヘモジデリン貪食を伴うクッパー細胞の軽度の肥大が
20 mg/kg群の雌6例,100 mg/kg群の雌雄全例,軽度の髄外造血が100 mg/kg群の雄全例および雌1例に認められた.腎臓では,近位を主とする尿細管上皮のリポフスチン様物質の軽度の沈着が100 mg/kg群の雌雄全例に認められた.脾臓では,軽度から中等度のうっ血が20 mg/kg群の雌雄各3例,100 mg/kg群の雌雄全例,髄外造血の軽度から中等度の亢進が20 mg/kg群の雄3例および雌全例,100 mg/kg群の雌雄全例,ヘモジデリン顆粒の軽度の増加が20 mg/kg群の雄1例および雌2例,100 mg/kg群の雌雄全例に認められた.
回復期間終了時には,肝臓では,ヘモジデリン貪食を伴うクッパー細胞の軽度の肥大が
100 mg/kg群の雄6例および雌全例に認められた.腎臓では,近位を主とする尿細管上皮のリポフスチン様物質の軽度の沈着が100 mg/kg群の雌雄全例に認められた.脾臓では,軽度のうっ血が100 mg/kg群の雄6例,髄外造血の軽度の亢進が100 mg/kg群の雄1例,ヘモジデリン顆粒の軽度から中等度の増加が100 mg/kg群の雌雄全例に認められた.
その他,エチルメチルケトキシム投与による異常は認められなかった.
考察
赤血球系に及ぼす影響として,血液学検査では網状赤血球率の上昇が雌雄の
20 mg/kg以上の群に,赤血球数,ヘマトクリット値および血色素量の減少が雄の100 mg/kg群および雌の20 mg/kg以上の群に,平均赤血球容積および平均赤血球ヘモグロビン量の増加が雌雄の100 mg/kg群に,血液生化学検査では総ビリルビンの増加が雄の100 mg/kg群に,カリウムの増加が雌雄の100 mg/kg群に認められた.また,肝臓ではヘモジデリン貪食を伴うクッパー細胞の肥大が雄の100 mg/kg群および雌の20 mg/kg以上の群に,髄外造血が雌雄の100 mg/kg群に認められた.腎臓では近位を主とする尿細管上皮のリポフスチン様物質の沈着が雌雄の100 mg/kg群に認められた.脾臓では重量の増加および体重重量比の上昇が雄の100 mg/kg群および雌の20 mg/kg以上の群に,腫大が雄の20 mg/kg以上の群および雌の100 mg/kg群に認められ,病理組織学的にうっ血,髄外造血の亢進およびヘモジデリン顆粒の増加が雌雄の20 mg/kg以上の群に認められた.
以上の変化は,いずれも溶血性貧血の状態を示唆するものであり,エチルメチルケトキシム投与による影響と考えられた.
これに関連して,血小板数の増加が雌の
20 mg/kg以上の群,白血球数の増加が雌雄の100 mg/kg群に認められたが,溶血性貧血が生じた場合に,白血球数および血小板数が増加することが知られており1, 2),エチルメチルケトキシム投与により生じた溶血に伴って反応的に生じたものと考えられた.その他,投与期間終了時に,雄の100 mg/kg群でプロトロンビン時間の短縮が認められたが,背景データの範囲内の変動であり,エチルメチルケトキシム投与との関連はないと考えられた.
血液生化学検査では,
A/G比およびアルブミン分画の上昇,α1-グロブリン分画の低下,総コレステロールの増加が雄の100 mg/kg群に認められたことから,エチルメチルケトキシム投与により肝機能に何らかの影響を及ぼしていたものと考えられた.回復期間終了時には,雄の100 mg/kg群で無機リンの増加が認められたが,投与終了時における対照群の測定値と比較するとむしろ減少を示していることから,生理的な変動であり,エチルメチルケトキシム投与との関連はないと考えられた.また,雌の100 mg/kg群でγ-GTPおよび尿素窒素の増加が認められたが,投与終了時における対照群の測定値と比較すると明らかな差はないことから,生理的な変動であり,エチルメチルケトキシム投与との関連はないと考えられた.
器官重量では,肺の体重重量比の上昇が雄の
100 mg/kg群,心臓の体重重量比の上昇が雌の100 mg/kg群に認められた.これらの変化はラットの14日間反復経口投与毒性試験においても認められており,エチルメチルケトキシム投与による溶血性貧血に伴う低酸素状態に対する代償性変化であると考えられた.また,回復期間終了時に,雄の100 mg/kg群で精巣重量の増加が認められたが,背景データの範囲内の変動であり,エチルメチルケトキシム投与との関連はないと考えられた.
尿検査では,クロールの減少が雌の
4 mg/kg以上の群,ナトリウムおよびカリウムの減少が雌の4および100 mg/kg群に認められたが,用量依存性は明らかではなく,血中電解質や腎臓の病理組織学検査等に関連した変化および異常が認められていないことから,その毒性学的意義はないものと考えられた.また,回復期間最終週に,雌の100 mg/kg群で尿量,ナトリウム,クロールおよびカルシウムの減少が認められたが,投与期間最終週における対照群の測定値と比較すると明らかな差はなく,エチルメチルケトキシム投与との関連はないと考えられた.
剖検では,脾臓の腫大が
4 mg/kg群の雄1例に認められたが,この例では赤血球恒数および脾臓の病理組織学検査に変化や異常は認められておらず,エチルメチルケトキシム投与との関連は明らかではなかった.
なお,摂餌量の減少が,対照群と比較して雌の
100 mg/kg群で回復1日に認められたが,投与期間中および回復2日以降の推移に変化は認められておらず,エチルメチルケトキシム投与との関連はないと考えられた.
上述の変化は,
14日間の回復期間終了時には消失あるいは軽減が認められ,回復するものと考えられた.特に溶血性貧血については,血液学検査や肝臓・脾臓の病理組織学所見から回復するものと考えられた.なお,尿細管上皮のリポフスチン様物質の沈着については,その出現例数および程度に軽減は認められず,14日間の回復期間では完全には吸収されないことが示された.リポフスチン様物質の由来は特定できなかったが,溶血の結果生じた産物ではないかと考えられた.また,回復期間終了時に副腎の重量の増加および体重重量比の上昇が雄の100 mg/kg群に認められたが,投与期間終了時に同様の変化はみられず,病理組織学検査で異常が認められないことから,毒性学的意義はないものと考えられた.
以上のことから,雌雄の
20 mg/kg 以上の群に網状赤血球率の上昇および脾臓に対する影響等が認められたことから,本試験におけるエチルメチルケトキシム投与による無影響量は,雌雄ともに4 mg/kg/dayであると考えられた.
参考文献
| 1) | 巽 典之ら,Medical Technology 臨時増刊,19,596 (1991). |
| 2) | 桑島 実,Medical Technology 別冊,303,(1993). |
| 連絡先 |
| 試験責任者: | 小林裕幸 |
| 試験担当者: | 茂野 均,長谷淳一,古川正敏 |
| 運営管理者: | 小林茂吉 |
| (株)化合物安全性研究所 |
| 〒004 北海道札幌市豊平区真栄363番24号 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Hiroyuki Kobayashi(Study director)
Hitoshi Shigeno,
Jun-ichi Nagaya,
Masatoshi Furukawa,
Shigeyoshi Kobayashi(Management) |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Toyohira-ku, Sapporo, Hokkaido,004, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |










