o-ジクロロベンゼンが培養細胞に及ぼす細胞遺伝学的影響について,チャイニーズ・ハムスター培養細胞(CHL/IU)を用いて染色体異常試験を実施した.
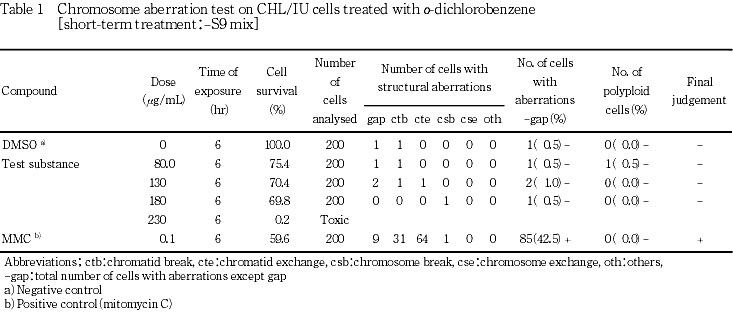
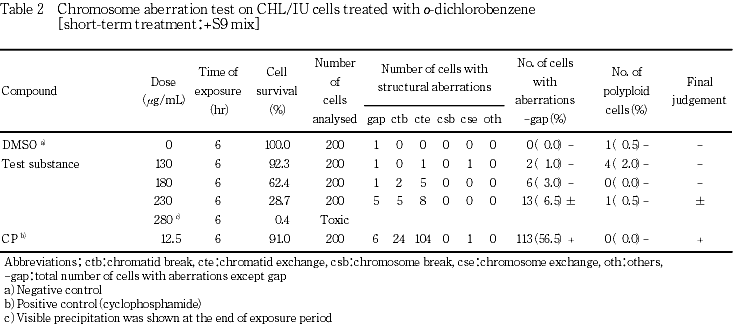
細胞増殖抑制試験結果をもとに,短時間処理法-S9処理ならびに+S9処理とも380 μg/mLを最高処理濃度とし,80.0〜380 μg/mLの7用量を設定した.S9 mix存在下および非存在下で6時間処理(18時間の回復時間)後,標本を作製し,検鏡することにより染色体異常誘発性を検討した.-S9処理では80.0〜230 μg/mL,+S9処理では130〜280 μg/mLのそれぞれ4用量(公差50 μg/mL)について顕微鏡観察を実施した.
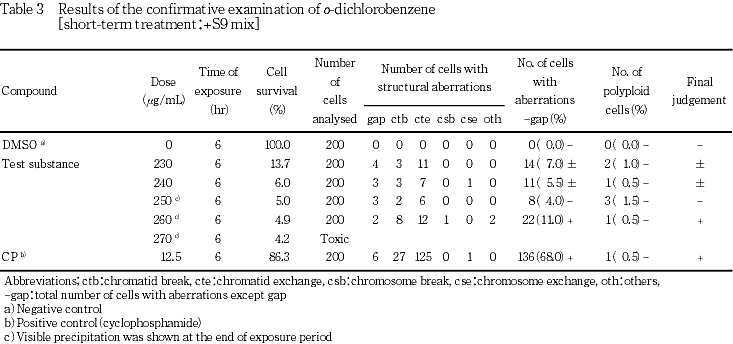
その結果,S9 mix非存在下では染色体構造異常が認められなかったが,S9 mix存在下では染色体構造異常の僅かな誘発がみられ疑陽性結果(±)が得られた.従って,180〜280 μg/mLの11用量(公差10 μg/mL)を用いた確認試験を実施した.顕微鏡観察については230〜270 μg/mLの5用量について実施した.その結果,用量依存を僅かに伴った染色体構造異常の誘発が認められた.
以上の結果より,本試験条件下ではo-ジクロロベンゼンは,染色体異常を誘発する(陽性)と結論した.
| 成 分 | S9 mix 1 mL中の量 |
| S9 | 0.3 mL |
| MgCl2 | 5 μmol |
| KCl | 33 μmol |
| G-6-P | 5 μmol |
| NADP | 4 μmol |
| HEPES緩衝液(pH 7.2) | 4 μmol |
| 精製水 | 残 量 |
細胞を10 vol%中性緩衝ホルマリン液(和光純薬工業(株))で固定した後,0.1 w/v%クリスタル・バイオレット(関東化学(株))水溶液で10分間染色した.色素溶出液(30 vol%エタノール,1 vol%酢酸水溶液)を適量加え,5分間程度放置して色素を溶出した後,580 nmでの吸光度を測定した.各用量群について溶媒対照群での吸光度に対する比,すなわち細胞生存率を算出し,さらにプロビット法を用いて50 %細胞増殖抑制濃度を算出した.
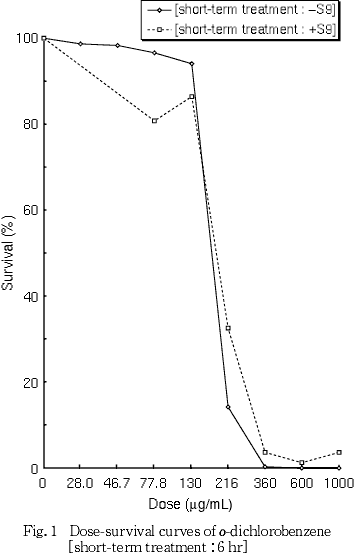
その結果,細胞増殖を50 %抑制する濃度は,短時間処理法-S9処理で176 μg/mLおよび+S9処理で188 μg/mLと算出された(Fig. 1).
なお,被験物質暴露終了時,-S9処理の600 μg/mL以上および+S9処理の360 μg/mL以上で油滴状の析出がみられた.

+S9処理において染色体構造異常の出現に関し疑陽性と判定されたことから,280 μg/mLを最高処理濃度とした確認試験を実施し,公差10 μg/mLで減じた計11用量を設定した.
なお,陽性対照として,-S9処理でマイトマイシンC(MMC:協和醗酵工業(株))を0.1 μg/mL,+S9処理でシクロホスファミド(CP:塩野義製薬(株))を12.5 μg/mLの用量で試験した.
すべての標本をコード化した後,マスキング法で観察した.
各試験群の構造異常を有する細胞あるいは倍数性細胞の出現頻度を,石館ら3)の基準に従って判定した.染色体異常を有する細胞の出現頻度が5 %未満を陰性(-),5 %以上10 %未満を疑陽性(±),10 %以上を陽性(+)とした.最終的には再現性あるいは用量に依存性が認められた場合に陽性と判定した.
なお,統計学的手法を用いた検定は実施しなかった.
また,分裂中期像の20 %にいずれかの異常を誘発するのに必要な被験物質濃度であるD20値を最小二乗法により算出し,一定濃度(mg/mL)あたりの交換型異常(cte)出現数を示す比較値であるTR値を,染色分体交換の出現頻度(%)を被験物質濃度(mg/mL換算)で割ることにより算出した.
本被験物質処理群の+S9処理で,染色体構造異常の出現頻度が疑陽性と判定されたことから,確認試験を実施した.その結果,染色体構造異常の誘発において用量依存的な増加傾向が認められ(Table 3),260 μg/mLでは強い細胞増殖抑制作用がみられるものの,陽性判定基準の10 %を超えるものであった.一方,陽性対照では染色体構造異常の顕著な誘発が認められた.
変異原性の強さに関する相対的比較値であるD20値は0.699(mg/mL),TR値は23.1と算出され,既知変異原性物質に比較してo-ジクロロベンゼンの変異原性は弱いことを示していた.なお,被験物質暴露終了時,短時間処理法-S9処理では380 μg/mLで,+S9処理では280 μg/mL以上で,確認試験では250 μg/mL以上で,油滴状の析出物が認められた.
以上の試験結果から,本試験条件下においてo-ジクロロベンゼンのチャイニーズハムスター培養細胞に対する染色体異常誘発性に関し,陽性と判定した.
なお,本被験物質についてはAmes試験で陰性4)との報告がある.一方,ヒト鼻粘膜細胞に染色体異常を誘発する5)との報告があり,本試験の染色体異常を誘発するという結果と一致した.類縁体であるp-ジクロロベンゼンについてはAmes試験で陰性6),染色体異常試験で陰性3),ヒトリンパ球に対して姉妹染色体交換を誘発する7)との報告があるが,m-ジクロロベンゼンの変異原性に関する報告はなかった.
| 1) | A. Matsuoka, M. Hayashi and M. Ishidate Jr., Mutat. Res., 66, 277(1979). |
| 2) | 日本環境変異原学会・哺乳動物試験分科会編,“化学物質による染色体異常アトラス,”朝倉書店,東京,1988, pp.31-35. |
| 3) | 石館基監修,“<改訂>染色体異常試験データ集,”エル・アイ・シー,東京,1987. |
| 4) | 石館基監修,“微生物を用いる変異原性試験データ集,”エル・アイ・シー,東京,1991, pp.164-165. |
| 5) | C. Zapata-Gayon, N. Zapata-Gayon and A. Gonzalez-Angulo, Arch. Environ. Health, 37(4), 231(1982). |
| 6) | E. Loeser and M. H. Litchfield, Food Chem. Toxicol., 21(6), 825(1983). |
| 7) | E. Carbonell, M. Puig, N. Xamena, A. Creus and R. Marcos, Mutat. Res. 263(1), 57(1991). |
| 連絡先 | |||
| 試験責任者: | 益森勝志 | ||
| 試験担当者: | 板倉真由実,菊池正憲,梶原玲子,鈴木ゆみ子 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Shoji Masumori(Study director) Mayumi Itakura, Masanori Kikuchi, Reiko Kajihara, Yumiko Suzuki | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-Pyo Center) | ||||
| 582-2 Arahama, Shioshinden, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||