2-(4-モルホリニルジチオ)ベンゾチアゾールのラットを用いる
経口投与簡易生殖毒性試験
Preliminary Reproduction Toxicity Screening Test
of 2-(4-Morpholinyldithio)benzothiazole by Oral Administration in Rats
要約
2-(4-モルホリニルジチオ)ベンゾチアゾールのラットを用いる経口投与簡易生殖毒性試験を行い,雌雄動物に対する毒性影響を検討するとともに,性腺機能,交尾行動,受胎および分娩などの生殖行動に及ぼす影響について検討した.投与量は,1000 mg/kgを高用量とし,以下300および100 mg/kgとした.対照として媒体(0.5 %カルボキシメチルセルロースナトリウム水溶液)投与群を設けた.各群の使用動物数は雌雄各12例とした.
1.反復投与毒性
死亡および瀕死例は,いずれの群にも認められなかった.一般状態では,いずれの群にも異常はみられなかった.体重は,1000 mg/kg群の雄で低値,雌で妊娠期に低値がみられた.摂餌量は,交配前に300 mg/kg群の雌雄および1000 mg/kg群の雄で一過性の低値,1000 mg/kg群の雌で低値がみられた.剖検所見,器官重量および病理組織学検査において,雌雄とも投与に起因する変化はみられなかった.精子検査において,投与に起因する変化はみられなかった.
2.生殖発生毒性
発情回数,交尾率,交尾所要日数,受胎雌数,妊娠期間,分娩状態,哺育状態,受胎率,妊娠黄体数,着床数,着床率および出産率には,投与に起因する変化はみられなかった.
児動物では,総出産児数,死産児数,新生児数,性比,分娩率,児の産出率,出生率,一般状態,4日の新生児数,新生児の4日の生存率,外表異常,体重および剖検所見には投与に起因する変化はみられなかった.
以上のように,2-(4-モルホリニルジチオ)ベンゾチアゾールの無影響量は,雌雄とも300 mg/kg投与により摂餌量の一過性の低値が認められたことから雌雄とも100 mg/kg/dayと考えられる.生殖発生毒性学的な無影響量は,雌雄とも1000 mg/kg投与しても交尾能,受胎能などに影響が認められなかったことから1000 mg/kg/dayと考えられる.児動物への無影響量は,1000 mg/kg投与しても生存性および体重などに影響が認められなかったことから1000 mg/kg/dayと考えられる.
方法
1.被験物質および媒体
2-(4-モルホリニルジチオ)ベンゾチアゾールは,融点(とけ始め)が131.9 ℃,比重が1.50〜1.52であり,水に0.006 g/100 mL(20.8 ℃),メタノールに0.39 g/100 mL(23.2 ℃),アセトンに1.93 g/100 mL(25.5 ℃),トルエンに3.90 g/100 mL(21.0 ℃)溶解する淡黄白色ペレット状物質である[Lot No.202001,純度:98.4 %,大内新興化学工業(東京)].入手後は,室温・遮光・気密条件下で保管した.投与期間終了後に被験物質を分析し,使用期間中安定であったことを確認した.
2-(4-モルホリニルジチオ)ベンゾチアゾールは,微粉砕後,0.5 %カルボキシメチルセルロースナトリウム水溶液で懸濁して調製した.なお,被験物質の調製に際して,純度による換算を実施した.2〜200 mg/mLの調製液は,冷蔵・遮光条件下で7日間保存後,さらに室温・遮光条件下で24時間保存しても安定性に問題のないことが確認されている.各濃度の調製液は,週1回以上の頻度で調製し,調製後7日以内に使用した.雄投与開始日および雄投与終了日に使用した投与検体中の被験物質濃度を測定した結果,被験物質の濃度および均一性に問題はなかった.
2.使用動物および飼育条件
8週齢のSprague-Dawley系雌雄ラット[Crj:CD (SD)IGS,SPF]を日本チャールス・リバーから購入した.入手した動物は,5日間の検疫期間およびその後7日間の馴化期間を設け,一般状態および体重推移に異常がみられず,また性周期観察で異常が認められなかった動物(発情期が認められ,4日あるいは5日周期と考えられた動物)を群分けした.群分けは,コンピュータを用いて体重を層別に分けた後に,無作為抽出法により各群の平均体重および分散がほぼ等しくなるように投与開始日に行った.
動物は,室温20〜26 ℃,湿度40〜70 %,明暗各12時間(照明:午前6時〜午後6時),換気回数12回/時に維持されている飼育室で飼育した.検疫・馴化期間中はステンレス製ケージを用いて1ケージ当たり5匹までの群飼育とし,群分け後はステンレス製ケージを用いて個別飼育した.母動物は,妊娠18日以降オートクレーブ処理した床敷(サンフレーク,日本チャールス・リバー)を入れたプラスチック製ケージで個別飼育し,自然分娩および哺育させた. 飼料は,固型飼料(CRF-1,オリエンタル酵母工業)を自由に摂取させた.飲料水は,水道水を自由に摂取させた.
3.投与経路,投与方法,投与量および投与期間
投与経路は経口投与を選択した.投与に際しては,金属製経口胃ゾンデを取り付けたポリプロピレン製ディスポーザブル注射筒を用いて,強制経口投与した.投与液量は,雄では投与日あるいは投与日に最も近い測定日の体重を基準とし,5 mL/kgで算出した.雌では,交配前および交配期間中は投与日あるいは投与日に最も近い測定日の体重を,妊娠期間中には妊娠0,7,14および21日の体重を,授乳期間中には哺育0日の体重を基準とし,5 mL/kgで算出した.投与回数は1日1回とした.投与開始日の週齢は雌雄とも10週齢であり,体重範囲は雄が351〜387 g,雌が235〜259 gであった.
予備試験(投与段階:0,250,500および1000 mg/kg,各群雄5例)において,1000 mg/kg投与により体重の低値傾向および摂餌量の低値がみられた.そこで,当試験の投与量は,1000 mg/kgを高用量とし,以下公比約3により300および100 mg/kgとした.また,対照として媒体(0.5 %カルボキシメチルセルロースナトリウム水溶液)のみを同容量投与する群を設けた.各群の使用動物数は,雌雄各12例とした.
投与期間は,雄では交配前14日間とその後36〜38日間の合計50〜52日間とし,雌では交配前14日間,交配期間中(最長9日間),妊娠期間中および哺育3日までの合計41〜49日間とした.なお,投与開始日を投与1日とした.
4.観察および検査項目
1) 一般状態
一般状態および死亡の有無は,投与前・後の1日2回観察した.
2) 体重測定
雄の体重は,1週間に2回測定した.雌の体重は,交配開始前14日間および交配期間中は1週間に2回,妊娠期間中は妊娠0,7,14および21日に,哺育期間中は哺育0および4日に測定した.
3) 摂餌量測定
雄の摂餌量は,交配開始前14日間および交配期間終了後から1週間に2回測定した.
雌の摂餌量は,交配開始前14日間までは1週間に2回測定した.また,妊娠期間中は妊娠1,8,15および20日に,哺育期間中は哺育4日に測定した.
4) 雄の剖検および器官重量測定
雄は,最終投与の翌日(投与51〜53日)にジエチルエーテル麻酔下で腹大動脈から放血致死させた後に剖検した.精巣,精巣上体および精巣上体尾部は重量を測定した.なお,各器官重量(精巣上体尾部を除く)を最終体重で除して相対重量も算出した.精巣および精巣上体は,ブアン液で2〜3時間固定後,10 %中性緩衝ホルマリンに再固定した.
5) 精子検査
(1) 精子原液の調製
右精巣上体の尾部は,37 ℃に加温した精子培養液(0.5 %牛血清アルブミン加Mediumu 199)中で分割し,約5分間静置後,精子原液を作製した.この精子原液を用いて精子の活動性,精子の生存性および精子の形態の各検査を実施した.
(2) 精子の活動性
精子原液を精子培養液で希釈し,約30分間培養(培養条件:37 ℃,5 %炭酸ガス,95 %空気)後に精子希釈液をサンプルチャンバー(MICROSLIDES, #HTR1099, VitroCom)に入れ,TOX IVOS(Hamilton Thorne Research)を用いて,運動精子率,前進精子率,基準点移動速度,最短距離移動速度,総移動速度,精子頭部の振幅および精子頭部の横切り回数を算出した.
(3) 精子の生存性
精子原液をCalcein acetoxy methyl esterとEthidium homodimer-1で二重染色(炭酸ガス培養器内で約2時間培養)後,蛍光顕微鏡下で精子を生存精子,培養途中死亡精子および死滅精子とに分類し1),生存精子率および生き残り精子率を求めた.
(4) 精子の形態
精子原液をスライドガラスに塗抹し,10 %中性緩衝ホルマリンで固定後,1 %エオジン染色液で染色した.顕微鏡下で精子の形態を観察し,総奇形精子率,頭部の奇形精子率および尾部の奇形精子率を求めた.
(5) 精子数
精子数は,左精巣上体尾部を凍結(-80 ℃)保存後,0.1 % Triton X-100中でホモジナイズして作製した精子懸濁液をTOX IVOS(Hamilton Thorne Research)を用いて算出した.なお,左精巣上体尾部1 g当たりの精子数も算出した.
6) 親動物の生殖発生
雌の性周期は,投与開始日から交尾確認日まで毎日1回観察した.
14日間投与した雌雄を同一群内で1対1に組み合わせて同居交配した.交配期間は14日を限度として,交尾を確認するまでの連続同居交配とした.
交尾確認は毎朝ほぼ一定時刻に行い,腟垢内に精子または腟栓を確認した雌を交尾動物として,その日を妊娠0日として起算した.
交尾雌は自然分娩させ,分娩状態の異常の有無,分娩終了の確認を妊娠21日から妊娠25日の午前10時まで毎日行った.午前10時に分娩が終了していた場合,その日を哺育0日とした.
母動物は,哺育状態を哺育4日まで毎日観察した.
7) 母動物の剖検および器官重量測定
母動物は,哺育4日にジエチルエチルエーテル麻酔下で腹大動脈から放血致死させた後に剖検し,妊娠黄体数および着床数を算定した.卵巣および子宮は重量を測定した.なお,各器官重量を最終体重で除して相対重量も算出した.卵巣は,10 %中性緩衝ホルマリンで固定した.
8) 病理組織学検査
対照群および1000 mg/kg群の雄について,精巣および精巣上体の頭部のHE染色組織標本を作製し,病理組織学検査を実施した.対照群および1000 mg/kg群の雌について,卵巣のHE染色組織標本を作製し,病理組織学検査を実施した.
9) 児動物(F1)
出産時に総出産児数と性,死産児数,新生児数および外表異常の有無を観察した.児動物は,一般状態および死亡の有無を毎日1回観察した.体重は,哺育0日(出生日)および4日に測定した.生存児は,哺育4日にジエチルエーテル麻酔下で腹大動脈から放血致死させた後に剖検した.
5.統計解析
有意差検定は以下に示したように,対照群と各投与群の間で行い,危険率を5 %とした.
体重,摂餌量,器官の絶対重量および相対重量,精子検査成績,発情回数,交尾所要日数,妊娠期間,妊娠黄体数,着床数,着床率,総出産児数,新生児数,死産児数,分娩率,児の産出率,出生率,4日の新生児数,新生児の4日の生存率,外表異常の出現率および性比は,各群で平均値および標準偏差を算出した.その後,Bartlett法による等分散性の検定を行い,等分散の場合にはDunnett法により行った.一方,等分散と認められなかった場合は,順位を利用したDunnett型の検定法により行った.
交尾率,受胎率および出産率は,χ2検定により行った.
結果
1.反復投与毒性
1) 一般状態
(1) 雄
死亡および瀕死例は,いずれの群にも認められなかった.
一般状態において,いずれの群にも異常はみられなかった.
(2) 雌
死亡および瀕死例は,いずれの群にも認められなかった.
一般状態において,いずれの群にも異常はみられなかった.
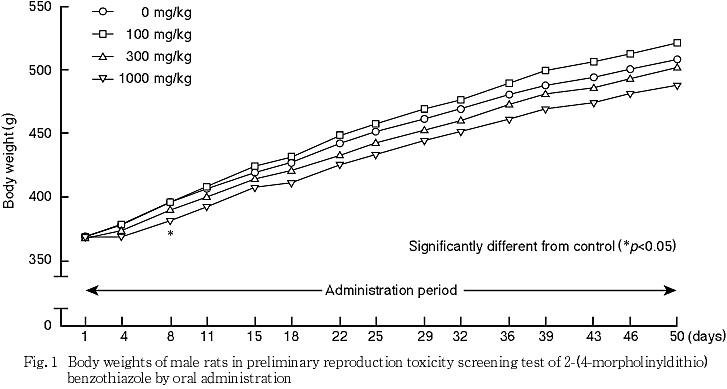
2) 体重(Fig. 1および2)
(1) 雄
100および300 mg/kg群では,対照群と比べて各測定日の体重に有意差はみられなかった.1000 mg/kg群では,対照群と比べて投与期間を通して体重は低値で推移し,投与8日に有意な低値がみられた.
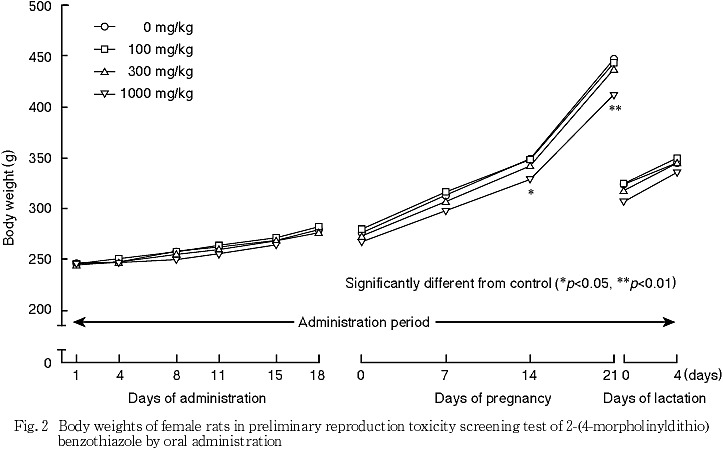
(2) 雌
交配開始前および交配期間中には,各投与群とも対照群と比べて各測定日の体重に有意差はみられなかった.
妊娠期間中には,100および300 mg/kg群では対照群と比べて各測定日の体重に有意差はみられなかった.1000 mg/kg群では,対照群と比べて妊娠14および21日に体重の有意な低値がみられた.
哺育期間中には,各投与群とも対照群と比べて各測定日の体重に有意差はみられなかった.
3) 摂餌量(Fig. 3および4)
(1) 雄
100 mg/kg群では,対照群と比べて投与9日に摂餌量の有意な高値がみられたが,投与量に関連した変化ではなかった.300および1000 mg/kg群では,対照群と比べて投与2日に摂餌量の有意な低値がみられた.
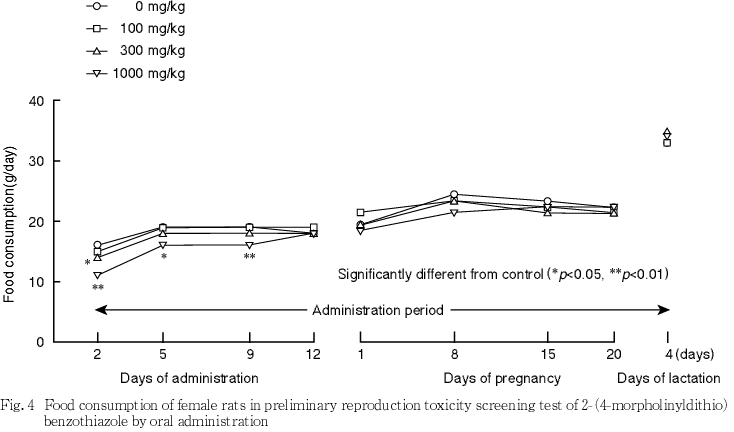
(2) 雌
交配開始前には,100 mg/kg群では対照群と比べて各測定日の摂餌量に有意差はみられなかった.300 mg/kg群では,対照群と比べて投与2日に摂餌量の有意な低値がみられた.1000 mg/kg群では,対照群と比べて投与2,5および9日に摂餌量の有意な低値がみられた.
妊娠期間中および哺育期間中には,各投与群とも対照群と比べて各測定日の摂餌量に有意差はみられなかった.

4) 剖検
(1) 雄
対照群,100および300 mg/kg群では,異常はみられなかった.1000 mg/kg群では,精巣上体(左)に黄白色結節が1例にみられたが,偶発所見と考えられる.
(2) 雌
いずれの群とも,異常はみられなかった.
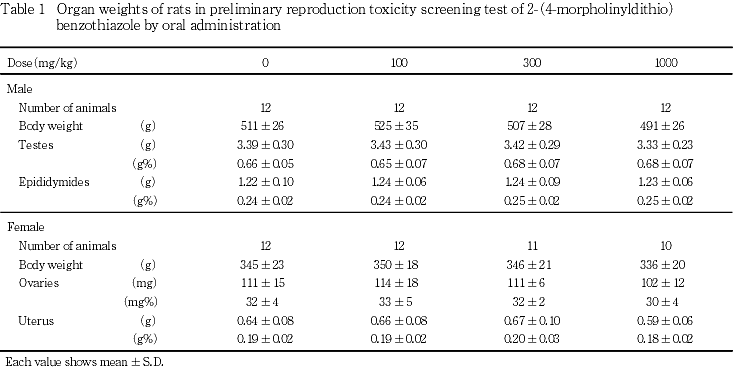
5) 器官重量(Table 1)
(1) 雄
剖検日の体重において,各投与群とも対照群と比べて有意差はみられなかった.
器官重量において,各投与群とも対照群と比べて各器官の絶対重量および相対重量に有意差はみられなかった.
(2) 雌
剖検日の体重において,各投与群とも対照群と比べて有意差はみられなかった.
器官重量において,各投与群とも対照群と比べて各器官の絶対重量および相対重量に有意差はみられなかった.
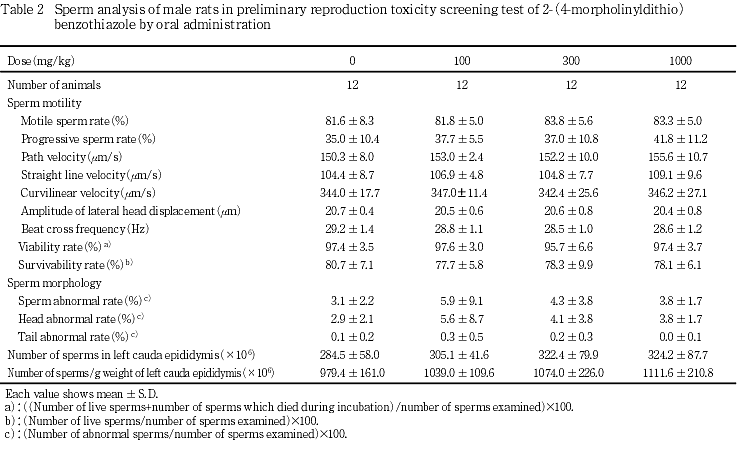
6) 精子検査(Table 2)
各投与群とも,対照群と比べて各検査項目に有意差はみられなかった.
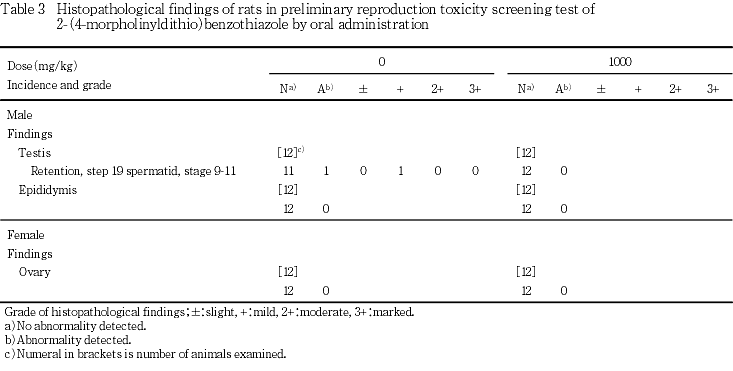
7) 病理組織学検査(Table 3)
(1) 雄
精巣:対照群では,Stage 9-11の精細管での精子細胞(Step 19)の残留が1例にみられた.1000 mg/kg群では,異常はみられなかった.
精巣上体:対照群および1000 mg/kg群とも,異常はみられなかった.
(2) 雌
卵巣:対照群および1000 mg/kg群とも,異常はみられなかった.
2.生殖発生毒性
1) 親動物の生殖発生
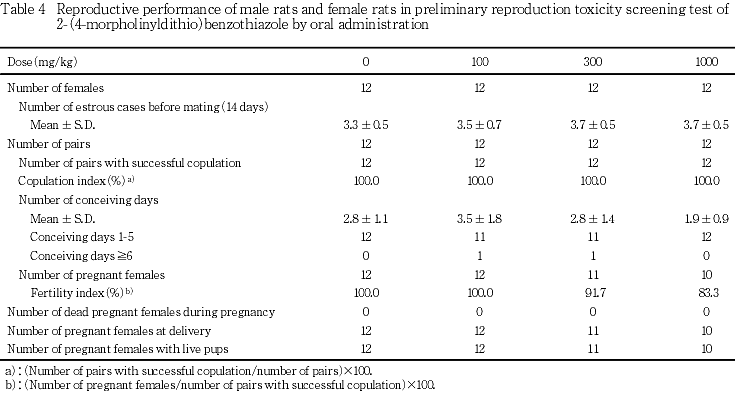
(1) 発情回数,交尾率,受胎雌数および受胎率(Table 4)
交配開始前の投与期間の発情回数は,各投与群とも対照群と比べて有意差はみられなかった.
交尾率は,いずれの群とも100 %であった.交尾所要日数は,各投与群とも対照群との間に有意差はみられなかった.受胎率は,各投与群とも対照群との間に有意差はみられなかった.
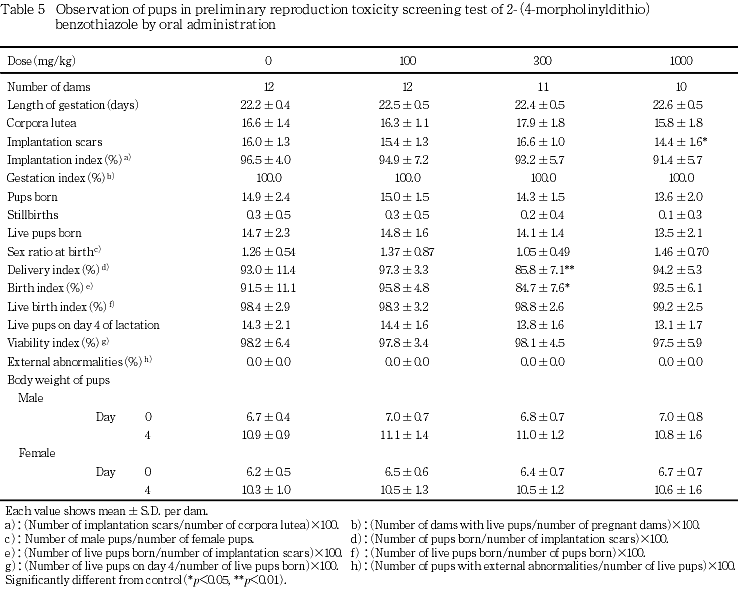
(2) 妊娠期間,分娩状態,妊娠黄体数,着床率および出産率(Table 5)
妊娠期間は,各投与群とも対照群と比べて有意差はみられなかった.
分娩状態において,いずれの群とも母動物に異常はみられなかった.
100および300 mg/kg群では,対照群と比べて妊娠黄体数,着床数および着床率に有意差はみられなかった.1000 mg/kg群では,対照群と比べて着床数の有意な低値がみられたが,妊娠黄体数および着床率に有意差は認められなかった.なお,1000 mg/kg群の着床数は,当試験施設の背景データの範囲内にあること,ならびに当試験の対照群の妊娠黄体数が若干多かったため,それに伴い着床数が多かったことにより生じた変化と考えられ,投与に基づくものではないと判断される.
出産率は,いずれの群とも100 %であった.
哺育状態において,いずれの群とも異常はみられなかった.
2) 児動物(F1)に及ぼす影響
(1) 分娩率および出生率(Table 5)
100および1000 mg/kg群では,対照群と比べて総出産児数,死産児数,新生児数,性比,分娩率,児の産出率および出生率に有意差はみられなかった.300 mg/kg群では,対照群と比べて分娩率および児の産出率の有意な低値がみられたが,投与量に関連した変化ではなかった.
(2) 児動物の一般状態および生存率(Table 5)
各投与群とも,対照群と比べて4日の新生児数および新生児の4日の生存率に有意差はみられなかった.
新生児の外表異常は,いずれの群にもみられなかった.
児動物の一般状態において,いずれの群とも異常はみられなかった.
(3) 児動物の体重(Table 5)
各投与群とも,対照群と比べて哺育0および4日の雌雄体重に有意差はみられなかった.
(4) 児動物の剖検
いずれの群とも,異常はみられなかった.
考察
2-(4-モルホリニルジチオ)ベンゾチアゾールのラットを用いる経口投与による簡易生殖毒性試験を行い,雌雄動物に対する毒性影響を検討するとともに,性腺機能,交尾行動,受胎および分娩などの生殖行動に及ぼす影響について検討した.
死亡および瀕死例は,雌雄ともいずれの群にも認められなかった.一般状態では,雌雄ともいずれの群にも異常はみられなかった.体重は,1000 mg/kg群の雄でほぼ投与期間を通して低値,雌で妊娠期に低値がみられた.摂餌量は,交配前に300 mg/kg群の雌雄および1000 mg/kg群の雄で一過性の低値,1000 mg/kg群の雌で低値がみられた.剖検,器官重量および病理組織学検査において,雌雄とも投与に起因する変化はみられなかった.精子検査において,投与に起因する変化はみられなかった.
親動物の生殖発生では,発情回数,交尾率,交尾所要日数,受胎率,出産率,分娩状態,哺育状態,妊娠黄体数,着床数,着床率および妊娠期間に投与に起因する変化はみられなかった.
児動物では,総出産児数,死産児数,新生児数,性比,分娩率,児の産出率,出生率,一般状態,4日の新生児数,新生児の4日の生存率,外表異常,体重および剖検所見に投与に起因する変化はみられなかった.
以上のように,2-(4-モルホリニルジチオ)ベンゾチアゾールの無影響量は,雌雄とも300 mg/kg投与により摂餌量の一過性の低値が認められたことから雌雄とも100 mg/kg/dayと考えられる.生殖発生毒性学的な無影響量は,雌雄とも1000 mg/kg投与しても交尾能,受胎能などに影響が認められなかったことから1000 mg/kg/dayと考えられる.児動物への無影響量は,1000 mg/kg投与しても生存性および体重などに影響が認められなかったことから1000 mg/kg/dayと考えられる.
文献
| 1) | Kato M et al.: Evaluation of mitochondrial function and membrane integrity by dual fluorescent staining for assessment of sperm status in rats. J Toxicol Sci, 27: 11-18(2002). |
| 連絡先 |
| 試験責任者: | 古橋忠和 |
| 試験担当者: | 長瀬孝彦,内藤一嘉,藤村高志,
岡田雅昭,小澤雅代,小山内志保 |
| (株)日本バイオリサーチセンター羽島研究所 |
| 〒501-6251 岐阜県羽島市福寿町間島6-104 |
| Tel 058-392-6222 | Fax 058-392-1284 | |
| Correspondence |
| Authors: | Tadakazu Furuhashi(Study director)
Takahiko Nagase, Kazuyoshi Naito,
Takashi Fujimura, Masaaki Okada,
Masayo Ozawa, Shiho Osanai |
| Nihon Bioresearch Inc. |
| 6-104, Majima, Fukuju-cho, Hashima, Gifu, 501-6251, Japan |
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | |









