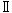 栄研 7,栄研化学)と尿自動分析装置(US-2100,栄研化学)を用いて検査した.尿沈渣は,沈渣を尿沈渣染色液(新Sternheimer法,国際試薬)で染色後に顕微鏡下で観察した.なお,採尿は,当日の投与前に行った.
栄研 7,栄研化学)と尿自動分析装置(US-2100,栄研化学)を用いて検査した.尿沈渣は,沈渣を尿沈渣染色液(新Sternheimer法,国際試薬)で染色後に顕微鏡下で観察した.なお,採尿は,当日の投与前に行った.
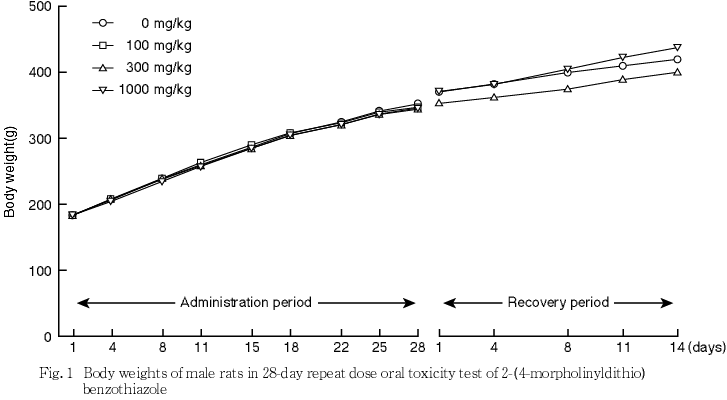
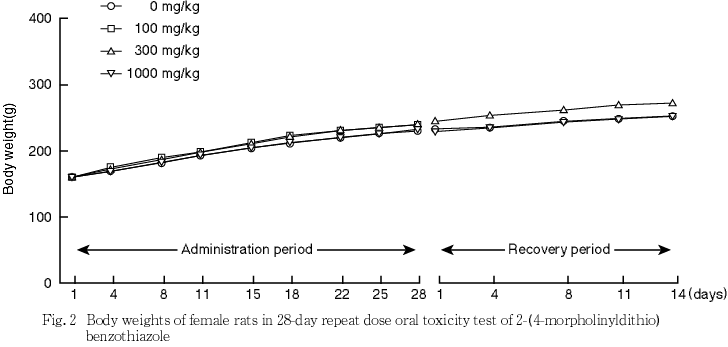
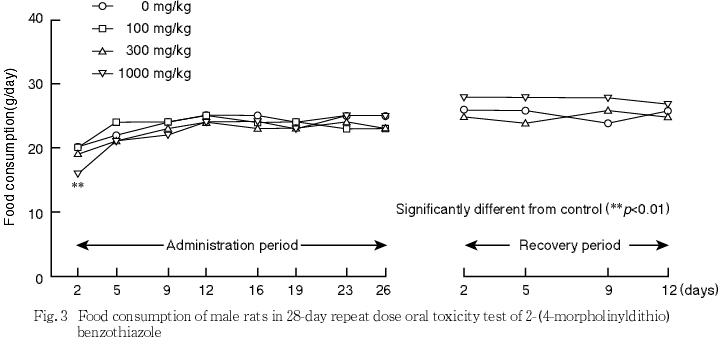
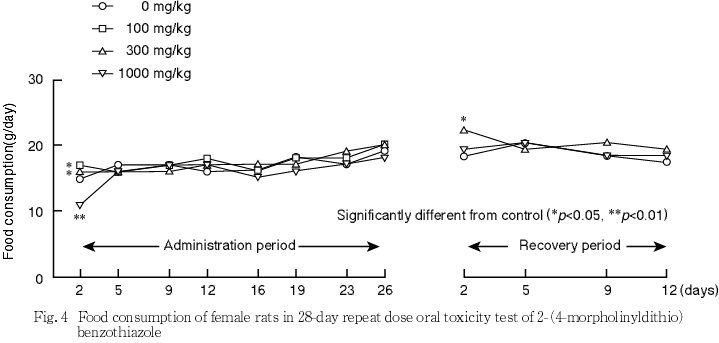
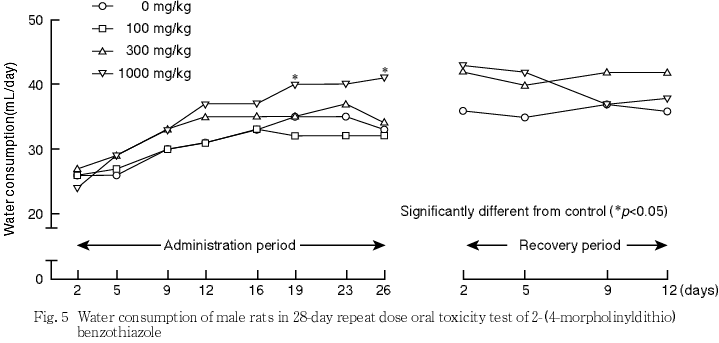
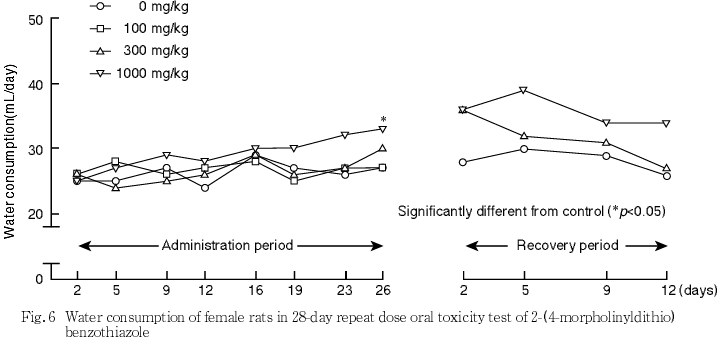
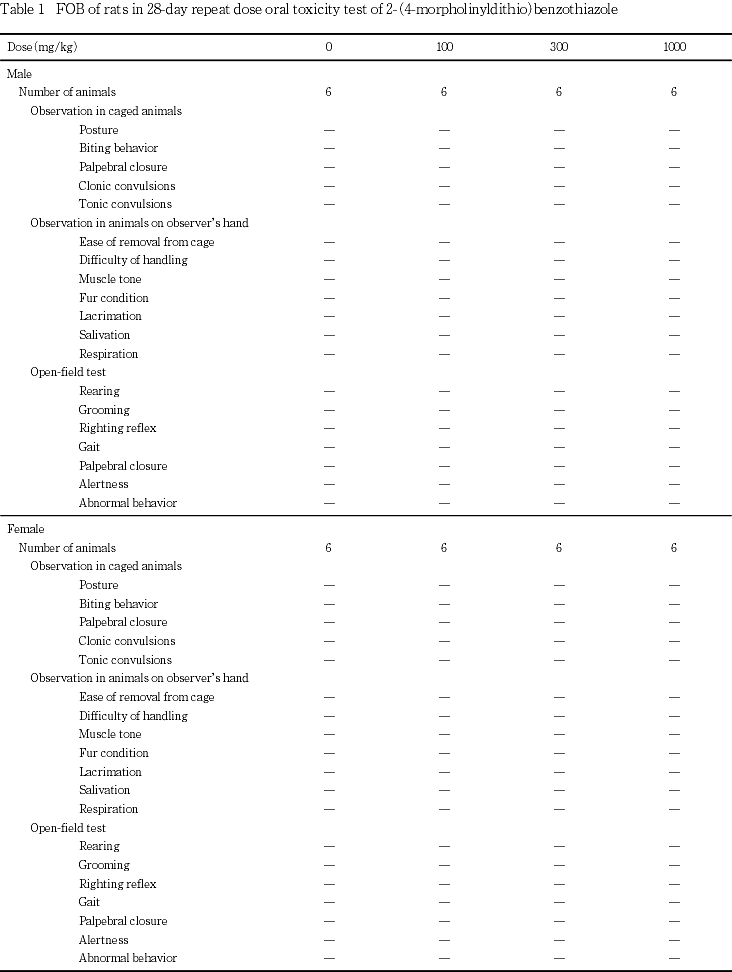
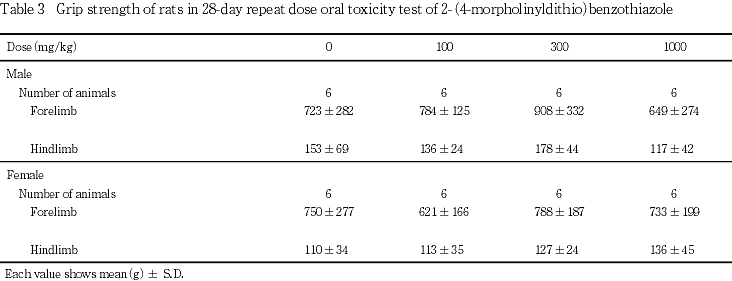
死亡および瀕死例は,いずれの群にも認められなかった.一般状態では,いずれの群にも異常はみられなかった.体重では,投与に起因する変化はみられなかった.摂餌量は,1000 mg/kg群の雌雄で一過性の低値がみられた.摂水量は,1000 mg/kg群の雌雄で一過性の高値がみられた.行動機能(FOB),感覚反応,握力,自発運動量,尿検査,血液学検査および血液生化学検査において,投与に起因する変化はみられなかった.
剖検において,いずれの群にも異常はみられなかった.器官重量において,300 mg/kg群の雌ならびに1000 mg/kg群の雌雄で肝臓の絶対重量の高値傾向および相対重量の高値がみられた.回復期間終了時には,雌雄とも肝臓の重量変化はみられなかった.病理組織学検査では,投与に起因する変化はみられなかった.
以上のように,2-(4-モルホリニルジチオ)ベンゾチアゾールの無影響量は,雄では1000 mg/kg投与により摂餌量の一過性の低値ならびに肝臓の絶対重量および相対重量の高値傾向あるいは高値が認められたことから300 mg/kg/day,雌では300 mg/kg投与により肝臓の絶対重量および相対重量の高値傾向あるいは高値が認められたことから100 mg/kg/dayと考えられる.
2-(4-モルホリニルジチオ)ベンゾチアゾールは,微粉砕後,0.5 %カルボキシメチルセルロースナトリウム水溶液で懸濁して調製した.なお,被験物質の調製に際して,純度による換算を実施した.2〜200 mg/mLの調製液は,冷蔵・遮光条件下で7日間保存後,さらに室温・遮光条件下で24時間保存しても安定性に問題のないことが確認されているため,各濃度の調製液は,週1回以上の頻度で調製し,調製後7日以内に使用した.雄投与開始日および雄投与終了日に使用した投与検体中の被験物質濃度を測定した結果,被験物質濃度および均一性に問題はなかった.
動物は,室温20〜26 ℃,湿度40〜70 %,明暗各12時間(照明:午前6時〜午後6時),換気回数12回/時に維持されている飼育室で飼育した.検疫・馴化期間中はステンレス製ケージを用いて1ケージ当たり5匹までの群飼育とし,群分け後はステンレス製ケージを用いて個別飼育した.飼料は,固型飼料(CRF-1,オリエンタル酵母工業)を自由に摂取させた.飲料水は,水道水を自由に摂取させた.
各群の動物数は,対照群,300および1000 mg/kg群では投与期間終了時剖検例雌雄各6例と回復期間終了時剖検例雌雄各6例の雌雄各12例,100 mg/kg群では投与期間終了時剖検例雌雄各6例とした.
予備試験(投与段階:0,250,500および1000 mg/kg,各群雄5例)において,1000 mg/kg投与により体重の低値傾向および摂餌量の低値がみられた.そこで,当試験の投与量は,1000 mg/kgを高用量とし,以下公比約3により300および100 mg/kgとした.また,対照として媒体(0.5 %カルボキシメチルセルロースナトリウム水溶液)のみを同容量投与する群を設けた.
投与期間は,28日間連続投与とした.また,28日間の投与後に対照群,300および1000 mg/kg群について14日間の回復期間を設けた.なお,投与開始日を投与1日とし,最終投与の翌日を回復1日とした.
(a)姿勢,かみつき行動,眼瞼閉鎖状態および痙攣はケージ内で観察した.
(b)ケージからの出し易さ,扱い易さ,筋の緊張,毛の状態,流涙,流涎および呼吸は手に持って観察した.
(c)立ち上がり回数,毛づくろい回数,正向反射,歩行状態,眼瞼閉鎖状態,覚醒度および行動異常はオープンフィールド内で観察した.
新鮮尿:色調は,外観判定とした.pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンは,尿検査試験紙(ウロペーパー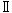 栄研 7,栄研化学)と尿自動分析装置(US-2100,栄研化学)を用いて検査した.尿沈渣は,沈渣を尿沈渣染色液(新Sternheimer法,国際試薬)で染色後に顕微鏡下で観察した.なお,採尿は,当日の投与前に行った.
栄研 7,栄研化学)と尿自動分析装置(US-2100,栄研化学)を用いて検査した.尿沈渣は,沈渣を尿沈渣染色液(新Sternheimer法,国際試薬)で染色後に顕微鏡下で観察した.なお,採尿は,当日の投与前に行った.
24時間尿:尿量は,比重と重量から算出した.比重は,屈折率により屈折型尿比重計(ユリペット-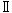 D,ニコン)を用いて測定した.
D,ニコン)を用いて測定した.
赤血球数(RBC),ヘモグロビン,ヘマトクリット,血小板数および白血球数(WBC)は,EDTA-2K処理した血液について,多項目自動血球計数装置(Sysmex K-4500,シスメックス)を用いて測定した.さらに,平均赤血球容積(MCV),平均赤血球血色素量(MCH)および平均赤血球血色素濃度(MCHC)を算出した.
網状赤血球比率は,EDTA-2K処理した血液をBrecher法により超生体染色後,Giemsa染色標本を作製して顕微鏡下で赤血球1000個中の網状赤球数を計数して算出した.
白血球百分率は,EDTA-2K処理した血液のMay-Giemsa染色標本を作製して顕微鏡下で白血球100個を分類計数して算出した.
プロトロンビン時間(PT),活性化部分トロンボプラスチン時間(APTT)およびフィブリノーゲンは,3.13 %クエン酸ナトリウムで処理後,遠心分離(約4 ℃,3000 rpm,15分間)して得た血漿について,散乱光検出方式により血液凝固分析装置(コアグマスター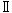 ,三共)を用いて測定した.
,三共)を用いて測定した.
ASTはMDH-UV法,ALTはLDH-UV法,ALPはρ-ニトロフェニルリン酸基質法,γ-GTPはL-γ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法,総蛋白はBiuret法,総ビリルビンは安定化ジアゾニウム塩法,尿素窒素はウレアーゼ・GlDH法,クレアチニンはクレアチニナーゼ・F-DAOS法,ブドウ糖はヘキソキナーゼ・G-6-PDH法,総コレステロールはCOD・HDAOS法,トリグリセライドはGPO・HDAOS法,Caはο-CPC法,無機リンはPNP・XDH法,Na,KおよびClはイオン選択電極法により,いずれも生化学自動分析装置(AU 400,オリンパス光学工業)を用いて測定した.
アルブミンは総蛋白および蛋白分画[電気泳動法,自動電気泳動装置(AES 310,オリンパス光学工業)]から,A/G(アルブミン/グロブリン)は蛋白分画から算出した.
回復期間終了時剖検例において,1000 mg/kg群の雄で副腎重量の高値が認められたため,回復期間終了時剖検例の対照群および1000 mg/kg群の雄の副腎についても同様に検査した.
体重,摂餌量,摂水量,握力,自発運動量,尿量,尿比重,血液学検査成績,血液生化学検査成績および器官の絶対および相対重量は,各群で平均値および標準偏差を算出した.その後,Bartlett法による等分散性の検定を行い,等分散の場合にはDunnett法により行った.一方,等分散と認められなかった場合は,順位を利用したDunnett型の検定法により行った.
一般状態において,いずれの群にも異常はみられなかった.
一般状態において,いずれの群にも異常はみられなかった.

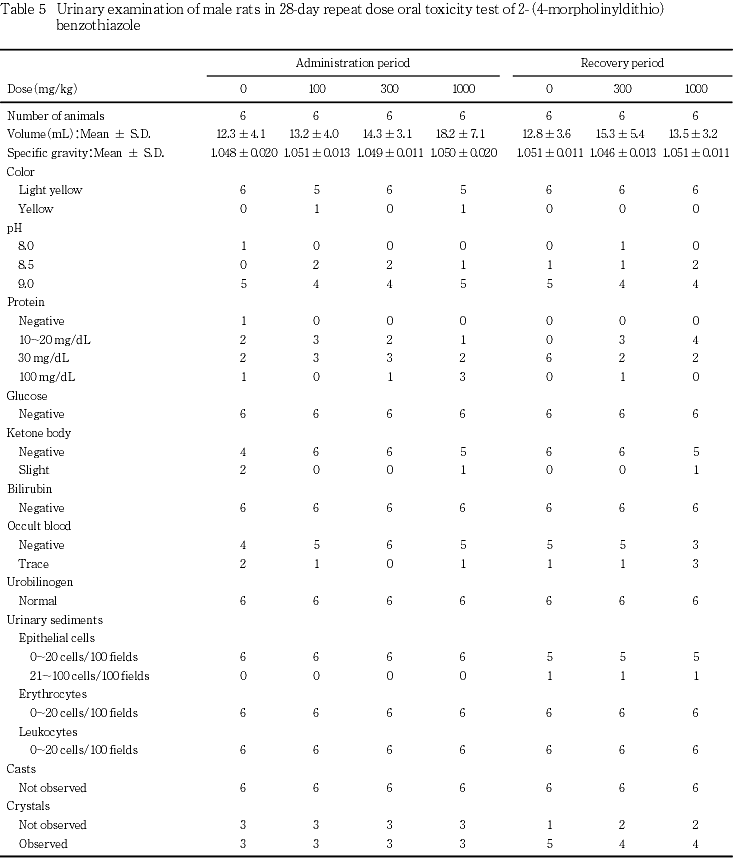
色調,pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンおよび沈渣は,各投与群とも対照群とほぼ同程度であった.
色調,pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンおよび沈渣は,各投与群とも対照群とほぼ同程度であった.
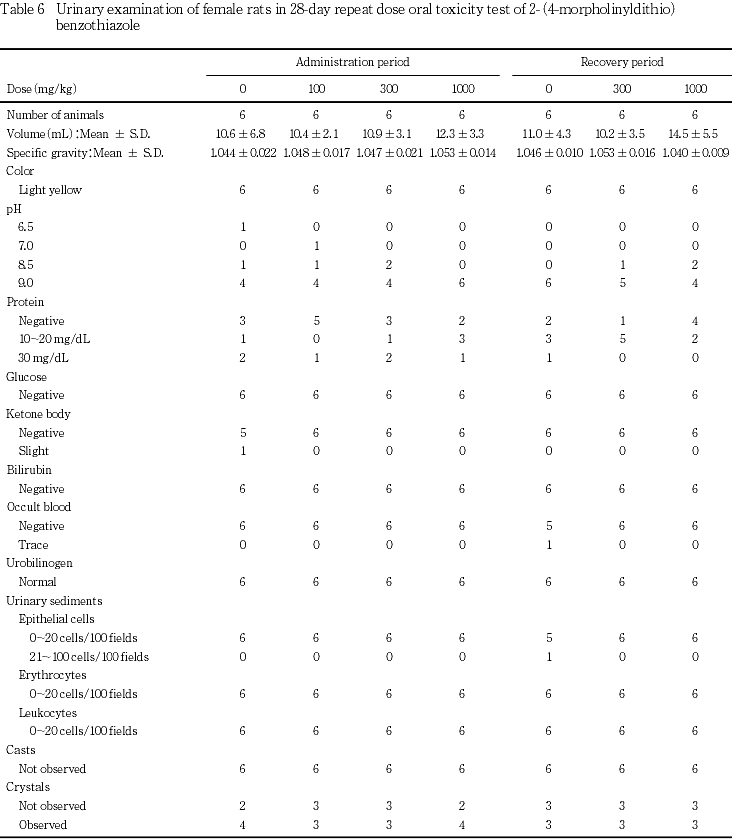
色調,pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンおよび沈渣は,各投与群とも対照群とほぼ同程度であった.
色調,pH,蛋白質,ブドウ糖,ケトン体,ビリルビン,潜血,ウロビリノーゲンおよび沈渣は,各投与群とも対照群とほぼ同程度であった.
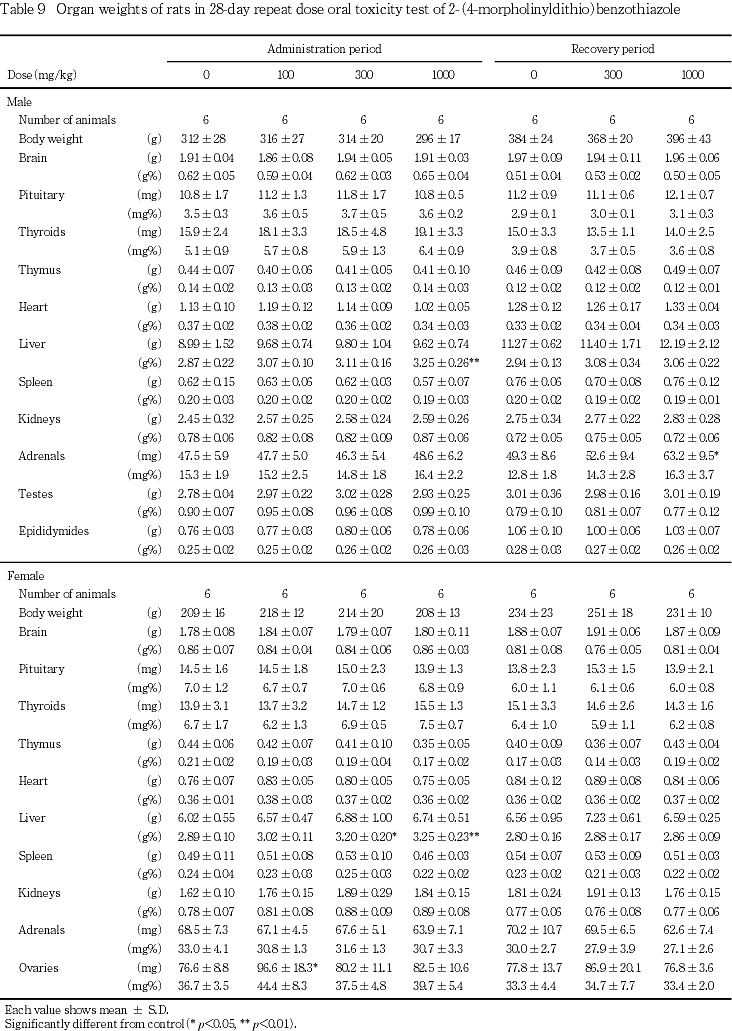
器官重量において,100および300 mg/kg群では対照群と比べて各器官の絶対および相対重量に有意差はみられなかった.1000 mg/kg群では,対照群と比べて肝臓の相対重量の有意な高値,有意差はないものの肝臓の絶対重量の高値傾向がみられた.
器官重量において,100 mg/kg群では対照群と比べて卵巣の絶対重量の有意な高値がみられたが,投与量に関連した変化ではないことから,投与に基づく変化ではないと判断される.300および1000 mg/kg群では,対照群と比べて肝臓の相対重量の有意な高値,有意差はないものの肝臓の絶対重量の高値傾向がみられた.
器官重量において,300 mg/kg群では対照群と比べて各器官の絶対および相対重量に有意差はみられなかった.1000 mg/kg群では,対照群と比べて副腎の絶対重量の有意な高値,有意差はないものの副腎の相対重量の高値傾向がみられた.
器官重量において,各投与群とも対照群と比べて各器官の絶対および相対重量に有意差はみられなかった.
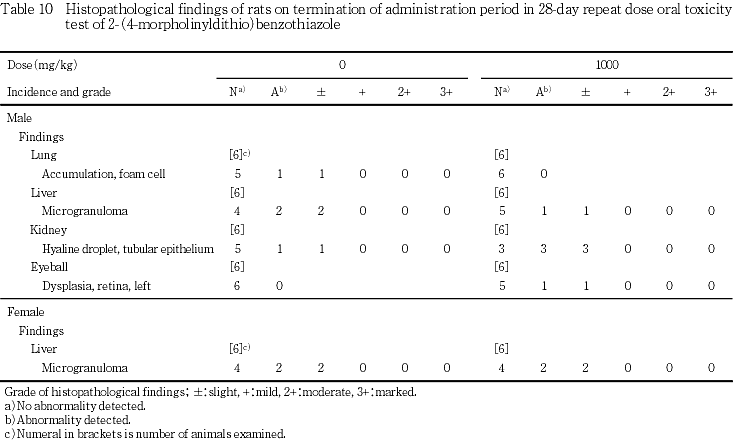
肝臓:対照群では,微小肉芽腫が2例にみられた.1000 mg/kg群では,微小肉芽腫が1例にみられた.
腎臓:対照群では,尿細管上皮の硝子滴が1例にみられた.1000 mg/kg群では,尿細管上皮の硝子滴が3例にみられた.
眼球:1000 mg/kg群では,左網膜に異形成が1例にみられた.
なお,これらの変化は,対照群でも通常観察される変化であることから,偶発的変化と判断される.
なお,この変化は,対照群でも通常観察される変化であることから,偶発的変化と判断される.
死亡および瀕死例は,いずれの群にも認められなかった.一般状態では,いずれの群にも異常はみられなかった.体重では,投与に起因する変化はみられなかった.摂餌量は,1000 mg/kg群の雌雄で一過性の低値がみられた.また,2-(4-モルホリニルジチオ)ベンゾチアゾールのラットを用いる簡易生殖毒性試験1)においても,1000 mg/kg群の雌雄で摂餌量の低値が認められている.摂水量は,1000 mg/kg群の雌雄で一過性の高値がみられた.
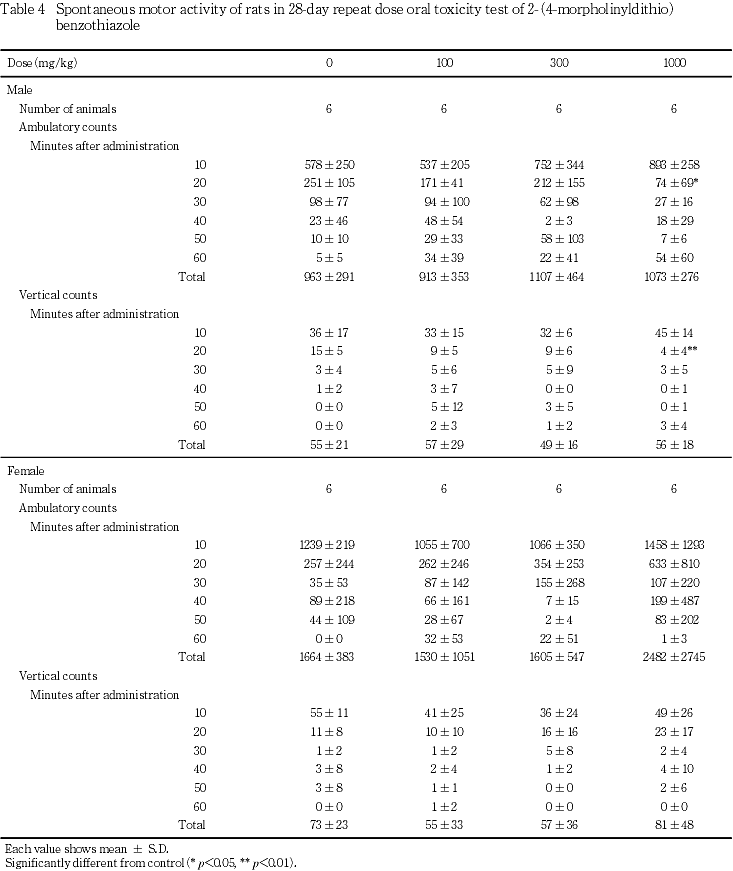
行動機能(FOB),感覚反応,握力および自発運動量では,投与に起因する変化はみられなかった.
尿検査において,投与に起因する変化はみられなかった.
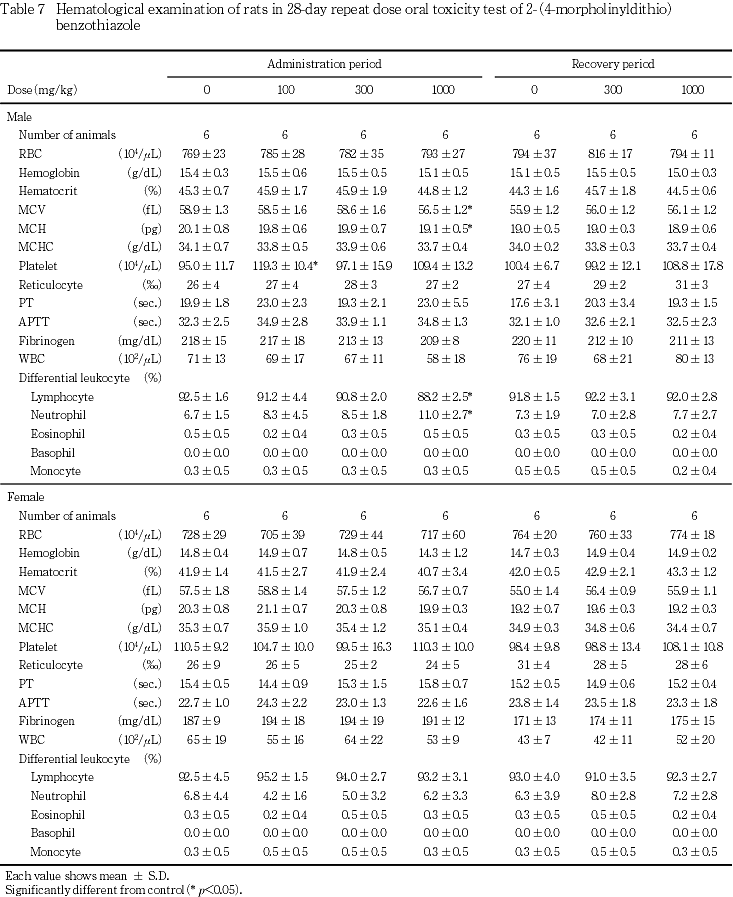
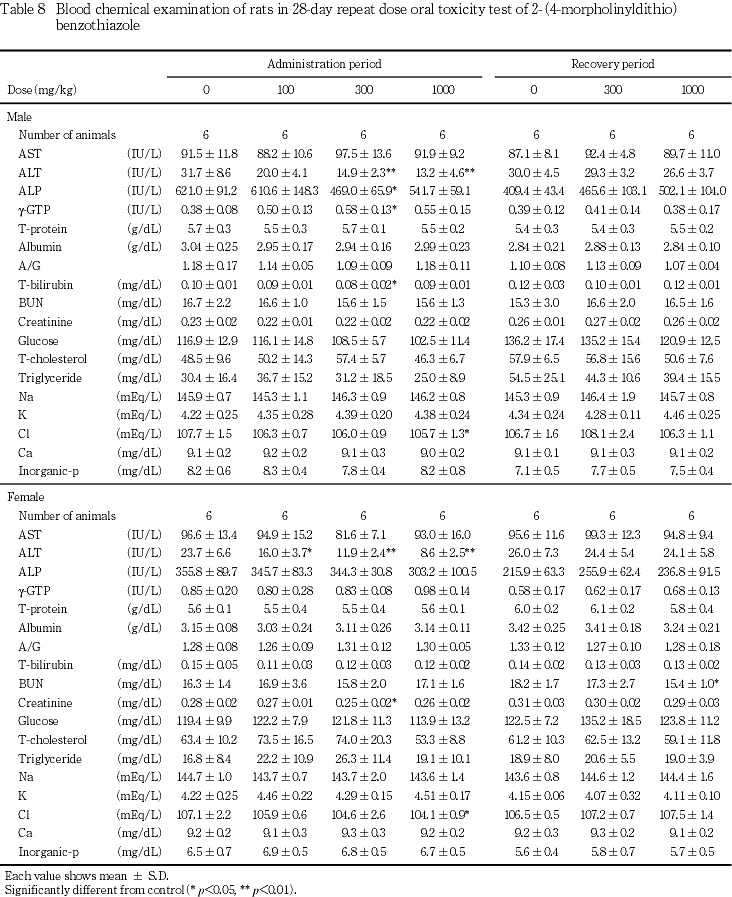
血液学検査において,投与に起因する変化はみられなかった.
血液生化学検査において,100 mg/kg群の雌,300および1000 mg/kg群の雌雄でALTの低値がみられたが,回復期間終了時には異常は認められなかった.類似化学物質N,N-ジシクロヘキシル-2-ベンゾチアゾールスルフェンアミド2)およびN-シクロヘキシル-2-ベンゾチアゾールスルフェンアミド3)でも,ラットにおいてALTの低値が同様に認められている.また,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミド4)は,ラットではALT活性の測定系に干渉するとの報告がある.そこで,ラット血清に2-(4-モルホリニルジチオ)ベンゾチアゾールを添加し,37 ℃で2時間インキュベーションした結果,同物質を添加しない血清に比べてALT活性は明らかに低値であり,2-(4-モルホリニルジチオ)ベンゾチアゾールはALT測定系に何らかの干渉作用があると考えられる.したがって,当試験におけるALTの低値は,毒性学的意義は小さいと考えられ,特に問題とすべき変化ではないと判断される.
剖検において,いずれの群にも異常はみられなかった.
器官重量において,300 mg/kg群の雌ならびに1000 mg/kg群の雌雄で肝臓の絶対重量の高値傾向および相対重量の高値がみられた.回復期間終了時には,雌雄とも肝臓の重量変化はみられなかった.雌雄における肝臓の相対重量の高値および絶対重量の高値傾向は,病理組織学的影響がみられなかったことから,軽微な変化と考えられる.なお,回復期間終了時に1000 mg/kg群の雄で認められた副腎の絶対重量の高値および相対重量の高値傾向は,病理組織学的影響がみられなかったこと,投与期間終了時には副腎の重量変化は認められなかったことから,投与に起因するものではないと考えられる.
病理組織学検査では,投与に起因する変化はみられなかった.
以上のように,2-(4-モルホリニルジチオ)ベンゾチアゾールの無影響量は,雄では1000 mg/kg投与により摂餌量の一過性の低値ならびに肝臓の絶対重量および相対重量の高値傾向あるいは高値が認められたことから300 mg/kg/day,雌では300 mg/kg投与により肝臓の絶対重量および相対重量の高値傾向あるいは高値が認められたことから100 mg/kg/dayと考えられる.
| 1) | 古橋忠和ら:2-(4-モルホリニルジチオ)ベンゾチアゾールのラットを用いる経口投与簡易生殖毒性試験.化学物質毒性試験報告,11:96-104(2004). |
| 2) | 伊藤義彦ら:N,N-ジシクロヘキシル-2-ベンゾチアゾールスルフェンアミドのラットを用いる反復経口投与毒性試験・生殖発生毒性併合試験.化学物質毒性試験報告,3:443-453(1996). |
| 3) | 伊藤義彦ら:N-シクロヘキシル-2-ベンゾチアゾールスルフェンアミドのラットを用いる28日間反復経口投与毒性試験.化学物質毒性試験報告,5:195-204(1997). |
| 4) | 長尾哲二ら:N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドのラットを用いる反復経口投与毒性・生殖発生毒性併合試験.化学物質毒性試験報告,5:163-175(1997). |
| 連絡先 | |||
| 試験責任者: | 古橋忠和 | ||
| 試験担当者: | 長瀬孝彦,内藤一嘉,藤村高志, 岡田雅昭,木村 均,吉島賢一, 伊藤 格 | ||
| (株)日本バイオリサーチセンター羽島研究所 | |||
| 〒501-6251 岐阜県羽島市福寿町間島6-104 | |||
| Tel 058-392-6222 | Fax 058-392-1284 | ||
| Correspondence | ||||
| Authors: | Tadakazu Furuhashi(Study director) Takahiko Nagase, Kazuyoshi Naito, Takashi Fujimura, Masaaki Okada, Hitoshi Kimura, Ken-ichi Yoshijima, Tadashi Itou | |||
| Nihon Bioresearch Inc. | ||||
| 6-104, Majima, Fukuju-cho, Hashima, Gifu, 501-6251, Japan | ||||
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | |||