N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドのラットを用いる
反復経口投与毒性・生殖発生毒性併合試験
Combined Repeat Dose and Reproductive/Developmental Toxicity Screening Test of
N-tert-Buthyl-2-benzothiazolesulfenamide by Oral Administration in Rats
要約
N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドは,2原子のイオウを含有するヘテロ環系化合物である.ゴム製造過程における硬化促進剤として広く使用されているため,ゴム加工に携わる労働者にとって職業的に暴露される機会の多い化学物質である1).しかし,その毒性については,ラットに対するLD50値(経口投与では 6310 mg/kg 以上,経皮投与では 7940 mg/kg 以上)およびウサギの眼刺激試験成績(軽度な刺激性)2)が報告されている程度で,中および長期に亘る反復投与毒性については明らかにされていない.
生殖発生毒性に関しては,鶏胚におけるLD50値と胚死亡および奇形の発現に関するED50値がそれぞれ 0.36 μmole/egg および 0.30 μmole/egg と報告されているが3),哺乳動物を用いた評価は行われていない.そこで,今回,OECDによる既存化学物質の安全性点検に係わる毒性調査研究事業の一環として,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの0(溶媒対照),40,200 および 1000 mg/kg を Sprague-Dawley 系(Crj:CD)ラットの雌雄(各13匹/群)に交配前2週間および交配期間2週間経口投与し,さらに雄では交配期間終了後2週間,雌では妊娠期間を通して分娩後の哺育3日まで投与を継続して,親動物に対する反復投与毒性および生殖能力ならびに次世代児の発生・発育に及ぼす影響について検討した.
その結果,雄では,200 mg/kg 以上の投与量は,投与後一過性の流涎を惹起し,1000 mg/kg 投与は,摂餌量および体重増加を抑制した.また,すべての投与群において,腎臓に eosinophilic body を認める動物の頻度が増加し,1000 mg/kg 投与群では病変の程度も増強され,腎臓重量およびその比体重値が増加した.肝臓では,200 mg/kg 以上の投与群において,小葉中心部の肝細胞に軽度な肥大が認められ,1000 mg/kg 投与群ではその程度が増強され,肝臓重量の比体重値が増加した.また,1000 mg/kg の投与により門脈周囲性の肝細胞脂肪化の減弱が認められた.さらに,200 mg/kg 以上の投与群において,総ビリルビン濃度が僅かに増加し,脾臓におけるベルリンブルー染色陽性の色素沈着が用量に依存して増強され,1000 mg/kg 投与群では,血色素量およびヘマトクリット値も僅かに減少し,溶血性貧血が惹起された.この他,1000 mg/kg 投与群では総コレステロール濃度が軽度に増加した.
雌動物では,200 mg/kg 以上の投与量は,投与後一過性の流涎を惹起し,1000 mg/kgの投与は,交配前および妊娠期の摂餌量を抑制し,妊娠初期の体重増加を軽度に抑制した.また,200 mg/kg 以上の投与群の腎臓には,近位尿細管に軽度な空胞変性が認められ,腎臓重量比体重値が軽度に増加した.また,200 mg/kg 以上の投与群の肝臓では,小葉中心部肝細胞が軽度に肥大するものが増加し,1000 mg/kg 投与群では肝臓重量比体重値が増加した.1000 mg/kg 投与群の脾臓には,褐色色素の沈着が増強する傾向が認められたが,ベルリンブルー染色陽性色素の沈着は対照群と同程度であった.
一方,生殖発生毒性に関しては,1000 mg/kg までのN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドを投与しても,交尾および排卵に影響は認められなかったが,対照群と比較して有意差はなかったものの,40 mg/kgおよび 1000 mg/kg 投与群の受胎率が低値を示した.200 mg/kg 投与群の動物は全例が受胎したことから,40 mg/kg 投与群の変化は偶発的変化であると判断されるが,1000mg/kg 投与群については投与との関連性の有無は不明であった.分娩異常および哺育異常はいずれの投与群にも認められなかった.出生児の生存性,性比および体重には影響は認められず,形態異常も観察されなかった.
これらのことから本試験条件下では,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの反復投与毒性に関する無影響量は,雄では40 mg/kg/dayを下回る量であり,雌では40 mg/kg/dayであると結論される.また,生殖発生毒性に関する無影響量は,雌雄ともに 200 mg/kg/dayであると結論される.
方法
1.被験物質
N-tert-ブチル-2-ベンゾチアゾールスルフェンアミド〔融点:104℃,ロット番号:509067,純度:96.4%(主な不純物:ジベンゾチアジルジスルフィド,0.99%)〕は,帯黄灰白色ペレットである.本被験物質は,大内新興化学工業(株)から入手し,使用時まで密封,冷蔵条件下で保管した.
被験物質は,5%アラビアゴム〔日本薬局方アラビアゴム末:宮澤薬品(株),ロット番号:JD03,日本薬局方注射用水:三亜製薬(株),製造番号:DH004〕に懸濁して,いずれの用量においても1回の投与液量が 5 ml/kg になるように含量を調整し,投与液とした.投与液は,冷蔵,遮光条件下で保管し,調製後7日以内に投与した.投与液中の被験物質は,室温,遮光条件下で少なくとも7日間安定であることを確認した.また,使用した投与液を振盪攪拌した後には,所定量のN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドが均一に含有されていたことを確認した.
2.使用動物および飼育条件
試験には,雌雄とも7週齢にて購入した日本チャールズリバー(株)日野飼育センター生産の Sprague-Dawley 系(Crj:CD,SPF)ラットを使用した.動物は,入荷後1週間,馴化と検疫を兼ねて予備飼育し,一般状態に異常が認められなかったものを試験に供した〔群分け時体重範囲:雄 268.4〜305.2 g,雌 174.4〜204.1 g〕.
各動物は,基準温湿度24±1 ℃および50〜65%,換気回数約 15 回/時間,照明 12 時間(午前7時〜午後7時)に制御された飼育室で,金属製金網床ケージ(日本ケージ)に個別に収容して飼育し,固型飼料(CE-2,日本クレア)および飲料水を自由に摂取させた.妊娠14日(精子観察日=妊娠0日)以後の雌動物は,ラット用繁殖ケージ(35 × 40 × 18 cm,日本クレア(株))に収容し,床敷として紙パルプ製チップ(ALPHA-dri,加商(株))を適宜供給した.
3.群分け
雌雄とも初回投与日の体重をもとに体重別層化無作為抽出法に準じて群分けし,各群とも雌雄各13匹を配した.
4.投与量,群構成,投与期間および投与方法
投与量は,先に実施した14日間反復経口投与による予備試験において,250 mg/kg 以上は雌に対して,また,500 mg/kg 以上は雄に対して変化を惹起したが,最高用量の 1000 mg/kg を投与しても瀕死あるいは死亡に至る動物が認められなかったので,本試験においてもこれを最高用量とし,以下公比5で減じ,中間用量には 200 mg/kg,最低用量には 40 mg/kg を設定した.対照群のラットには,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの媒体とした5%アラビアゴムを投与群と同一条件で投与した.各用量の投与検体は,雄に対しては交配前14日間と交配期間14日間および交配期間終了後14日間の連続42日間,また,雌に対しては交配前14日間と最長14日間の交配期間中(交尾まで)ならびに交尾雌では妊娠期を通して分娩後の哺育3日(分娩日=哺育0日)まで毎日1回,ラット用胃管を用いて経口投与した.毎日の投与は,原則として一定時刻の間(通常13時〜15時)に行い,各動物の投与液量(5 ml/kg)は,雄ならびに交配前および交配期間中の雌については週1回の測定体重をもとに,また,交尾成立後の雌については妊娠0日(交尾確認日)の体重をもとにそれぞれ算定した.
5.観察方法
1) 親動物
A.一般状態
雌雄とも,全例について試験期間中毎日観察した.
B.体重
雌雄とも,全例について体重を試験期間中週1回〔雄:投与1,8,15,22,29,36,42日,雌:投与1,8,15日〕および解剖日に測定し,投与22日までに交尾しなかった雌は,投与22日にも体重を測定した.また,交尾成立雌では,妊娠0,7,14,20日,分娩した雌では,哺育0および4日(解剖日)に体重を測定した.
C.摂餌量
雌雄とも,全例について体重測定日と同日に餌重量を測定し,摂餌量を算定した.2週間の交配期間中の摂餌量は測定しなかった.交尾成立雌では妊娠0〜7,7〜14,14〜20日,分娩した雌では哺育0〜4日の摂餌量を測定した.
D.交配
交配は,投与15日(投与開始日=投与1日)の夕方から最長2週間,同群内の雌雄を1対1 で同居させて行った.交尾成立の確認は,毎朝,腟栓および腟垢中の精子の存在を調べることにより行い,交尾が確認された雌は,その日を妊娠0日と起算して雄から分離し,個別に飼育した.交配結果から,各群について交尾率〔交尾動物数/同居動物数)× 100〕,受胎率〔(受胎動物数/交尾動物数)× 100〕,同居開始日から交尾確認日までの日数およびその間に回帰した発情数を求めた.
E.分娩・哺育状態
各群とも交尾成立雌は,全例を自然分娩させた.分娩状態は,直接観察が可能なものについてのみ行い,それ以外の動物については分娩後の徴候から分娩困難や遅延などの分娩障害の有無を判断した.分娩後は,哺育状態を観察した.
F.分娩日の算定
分娩の確認は,午前9時〜11時に限定し,この時間帯に分娩が完了していることを確認した動物について,その日を哺育0日と規定した.午前11時を過ぎて分娩した動物については,翌日を分娩日とした.分娩を確認した全例について妊娠期間(妊娠0日から分娩日までの日数)を算定し,出産率〔(生児出産雌数/妊娠雌数)× 100〕を各群について求めた.
G.最終検査
a) 雄動物
イ.剖検,器官重量測定および病理組織検査
最終投与日の投与終了後から絶食を開始し,翌日(投与43日相当日)にペントバルビタール麻酔下で放血・致死させて剖検した.その際,全例について肝臓,腎臓,胸腺,脾臓,精巣および精巣上体の重量を測定した.また,これらの器官のうち,精巣および精巣上体はブアン液に固定し,その他の器官ならびに脳,心臓,副腎および膀胱は,10% ホルマリン液に固定した.これらの器官のうち,肝臓,腎臓および脾臓は各群の全例について,その他の器官は,対照群および 1000 mg/kg 投与群の全例について常法に従ってパラフィン切片とし,ヘマトキシリン-エオジン染色を行って病理組織検査を行った.また,腎臓については,対照群および 1000 mg/kg 投与群の一部の動物についてperiodic acid shiff(PAS)染色を行い,脾臓については,全例についてベルリンブルー染色を行った.
ロ.血液検査
全例について,剖検に先立ち,ペントバルビタール麻酔下で腹部後大静脈より抗凝固剤として EDTA 処理した注射筒を用いて採血し,赤血球数(RBC),白血球数(WBC),血色素量(Hb),平均赤血球容積(MCV),ヘマトクリット値(Ht),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC),血小板数を多項目血液自動測定機(Coulter Counter Model S-PLUS IV)により測定し,白血球百分比は Wright-Giemsa染色を行い,光学顕微鏡下で観察して算出した.
ハ.血液生化学検査
全例について,血液検査のための採血に引き続き,抗凝固剤としてヘパリン処理した注射筒を用いて採血し,血漿を分離して遠心方式生化学自動分析装置 COBAS- FARA および全自動電解質分析装置 EA-05(A & T)を用い,総蛋白濃度(ビウレット法),アルブミン濃度(BCG 法),総コレステロール濃度(COD・DAOS 法),ブドウ糖濃度(グルコキナーゼG6PDH 法),尿素窒素濃度(ウレアーゼGl.DH 法),クレアチニン濃度(Jaff 法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT活性(SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OCPC法),無機リン濃度(モリブデン酸直接法),γ-GTP活性(γ-グルタミル-3-カルボキシ-4- ニトロアニリド基質法),ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法), A/G比(計算)について分析した.なお,GPT活性については,血清中に存在するN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドがGPT活性の測定系を干渉することが明らかとなったため,測定を実施しなかった.
法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT活性(SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OCPC法),無機リン濃度(モリブデン酸直接法),γ-GTP活性(γ-グルタミル-3-カルボキシ-4- ニトロアニリド基質法),ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法), A/G比(計算)について分析した.なお,GPT活性については,血清中に存在するN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドがGPT活性の測定系を干渉することが明らかとなったため,測定を実施しなかった.
b) 雌動物
交尾不成立雌は交配期間終了日に,交尾したが分娩しない雌は妊娠25日相当日に,それぞれ致死量のペントバルビタールを投与後に放血・致死させ,剖検した.分娩した雌は哺育4日に同様にして剖検した.妊・不妊のいずれの例においても卵巣および子宮を摘出し,子宮については Salewski 法4)を応用して着床痕を染色して着床数を確認した.卵巣は,実体顕微鏡下で黄体数を数え,ブアン液に固定して保存した.不妊例および交尾不成立例の卵巣については,病理組織検査を行った.また,肝臓,腎臓,脾臓および胸腺の重量を全例について測定した.これらの器官および脳,心臓,副腎,子宮および膀胱は 10 % ホルマリン液に固定して保存した.これらの器官のうち,肝臓,腎臓および胸腺は各群の全例について,その他の器官は,1000 mg/kg 投与群および対照群の全例について組織切片を作製し,ヘマトキシリンーエオジン染色を施して病理組織検査を行った.また,脾臓については,全例についてベルリンブルー染色を行った.
2) 出生児
A.産児数の算定
哺育0日に産児数(生存児+死亡児)を調べ,児の分娩率〔(産児数/着床痕数)×100〕および出生率〔(出産生児数/着床痕数)×100〕を求めた.また,産児の外表奇形の有無および性別を調べ,生存児の性比〔(雄の生児数/出産生児数)×100〕を算出した.
B.死亡児数の算定
死亡児数を毎日調べ,哺育0日の生存率〔(生児数/産児数)×100〕および新生児の生後4日の生存率〔(哺育4日の生児数/哺育0日の生児数)×100〕を求めた.死亡児は剖検し,胸腔および腹腔内の器官を除去した後,エタノールに固定して保存した.
C.体重測定
哺育0日および4日に一腹単位で雌雄別に体重(litter 重量)を測定し,〔litter重量/測定児数〕を各腹について求めた.
D.剖検
哺育4日に全例をエーテル吸入により致死させ,剖検した.胸腔および腹腔内の器官は一括して摘出し,一腹ごとに 10 % ホルマリン液に固定して保存した.カーカスは,一腹ごとにエタノールに固定して保存した.
6.統計解析
交尾率,受胎率および産児の形態異常発現頻度については Yates の補正を含むχ^2検定を行った.病理組織所見については,グレード分けしたデータについてはMann-Whitney のU検定5,6)により,また,陽性グレードの合計値は Fisher 直接確率の片側検定6)により対照群と各投与群との差について有意差検定を行った.その他のすべてのデータは,個体ごとに得られた値あるいは一腹ごとの平均値を1標本として,各群の分散が0より大きい場合は,先ず,Bartlett 法7)により各群の分散の一様性について検定した.その結果,分散が一様とされた場合には,一元配置型の分散分析7)を行い,群間に有意性が認められた場合には Dunnett 法8)あるいはScheff 法9)により対照群と各投与群との間で平均値の差の検定を行った.分散が一様でなかった場合,および分散が0となる群が存在するときは,Kruskal-Wallis 順位検定10)を行い,群間に有意性が認められた場合に,対照群と各投与群との差について Dunnett 法8)あるいは Scheff
法9)により対照群と各投与群との間で平均値の差の検定を行った.分散が一様でなかった場合,および分散が0となる群が存在するときは,Kruskal-Wallis 順位検定10)を行い,群間に有意性が認められた場合に,対照群と各投与群との差について Dunnett 法8)あるいは Scheff 法9)の検定を行った.有意水準は5%および1%とした.
法9)の検定を行った.有意水準は5%および1%とした.
結果
Ⅰ.反復投与毒性(親動物所見)
1) 死亡例,瀕死屠殺例,一般状態
雌雄ともにいずれの投与群にも死亡あるいは瀕死動物は認められなかった.
雌雄ともに,200 mg/kg 以上の投与群において,投与後一過性の流涎が観察された.流涎は,1000 mg/kg 投与群では,200 mg/kg 投与群と比べてより早い時期から観察され始めた.また,投与期間が進行するに従い,1000 mg/kg 投与群では投与直前から流涎を示す動物も観察された.その他の変化としては,40 mg/kg 投与群の少数例に脱毛,痂皮形成あるいは腟口周囲の血様汚染が観察された.
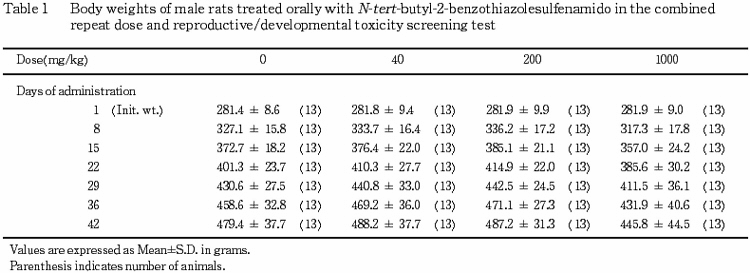
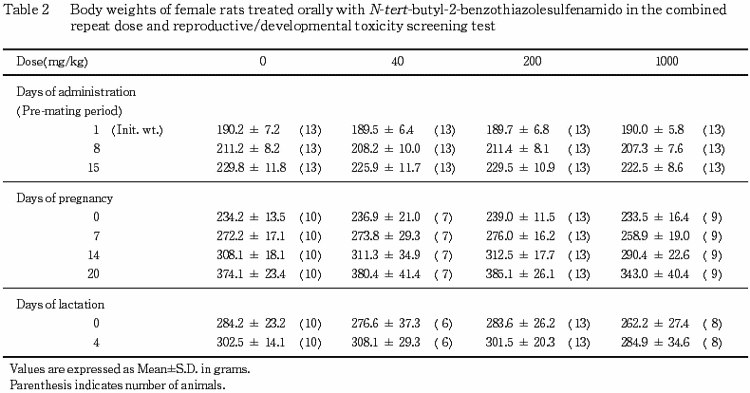
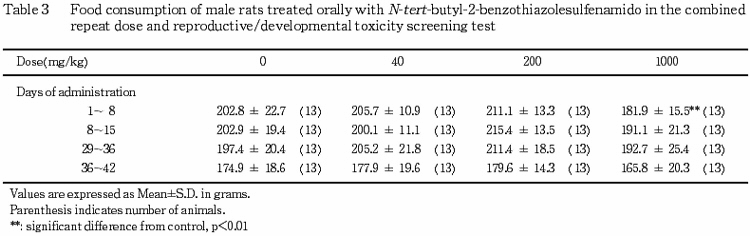
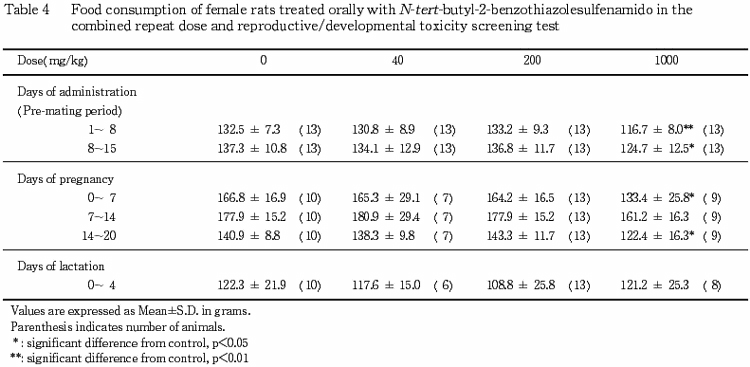
2) 体重,摂餌量(Tables 1〜6)
雄では,200 mg/kg 以下の投与群の体重推移および摂餌量には投与の影響は認められなかった.1000 mg/kg 投与群では,体重増加が軽度に抑制され,投与1〜8日の摂餌量が対照群と比較して有意(p<0.01)な低値を示した.
雌では,200 mg/kg 以下の投与群ではいずれの時期の体重および摂餌量にも対照群と比較して有意差は認められなかった.1000 mg/kg 投与群では,交配前期間および妊娠7〜14日を除く妊娠期の摂餌量が対照群と比較して有意(p<0.05,p<0.01)な低値を示し,妊娠および哺育期の体重増加に抑制傾向が認められたが,交配前の体重増加および哺育期の摂餌量は対照群と同様に推移した.
3) 解剖時検査所見
A.雄
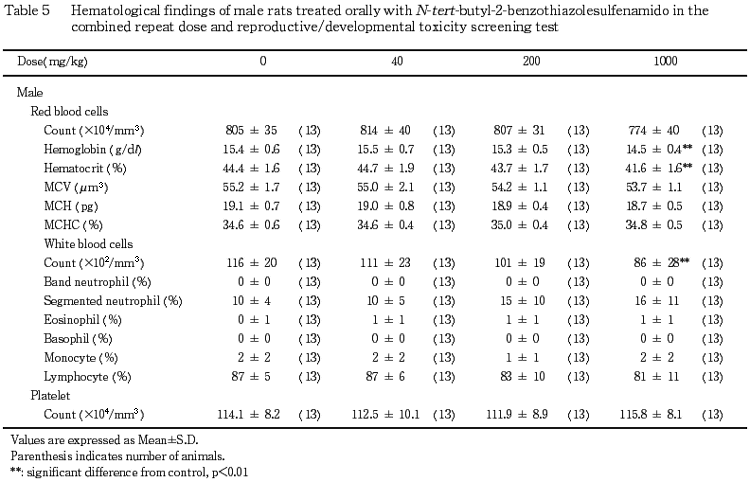
(1) 血液検査所見(Table 7)
200 mg/kg 以下の投与群では,いずれの項目にも影響は認められなかった.1000 mg/kg 投与群では,血色素量およびヘマトクリット値が,対照群と比較して有意(p<0.01)に低下した.また,赤血球数および平均赤血球容積も有意差は認められなかったが,低値の傾向を示した.このほか 1000 mg/kg 投与群では,白血球数も有意(p<0.01)に減少したが,その他の項目に有意差は認められなかった.
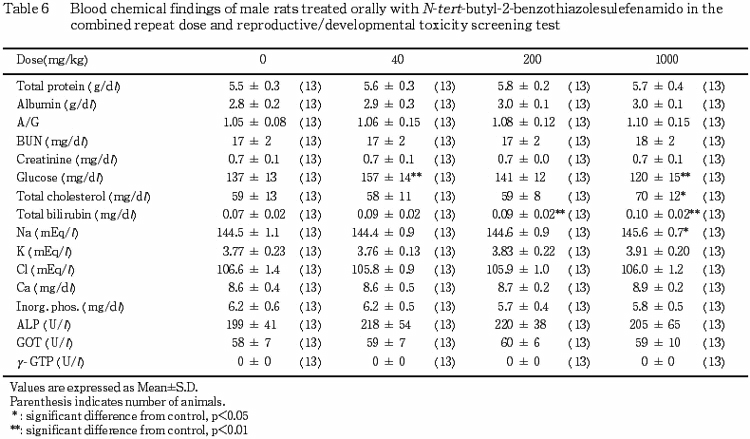
(2) 血液生化学検査所見(Table 8)
各投与群において総ビリルビン濃度が増加の傾向を示し,200 mg/kg 以上の投与群では,有意差(p<0.01)も認められた.また,1000 mg/kg 投与群では,総コレステロール濃度およびナトリウム濃度が有意(p<0.05)な高値を示した.ブドウ糖濃度は,対照群と比較して,40 mg/kg 投与群が有意な(p<0.01)高値を,また,1000 mg/kg 投与群が有意な(p<0.01)低値を示した.その他の項目には対照群と投与群との間で有意差は認められなかった.
(3) 剖検所見
肝臓では 1000 mg/kg 投与群の5例に暗色化,40 mg/kg 投与群の3例に淡色あるいは黄色化がみられた.
腎臓では 200 mg/kg 投与群の1例,1000 mg/kg 投与群の3例に淡色化が,200 および 1000 mg/kg 投与群の各1例に尿細管の明瞭化が認められた.
その他,胸腺では対照群の1例,1000 mg/kg 投与群の2例に小型化が,対照群,200および 1000 mg/kg 投与群の各1例に赤色域が認められ,腺胃については 200 mg/kg 投与群の1例の粘膜に褐色点がみられた.
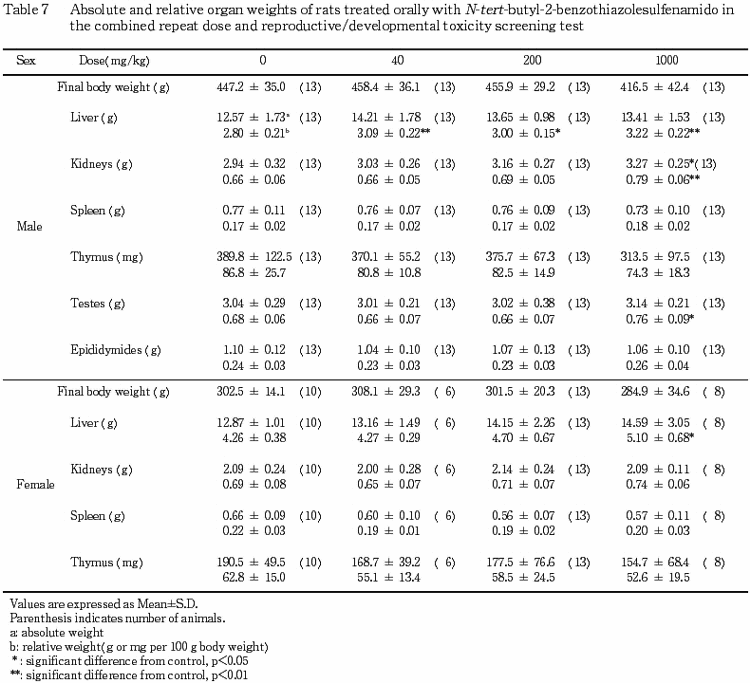
(4) 器官重量(Table 9)
すべての投与群において肝臓重量比体重値が対照群と比較して有意(p<0.05,p<0.01)に増加した.また,1000 mg/kg 投与群では,腎臓重量およびその比体重値ならびに精巣重量比体重値が有意(p<0.05,p<0.01)な高値を示した.胸腺,脾臓および精巣上体については,いずれの投与群も重量および比体重値ともに,対照群との間で有意差は認められなかった.
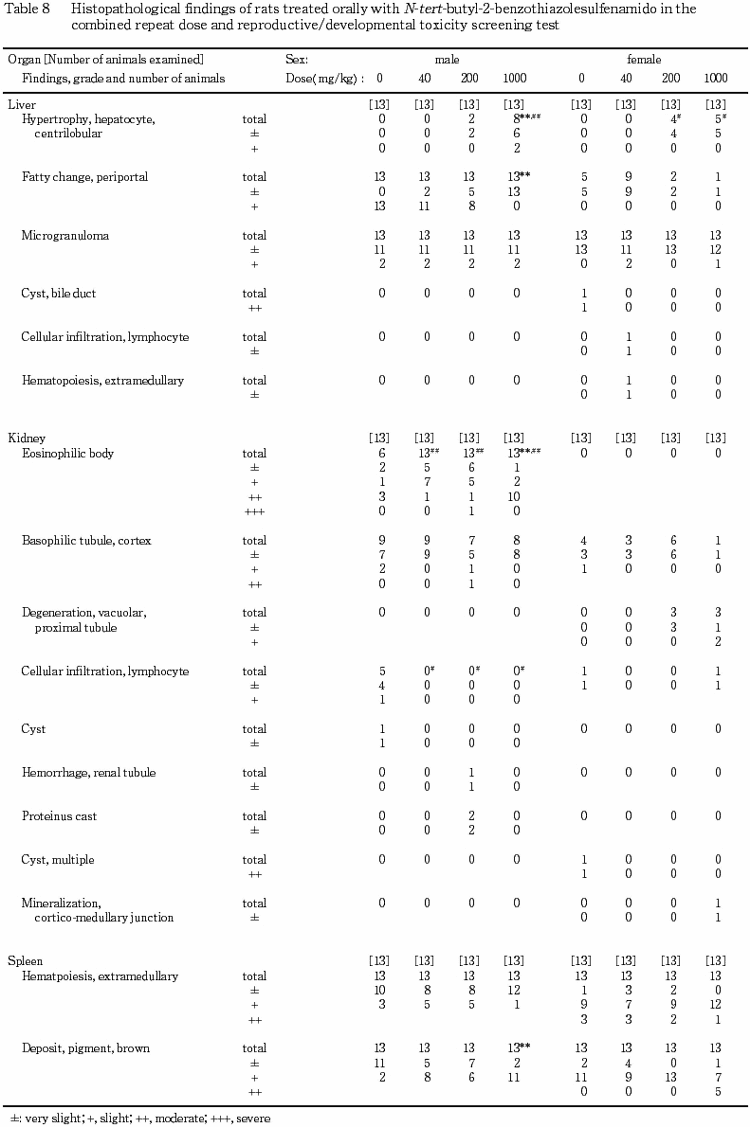
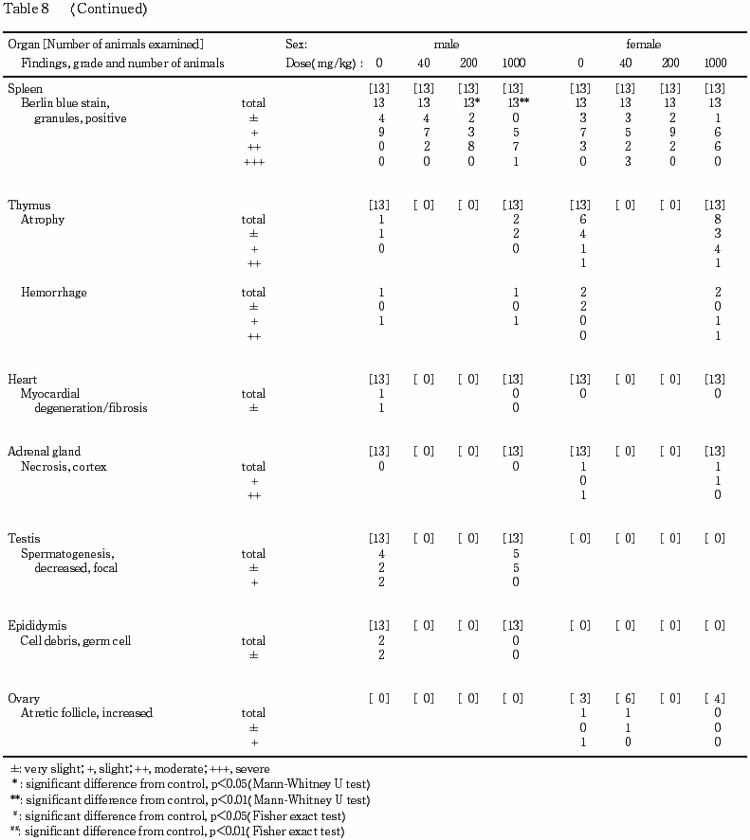
(5) 病理組織検査所見(Table 10)
各器官における観察所見を以下に示す.
(肝臓)
200 mg/kg 投与群の2例,1000 mg/kg 投与群の8例の小葉中心部に肝細胞の肥大が認められた.そのうち,1000 mg/kg 投与群の2例は,他と比較してその程度がやや強く,1000 mg/kg 投与群では,肝細胞肥大の程度および頻度ともに対照群と比較して有意(p<0.01)に増加した.また,全例に門脈周囲性の肝細胞脂肪化や小肉芽腫がみられたが,そのうち,1000 mg/kg 投与群の脂肪化の程度は,対照群と比較して軽いものであった(p<0.01).
(腎臓)
対照群の6例,各投与群の全例に eosinophilic body が認められ,その頻度はすべての投与群が対照群と比較して有意(p<0.01)に高かった.また,1000 mg/kg投与群では病変の強さも有意(p<0.01)に増強された.Eosinophilic body がみられた1000 mg/kg 投与群の3例および対照群の2例についてPAS 染色を行った結果,1000 mg/kg 投与群,対照群いずれにも陽性反応は認められなかった.また,対照群および各投与群の数例の皮質に好塩基性の尿細管がみられたが,対照群と各投与群とを比較すると,程度および頻度のいずれにも有意差は認められなかった.リンパ球浸潤が対照群の5例にのみ認められた.そのため,各投与群におけるリンパ球浸潤を示す動物の頻度が対照群と比較して有意(p<0.05)に低下した.その他,少数例に尿細管の出血,蛋白円柱あるいは嚢胞が認められた.
(脾臓)
全例に髄外造血および褐色色素の沈着がみられ,そのうち 1000 mg/kg 投与群では,対照群と比較すると褐色色素の沈着の程度が有意(p<0.01)に増強していた.ベルリンブルー染色においても同様の変化が認められ,200 mg/kg 以上の投与群においてベルリンブルー陽性の色素沈着の程度が対照群と比較して有意(p<0.05,p<0.01)に増強されていた.
(その他)
胸腺では対照群の1例,1000 mg/kg 投与群の2例に萎縮,対照群および 1000 mg/kg 投与群の各1例に出血が,心臓では対照群の1例に心筋の変性/線維化がみられ,精巣では対照群の4例,1000 mg/kg 投与群の5例に限局性に精子形成の減少がみられ,そのうち対照群の2例の精巣上体には,生殖細胞の細胞残屑が認められた.副腎および膀胱には,異常は認められなかった.
B.雌
(1) 剖検所見
肝臓では 200 mg/kg 投与群の3例,1000 mg/kg 投与群の5例に暗赤色化が認められた.また,対照群および 1000 mg/kg 投与群の各1例に淡色あるいは黄色化を伴う腫大がみられ,そのうち対照群の例では,表面が顆粒状を呈していた.
腎臓では 1000 mg/kg 投与群の5例に淡色化が認められ,対照群の1例の皮髄境界部に嚢胞が認められた.
脾臓では 200 mg/kg 投与群の1例に小型化が認められた.
その他,胸腺では 200 および 1000 mg/kg 投与群の各1例に淡色化,対照群および200 mg/kg 投与群の各1例に黒色点,40 mg/kg 投与群の1例,200 mg/kg 投与群の3例,1000 mg/kg 投与群の2例に赤色域,対照群および各投与群の数例に小型化がみられ,副腎では対照群に黄白色域,腺胃では 200 mg/kg 投与群の粘膜に褐色点,子宮では1000 mg/kg 投与群の右子宮角に淡色の結節,40 mg/kg 投与群に肥厚がそれぞれ1例認められた.
(2) 器官重量(Table 9)
40 mg/kg 投与群の哺育4日出生児生存例では,いずれの器官についても重量および比体重値ともに対照群との間に有意差は認められなかった.200 mg/kg 以上の投与群では,肝臓重量およびその比体重値が増加の傾向を示し,1000 mg/kg 投与群の比体重値が対照群と比較して有意(p<0.05)な高値を示した.1000 mg/kg 投与群では,腎臓についても比体重値が高値の傾向を示したが,対照群との間に有意差はなかった.その他の器官については重量および比体重値ともに対照群と同等であった.
交尾不成立あるいは妊娠25日相当日まで分娩しなかったため,途中剖検した動物では,1000 mg/kg 投与群の肝臓および腎臓の比体重値が高値の傾向を示した.
(3) 病理組織所見(Table 10)
各器官における観察所見を以下に示す.
(肝臓)
200 mg/kg 投与群の4例,1000 mg/kg 投与群の5例の小葉中心部に肝細胞の肥大が認められ,対照群と比較すると,その頻度はこれらの投与群で有意(p<0.05)に増加していた.また,全群の動物に門脈周囲性の肝細胞脂肪化や小肉芽腫がみられたが,対照群と各投与群との間に頻度および程度の差は認められなかった.その他,胆管の嚢胞が対照群の1例にみられ,リンパ球浸潤または髄外造血が 40 mg/kg 投与群に1例ずつみられた.
(腎臓)
200 および 1000 mg/kg 投与群の3例の近位尿細管に空胞変性がみられ,そのうち1000 mg/kg 投与群の2例は 200 mg/kg 投与群と比較してその程度がやや増強していたが,対照群と各投与群間に程度および頻度の差は認められなかった.また,対照群,各投与群共に皮質に好塩基性の尿細管がみられたが,対照群と各投与群間に程度および頻度の差は認められなかった.その他,多発性の嚢胞が対照群の1例に,皮髄境界部の鉱質沈着が 1000 mg/kg 投与群の1例に,リンパ球浸潤が対照群および 1000 mg/kg 投与群の各1例にそれぞれ認められた.
(脾臓)
全例に髄外造血および褐色色素の沈着がみられ,そのうち 1000 mg/kg 投与群では,対照群と比較すると褐色色素の沈着の程度がやや増強する傾向が認められた.しかし,ベルリンブルー染色陽性の色素の沈着については,程度および頻度に対照群と各投与群間で差は認められなかった.
(その他)
胸腺では対照群の6例,1000 mg/kg 投与群の8例に萎縮,対照群および 1000 mg/kg投与群の各2例に出血がみられ,副腎では対照群および 1000 mg/kg 投与群の各1例の皮質に壊死が認められた.心臓および膀胱には,異常は認められなかった.
不妊および未交尾の雌の卵巣では,対照群および 40 mg/kg 投与群の各1例に軽度またはごく軽度な閉鎖卵胞の増加がみられたが,その他に異常は認められなかった.
Ⅱ.生殖発生毒性
1.生殖学的検査所見
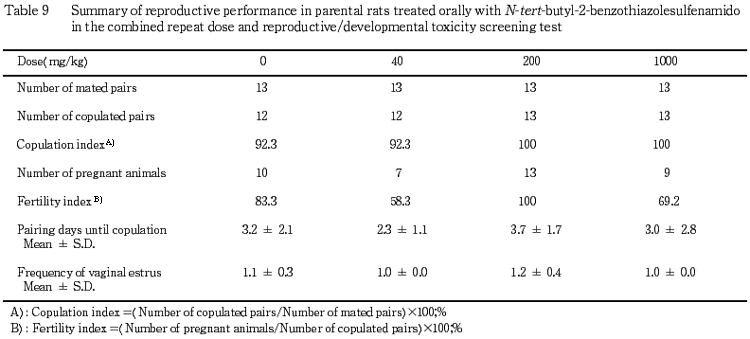
1) 交配成績(Table 11)
交尾率および同居開始から交尾成立までに要した日数ならびにその間に回帰した発情期の回数に,対照群と各投与群との間で有意差は認められなかった.受胎率については,40 mg/kg および 1000 mg/kg 両投与群が低値の傾向を示したが,対照群との間に有意差は認められなかった.200 mg/kg 投与群では,13例全例の妊娠が成立した.
2) 分娩および哺育状態
観察が可能であった動物については,分娩状態の異常は観察されなかった.
哺育状態の異常は,いずれの動物にも認められなかった.
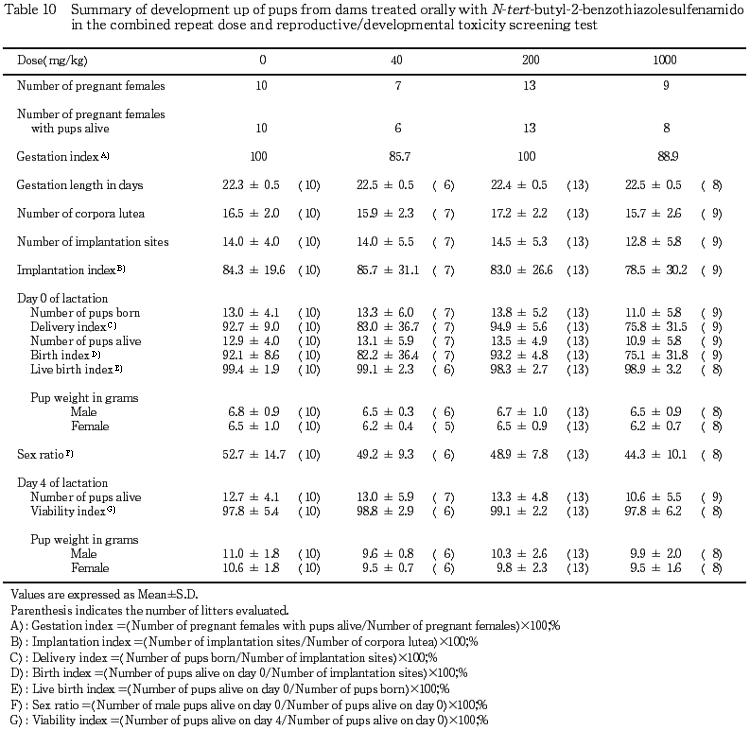
3) 出産率および妊娠期間(Table 12)
40 および 1000 mg/kg 投与群に1例ずつ全胚死亡例が認められたが,出産率および妊娠期間に対照群と各投与群の間で有意差は認められなかった.
4) 妊娠黄体数,着床数および着床率(Table 12)
妊娠動物の黄体数,着床数および着床率に対照群と各投与群との間で有意差は認められなかった.
2.産児所見
1) 一般状態および生存性(Table 12)
いずれの群の産児にも一般状態の異常は観察されなかった.
児の生存性についても,分娩率,生児出産率,出生率および哺育4日の新生児生存率には対照群と各投与群との間に有意差は認められなかった.
性比についても対照群と各投与群との間で有意差は認められなかった.
2) 体重(Table 12)
雌雄ともにいずれの投与群も,対照群と同様に推移した.
3) 形態
出生児の生存産児に,外表奇形は観察されなかった.また,哺育4日における産児の剖検においても,異常は認められなかった.死亡児の剖検では,異常はいずれの投与群にも認められなかった.
考察
病理組織検査において,雄では,すべての投与群においてeosinophilic body の形成が認められ,1000 mg/kg 投与群ではその程度に増強の傾向が認められた.Eosinophilic body は雄ラットに一般的に観察される所見であるが,各投与群においてこれを認める動物の頻度が有意に増加した.また,1000 mg/kg 投与群では,これに付随した変化として腎臓重量およびその比体重値も有意に増加した.これらのことから,eosinophilic body 形成頻度の増加はN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの影響であると考えられ,無影響量は本試験から求められなかった.このほか雄では,対照群に認められた腎臓のリンパ球浸潤が各投与群では認められなかったが,これは毒性変化ではない.雌では,200 mg/kg 以上の投与群において近位尿細管に空胞変性を呈するものが認められた.その頻度には対照群との間で有意差は認められなかったが,対照群には認められていない変化であり,1000 mg/kg 投与群ではその程度に増強の傾向が認められたことから,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの影響であると考えられる.雌の腎臓重量変化には影響は認められず,雄の血液生化学検査でも腎障害を示唆する変化は認められなかったことから,腎臓に及ぼす影響は軽度であると考えられる.
肝臓についても雌雄ともに 200 mg/kg 以上の投与群において,小葉中心部の肝細胞の肥大する例が認められた.対照群と比較すると,雌では 200 mg/kg 以上の投与群においてその頻度が有意に増加し,雄では 1000 mg/kg 投与群において頻度および程度が有意に増加したことから,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの影響と考えられる.肝臓重量比体重値は,雄ではすべての投与群において,また,雌では 1000 mg/kg 投与群において,対照群と比較して有意な増加が認められた.しかし,200 mg/kg 投与群の雄の肝臓重量比体重値は 40mg/kg 投与群のそれより低く,200 mg/kg 投与群では,肝細胞の肥大が肝臓重量比体重値の変動に反映されていなかった.これは,200 mg/kg 投与群で認められた肝細胞肥大がごく軽度に分類される程度の変化であり,その頻度も13例中2例と僅かであったことによると考えられる.従って,200 mg/kg 以下の投与群の雄に認められた肝臓重量比体重値の増加はN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドによる影響であるとは判断されなかった.また,1000 mg/kg 投与群における肝細胞の肥大もごく軽度から軽度の範囲に分類される程度の変化であり,血液生化学検査においても総コレステロール濃度の僅かな増加以外に肝臓機能に関連した測定項目の変動は認められなかったことから,肝臓に対する影響は軽度であると考えられる.このほか,1000 mg/kg 投与群では門脈周囲性の肝細胞脂肪化の程度の減弱が認められた.
雄動物について実施した血液生化学検査において,200 mg/kg 以上の投与群の総ビリルビン濃度が軽度に増加した.これらの投与群では,脾臓におけるベルリンブルー染色陽性の色素沈着の程度も増強され,さらに 1000 mg/kg 投与群では,血液検査において赤血球数が低値の傾向を示し,血色素量およびヘマトクリット値が有意に減少した.これらのことから,200 mg/kg 以上の投与は溶血を惹起し,さらに,1000 mg/kg 投与は溶血性貧血を惹起するものと考えられる.40 mg/kg 投与群については,総ビリルビン濃度は200 mg/kg 投与群と同程度の値であったが,対照群との間に有意差は認められず,脾臓の病理組織検査においても対照群との間に有意差は認められなかったことから,溶血は惹起されなかったものと考えられる.雌の病理組織検査では,1000 mg/kg 投与群の脾臓に褐色色素の沈着に増強の傾向が認められた.しかし,ベルリンブルー染色陽性の色素沈着に関しては,対照群と差は認められなかったことから,雌には溶血性の変化はなかったものと推測される.
以上のように,各器官に認められたN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの影響はいずれも軽度であったが,1000 mg/kg 投与群では雄の体重増加ならびに雌雄の摂餌量に有意な低下が認められたことから,雌雄動物に対する軽度の毒性量があると考えられた.
このほか,雄の血液検査において 1000 mg/kg 投与群の白血球数が減少したが,脾臓の病理組織検査では,白血球の産生像に異常は観察されなかった.また,白血球百分比は対照群と同様であったことから,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドとの関連性は明らかではなかった.
生殖発生毒性については,200 mg/kg 投与群では全例が交尾し,雌の全例が正常に分娩した.しかし,40 および 1000 mg/kg 両投与群では,交尾率は対照群と同程度であったが,受胎率は,対照群との間に有意差は認められなかったものの低値であった.これらの投与群において不妊であった動物は,1例を除き,いずれも交尾確認時に腟内に精子が存在することを確認している.従ってこれらの動物では精子の射入を伴う正常な交尾があったものと考えられる.1000 mg/kg 投与群では,精巣重量比体重値も増加したが,これは,同群の解剖時体重が対照群と比較して低値であったことによるもので,精巣および精巣上体の病理組織検査では,妊孕性の有無に関連した異常所見は認められなかった.また,不妊動物の卵巣にも病理組織学的異常は観察されず,本試験において40 および 1000 mg/kg 両投与群の受胎率が低値を示した原因は不明であった.しかし,200 mg/kg 投与群では全例が受胎したことから,40 mg/kg 投与群における受胎率低下はN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドによる影響であるとは考えられない.一方,1000 mg/kg 投与群の受胎率は,40 mg/kg 投与群のそれと同程度であるが,本試験における低受胎率の原因が不明であるため,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの影響は否定できなかった.分娩および哺育には影響は認められなかった.胚・胎児死亡および産児の形態異常などの増加は認められず,出生後の生存性および体重増加にも影響は認められなかった.
これらのことから本試験条件下では,N-tert-ブチル-2-ベンゾチアゾールスルフェンアミドの反復投与毒性に関する無影響量は,雄では 40 mg/kg/day を下回る量であり,雌では 40 mg/kg/dayであると推察される.また,生殖発生毒性に関する無影響量は雌雄ともに 200 mg/kg/day と推察される.
文献
| 1) | B.Holmberg,B.Sj gren,J.Toxicol.Environ.Health,6,1201(1979). gren,J.Toxicol.Environ.Health,6,1201(1979). |
| 2) | D.J. Randall,R.M. Bannister, Acute Toxicity Data in 'J. American CollegeToxicol.',1,104(1990). |
| 3) | A.Korhonen,K.Hemminki,H.Vanio,Arch.Environ.Contam.Toxicol.,11,753(1982). |
| 4) | E.Salewski,Naunyn-Schmiedeberg's Arch.Exp.Pathol.Pharmakol.,247,367(1964). |
| 5) | 丹後俊郎,"医学への統計学(古川俊之 監修)," 朝倉書店,東京,1985. |
| 6) | 石居進,"生物統計学入門," 培風館,東京,1992. |
| 7) | 佐久間昭,"薬効評価-計画と解析," 東京大学出版会,東京,1977. |
| 8) | C. W. Dunnett, Biometrics, 20, 482(1964). |
| 9) | H. Scheff , Biometrika, 40, 87(1953). , Biometrika, 40, 87(1953). |
| 10) | W. H. Kruskal, W. A. Wallis, J. Amer. Statist. Assoc., 47,583(1952). |
| 連絡先: |
| 試験責任者: | 長尾哲二 |
| 試験担当者: | 代田眞理子,松本亜紀,関誠 |
| (財)食品薬品安全センター秦野研究所 |
| 〒257 神奈川県秦野市落合729-5 |
| Tel 0463-82-4751 | Fax 0463-82-9627 | |
| Correspondence |
| Authors: | Tetsuji Nagao(Study director)
Mariko Shirota,Aki Matsumoto,
Makoto Seki |
| Hatano Research Institute,Food and Drug Safety Center |
| 729-5 Ochiai,Hadano,Kanagawa,257,Japan |
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |
 法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT活性(SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OCPC法),無機リン濃度(モリブデン酸直接法),γ-GTP活性(γ-グルタミル-3-カルボキシ-4- ニトロアニリド基質法),ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法), A/G比(計算)について分析した.なお,GPT活性については,血清中に存在するN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドがGPT活性の測定系を干渉することが明らかとなったため,測定を実施しなかった.
法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT活性(SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OCPC法),無機リン濃度(モリブデン酸直接法),γ-GTP活性(γ-グルタミル-3-カルボキシ-4- ニトロアニリド基質法),ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法), A/G比(計算)について分析した.なお,GPT活性については,血清中に存在するN-tert-ブチル-2-ベンゾチアゾールスルフェンアミドがGPT活性の測定系を干渉することが明らかとなったため,測定を実施しなかった.











 gren,J.Toxicol.Environ.Health,6,1201(1979).
gren,J.Toxicol.Environ.Health,6,1201(1979).