細胞増殖抑制試験結果をもとに,連続処理法の24時間処理で5000 μg/mL,48時間処理で3600 μg/mL,短時間処理法では5000 μg/mLを最高処理濃度とした.連続処理法は,最高処理濃度の1/2,1/4および1/8ををそれぞれ高濃度,中濃度および低濃度とした.また,短時間処理法では-S9処理で最高処理濃度の1/2および1/4をそれぞれ中濃度および低濃度として設定した.連続処理法では,S9 mix非存在下における24時間および48時間連続処理後,短時間処理法ではS9 mix存在下および非存在下で6時間処理(18時間の回復時間)後,標本を作製し,検鏡することにより染色体異常誘発性を検討した.
その結果,いずれの処理法においても倍数性細胞の誘発作用は認められなかったが,染色体構造異常の僅かな誘発傾向が観察され,連続処理法の24時間処理では陽性判定基準と同じ10 %を示した.
しかしながら明確な用量依存性が認められなかったことから,連続処理法の24時間処理において確認試験を実施した.確認試験では,最高処理濃度を3500 μg/mLとし,公差500で減じた5用量を設定した.
その結果,僅かながらも染色体構造異常の用量依存的な誘発作用が認められた.
以上の結果より,本試験条件下ではo-アセトアセトトルイジドは,染色体異常を誘発する(陽性)と結論した.
細胞を10 vol%中性緩衝ホルマリン液(和光純薬工業(株))で固定した後,0.1 w/v%クリスタル・バイオレット(関東化学(株))水溶液で10分間染色した.色素溶出液(30 vol%エタノール,1 vol%酢酸水溶液)を適量加え,5分間程度放置して色素を溶出した後,580 nmでの吸光度を測定した.各用量群について溶媒対照群での吸光度に対する比,すなわち細胞生存率を算出した.
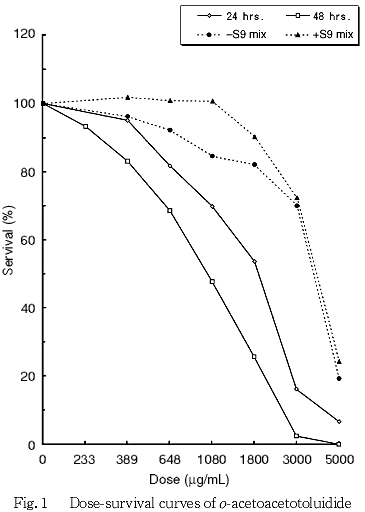
その結果,いずれの処理法においても顕著な細胞増殖抑制が観察された(Fig. 1).プロビット法を用いて算出した50 %細胞増殖抑制濃度は連続処理法24時間処理で1565 μg/mL,同48時間処理で940 μg/mL,短時間処理法-S9 mix処理で3392 μg/mLおよび同+S9 mix処理では3699 μg/mLであった.

また,連続処理法の24時間処理において明確な用量依存性は認められないものの染色体構造異常の出現頻度が10 %であったことから,確認試験を実施した.最高処理濃度を3500 μg/mLとし,公差500で減じた5用量を設定した.
なお,陽性対照として,連続処理法の場合,マイトマイシンC(MMC:協和醗酵工業(株))を,24時間処理で0.05 μg/mL,48時間処理で0.025 μg/mLの用量で,短時間処理法の場合,シクロホスファミド(CP:塩野義製薬(株))を,12.5 μg/mLの用量で試験した.
すべての標本をブラインド処理した後,観察した.
各試験群の構造異常を有する細胞あるいは倍数性細胞の出現頻度を,石館ら3)の基準に従って判定した.染色体異常を有する細胞の出現頻度が5 %未満を陰性(-),5 %以上10 %未満を疑陽性(±),10 %以上を陽性(+)とした.最終的には再現性あるいは用量に依存性が認められた場合に陽性と判定した.
なお,統計学的手法を用いた検定は実施しなかった.
短時間処理法での試験結果をTable 2に示した.被験物質処理群の場合,S9 mix非存在下および存在下のいずれにおいても,染色体構造異常の僅かな誘発傾向が観察されたが(出現頻度は9.0 %および5.0 %),倍数性細胞の誘発は認められなかった.一方,陽性対照物質のCPで処理した細胞ではS9 mix存在下でのみ染色体構造異常の顕著な誘発が認められた.
連続処理法の24時間処理において,染色体構造異常の出現頻度が1用量のみ陽性反応を示したことから確認試験を実施し,結果をTable 3に示した.被験物質処理群の場合,僅かながら染色体構造異常の用量依存的な誘発が認められた.なお,被験物質の影響により,3000 μg/mLにおいては観察可能な分裂中期像は180細胞のみであり,最高用量である3500 μg/mLでは観察可能な分裂中期像はほとんど観察されなかった.
なお,暴露終了時,連続処理法ならびに短時間処理法+S9 mix処理では最高用量で,短時間処理法-S9 mix処理では2500 μg/mL以上の用量で,粉末状被験物質が培養液中に散在しているのが観察された.
以上の試験結果から,本試験条件下においてo-アセトアセトトルイジドのチャイニーズハムスター培養細胞に対する染色体異常誘発性に関し,陽性と判定した.
| 1) | A. Matsuoka, M. Hayashi and M. Ishidate Jr., Mutat. Res., 66, 277(1979). |
| 2) | 日本環境変異原学会・哺乳動物試験分科会編,"化学物質による染色体異常アトラス,"朝倉書店,東京,1988, pp. 31-35. |
| 3) | 石館基監修,"<改訂>染色体異常試験データ集,"エル・アイ・シー社,東京,1987, pp. 19-24. |
| 連絡先 | |||
| 試験責任者: | 中嶋 圓 | ||
| 試験担当者: | 北澤倫世,益森勝志,熊平智司 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Madoka Nakajima(Study director) Michiyo Kitazawa, Shoji Masumori, Satoshi Kumadaira | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | ||||
| 582-2 Shioshinden Aza Arahama, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||