3-ヒドロキシ-2-ナフトエ酸について,マウスを用いる小核試験を実施した.
用量設定試験結果をもとに,BDF1系雄マウスに125, 250および500 mg/kgの3用量を1日1回2日間連続して強制経口投与し,最終投与後24時間に骨髄塗抹標本を作製し,検鏡することにより小核誘発性を検討した.
3-ヒドロキシ-2-ナフトエ酸投与による小核を有する多染性赤血球の誘発傾向は認められなかった.また観察全赤血球中の多染性赤血球の割合については,明確な減少傾向は認められなかった.
以上の結果より,本試験条件下では3-ヒドロキシ-2-ナフトエ酸は,小核を誘起しない(陰性)と結論した.
試験には,日本エスエルシーから購入した8週齢のBDF1系マウス(C57BL/6 × DBA/2,SPF)を,7日間検疫と馴化を兼ねて飼育した後,9週齢で試験に供した.
温度24.5 ± 2.5℃,湿度55 ± 20 %,換気回数1時間あたり18回,照明12時間(午前7時点灯,午後7時消灯)に設定した飼育室で動物を飼育した.床敷きとして,アルファドライ(Shepherd Specialty Papers)を入れたzyfone製飼育ケージに,検疫期間中は2匹,群分け後は3匹ずつ収容し,固型飼料(MF,オリエンタル酵母工業)と水道水(磐田市上水道給水)を自由に摂取させた.
被験物質の3-ヒドロキシ-2-ナフトエ酸(ロット番号:DC0201)は純度99.2 %の黄色粉末である.本剤は水に0.05 g/L可溶,アルコール,エーテルに易溶,クロロホルム,ベンゼンに可溶である.上野製薬(大阪)から提供された被験物質を使用した.被験物質は,使用時まで冷暗所に保管した.試験終了後,被験物質提供元において残余被験物質を分析した結果,安定性に問題はなかった.
被験物質を0.5 w/v%メチルセルロース溶液(0.5 w/v% MC,400 cP溶液,和光純薬工業)に懸濁させ,調製原液とした.調製原液を使用媒体を用いて順次所定濃度に希釈し,速やかに投与に用いた.各調製液は,投与初日ならびに投与2日目の用時に調製した.
240〜700 mg/kgの4用量(公比10/7)を用い,雄雌両性のマウスを用いて用量設定試験を実施した.その結果,雄雌とも490および700 mg/kgで1 g以上の体重減少が観察された.雄の700 mg/kgで2回目投与後1時間以内に1例の死亡が認められた.
以上の結果から,小核試験では最大耐量付近と考えられる500 mg/kgを最高用量とし,以下250および125 mg/kg(公比2)の3用量および陰性対照群を設定した.また,雄雌の毒性発現に顕著な差が認められなかったため小核試験は雄のみで実施することとした.
なお,陽性対照として,マイトマイシンC(MMC,協和醗酵工業)を0.5 mg/kgの用量で試験した.
いずれの試験群とも6匹に投与し,そのうちの5匹を評価に使用した.
被験物質の投与経路は経口とし,ディスポーザブルシリンジとテフロン製ゾンデを用いて1日1回,24時間間隔で2日間連続投与した.陽性対照物質の場合は腹腔内投与とし,マイクロシリンジと25G注射針を用いて1回投与した.
投与容量は体重10 g当たり0.1 mLとし,群分け時の体重から投与液量(mL)を求めた.
用量設定試験では,動物搬入時,検疫期間終了時(群分け時)および最終投与後24時間に電子天秤(PG802-S,Mettler Toledo AG)を用いて体重を測定した.また,死亡動物については死亡発見時に体重を測定した.初回投与後0,1および23.5時間ならびに最終投与後0,1および24時間に動物の一般状態を観察した後,各用量の最終投与後24時間での死亡率を求めた.
小核試験では,動物搬入時,検疫期間終了時(群分け時)および標本作製直前に電子天秤PG802-SあるいはPG2002 (Mettler Toledo AG)を用いて体重を測定した.また,死亡動物については死亡発見時に体重を測定した.陰性対照および被験物質投与群については,初回投与後1,22時間,最終投与後0,1時間ならびに標本作製時に,陽性対照群については,投与後0,1時間ならびに標本作製時に動物の一般状態を観察した.
Schmidの方法 1, 2)に従い,骨髄塗抹標本を作製した.最終投与後24時間(陽性対照群は投与後24時間)に動物を炭酸ガス吸入法で安楽死させた.大腿骨を摘出し少量の非働化(56℃,30分)済みウシ胎児血清(Invitrogen)を用いて骨髄細胞を洗い出し,遠心分離法により余剰血清を除いた後,各動物につき3枚の塗抹標本を作製した.十分に乾燥させた塗抹標本をメタノールで固定した後,各動物につき2枚の塗抹標本を3 %ギムザ液(Merck)で30分間染色した.0.01 mol/L ナトリウム・リン酸緩衝液(pH 6.8,Merck)および精製水で洗浄し,乾燥させた.さらに0.01 %クエン酸水溶液および精製水で洗浄した後,再び乾燥させた.生存動物全例について骨髄塗抹標本を作製した.
全ての標本をコード化した後,小核を観察した.
動物1匹当たり2000個の多染性赤血球(polychromatic erythrocyte:PCE)を顕微鏡下(×1000程度)で観察した.小核を有する多染性赤血球(micronucleated polychromatic erythrocyte:MNPCE)数を計測するとともに,骨髄に対する影響を調べるため全赤血球500個中の多染性赤血球数についても計測した.
小核の出現頻度は,小核を有する多染性赤血球数を観察した多染性赤血球数で割ることにより算出した.全赤血球に対する多染性赤血球の割合は,多染性赤血球数を観察した赤血球数で割ることにより算出した.
各試験群の小核多染性赤血球の出現頻度は陰性対照群と他の群(陽性対照群を含む)において,条件付き二項検定(Kastenbaum and Bowmanの推計学的方法:有意水準上側0.025)を行った.
観察赤血球中の多染性赤血球の割合は,陰性対照群と他の群(陽性対照群を含まない)においてDunnettの多重比較(有意水準両側0.05)を行い,陰性対照群と陽性対照群においてはAspin-Welchのt検定(有意水準両側0.05)を実施した.
陰性対照群と比較し,被験物質処理群あるいは陽性対照群において統計学的な有意差が認められた場合,陽性と判定した.
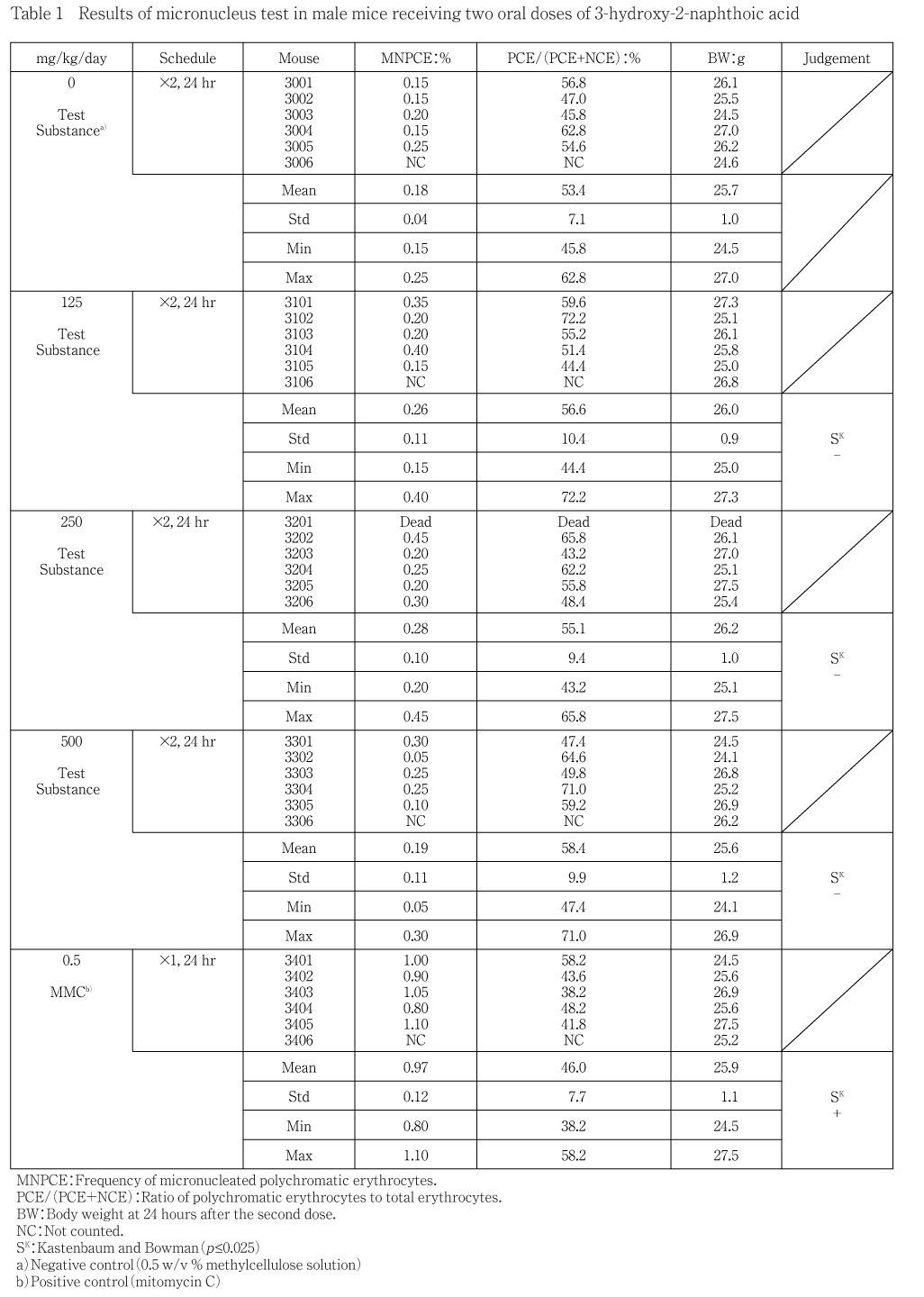
小核試験の結果をTable 1に示した.3-ヒドロキシ-2-ナフトエ酸投与により,250 mg/kgで2回目の投与直後に1例の死亡が認められた.なお,500 mg/kgにおいては2回目の投与直後に自発運動減少が1例に,腹臥位の毒性兆候が2例に認められた.また明確な体重の増加抑制作用は観察されなかった.個体別に多染性赤血球2000個を観察した結果,陰性対照群での小核(MNPCE)の出現頻度は0.18 %であった.また,観察全赤血球中における多染性赤血球の割合(PCE比)は53.4 %であった.3-ヒドロキシ-2-ナフトエ酸投与によるMNPCEの出現頻度は,125 mg/kg群で0.26 %,250 mg/kg群で0.28 %および500 mg/kg群で0.19 %であり,陰性対照群と比較して統計学的に有意な増加は認められなかった.また,被験物質の骨髄細胞に対する影響の指標であるPCE比は,125,250および500 mg/kg群でそれぞれ56.6,55.1および58.4 %であり,陰性対照群と比較して有意な減少は認められなかった.
一方,MMCを投与した陽性対照群ではMNPCEの出現頻度は0.97 %と明らかに増加し,陰性対照群に比べ統計学的に有意(p<0.025)な増加を示した.さらに,PCE比は46.0 %であった.
以上の試験結果から,本試験条件下において3-ヒドロキシ-2-ナフトエ酸のマウスに対する小核の誘発性は陰性と判定された.このことより,本物質の染色体構造異常ないし数的異常誘発性はないものと推定された.
なお,本被験物質(3-ヒドロキシ-2-ナフトエ酸)について,遺伝毒性ならびに発がん性に関する報告はなかった.
類縁体である2-ナフトール(2-Naphthol)についてはヒトリンパ球ならびにマウス骨髄での染色体異常試験で陰性 3)と報告されている.
類縁体であるナフタレン(Naphthalene),a-ナフチルアミン(a-Naphtylamine)はCHL細胞を用いた染色体異常試験で陽性 4),1-ナフトール-4-スルホン酸ナトリウム(1-Naphthol-4-sulfonic acid sodium salt)は細菌を用いる復帰変異試験5)およびCHL細胞を用いた染色体異常試験で陰性 6)との報告があった.
| 1) | Schmid W:The micronucleus test. Mutation Res, 31:9-15(1975). |
| 2) | Schmid W:The micronucleus test for cytogenetic analysis. In "Chemical Mutagens", Vol. 4, Hollaender A(ed.), Plenum press, New York(1976)pp. 31-53. |
| 3) | Kalski A, Strozynski H and Smok W:Assessment of genotoxic activity of azo dye thiadiazole derivatives with the help of a structural chromosome aberration test. Med Pr, 45(2):107-113(1994). |
| 4) | 祖父尼俊雄(監修):「染色体異常試験データ集〈改訂1998年版〉」エル・アイ・シー,東京(1999)p.348. |
| 5) | 野田篤ら:1-ナフトール-4-スルホン酸ナトリウムの細菌を用いる復帰変異試験.化学物質毒性試験報告,9:375-378(2002). |
| 6) | 野田篤ら:1-ナフトール-4-スルホン酸ナトリウムのチャイニーズ・ハムスター培養細胞を用いる染色体異常試験.化学物質毒性試験報告,9:379-382 (2002). |
| 連絡先 | |||
| 試験責任者: | 中嶋 圓 | ||
| 試験担当者: | 赤星まゆみ,柴本美恵子, 木下裕加,鈴木ゆみ子,上田摩弥, 嶋田佐和子,岩倉佳奈子, 萩原弘美,鈴木雅也 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田市塩新田582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | |||
| Authors: | Madoka Nakajima (Study director) Mayumi Akahoshi, Mieko Shibamoto, Yuka Kishita, Yumiko Suzuki, Maya Ueda, Sawako Shimada, Kanako Iwakura, Hiromi Hagiwara, Masaya Suzuki |
||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | |||
| 582-2 Shioshinden, Iwata-shi, Shizuoka, 437-1213, Japan | |||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | ||
