1,2-ジシアノベンゼンはフタロシアニン系染料,顔料の原料等として用いられている1).今回,1,2-ジシアノベンゼンを1,6および30 mg/kgの用量でSD系ラット(1群雌雄各12匹)に交配前14日から交配を経て雄は計44日間,雌は妊娠,分娩を経て哺育4日まで経口投与し,反復投与毒性および生殖発生毒性について検討した.
以上の結果から,1,2-ジシアノベンゼンの反復投与毒性に関する無影響量は雌では1 mg/kg/day,雄は6 mg/kg/dayと考えられた.生殖発生毒性に関する無影響量は親動物の雄で30 mg/kg/day,雌で6 mg/kg/day,児動物では6 mg/kg/dayと考えられた.
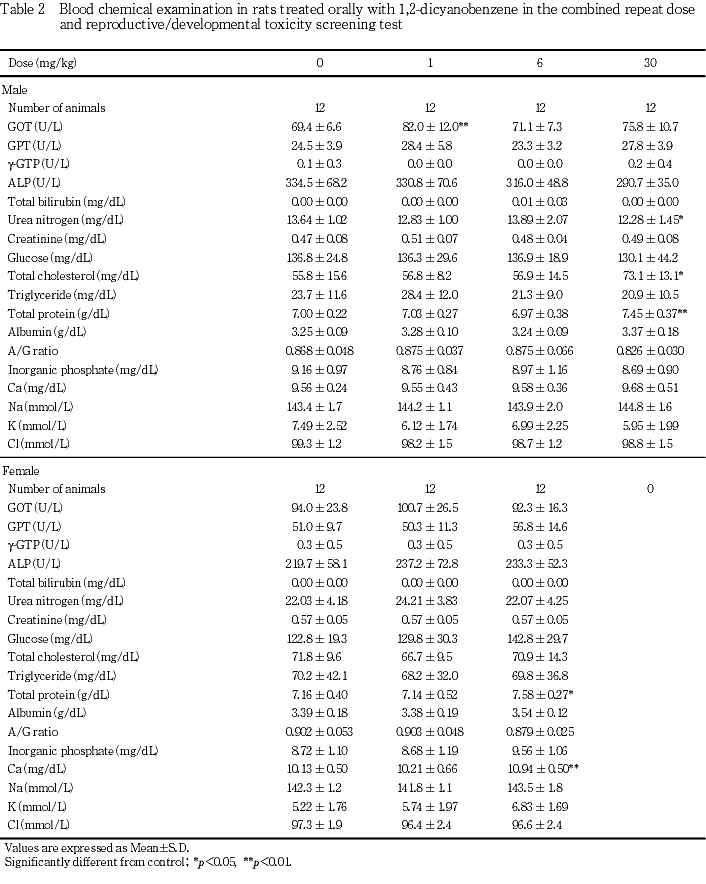
 法),グルコース(Glck-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
法),グルコース(Glck-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.

 から
から
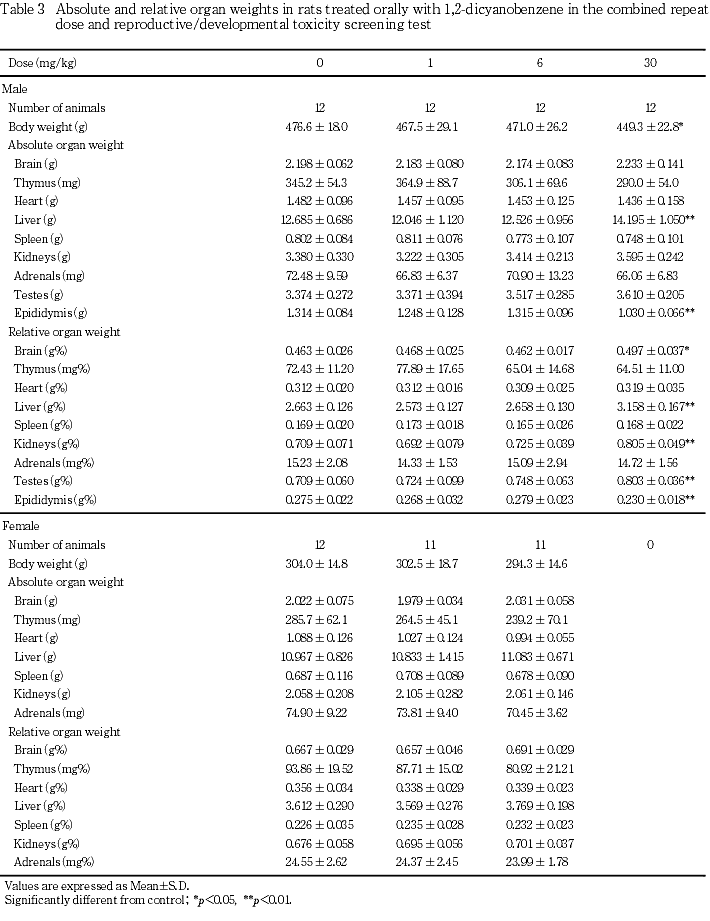
 の精細管に精子の遺残がみられる程度の軽度な変化であった.なお,1 mg/kg群でセルトリー細胞のみからなる精細管がび漫性にみられる中等度の変化が1例にみられたが,30 mg/kg群でみられる組織像とは異なるため,被験物質との関連はないと判断した.精巣上体では,管腔内の細胞残屑の出現および精子数の減少がみられ,30 mg/kg群の発現頻度がそれぞれ12および11例と有意な増加が認められた.30 mg/kg群の雌の死亡例では,下顎リンパ節,腸間膜リンパ節のリンパろ胞の萎縮,胸腺および脾臓の萎縮,腺胃のびらんおよび潰瘍,前胃の角化亢進,扁平上皮細胞の限局性過形成および潰瘍,副腎皮質束状帯細胞の肥大等が認められた.萎縮したリンパ組織ではリンパ球の核崩壊像が認められ,急性の変化であることが示唆された.また,死亡前に痙攣が確認された2例の脳および脊髄について,L.F.B.染色を施し精査したが,異常所見はみられず,死亡の直接の原因となる組織変化は認められなかった.
の精細管に精子の遺残がみられる程度の軽度な変化であった.なお,1 mg/kg群でセルトリー細胞のみからなる精細管がび漫性にみられる中等度の変化が1例にみられたが,30 mg/kg群でみられる組織像とは異なるため,被験物質との関連はないと判断した.精巣上体では,管腔内の細胞残屑の出現および精子数の減少がみられ,30 mg/kg群の発現頻度がそれぞれ12および11例と有意な増加が認められた.30 mg/kg群の雌の死亡例では,下顎リンパ節,腸間膜リンパ節のリンパろ胞の萎縮,胸腺および脾臓の萎縮,腺胃のびらんおよび潰瘍,前胃の角化亢進,扁平上皮細胞の限局性過形成および潰瘍,副腎皮質束状帯細胞の肥大等が認められた.萎縮したリンパ組織ではリンパ球の核崩壊像が認められ,急性の変化であることが示唆された.また,死亡前に痙攣が確認された2例の脳および脊髄について,L.F.B.染色を施し精査したが,異常所見はみられず,死亡の直接の原因となる組織変化は認められなかった.
その他,対照群を含む雌雄各群で種々の変化が認められたが,いずれも本系統のラットを用いた毒性試験においてしばしば認められる自然発生性の変化であり,被験物質投与群に多発する傾向はみられなかったことから,被験物質との関連はないと判断した.
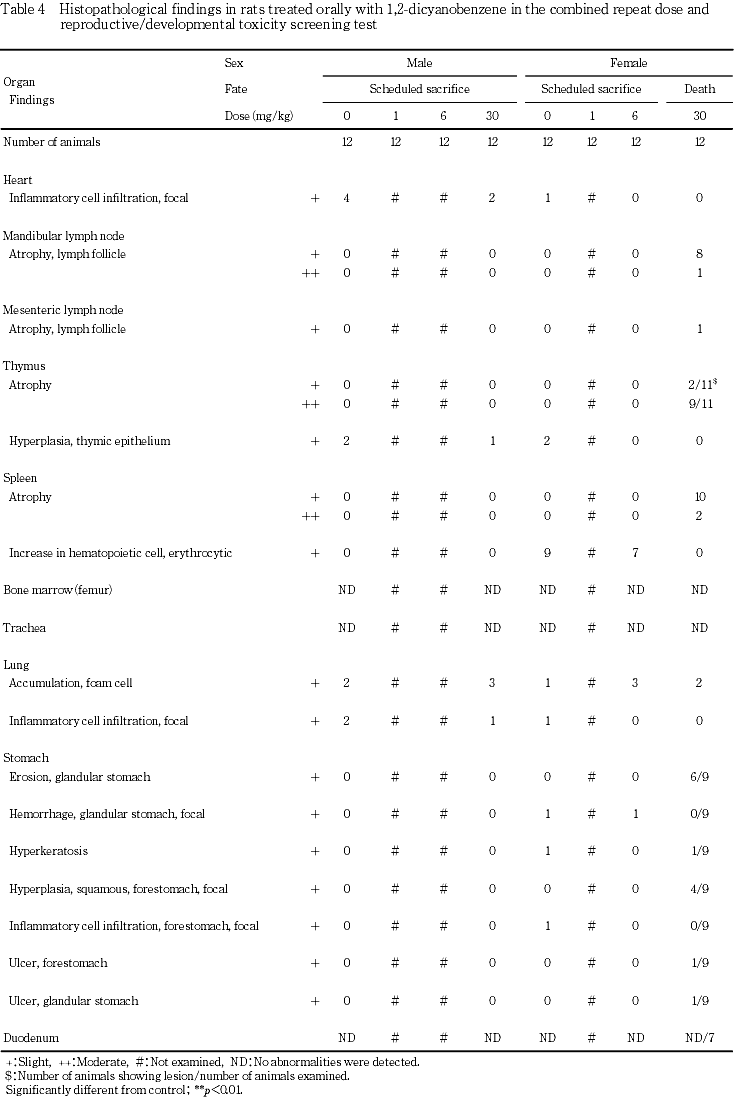
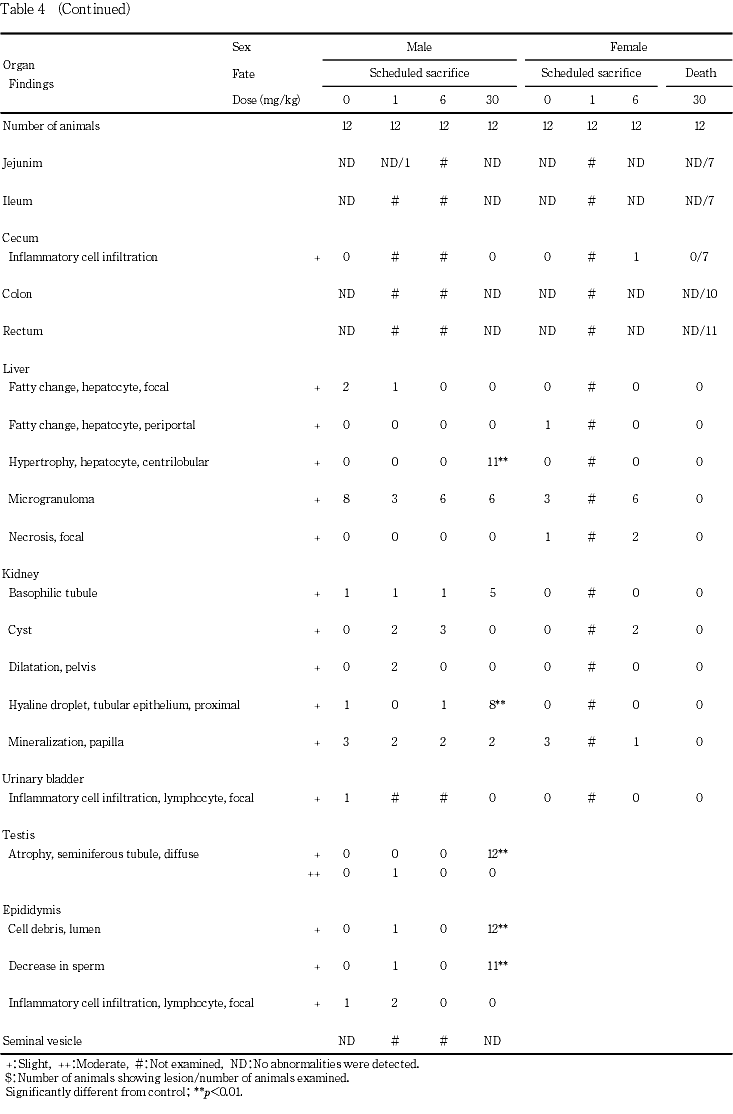
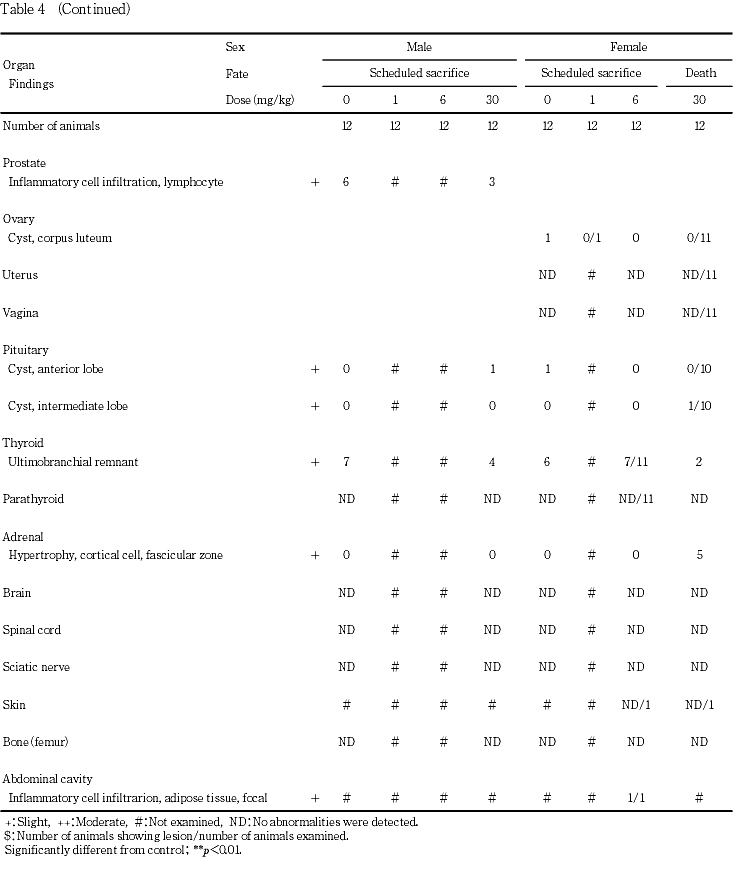

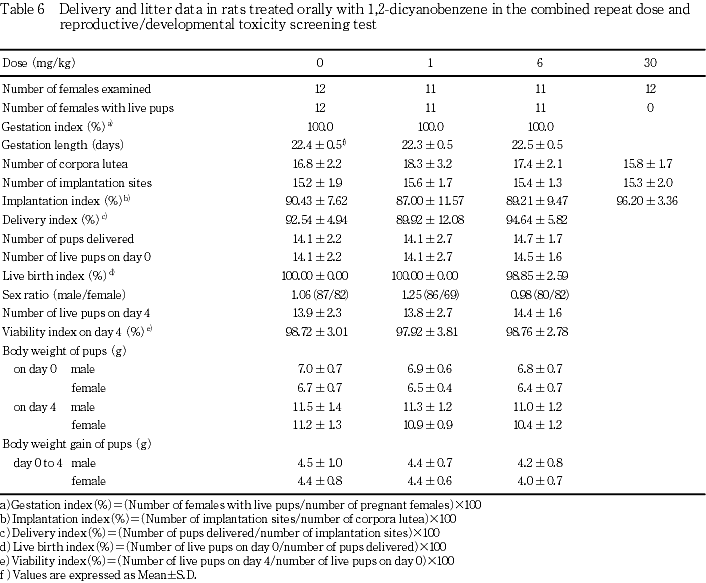
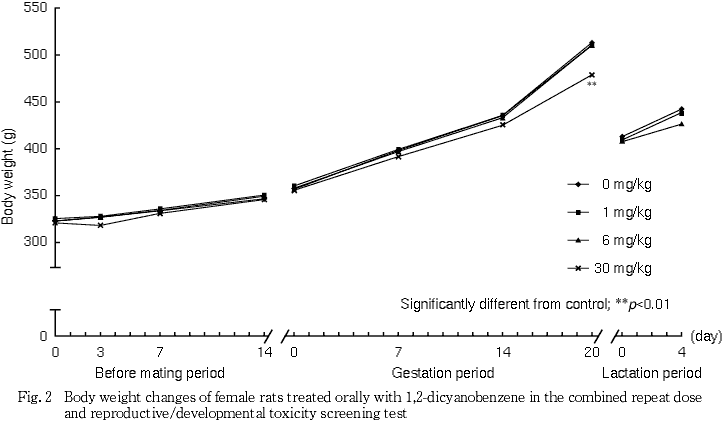
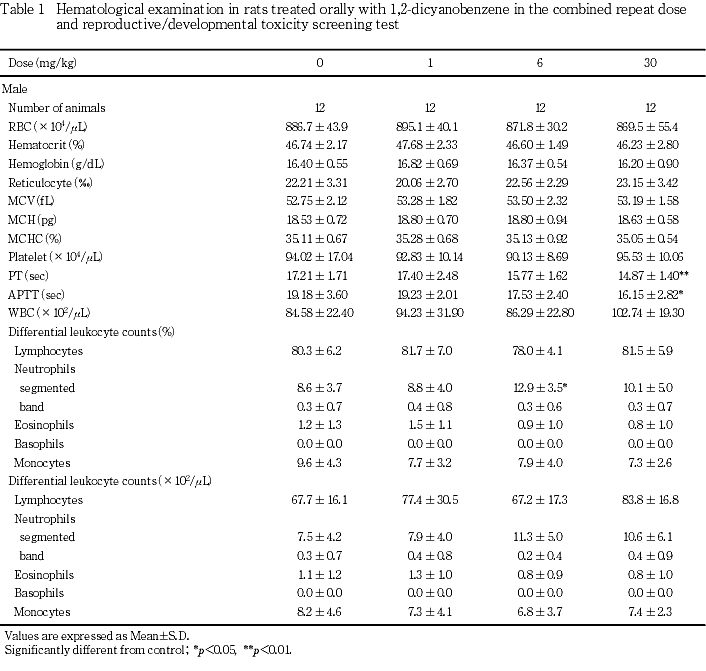
以上の結果から,本試験では反復投与による一般毒性学的影響として,6 mg/kg群の雌で総蛋白の増加がみられ,30 mg/kg群の雌雄で体重増加の抑制および摂餌量減少,雌で妊娠末期に痙攣がみられ全例が死亡した.さらに,雄で総蛋白,総コレステロールの増加,血清尿素窒素の減少,肝臓,腎臓,精巣および精巣上体に重量と組織学的変化が認められた.したがって,本試験条件下における反復投与毒性に関する無影響量は雌では1 mg/kg/day,雄は6 mg/kg/dayと考えられた.また,生殖発生に及ぼす影響として親動物では,30 mg/kg群の雄で異常は認められなかったが,雌は妊娠末期に全例が死亡したことから,生殖発生に関する親動物の無影響量は雄で30 mg/kg/day,雌で6 mg/kg/dayと考えられる.さらに,児動物では,6 mg/kg群で異常が認められなかったことから,生殖発生毒性に関する児動物の無影響量は6 mg/kg/dayと考えられる.
| 1) | 後藤稠,池田正之,原一郎,産業中毒便覧(増補版),“医歯薬出版,”東京,1984, p.1169. |
| 2) | P. Greaves, “Histopathology of Preclinical Toxicity studies,” Elsevier Amsterdam, 1990, pp.295-721. |
| 3) | 上田久,横浜医学,11(5), 87(1961). |
| 4) | Toxikologische Bewertung. Heidelberg, Berufs-genossenschaft der chemischen Industrie, 28, 31(1995). |
| 5) | 吉川博,医学と生物学,75(4), 131(1967). |
| 6) | K. Nakamura, et al., Kobe J. Med. Sci., 11, 63(1965). |
| 7) | C. Gopinath, D. E. Prentis and D. J. Lewis, “Atlas of Experimental Toxicological Pathology,” eds. by C. Gopinath, D. E. Prentis and D. J. Lewis, MTP Press, Lancaster, 1987, pp.43-60. |
| 8) | S. B. Swenberg, Toxicol. Appl. Pharmacol., 97, 35(1989). |
| 連絡先 | |||
| 試験責任者: | 東川国男 | ||
| 試験担当者: | 涌生ゆみ,青山涼子,豊田直人,鈴木美江 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-0255 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Kunio Higashikawa(Study director) Yumi Wako, Ryoko Aoyama, Naoto Toyota, Yoshie Suzuki | |||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | ||||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255 Japan | ||||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |||