2-tert-ブチルフェノールのラットを用いる28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of 2-tert-Butylphenol in Rats
要約
2-tert-ブチルフェノールは,農薬,香料,樹脂を製造する際の原料である1).今回,2-tert-ブチルフェノールを0,4,20,100および500 mg/kgの用量で雌雄のSD系ラットに28日間反復経口投与し,その毒性と回復性を検討した.
一般状態において,投与期間中に歩行失調が500 mg/kg群の雌雄で,流涎が100および500 mg/kg群の雌雄で,器官重量において,投与期間終了時に肝臓相対重量の高値が500 mg/kg群の雌雄で,それぞれ認められた.これらの変化は,回復期間中あるいは終了時には認められなかった.
この他,体重測定,摂餌量測定,血液学検査,血液生化学検査,尿検査,剖検,病理組織学検査の結果には,被験物質投与に起因すると考えられる変化はみられなかった.
以上,雌雄いずれも100および500 mg/kg群で被験物質投与に起因すると考えられる変化が認められた.一般状態において100 mg/kg群の雌雄で流涎がみられたことから,本試験条件下における2-tert-ブチルフェノールの無影響量(NOEL)は,雌雄いずれも20 mg/kg/dayと判断した.
方法
1. 被験物質
大日本インキ化学工業(株)(東京)から提供された2-tert-ブチルフェノール(ロット番号C169,純度99.97 %)を室温,窒素封入条件下で保存し使用した.被験物質の安定性は,被験物質提供者より保証する資料を入手し,確認した.被験物質はオリブ油(丸石製薬(株))に溶解調製し,窒素封入した.投与液の調製は週1回行い,投与に供するまで冷蔵保存した.投与液中の被験物質の冷蔵保存条件下での8日間の安定性は,投与開始前に0.4から200 mg/mLの範囲で確認した.また,初回調製時に各用量群の投与液を分析し,被験物質の濃度が設定濃度±10 %以内であることを確認した.
2. 試験動物および動物飼育
日本チャールス・リバー(株)からCrj:CD(SD)IGSラット(SPF)を入手し,7日間検疫・馴化した.投与開始前日に,体重層別化無作為抽出法によって各群の体重がほぼ均一となるように群分けした.1群の動物数は,雌雄各6匹とし,対照群,100および500 mg/kg群については雌雄各6匹の回復群(回復期間14日間)を設けた.投与開始時の週齢は5週齢,体重範囲は雄が154〜185 g,雌が134〜154 gであった.
検疫・馴化期間を含む全飼育期間を通して,温度22 ± 2℃,相対湿度55 ± 15 %,換気約12回/時(オールフレッシュエアー供給),照明12時間/日(7:00〜19:00)に自動調節した飼育室を使用した.動物を実験動物用床敷(ベータチップ,日本チャールス・リバー(株))を敷いたポリカーボネート製ケージに群分け前はケージあたり5匹(同性),群分け以降はケージあたり2匹(同性)収容し,飼育した.動物には,実験動物用固型飼料(MF,オリエンタル酵母工業(株))と,5 μmのフィルター濾過後,紫外線照射した水道水を自由に摂取させた.
3. 投与量および投与方法
予備試験として被験物質を500,1000および2000 mg/kgの用量で単回経口投与した結果,1000および2000 mg/kgの雌全例が死亡し,両群の雄で重度の自発運動の低下が認められた.さらに0,100,300および500 mg/kgの用量をSD系ラットに12日間反復経口投与した結果,歩行失調が500 mg/kg群の雌雄および300 mg/kg群の雌,肝臓の絶対・相対重量の高値が500 mg/kg群の雄,肝臓および腎臓の相対重量の高値が500 mg/kg群の雌で認められた.これらの予備試験の結果から,本試験の高用量は500 mg/kgとし,以下公比5で100,20および4 mg/kgの計4用量群を設定した.さらに溶媒(オリブ油)のみを投与する対照群を設けた.
投与期間は28日間とし,胃ゾンデを装着したシリンジを用いて1日1回,午前中に強制経口投与した.投与液量は10 mL/kgとし,至近日に測定した体重に基づいて算出した.
4. 観察および検査方法
下記の項目を検査した.なお,日と週の表記は投与開始日を第1日,第1〜7日を第1週とした.また,第29日以降を回復期間とした.
1) 一般状態,体重および摂餌量
全例について一般状態を毎日観察した.体重および摂餌量は投与開始日およびその後毎週1回測定した.摂餌量については各期間毎の1匹あたりの1日平均摂取量を算出した.
2) 血液学検査
第29日(最終投与日の翌日)および第43日(回復期間終了後)に全例を非絶食条件下で,チオペンタールナトリウムによる麻酔下で後大静脈より採血し,赤血球数(シースフローDCインピーダンス検出法),ヘモグロビン濃度(SLSヘモグロビン法),ヘマトクリット値(赤血球パルス波高値検出法),血小板数(シースフローDCインピーダンス検出法),白血球数(RF/DCインピーダンス検出法)を多項目自動血球分析装置(NE-4500,シスメックス(株))で,網赤血球率(アルゴンレーザーを用いたフローサイトメトリー法)を自動網赤血球測定装置(R-2000,シスメックス(株))で,プロトロンビン時間(PT;Quick一段法)および活性化部分トロンボプラスチン時間(APTT;活性化セファロプラスチン法)を血液凝固自動測定装置(KC 10A,アメルング社)で,白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROX HEG-70A,オムロン(株))で,それぞれ測定した.また,検査の結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.プロトロンビン時間および活性化部分トロンボプラスチン時間の測定には凝固阻止剤として3.2 %クエン酸三ナトリウム水溶液を使用し,遠心分離して得られた血漿を用いた.その他の項目の測定には,凝固阻止剤EDTA-2Kで処理した血液を用いた.
3) 血液生化学検査
第29日(最終投与日の翌日)および第43日(回復期間終了後)に採取した血液の一部を室温で約30分間静置後3000 rpmで10分間遠心分離し,得られた血清を用いて,ASAT(GOT;JSCC改良法),ALAT(GPT;JSCC改良法),gGT(SSCC改良法),ALP(JSCC改良法),総ビリルビン(BOD法),尿素窒素(Urease-GLDH法),クレアチニン(Jaff 法),グルコース(GlcK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形;(株)日立製作所)により測定した.また,検査の結果からA/G比を算出した.
法),グルコース(GlcK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形;(株)日立製作所)により測定した.また,検査の結果からA/G比を算出した.
4) 尿検査
各群雌雄6匹の新鮮尿を第23日(投与期間最終週)に採取して,pH,蛋白,グルコース,ケトン体,ビリルビン,潜血,ウロビリノーゲン(試験紙法;マルティスティックス,バイエル・三共(株))を尿分析装置(クリニテック100,バイエル・三共(株))で測定した.
5) 病理学検査
第29日(最終投与日の翌日)および第43日(回復期間終了後)に全例について,採血後,腹大動脈を切断・放血し,安楽死させた後剖検した.全例の脳,心臓,肺,肝臓,腎臓,副腎,胸腺,脾臓,精巣,卵巣,子宮,精巣上体,下垂体,甲状腺の重量を測定した.全例の脳,脊髄,下垂体,眼球およびハーダー腺,リンパ節(下顎・腸間膜),胸腺,気管,肺および気管支,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,膵臓,甲状腺および上皮小体,心臓,肝臓,脾臓,腎臓,副腎,膀胱,精巣,精巣上体,精嚢,前立腺腹葉,卵巣,子宮,大腿骨および骨髄,大腿筋および坐骨神経を採取し,眼球とハーダー腺はダビドソン液で,精巣および精巣上体はブアン液で,それ以外の器官・組織は10 %中性リン酸緩衝ホルマリン液で固定し,保存した.
投与期間終了時に採取した対照群と500 mg/kg群の雌雄全例の胸腺,心臓,肝臓,脾臓,腎臓,副腎,精巣,精巣上体,精嚢,卵巣,脳,脊髄(頚部,胸部,腰部),坐骨神経,大腿筋ならびに対照群を含む全動物の肉眼的異常部位は常法に従ってヘマトキシリン・エオジン(H.E)染色標本を作製し,鏡検した.
5. 統計解析
計量データは,Bartlett法で等分散の検定を行い,分散が等しい場合は一元配置分散分析,分散が等しくない場合はKruskal-Wallisの検定を行った.群間に有意な差が認められた場合はDunnett法またはDunnett型の多重比較検定を行った.尿検査データおよび病理組織所見は,a × bのx2検定を行い,有意差が認められた場合はArmitageのx2検定で対照群と各用量群を比較した.有意水準は5 %とした.
結果
1. 一般状態
被験物質投与に起因する変化として,歩行失調,自発運動の低下,流涎が認められた.歩行失調は投与期間中に500 mg/kg群で雄9例,雌全例に散発的に認められた.本変化は第1日からみられ,投与後に発現し,投与後5時間以内に消失した.自発運動の低下は500 mg/kg群の雌2例に1度または散発的に認められた.本変化は投与後に発現し,発現翌日の投与前までに消失した.流涎が100 mg/kg群の雄6例,雌2例,500 mg/kg群の雄全例,雌11例にみられた.本変化は100 mg/kg群の雄で第13日,雌で第14日,500 mg/kg群の雌雄で第7日以降の投与後30分以内にみられる一過性の変化であった.また,500 mg/kg群の雌1例では投与前の流涎がみられた.これらの変化は回復期間中にはみられなかった.
2. 体重(Fig. 1)
いずれの被験物質投与群においても,対照群と同様に推移した.
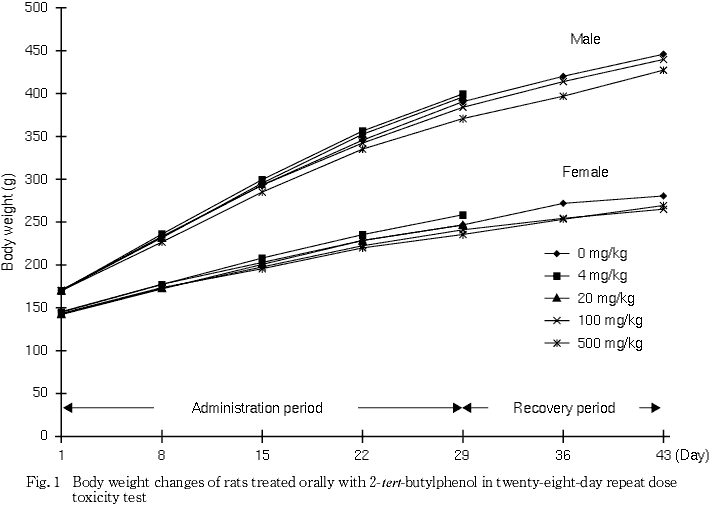
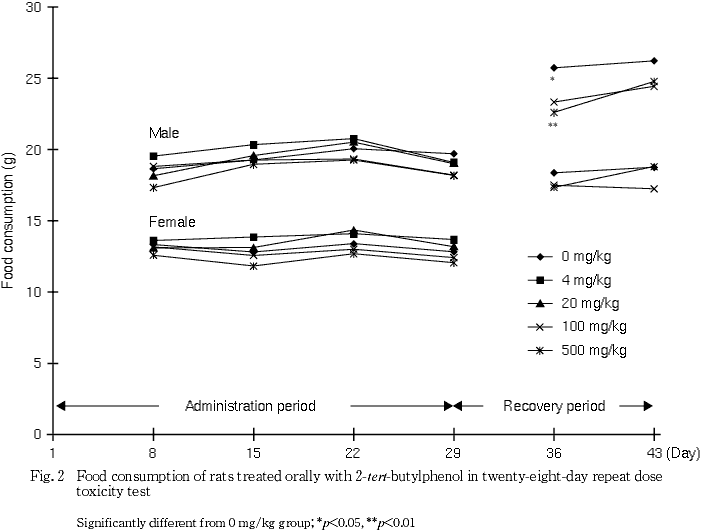
3. 摂餌量(Fig. 2)
被験物質投与に起因すると思われる変化は認められなかった.
回復期間中の第36日に100および500 mg/kg群の雄で低値がみられたが,投与期間中および回復終了時にみられない軽微な変化であり,被験物質投与とは関連のない変化と判断した.
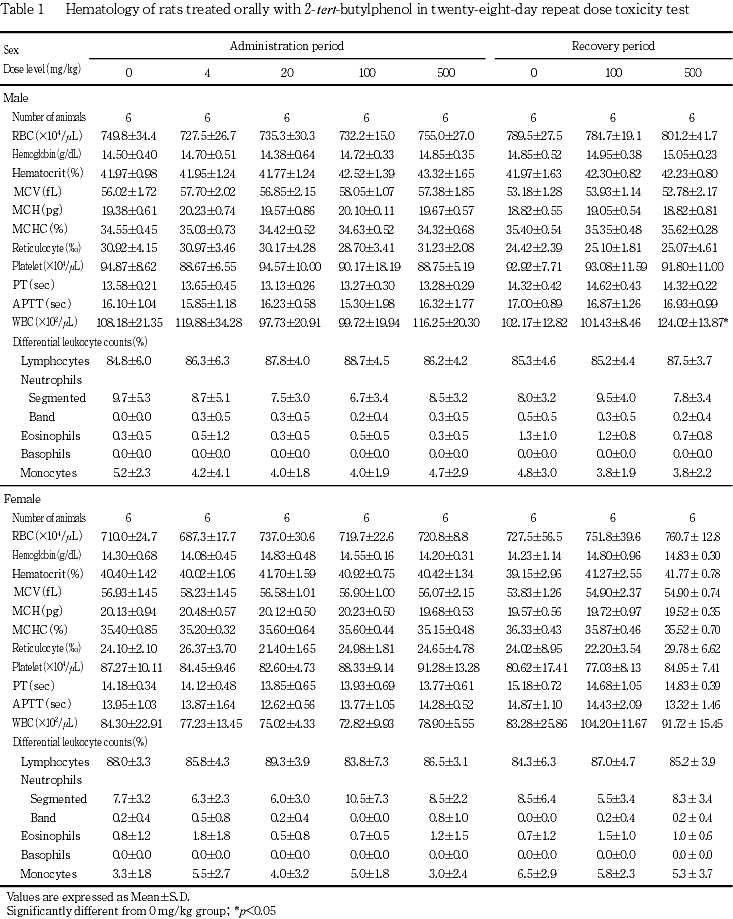
4. 血液学検査(Table 1)
投与期間終了時および回復期間終了時の検査で,被験物質投与に起因すると思われる変化は認められなかった.
回復期間終了時に500 mg/kg群の雄で白血球数の高値がみられたが,軽微な変化であり,投与期間終了時にはみられないことから,被験物質投与とは関連のない変化と判断した.
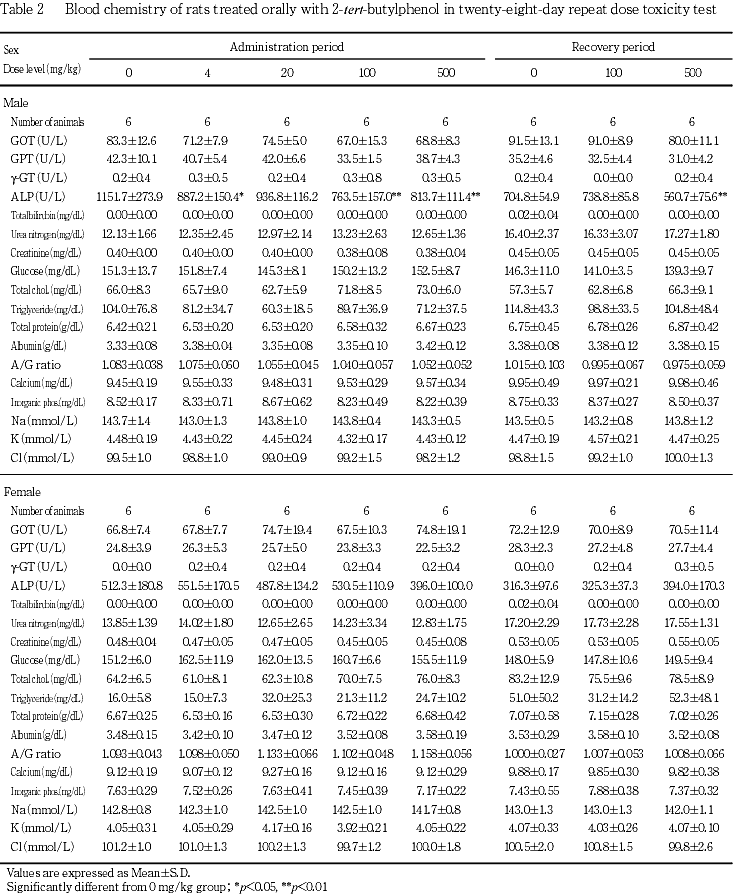
5. 血液生化学検査(Table 2)
投与期間終了時および回復期間終了時の検査で,被験物質投与に起因すると思われる変化は認められなかった.
ALPの低値が投与期間終了時に4,100,500 mg/kg群の雄で,回復期間終了時に500 mg/kg群の雄で認められた.しかし,いずれも軽微な変化であり,正常範囲内の変動であることから,被験物質投与と関連のない変化と判断した.
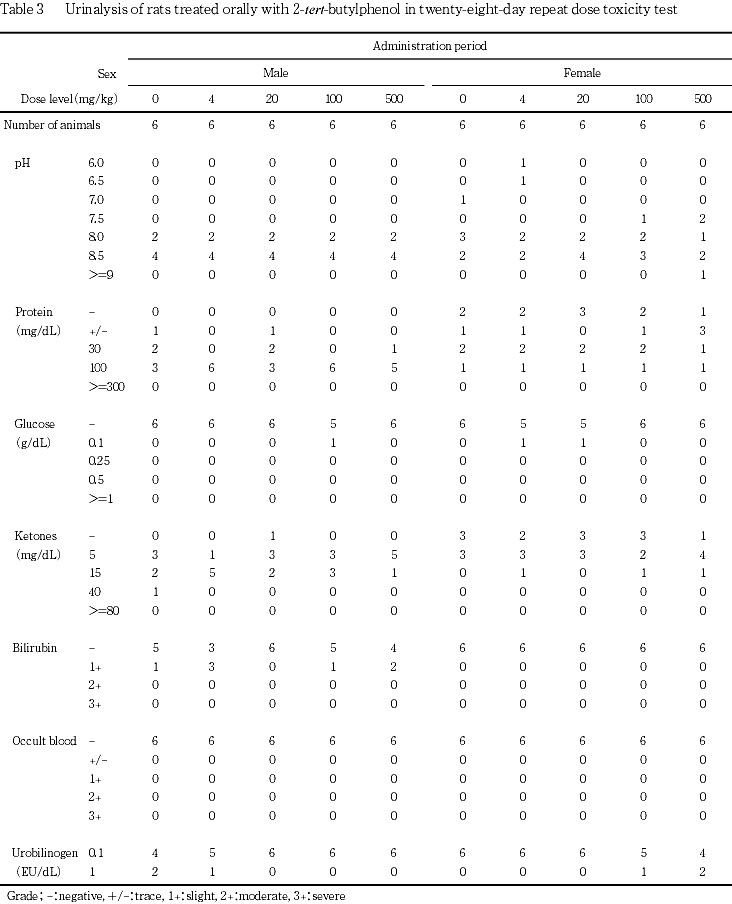
6. 尿検査(Table 3)
投与期間最終週の検査で,変化は認められなかった.
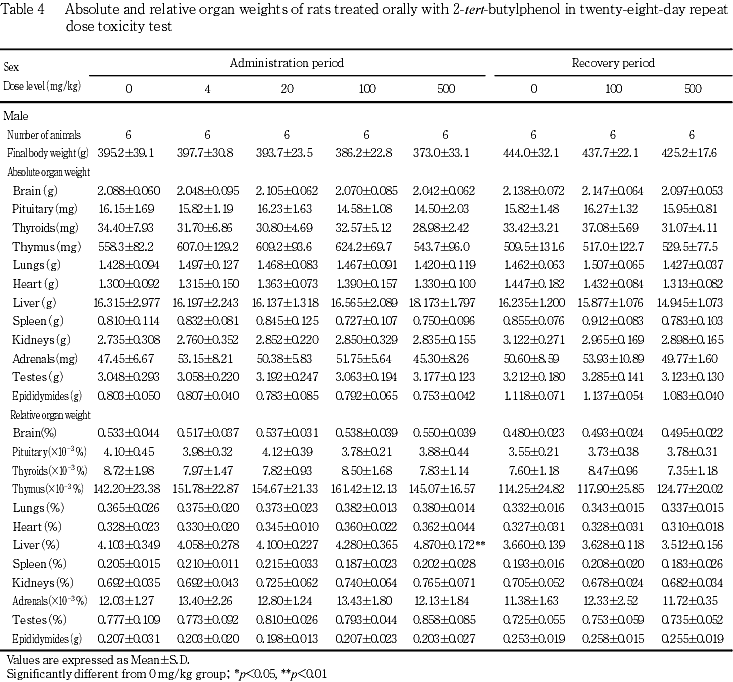
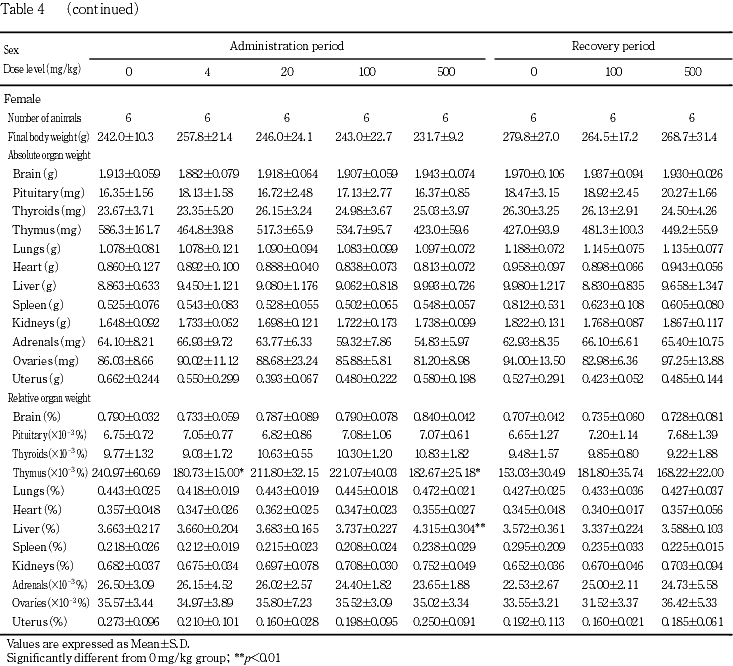
7. 器官重量(Table 4)
投与期間終了時に肝臓相対重量の高値が500 mg/kg群の雌雄で認められた.回復期間終了時には,本変化はみられなかった.
投与期間終了時に胸腺相対重量の低値が4および500 mg/kg群の雌でみられたが,いずれも軽微な変化であり,絶対重量には有意な差はみられないこと,正常範囲内の変動であることから,被験物質投与と関連のない変化と判断した.
8. 剖検所見
投与期間終了時の検査で被験物質投与に起因すると思われる変化は認められなかった.
投与期間終了時および回復期間終了時に被験物質投与群で胸腺の頚部残留,腎臓ののう胞,肺の褐色斑,子宮の膨満,甲状腺の小型が散発的に認められた.これらはいずれもラットで認められる偶発病変であり,その発現に用量との関連がないことから被験物質投与に起因した変化ではないと判断した.
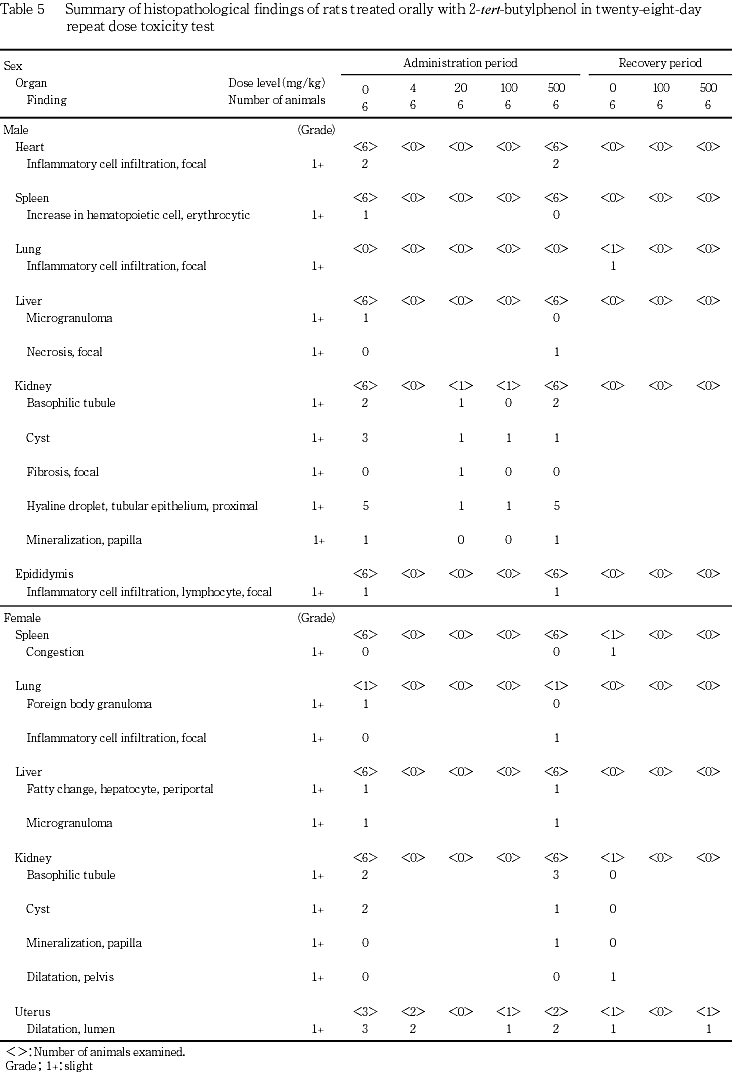
9. 病理組織学所見(Table 5)
投与期間終了時の解剖動物の500 mg/kg群の雌雄に被験物質投与に起因すると思われる変化は認められなかった.
被験物質投与群で心臓の炎症性細胞浸潤巣,肝臓の門脈周囲性の肝細胞脂肪化,小肉芽腫および壊死巣,腎臓の好塩基性尿細管,のう胞,線維化巣,近位尿細管上皮の硝子滴および乳頭部の鉱質沈着,精巣上体の炎症性細胞浸潤巣,肺の炎症性細胞浸潤巣,子宮腔の拡張が認められたが,いずれもラットを用いた毒性試験でしばしば自然発生性に認められる変化であり,その発現に用量との関連がないことから,被験物質投与に起因した変化ではないと判断した.
考察
2-tert-ブチルフェノールを0,4,20,100および500 mg/kgの用量で雌雄のSD系ラットに28日間反復経口投与し,その毒性と回復性を検討した.
一般状態において,投与期間中に歩行失調が500 mg/kg群の雌雄,流涎が100および500 mg/kg群の雌雄に認められた.歩行失調は投与後5時間以内にみられる一過性の変化であった.類似化合物であるフェノールでは,吸入暴露によりラットに一過性の協調運動失調を起こすことが報告されている2).また,有機溶剤の大量投与では,一過性の中枢神経障害により協調運動失調が起こることが知られている3).病理組織学的検査では,歩行失調に関連すると思われる変化は認められなかった.流涎は,主に投与後短時間に発現する一過性の変化であり,被験物質の直接的な刺激による可能性が考えられるが,500 mg/kg群では歩行失調と併せてみられることから,中枢神経障害に起因する可能性も否定できない.この他に投与期間中に500 mg/kg群の雌で自発運動の低下が散見された.これらの症状は回復期間中にはみられなかった.
器官重量測定において,投与期間終了時に肝臓相対重量の高値が500 mg/kg群の雌雄で認められた.しかし,肝臓の絶対重量には有意な変化はなく,病理組織学的にも相対重量の変動に関連する変化は認められなかった.回復期間終了時には,本変化はみられなかった.
体重測定,摂餌量測定,血液学検査,血液生化学検査,尿検査,剖検,病理組織学検査の結果には,被験物質投与に起因すると考えられる変化はみられなかった.
以上,雌雄いずれも100および500 mg/kg群で被験物質投与に起因すると考えられる変化が認められた.一般状態において100 mg/kg群の雌雄で流涎がみられたことから,本試験条件下における2-tert-ブチルフェノールの無影響量(NOEL)は,雌雄いずれも20 mg/kg/dayと判断した.
文献
| 1) | 化学工業日報社編,“1994年度版 新化学インデックス,”化学工業日報社,東京,p.549. |
| 2) | C. W. Flickinger, American Industrial Hygiene Association Journal, 37, 596(1976). |
| 3) | L. S. Andrews, R. Sunder,“トキシコロジー,”eds. by C. D. Klaassen, M. O. Amdur, J. Doull, 3, 同文書院,東京,1988, pp.659-692. |
| 連絡先 |
| 試験責任者: | 山下弘太郎 |
| 試験担当者: | 伊勢記代子,涌生ゆみ,豊田直人,鈴木美江 |
| (株)三菱化学安全科学研究所 鹿島研究所 |
| 〒314-0255 茨城県鹿島郡波崎町砂山14 |
| Tel 0479-46-2871 | Fax 0479-46-2874 | |
| Correspondence |
| Authors: | Kotaro Yamashita(Study director)
Kiyoko Ise, Yumi Wako, Naoto Toyota, Yoshie Suzuki |
| Kashima Laboratory, Mitsubishi Chemical Safety Institute Ltd. |
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255, Japan. |
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |

 法),グルコース(GlcK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形;(株)日立製作所)により測定した.また,検査の結果からA/G比を算出した.
法),グルコース(GlcK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),カルシウム(OCPC法),無機リン(PNP-XOD-POD法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形;(株)日立製作所)により測定した.また,検査の結果からA/G比を算出した.







