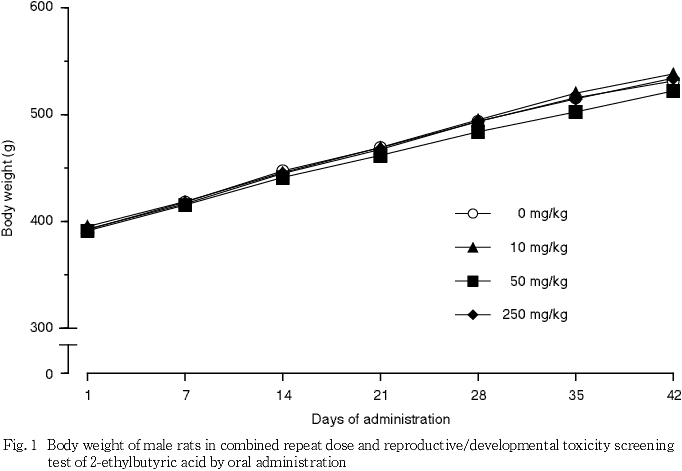
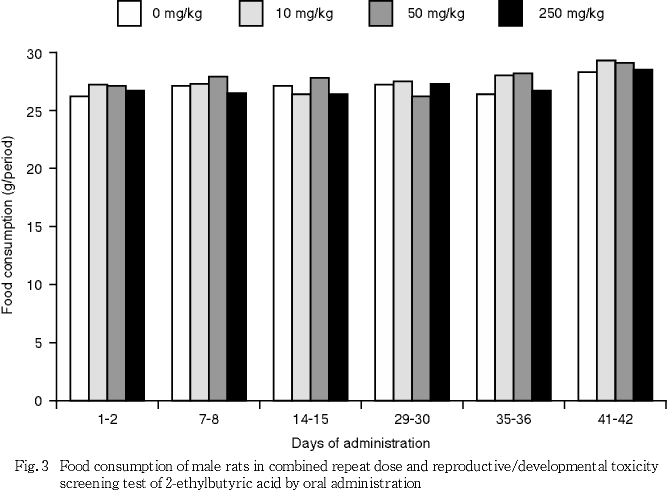
雌雄ともに250 mg/kg投与群において,投与後一過性の流涎が1例ずつに認められた他に,被験物質投与に起因した一般状態の異常は認められなかった.また,体重増加および摂餌量にも投与の影響は認められなかった.
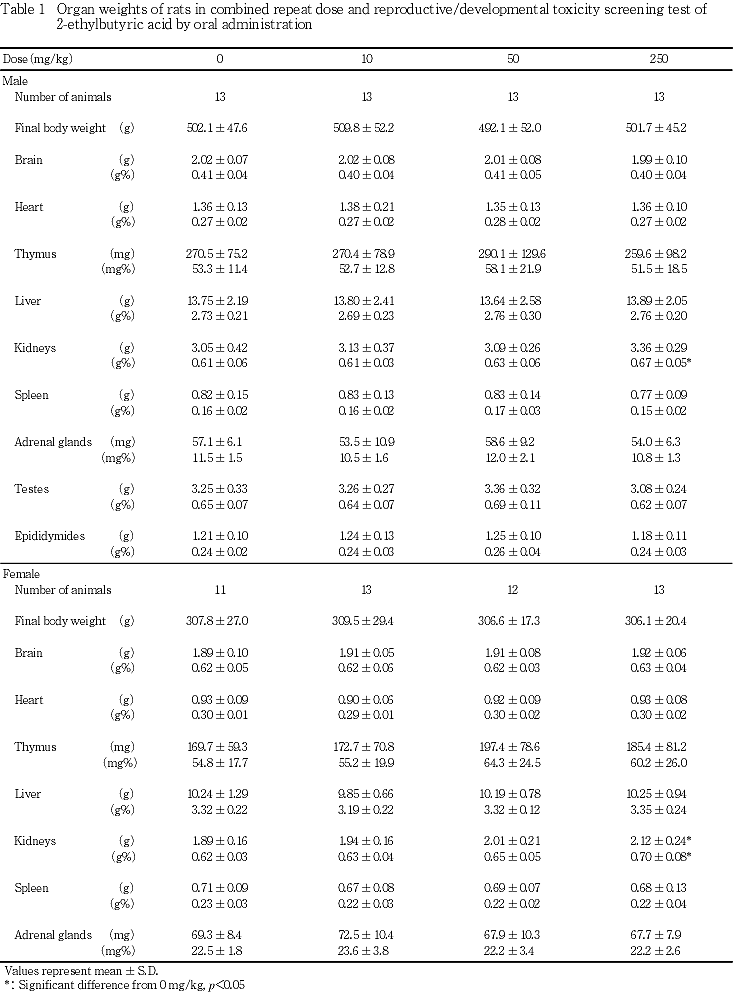
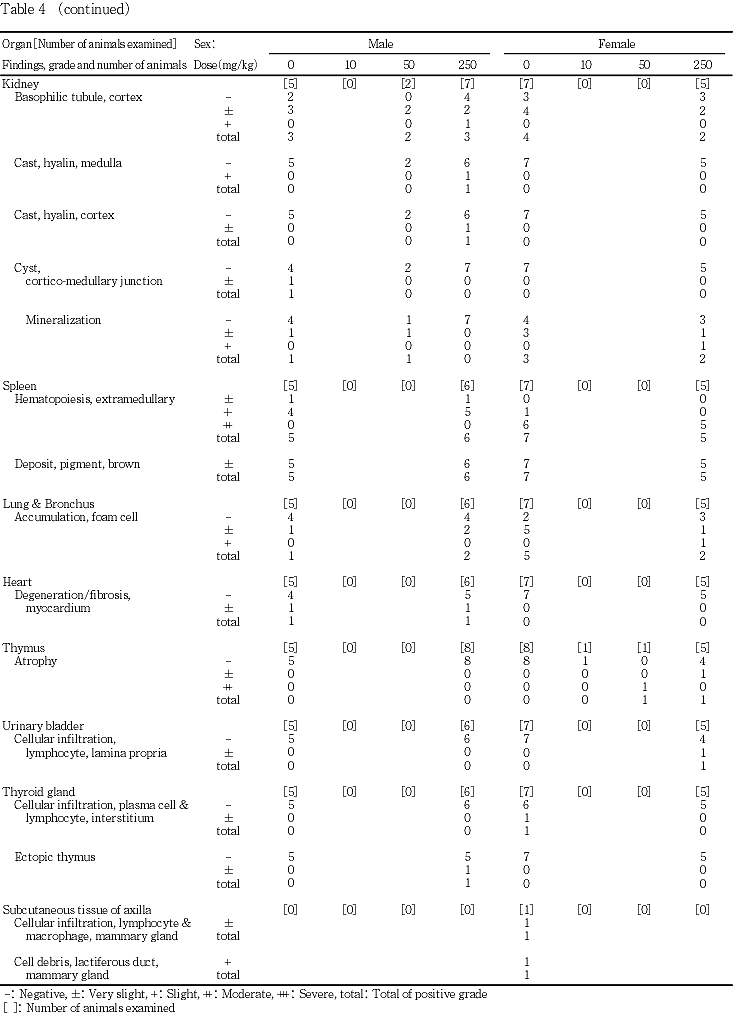
雌雄ともに250 mg/kg投与群において腎臓重量がやや増加したが,病理組織学検査では被験物質投与に起因すると考えられる異常は認められなかった.その他の器官の重量および病理組織学検査所見にも被験物質投与の影響は認められなかった.
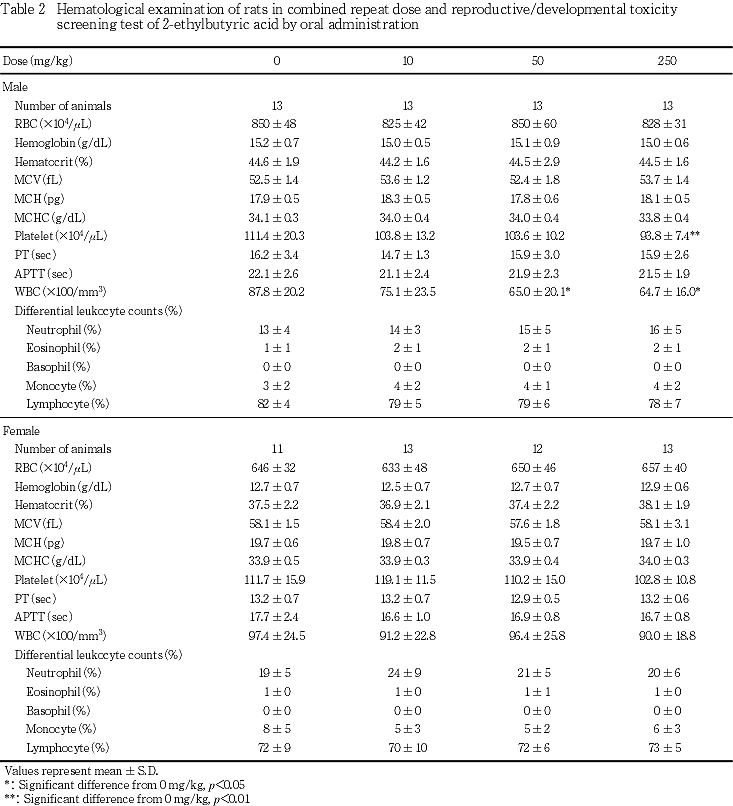
血液学検査では,50 mg/kg以上の投与群の雄において白血球数が軽度に減少し,250 mg/kg投与群において血小板数が減少したが,雌では被験物質投与の影響は認められなかった.血液生化学検査成績については,雌雄ともに被験物質投与の影響は認められなかった.
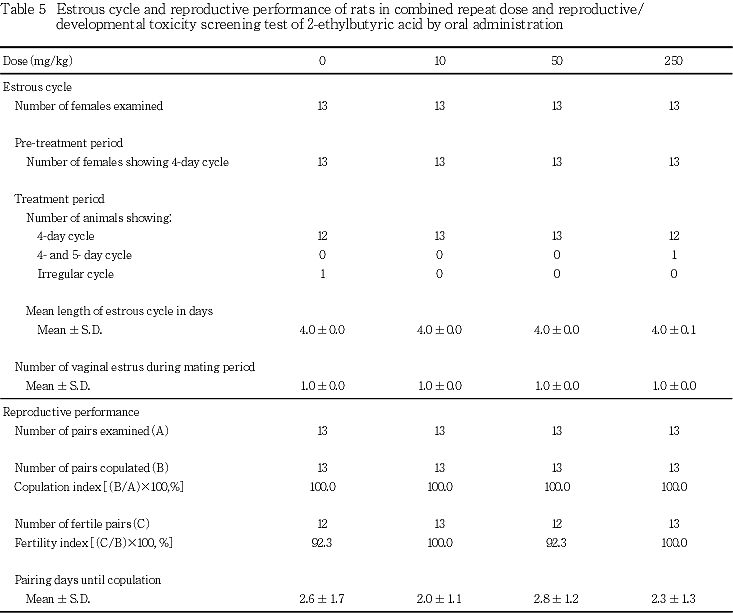
被験物質各投与群の妊娠期間は対照群と同様であり,出産率にも被験物質投与の影響は認められなかった.また,妊娠黄体数,着床数,着床率,産児数および分娩率といった出生までの胚および胎児の生存性にも投与の影響は認められなかった.しかし,50 mg/kg以上の投与群において,少数例に産児を集める行動や胎盤を処理する行動の欠如,あるいは分娩の遷延といった分娩異常が認められた.さらに,250 mg/kg投与群では出産生児数が減少し,生児出産率および出生率が減少し,このために,哺育4日における生存児数も減少した.哺育0日および4日における性比ならびに新生児の4日の生存率には投与の影響は認められず,出生児の体重にも投与の影響は認められなかった.形態異常を示す出生児も認められなかった.
以上の試験成績から,本試験条件下における2-エチル酪酸の無作用量は,反復投与毒性に関しては,雄では10 mg/kg/dayであり,雌では50 mg/kg/dayと推定された.生殖発生毒性に関しては,雄では250 mg/kg/dayであり,雌では10 mg/kg/dayと推定され,出生児では50 mg/kg/dayであると推定された.
投与検体は,被験物質を秤量してコーン油(英名:corn oil,ナカライテスク(株)Lot,No. V9F1299)に溶解し,いずれの用量においても1回の投与液量が2 mL/kg体重になるように含量を調製した.投与検体の安定性については,冷蔵,遮光条件下における8日間の安定性を確認しているので,1週間に1回以上の頻度で調製し,調製後7日以内に使用した.投与検体中に含まれる被験物質の含量は秦野研究所において確認した.
各動物は,基準温度24 ± 1 ℃,基準湿度50~65 %,換気回数約15回/時間,照明12時間(7~19時点灯)にそれぞれ制御された飼育室で,金属製金網床ケージに個別に収容し,固型飼料(CE-2,日本クレア(株))および飲料水(水道水,秦野市水道局給水)を自由に摂取させて飼育した.妊娠18日(腟栓あるいは精子発見日=妊娠0日)以後の母動物は,ラット用プラスチック製繁殖ケージに収容し,哺育5日(哺育0日=分娩日)まで紙パルプ製チップ(ALPHA-dri,加商(株))を床敷として供給して飼育した.
分娩を確認した全例について妊娠期間(妊娠0日〜分娩日の日数)を算定し,出産率〔(生児出産雌数/受胎動物数)× 100,%〕を各群について求めた.また,哺育1日から毎日,哺育状態を観察し,哺育5日の剖検において数えられた着床数および妊娠黄体数から着床率〔(着床数/妊娠黄体数)× 100,%〕を算出した.
出生児は,哺育0日に,雌雄別に産児数(生存児+死亡児)を調べ,分娩率〔(産児数/着床痕数)× 100,%〕,生児出産率〔(出産生児数/着床痕数)× 100,%〕および出生率〔(出産生児数/産児数)× 100,%〕を算出した.生存児については外表奇形の有無を観察した.翌日(哺育1日)から哺育4日まで毎日一般状態を観察し,生児数と死亡児数を雌雄別に数えて新生児の4日の生存率〔(哺育4日の生児数/哺育0日の生児数)× 100,%〕を算出した.生存児については,哺育0および4日に個別の体重を測定し,各腹ごとに雌雄別の平均値を算出するとともに哺育0および4日における性比〔(哺育0あるいは4日雄生児数/哺育0あるいは4日雌生児数)× 100〕を算出した.
投与42日に絶食を開始し,その18〜24時間後にペントバルビタールナトリウム麻酔下で腹部後大静脈から抗凝固剤としてクエン酸ナトリウムを用いて血液を採取し,プロトロンビン時間および活性部分トロンボプラスチン時間測定に用いた.次いで,腹部後大静脈から抗凝固剤としてEDTA-3Kを用いて採血し,その他の血液学検査に用いた.さらに,腹部後大静脈から抗凝固剤としてヘパリンを用いて採血し,血液生化学検査に用いた.動物は,採血終了後に放血致死させ解剖し,器官・組織の肉眼観察を行った.また,全例について,脳,下垂体,脊髄,上部気道を含む上顎,甲状腺,心臓,肺,気管,気管支,肝臓,腎臓,胸腺,脾臓,副腎,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,膀胱,下顎リンパ節,腸間膜リンパ節,坐骨神経,大腿骨髄,精巣,精巣上体,前立腺腹葉,凝固腺を含む精嚢,病変部を採取し,脳,心臓,胸腺,肝臓,腎臓,脾臓,副腎,精巣および精巣上体の重量を測定して相対重量を算出した.採取した器官および組織のうち,精巣ならびに精巣上体はブアン液(長期保存は0.1 Mリン酸緩衝10 %ホルマリン溶液を使用)に固定し,その他は0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.肺は,摘出前に0.1Mリン酸緩衝10 %ホルマリン溶液を注入してから固定・保存した.
(2) 雌
死亡例は発見後直ちに剖検した.交尾したが分娩しなかった例については妊娠25日相当日に,また,分娩した例は哺育4日に絶食を開始し,いずれも絶食開始18〜24時間後にペントバルビタールナトリウム麻酔下で雄と同様に採血後,放血致死させ解剖し,器官・組織の肉眼観察を行った.また,全例について脳,下垂体,脊髄,上部気道を含む上顎,甲状腺,心臓,肺,気管,気管支,肝臓,腎臓,胸腺,脾臓,副腎,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,膀胱,下顎リンパ節,腸間膜リンパ節,坐骨神経,大腿骨髄,卵巣,子宮,腟および病変部を採取し,脳,心臓,胸腺,肝臓,腎臓,脾臓および副腎の重量を測定して相対重量を算出した.子宮については着床数を数え,分娩した雌の卵巣については実体顕微鏡下で妊娠黄体数を数えた後,いずれも0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.肺は雄と同様に0.1 Mリン酸緩衝10 %ホルマリン溶液をよる注入固定を行った.
(3) 出生児
死亡児は発見後速やかに剖検し,0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.生存児は全例を哺育4日にエーテル吸入により致死させ剖検し,異常の認められた器官を0.1 Mリン酸緩衝10 %ホルマリン溶液に固定し保存した.
雌では採取した器官および組織のうち,卵巣は全例について,その他は不妊例を除く対照群7例および250 mg/kg投与群5例について雄と同様に病理組織標本を作製し,病理組織学検査を実施した.
病変部については雌雄ともに脱毛を除き病理組織学検査を行った.
雌では対照群の1例が投与38日の分娩中に死亡した.死亡するまで異常は全く観察されなかったが,病理組織学検査において肺および腎臓糸球体の毛細血管内にフィブリン血栓が認められたことから,フィブリン血栓に関連した原因により死亡したものと推測される.この他に死亡および瀕死例はなかった.雌の一般状態については,250 mg/kg投与群の1例に投与後一過性の流涎が認められた他に被験物質投与に起因すると考えられる異常は観察されなかった.

雌ではいずれの検査項目についても対照群と被験物質投与群との間で有意差は認められなかった.
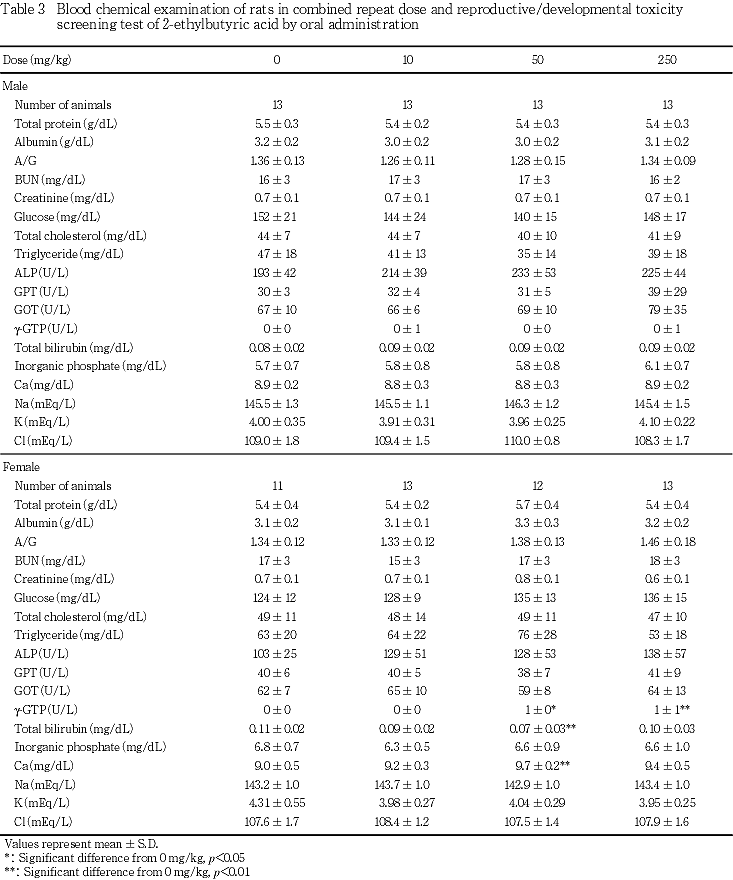
雌では,50 mg/kg以上の投与群においてγ-GTP活性が対照群と比較して軽度ながら有意(p<0.05,p<0.01)に上昇した.また,対照群と比較すると,50 mg/kg投与群において総ビリルビン濃度の有意(p<0.01)な減少およびカルシウム濃度の有意(p<0.01)な増加が認められたが,その他の投与群については対照群との間に有意差は認められなかった.上記以外の項目については,対照群と被験物質投与群との間で有意差は認められなかった.
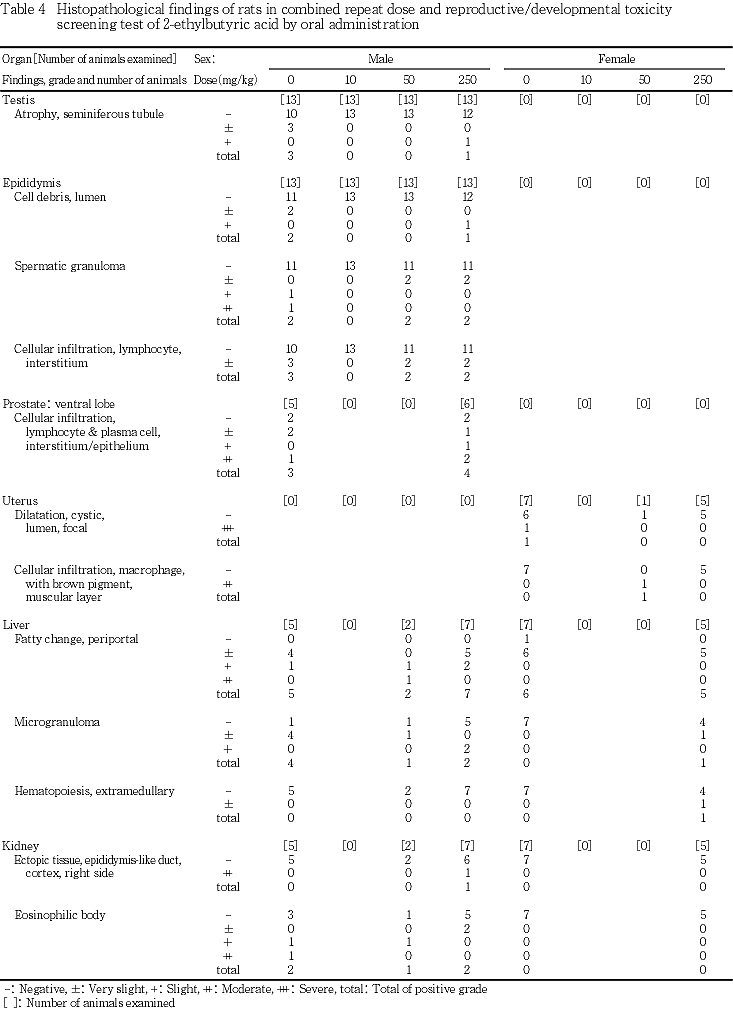
雌では,妊娠26日相当日に剖検した不妊例2例については,対照群の1例に所見は認められなかったが,50 mg/kg投与群の1例の胸腺に小型化が認められた.哺育5日の定期解剖では胸腺の小型化が対照群を含む各投与群に1例ずつ認められた.また,対照群の2例および10 mg/kg投与群の1例の腺胃粘膜に赤色点が認められ,10 mg/kg投与群の別の1例において前胃粘膜の肥厚が観察された.50 mg/kg投与群では1例の左側子宮角に赤色域が観察された.この他,対照群では1例に左側子宮角の限局性拡張が認められ,一般状態の観察において右腋窩皮下に結節の認められた例にはその部位に腫瘤が認められた.
雌でも子宮,肝臓,腎臓,脾臓,肺および気管,胸腺,膀胱,甲状腺に所見が認められたが,いずれも被験物質投与に起因した変化ではなかった.また,対照群の1例において右腋窩皮下に腫瘤が認められた例には,腋窩部の乳腺にリンパ球およびマクロファージの浸潤が認められ,乳管内には細胞残屑が認められた.
哺育状態の異常はいずれの投与群の動物にも認められなかった.
出生児の生存性を対照群と比較すると,250 mg/kg投与群において出産生児数,生児出産率および出生率が有意(p<0.05,p<0.01)に低下した.産児数および分娩率もやや低下したが,有意差は認められなかった.哺育0日における性比については対照群と被験物質投与群との間で有意差は認められなかった.哺育期間中はいずれの投与群においても死亡児が増加することはなく,新生児の4日の生存率は対照群と被験物質投与群との間で有意差は認められなかった.しかし,250 mg/kg投与群では哺育0日において低下していた生児数がそのまま維持されたため,対照群と比較すると,哺育4日における生児数に有意差(p<0.05)が認められた.哺育4日における性比については対照群と被験物質投与群との間で有意差は認められなかった.
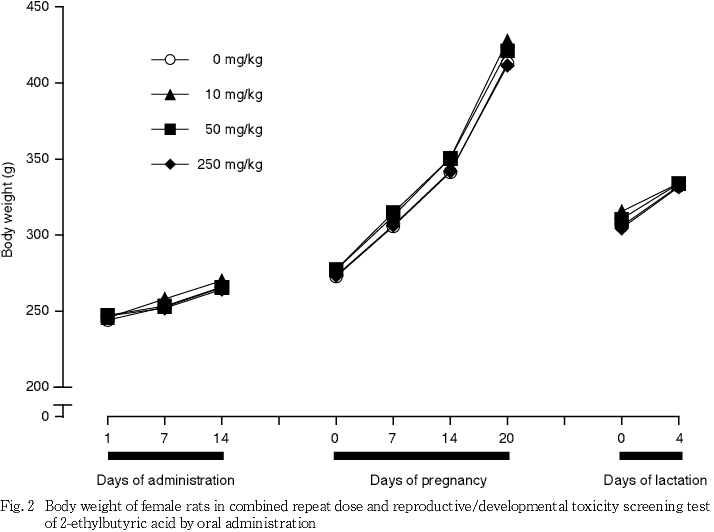
体重については雌雄ともにいずれの時期も対照群と被験物質投与群との間で有意差は認められなかった.
生存産児の形態観察(表には示さず)では,分娩途中で母動物が死亡した対照群の1腹の雌産児2例に,胸部および両前肢皮下に血液の貯留,皮膚の乾燥,ならびに左側後肢末端の皮下血腫および尾の小血腫あるいは吻部および両後肢の皮下血腫が認められたが,内臓に異常は観察されなかった.死亡児の形態に異常は観察されなかった.哺育4日における剖検では50 mg/kg投与群の1腹の雌2例に曲尾が観察された他に,いずれの投与群にも異常は観察されなかった.

予備試験では1000 mg/kgの反復投与を受けた雄が呼吸異常を示して瀕死状態に至ったが,本試験では瀕死あるいは死亡動物は認められなかった.Narotskyら1)は,器官形成期にあたる妊娠時期に2-エチル酪酸を150あるいは250 mg/kg経口投与すると母動物が誤嚥により呼吸異常を示して死亡することを報告し,これは被験物質の消化管に対する刺激作用によるものであると推定している.予備試験において瀕死状態に至った動物に誤嚥は認められなかったが,呼吸異常の成因を知るために本試験では病理組織学検査に上部気道を加えた.また,予備試験のそれより最高用量を減らし,胃管の外壁に被験物質が全く付着しないように投与したところ,死亡および瀕死のみならず呼吸異常も観察されなかった.病理学検査においても上部気道から肺に至るまで呼吸器に異常は観察されなかったため,予備試験でみられた呼吸異常の成因を知ることはできなかった.
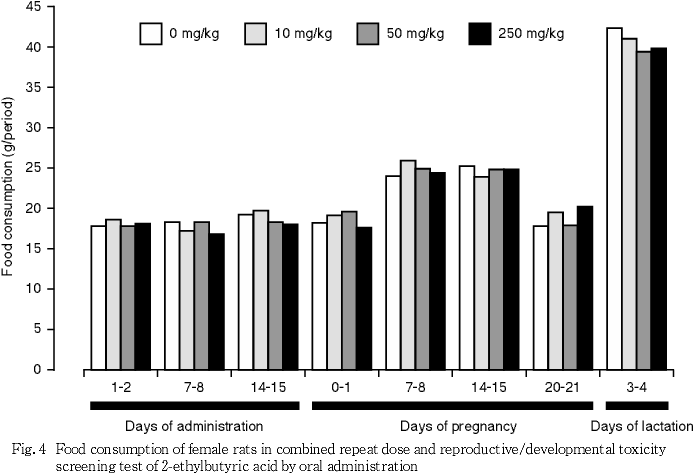
体重増加および摂餌量には被験物質投与の影響は認められなかった.
雌雄ともに,250 mg/kg投与群において腎臓重量あるいはその相対重量が増加した.高用量群に認められた変化であり,予備試験においても腎臓重量の増加が雌雄に認められていたことから被験物質投与による影響であると考えられる.しかし,血液生化学検査では腎機能を示す各指標に被験物質投与の影響は認められず,病理組織学検査においても異常は観察されなかったことからその成因は不明である.その他の器官の重量には雌雄ともに被験物質投与の影響は認められなかった.
血液学検査では,50 mg/kg以上の投与群の雄において白血球数が軽度に減少し,250 mg/kg投与群では血小板数も減少した.いずれも軽微な変化であるが,用量に依存して変動していることから被験物質投与に起因した変化であると考えられる.白血球数の減少については,リンパ球以外の白血球比率はむしろ対照群より高い値を示していたことから,リンパ球数の減少に由来するものと推測される.雌動物の血液学検査には投与の影響は認められなかった.
雌の血液生化学検査において50 mg/kg以上の投与群のγ-GTP活性がやや上昇した.しかしその程度はごく軽微であり,50 mg/kgおよび250 mg/kg両群間で被験物質の用量に関連した変化が認められなかった.また,その他の肝機能を表す指標に投与の影響は認められず,肝臓重量および肝臓の病理組織学検査においても投与に起因する異常は観察されなかったことから,50 mg/kg以上の投与群において認められたγ-GTP活性の僅かな上昇は偶発的変化であると判断された.その他の変化はいずれも被験物質の投与量とは無関係に認められた変化であることから被験物質投与による影響ではないものと考えられる.雄の血液生化学検査成績には投与の影響は認められなかった.
病理学検査ではいずれの器官にも被験物質投与の影響は認められなかった.
対照群の1例が分娩中にフィブリン血栓に関連した原因により死亡した.分娩状態の異常は50 mg/kg以上の投与群にも少数例ずつ認められたが,いずれも分娩翌日以降の哺育状態には異常が認められなかったことから,対照群の死亡例とは異なる原因により分娩状態に異常をきたしたものと推測される.
250 mg/kg投与群において出産生児数が減少した.着床数には投与の影響は認められず,産児数は軽度な減少に留まっていたことから,出生時の死亡が増加したことによるものと考えられる.250 mg/kg投与では,1例ではあるが,分娩状態の異常が認められ,その例では生児出産率および出生率も著しい低値(いずれも38.5 %)を示した.その他の動物の分娩状態に異常は認められなかったが,250 mg/kg投与では生児出産率および出生率が有意に低下していたことから,250 mg/kgの2-エチル酪酸投与は分娩に影響を及ぼし,産児の生存性を低下させるものと考えられる.50 mg/kg投与群においても2例に分娩の異常が観察された.2例のうち1例は生児出産率および出生率がやや低かった(いずれも68.8 %).また,50 mg/kg投与群の生児出産率および出生率は対照群との間に有意差は認められなかったが,やや低い値を示していたことから50 mg/kg投与も分娩に影響を及ぼす可能性があるものと推測される.10 mg/kg投与群では分娩および出生児の生存性のいずれにも投与の影響は認められなかった.出生児の性比および発育ならびに分娩翌日以降の生存性についてはいずれの投与群においても被験物質投与の影響は認められなかった.
2-エチル酪酸は,催奇形物質であるバルプロ酸と類似した化学構造を有する化学物質である.本試験では50 mg/kg投与群の同腹の2例に曲尾が認められた.曲尾は本系統のラットでしばしば観察される奇形であり,用量とは無関係に1腹のみに観察されたことから,本例は自然発生によるものと判断された.従って,250 mg/kgまでの投与量の2-エチル酪酸に催奇形性はないものと判断された.
| 1) | M. G. Narotsky, E. Z. Francis, R. J. Kavlock, Fundam. Appl. Toxicol., 22, 251(1994). |
| 連絡先 | |||
| 試験責任者: | 代田眞理子 | ||
| 試験担当者: | 佐藤昌子,一原佐知子 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Mariko Shirota(Study director) Masako Sato, Sachiko Ichihara | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||