2,6-ジメチルアニリンの培養細胞に及ぼす細胞遺伝学的影響について,チャイニーズ・ハムスター培養細胞(CHL/IU)を用いて染色体異常試験を実施した.
細胞増殖抑制試験結果をもとに,短時間処理法S9 mix非存在下では1212 μg/mLを最高処理濃度とした152〜1212 μg/mLの濃度範囲で4用量を,S9 mix存在下では1212 μg/mLを最高処理濃度とした457〜1212 μg/mLの濃度範囲で7用量を設定した.S9 mix存在下および非存在下で6時間処理(18時間の回復時間)後,標本を作製し,検鏡することにより染色体異常誘発性を検討した.S9 mix非存在下では303,606,1212 μg/mLの3用量(公比2),S9 mix存在下では633,744,876 μg/mLの3用量(公比20/17)について顕微鏡観察を実施した.
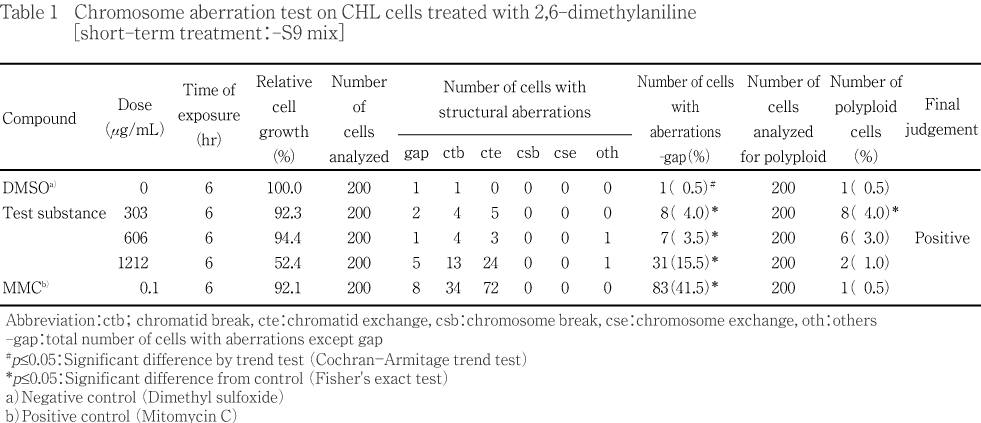
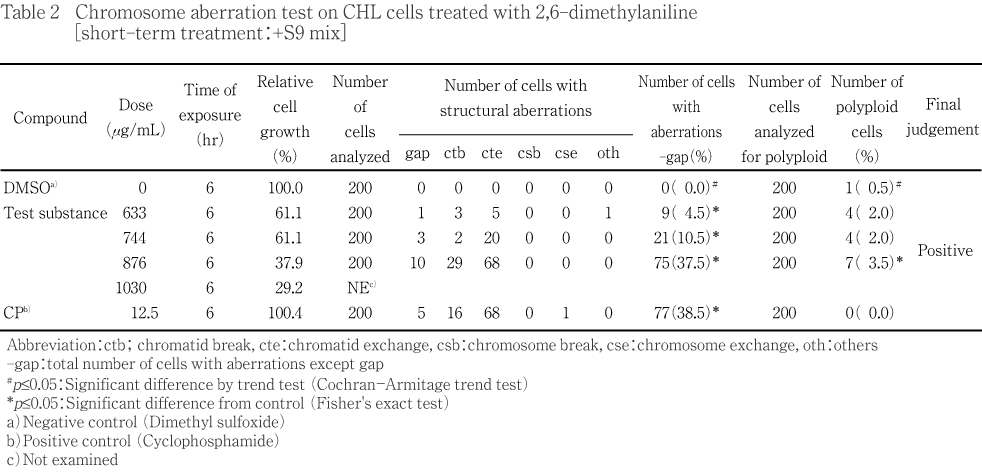
その結果,S9 mix非存在下および存在下のいずれにおいても用量相関性を伴い,統計学的に有意な染色体異常の誘発が認められた.
以上の結果より,本試験条件下では2,6-ジメチルアニリンは,染色体異常を誘発する(陽性)と結論した.
| 成分 | S9 mix 1 mL中の量 |
| S9 | 0.3 mL |
| MgCl2 | 5 μmol |
| KCl | 33 μmol |
| G-6-P | 5 μmol |
| NADP | 4 μmol |
| HEPES緩衝液(pH 7.2) | 4 μmol |
| 蒸留水 | 0.1 mL |
被験物質の2,6-ジメチルアニリン(ロット番号: WAQ5400)は純度99.8 %の暗褐色澄明の液体である.本剤はDMSOに易溶である.和光純薬工業(静岡)から購入した被験物質を使用した.被験物質は,使用時まで室温,遮光で保管した.試験終了後,被験物質購入元において残余被験物質を分析した結果,安定性に問題はなかった.
試験の都度,モレキュラーシーブを用いて脱水処理を行ったDMSOで被験物質を溶解し,調製原液とした.調製原液を使用溶媒を用いて順次所定濃度に希釈した後,速やかに処理を行った.
12ウエルの細胞培養用マルチプレートに細胞を播種し,培養3日後に被験物質液を処理した.短時間処理法ではS9 mix非存在下(-S9処理)あるいは存在下(+S9処理)で6時間処理した後,新鮮な培養液に交換してさらに18時間培養を続けた.
細胞を10 vol%中性緩衝ホルマリン液(和光純薬工業)で固定した後,0.1 w/v%クリスタル・バイオレット(関東化学)水溶液で10分間染色した.色素溶出液(30 vol%エタノール,1 vol%酢酸水溶液)を適量加え,5分間程度放置して色素を溶出した後,分光光度計(105-50型:日立製作所)を用いて580 nmでの吸光度を測定した.各用量群について溶媒対照群での吸光度に対する比,すなわち相対細胞増殖率を算出し,さらにプロビット法を用いて50 %細胞増殖抑制濃度を算出した.
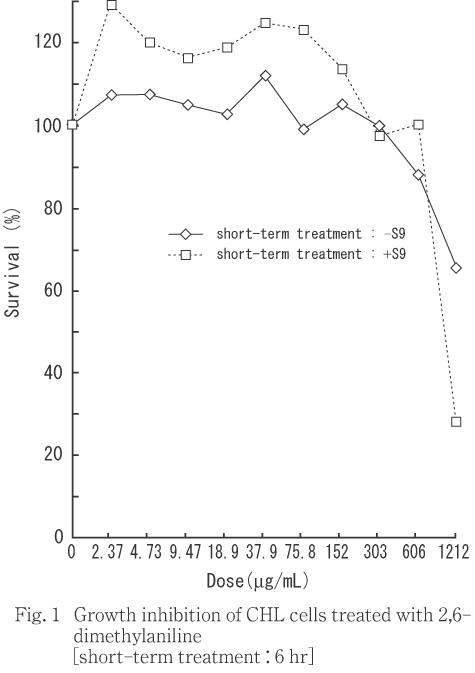
その結果,細胞増殖を50 %抑制する濃度は,短時間処理法+S9処理で1025 μg/mLと算出された.なお,短時間処理法-S9処理では,いずれの被験物質処理においても相対細胞増殖率が溶媒対照群の50 %以上であったので50 %細胞増殖抑制濃度は算出できなかった(Fig. 1).
被験物質処理開始および終了時にpHの変動,被験物質析出等の特筆すべき変化は,いずれの用量においても観察されなかった.
細胞増殖抑制試験結果をもとに,染色体異常試験では短時間処理法-S9処理および+S9処理とも1212 μg/mLを最高処理濃度とし,-S9処理では以下公比2で減じた4用量,+S9処理では公比20/17で減じた7用量ならびに溶媒対照群を設定した.
なお,陽性対照として,-S9処理でマイトマイシンC(MMC:協和醗酵工業)を0.1 μg/mL,+S9処理でシクロホスファミド(CP:塩野義製薬)を12.5 μg/mLの用量で試験した.
直径60 mmのプレートを用い,細胞増殖抑制試験と同様に被験物質等の処理を行った.培養終了2時間前に,最終濃度で0.2 μg/mLとなるようコルセミド(Invitrogen)を添加した.トリプシン処理で細胞を剥離させ,遠心分離により細胞を回収した.75 mmol/L塩化カリウム水溶液で低張処理を行った後,固定液(メタノール3容:酢酸1容)で細胞を固定した.空気乾燥法で染色体標本を作製した後,1.2 vol%ギムザ染色液で12分間染色した.

各プレートあたり100個,すなわち用量当たり200個の分裂中期像を顕微鏡下で観察し,染色体の形態的変化としてギャップ(gap),染色分体切断(ctb),染色体切断(csb),染色分体交換(cte),染色体交換(cse)およびその他(oth)の構造異常に分類した.同時に,倍数性細胞の出現率を記録した.染色体の分析は日本環境変異原学会・哺乳動物試験分科会による分類法2)に従って実施した.
すべての標本をコード化した後,染色体分析を実施した.
ギャップを含めない場合(-gap)について染色体構造異常の出現頻度を表示した.
各試験群の構造異常を有する細胞あるいは倍数性細胞の出現頻度を,Fisherの直接確率計算法(有意水準0.05)を用いて検定した.また用量依存性については,Cochran Armitageの傾向検定(有意水準0.05)を用いて検定した.溶媒対照群と比較し被験物質処理群において有意差が認められ,かつ,再現性あるいは用量に依存性が認められた場合に陽性と判定した.ただし,最終的な判定は試験条件下での生物的な妥当性も考慮して行った.
また,分裂中期像の20 %にいずれかの異常を誘発するのに必要な被験物質濃度であるD20値を最小二乗法により算出し,一定濃度(mg/mL)あたりの交換型異常(cte)出現数を示す比較値であるTR値を,染色分体交換の出現頻度(%)を被験物質濃度(mg/mL換算)で割ることにより算出した.
染色体標本作製時に各プレートの低張処理した細胞液を一定量採取し,ATP測定用試薬キット(ルシフェール250:キッコーマン)およびATPフォトメーター(ルミテスターC-100LU:キッコーマン)を用いて相対発光量(Relative Light Unit:RLU)を求めATP含量を測定した.陰性対照群におけるRLUに対する比(=相対細胞増殖率)を各用量群について求め,細胞増殖抑制度とした.
短時間処理法での試験結果をTable 1〜2に示した.2,6-ジメチルアニリン処理群の場合,染色体構造異常出現頻度は,-S9処理では303 μg/mLで4.0 %(p<0.05),606 μg/mLで3.5 %(p<0.05),1212 μg/mLで15.5 % (p<0.05),+S9処理では633 μg/mLで4.5 %(p<0.05),744 μg/mLで10.5 %(p<0.05),876 μg/mLで37.5 %(p<0.05)を示し,用量依存性(p<0.05)も確認された.倍数性細胞の出現頻度については,+S9処理において試験用量に依存した有意な増加(p<0.05)が観察された.また,-S9処理ならびに+S9処理とも試験用量に依存した相対細胞増殖率の減少が観察され,-S9処理では最高用量である1212 μg/mLでの相対細胞増殖率が52.4 %であった.+S9処理では染色体異常評価群中の高用量である876 μg/mLでの相対細胞増殖率は37.9 %であった.一方,S9 mix非存在下における陽性対照物質MMCで処理した細胞,およびS9 mix存在下における陽性対照物質CPで処理した細胞では染色体構造異常の顕著な誘発が認められた.
変異原性の強さに関する相対的比較値であるD20値の最小値は0.756(mg/mL),TR値の最大値は38.8(mg当たり)と算出された.数的異常については,統計学的に有意(p<0.05)な増加が認められたが,背景データによる基準値内であったことから陰性反応と判断した.なお,被験物質処理開始および終了時にpHの変動,被験物質析出等の特筆すべき変化は,いずれの用量においても観察されなかった.
以上の試験結果から,本試験条件下において2,6-ジメチルアニリンのチャイニーズ・ハムスター培養細胞に対する染色体異常誘発性に関し,陽性と判定した.
なお,本被験物質(2,6-ジメチルアニリン)について,マウスを用いた小核試験で陰性3,4),ラットあるいはマウスを用いたUDS試験で陰性5)との報告があった.また,ラットを用いた32P−ポストラベル試験で,DNA付加体の形成が確認され6),BALB/c-3T3細胞を用いたトランスフォーメーション試験で陽性との報告7)があった.さらにNTPデータでは,本被験物質がラット(雌雄)の2年間発がん試験(混餌)で,鼻腔に明確な腫瘍の形成を誘発することが示され8),また,遺伝毒性に関してはAmes試験では陰性もしくは弱い陽性,染色体異常試験では陽性,SCE試験では陽性,ショウジョウバエを用いた優性致死試験では陰性結果が示されていた9).また,鼻腔に発がん性を示すことから,国立医薬品食品衛生研究所変異遺伝部のグループ(鈴木ら)がトランスジェニックマウスを用いて突然変異を検討したところ,鼻腔細胞でのみ突然変異の蓄積を認めている(データ未発表).なお,本被験物質の代謝物であるN-ヒドロキシ-2, 6-ジメチルアニリンについてAmes試験で陽性10)との報告があった.
類縁体である2,3-ジメチルアニリン,2,4-ジメチルアニリンおよび2,5-ジメチルアニリンについてAmes試験で陽性11)との報告があった.
| 1) | Matsuoka A, Hayashi M, Ishidate M Jr: Chromosomal aberration tests on 29 chemicals combined with S9 mix in vitro. Mutation Res, 66:277-290(1979). |
| 2) | 日本環境変異原学会・哺乳動物試験分科会(編):「化学物質による染色体異常アトラス」,朝倉書店,東京(1988)pp. 31-35. |
| 3) | Parton JW, Probst GS, Garriott ML:The in vivo effect of 2,6-xylidine on induction of micronuclei in mouse bone marrow cells. Mutation Res, 206: 281-283.(1988). |
| 4) | Parton JW, Beyers JE, Garriott ML, Tamura RN: The evaluation of a multiple dosing protocol for the mouse bone-marrow micronucleus assay using benzidine and 2,6-xylidine. Mutation Res, 234: 165-168(1990). |
| 5) | Mirsalis JC, Tyson CK, Steinmetz KL, Loh EK, Hamilton CM, Bakke JP, Spalding JW: Measurement of unscheduled DNA synthesis and S-phase synthesis in rodent hepatocytes following in vivo treatment:testing of 24 compounds. Environ Mol Mutagen, 14:155-164(1989). |
| 6) | Jeffrey AM, Luo FQ, Amin S, Krzeminski J, Zech K, Williams GM:Lack of DNA binding in the rat nasal mucosa and other tissues of the nasal toxicants roflumilast, a phosphodiesterase 4 inhibitor, and a metabolite, 4-amino-3,5-dichloropyridine, in contrast to the nasal carcinogen 2,6-dimethylaniline. Drug Chem Toxicol , 25:93-107(2002). |
| 7) | Matthews EJ, Spalding JW, Tennant RW: Transformation of BALB/c-3T3 cells:IV.Rank- ordered potency of 24 chemical responses detected in a sensitive new assay procedure. Environ Health Perspect 101 Suppl 2: 319-345(1993). |
| 8) | National Toxicology Program. Natl Toxicol Program Tech Rep Ser, 278:1-138(1990). |
| 9) | National Toxicology Program. 2,6-XYLIDINE. Available from URL:http://ntp.niehs.nih.gov/ index.cfm?objectid=071A7019-D98F-0BEA-F9 A168FA705384FF |
| 10) | Matilde Marques M, Gamboa da Costa G, Blankenship LR, Culp SJ, Beland FA:The effect of deuterium and fluorine substitution upon the mutagenicity of N-hydroxy-2,6-dimethylaniline. Mutation Res, 506-507:41-48(2002). |
| 11) | Zimmer D, Mazurek J, Petzold G, Bhuyan BK: Bacterial mutagenicity and mammalian cell DNA damage by several substituted anilines. Mutation Res , 77:317-326(1980). |
| 連絡先 | |||
| 試験責任者: | 益森勝志 | ||
| 試験担当者: | 田中 仁,仲村渠奈美子,
尾h伸也,嶋田佐和子 古屋有佳子,鈴木ゆみ子, 鈴木雅也 | ||
| 7食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | |||
| Authors: | Shoji Masumori(Study director) Jin Tanaka, Namiko Nakandakari, Shin-ya Ozaki, Sawako Shimada, Yukako Furuya, Yumiko Suzuki, Masaya Suzuki | ||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | |||
| 582-2 Shioshinden , Fukude-cho, Iwata-gun,
Shizuoka, 437-1213, Japan | |||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | ||