細胞増殖抑制試験の結果をもとに,いずれの処理条件においても5000 μg/mLを最高濃度として,連続処理法の24,48時間処理および短時間処理法のS9 mix存在下では公比2で4用量,短時間処理法のS9 mix非存在下では公比2で5用量を設定した.
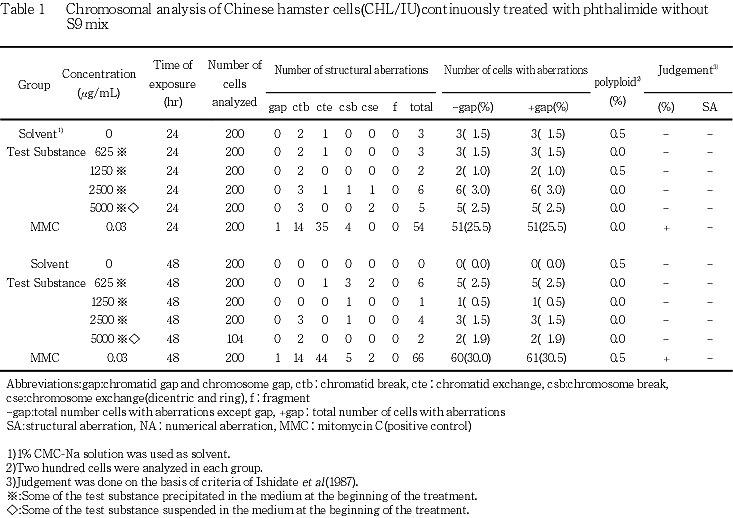
CHL/IU細胞を24時間および48時間連続処理した結果,いずれの処理群においても,染色体の構造異常細胞の誘発は観察されなかった.また,短時間処理法のS9 mix存在下の5000 μg/mLにおいて,染色体の構造異常細胞の出現頻度は10.0 %であった.一方,短時間処理法のS9 mix非存在下では,構造異常細胞の誘発は観察されなかった.また,数的異常細胞の誘発は全ての処理条件で5 %未満であった.
以上の結果より,本試験条件下ではフタルイミドは,染色体異常を誘発する(陽性)と結論した.
連続処理法では,細胞播種3日目に被験物質を加え,24時間および48時間処理した.また,短時間処理法では,細胞播種3日目にS9 mixの存在下および非存在下で6時間処理し,処理終了後新鮮な培養液でさらに18時間培養した.
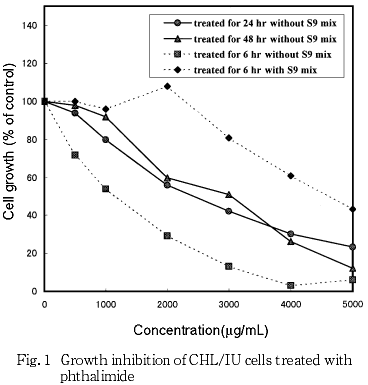
その結果,フタルイミドの約50 %の増殖抑制を示す濃度を,プロビット法により算出したところ,連続処理法の24時間および48時間処理ではそれぞれ2356, 2540 μg/mLであった.
また,短時間処理法のS9 mix存在下および非存在下における約50 %の増殖抑制を示す濃度は,それぞれ4524,991 μg/mLであった(Fig. 1).

陽性対照として,連続処理法は,マイトマイシンC(協和発酵工業(株),ロット番号:139AFK)を0.03 μg/mL,短時間処理法は,ベンゾ[a]ピレン(東京化成工業(株),ロット番号:AX01)を20 μg/mLに設定した.
構造異常および倍数性細胞については1群200個の分裂中期細胞を分析した.
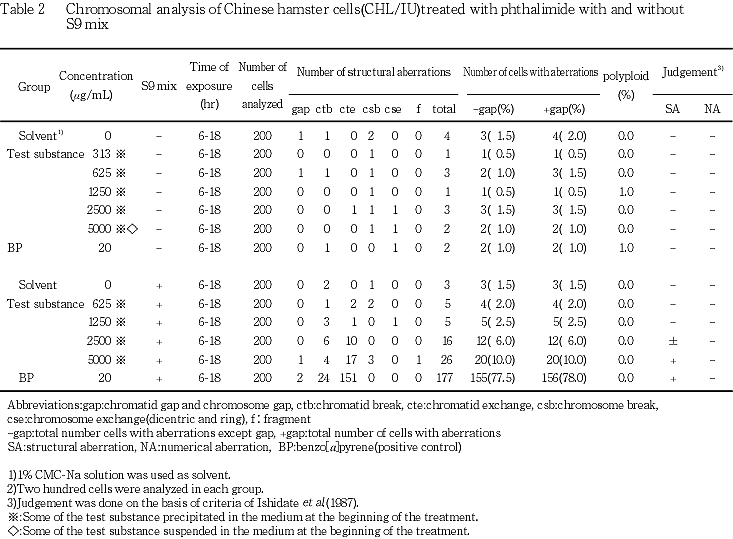
短時間処理法による染色体分析の結果をTable 2に示した.フタルイミドを加えてS9 mix存在下および非存在下で6時間処理した結果,S9 mix存在下の5000 μg/mLにおいて,構造異常細胞の出現頻度10.0 %であった.一方,数的異常細胞の出現頻度は5 %未満であった.
また,S9 mix非共存下では,染色体の構造異常および数的異常の誘発作用は認められなかった.
以上の結果から,フタルイミドは本試験条件下において,染色体異常誘発性を有すると結論した.
なお,Agar法によるマウスリンフォーマ試験において,類似化合物(phthalimidoの開環した物質,C6H4(CONH2)2)は,S9 mix存在下および非存在下の50 μg/mLでL5178Y(TK+/-)細胞に対して遺伝子突然変異を誘発しないと報告されている3).
| 1) | 日本環境変異原学会・哺乳動物試験分科会編,"化学物質による染色体異常アトラス,"朝倉書店,東京,1988,pp. 16-37. |
| 2) | 石館基監修,"〈改訂〉染色体異常試験データ集,"エル・アイ・シー社,東京,1987,p. 19. |
| 3) | D. B. McGregor et al., Environmental and Molecular Mutagenesis, 12, 85(1988). |
| 連絡先 | |||
| 試験責任者: | 太田絵律奈 | ||
| 試験担当者: | 中川宗洋,石毛裕子,穴澤由美子,玉川 恵 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-0255 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Erina Ohta(Study director) Munehiro Nakagawa, Yuko Ishige, Yumiko Anazawa, Megumi Tamagawa | |||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | ||||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255 Japan | ||||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |||