7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ��Υ�åȤ��Ѥ���
28����ȿ���и���Ϳ�����
Twenty-eight-day Repeat Dose Oral Toxicity Test
of Potassium 7-hydroxy-1,3-naphthalenedisulfonate in Rats
����
7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ���0(1 %�����������ʥȥꥦ����ϱ�)��100��300�����1000 mg/kg��1���������ͺ��7���뤤��14ɤ��Crj:CD(SD)��åȤ�28����ȿ���и���Ϳ����������Ƥ���������0�����1000 mg/kg���λ�ͺ��7ɤ���Ѥ���14���֤β�������ʻ���Ƹ�Ƥ���������η�̡��ʲ������Ӥ�������
���̾��֡��νš��ݱ��̡�Ǣ������˶������������ȿ��ظ����Ǥϡ�7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�ȴ�Ϣ�����Ѳ���ǧ����ʤ��ä�����ճظ����Ǥϡ��إޥȥ���å��͡��إ⥰���ӥ��̤�����ַ����ι��ͤ��뤤�Ϲ��ͷ����ʤ�Ӥ����ַ��Ψ�����ͤ����1000 mg/kg����ǧ���줿����������ظ����Ǥϡ������쥹�ƥ���������ͤ����300�����1000 mg/kg����ǧ���줿���ﴱ���̤Ǥϡ��¡�����н��̤�������н��̤����ͤ�ͺ��1000 mg/kg����ǧ���줿��
�ʾ�Τ��Ȥ��顤�ܻ�ˤ�����7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ���̵�ƶ���(NOEL)��ͺ��300 mg/kg/day�����100 mg/kg/day�Ǥ���ȹͤ���줿��
��ˡ
1.���︳ʪ���������Ϳ�դ�Ĵ��
7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ��(����:89.2 %��Lot No.:5501�����������ع���(��)���²λ�)�ϳ��������ä����ΤǤ��롥�������︳ʪ����̩���ƴ�����졤��Ž����¸������;�︳ʪ������¤�ȼԤ�ʬ�Ϥ�����Ϳ������ΰ��������ǧ���������ޤ�1 %�����������ʥȥꥦ����ϱ�(���������������������ʥȥꥦ�ࡤ��������(��)����������������������塤�䥯�ϥ�����(��))���Ѥ���������︳ʪ��������ǻ�٤Ȥʤ�褦�˷����������︳ʪ����Ĵ�����ѻ�Ĵ���Ȥ������ޤ���������Ĵ���դˤĤ���ǻ�٤�ʬ�Ϥ��������ͤΡ� 10 %����Ǥ��뤳�Ȥ��ǧ������
2.���ưʪ����ӻ�����
���ܥ��㡼�륹����С�(��)���������줿4�����Sprague-Dawley�ϥ�å�(Crj:CD(SD)IGS)�λ�ͺ��7���֤θ��֡��벽��Ԥä��塤��ͺ��42ɤ������5����ǻ�˶���������Ϳ�����ν��ϰϤ�ͺ��149��168 g����126��149 g�Ǥ��ä���ưʪ�ϡ�����22��24 �����41��56 %���������10��15��/���֤���Ӿ�������12����(8:00����20:00�ޤ�����)�����椵�줿�Хꥢ�����ƥ�λ��鼼�ǡ��֥饱�åȼ���°�����־��������˷�ʬ������5ɤ���⡤��ʬ����ϸ��̤ǻ��餷���������ϸǷ�����(CRF-1�����ꥨ����칩��(��))���°����´���Ѥ��ơ�������ϻ��ڻԿ�ƻ���ư������֤��뤤�ϵ�����Ѥ��ơ���ͳ���ݼ褵������
3.����Ϳ�̤������Ϳ��ˡ
��Ϳ�������Ǥ�1���������ͺ��5��Υ�åȤ�100��300�����1000 mg/kg��7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ���14����ȿ���и���Ϳ������̡�ͺ��1000 mg/kg�����νš��ݱ��̤���ӿ�¡�����н��̤ι��ͷ��������300�����1000 mg/kg���ǥ��륫��ե����ե������������ι��ͷ������ߤ�줿��
�ʾ�Τ��Ȥ��顤�����̷��ˤ�1000 mg/kg�����ꤷ���ʲ�������3�ǽ����ơ������̷��ˤ�300 mg/kg�������̷��ˤ�100 mg/kg����ˡ����ΤΤߤ���Ϳ�����оȷ���ä�����ͺ��4�������ꤷ����1����ưʪ���ϻ�ͺ�Ȥ�7ɤ�Ȥ����оȷ������1000 mg/kg���ˤ�2�������դ�����Ϳ���������νŤ˴�Ť����ز�̵������ˡ�ˤ�귲ʬ����Ԥä���
�Ƹ��Τ���Ϳ���̤���Ϳ���˺Ǥ�ᤤ¬�������νŤ˴�Ť���5 mL/kg�����̤ǥ�å��Ѱߥ���Ǥ��Ѥ��ơ�1��1��Ϣ³28���֡�����Ū�˰������Ϳ������
4.����������
1)�����̾��ִѻ�
��Ϳ�����椪��Ӳ���������ˡ�����ˤĤ���1��1��ʾ�����٤Ǵѻ�������
2)���ν�¬�ꤪ����ݱ���¬��
�νŤ�����ˤĤ��ơ���Ϳ1��(��Ϳ��)����Ϳ2��5��7��10��14��21�����28��(��Ϳ��λ��)������1����2��5��7�����14���ʤ�Ӥ�˶������¬�ꤷ����Ϳ1������28��������1������14�����ν������̤�����ν�����Ψ�Ф������ݱ��̤�˶������������νŤ�Ʊ������¬�ꤷ����
3)��Ǣ����
��Ϳ4������Ӳ���2�����������ե������˼��Ƥ������俩���Ǻ�Ǣ��Ԥ���Ʊ���˺�Ǣ��ΰ�����(����)��¬�ꤷ������3���֤���Ǣ�ˤĤ���pH�������������ȥ��Ρ������ӥ�Ρ����ӥ��ӥ������ȿ��(�ʾ塤�ޥ�ƥ����ƥ��å������Х����롦����)����Ĵ(����ѻ�)�ʤ�Ӥ�����(����)������21������Ǣ�ˤĤ���Ǣ��(����)�����(���ס�������)���ʥȥꥦ�प��ӥ��ꥦ��(�ʾ塤�������ˡ����ư������ٷ�480���������˥�)����������(����ũ��ˡ�������饤�ɥ�����CL-6M��ʿ�»���)�����륷����(OCPCˡ)�ʤ�Ӥ�̵�����(Fiske-SubbaRowˡ)(�ʾ塤��ưʬ������7150������Ω�����)��¬�ꤷ����
4)����ճظ���
��¸������ˤĤ�����16�����俩�����塤�����ƥ���첼��������̮���η줷��EDTA��2K�ǽ���������դ��Ѥ��ơ��ַ�����ʿ���ַ�����ѡ��쾮�Ŀ��������(�ʾ塤�ŵ���ˡ)���إ⥰���ӥ���(�������ȥإ⥰���ӥ�ˡ)(�ʾ塤�����륿��������T660���������륿��)���إޥȥ���å���(�ַ�����ʿ���ַ�����Ѥ�껻��)��ʿ���ַ��إ⥰���ӥ���(�ַ������إ⥰���ӥ��̤�껻��)��ʿ���ַ��إ⥰���ӥ�ǻ��(�إޥȥ���å��͡��إ⥰���ӥ��̤�껻��)�����ַ��Ψ(Brecherˡ)���������ɴʬ��(May-Gr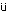 nwald-Giemsa����)��¬�ꤷ��������̮����μ褷��̵������դ��Ѥ��ƶŸǻ���(ή��Ǵ���Ѳ��ˤ�������¬��ˡ���ޥ�����������������������饤�ʡ�)��¬�ꤷ��������ˡ�ʢ����ư̮���μ褷����դ�����ʥȥꥦ��ǽ��������塤3000��ž/ʬ��10ʬ�ֱ�ʬΥ��������줿�������Ѥ��ơ��ץ��ȥ���ӥ����(�ȥ���ܥץ饹����ˡ)����ӳ�������ʬ�ȥ���ܥץ饹�������(���饸���ˡ)(�ʾ塤��նŸǼ�ư¬�����֥�����KC-10A���Х�������)��¬�ꤷ����
nwald-Giemsa����)��¬�ꤷ��������̮����μ褷��̵������դ��Ѥ��ƶŸǻ���(ή��Ǵ���Ѳ��ˤ�������¬��ˡ���ޥ�����������������������饤�ʡ�)��¬�ꤷ��������ˡ�ʢ����ư̮���μ褷����դ�����ʥȥꥦ��ǽ��������塤3000��ž/ʬ��10ʬ�ֱ�ʬΥ��������줿�������Ѥ��ơ��ץ��ȥ���ӥ����(�ȥ���ܥץ饹����ˡ)����ӳ�������ʬ�ȥ���ܥץ饹�������(���饸���ˡ)(�ʾ塤��նŸǼ�ư¬�����֥�����KC-10A���Х�������)��¬�ꤷ����
5)����������ظ���
��¸������ˤĤ�����16�����俩�����塤�����ƥ���첼�ǡ�ʢ����ư̮���μ褷����դ�3000��ž/ʬ��10ʬ�ֱ�ʬΥ��������줿�������Ѥ���GOT(IFCCˡ)��GPT(IFCCˡ)�����륫��ե����ե�������(Bessey-Lawryˡ)������æ���ǹ���(Wr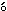 blewski & La Dueˡ)����-GTP(����L-��-���륿�ߥ�-��-�˥ȥ����˥�ɴ��ˡ)�����륳����(�إ������ʡ���ˡ)�������쥹�ƥ�����(����ˡ)���ȥꥰ�ꥻ���(ͷΥ���ꥻ������õ�ˡ)�����ӥ��ӥ�(�����ӥ��ӥ�ˡ)��Ǣ������(���쥢����������ɥե��Ρ���ˡ)�����쥢���˥�(Jaff
blewski & La Dueˡ)����-GTP(����L-��-���륿�ߥ�-��-�˥ȥ����˥�ɴ��ˡ)�����륳����(�إ������ʡ���ˡ)�������쥹�ƥ�����(����ˡ)���ȥꥰ�ꥻ���(ͷΥ���ꥻ������õ�ˡ)�����ӥ��ӥ�(�����ӥ��ӥ�ˡ)��Ǣ������(���쥢����������ɥե��Ρ���ˡ)�����쥢���˥�(Jaff ˡ)�����륷����(OCPCˡ)��̵�����(Fiske-SubbaRowˡ)��������(�ӥ���å�ˡ)����ӥ���֥ߥ�(BCGˡ)(�ʾ塤��ưʬ������7150������Ω�����)���ʥȥꥦ�प��ӥ��ꥦ��(�ʾ塤�������ˡ����ư������ٷ�480���������˥�)����������(����ũ��ˡ�������饤�ɥ�����CL-6M��ʿ�»���)��A/G��(��������֥ߥ��껻��)�ʤ�Ӥ�����ʬ��(��������������ơ������ŵ���ưˡ������ư�ŵ���ư����CTE-150�����)��¬�ꤷ����
ˡ)�����륷����(OCPCˡ)��̵�����(Fiske-SubbaRowˡ)��������(�ӥ���å�ˡ)����ӥ���֥ߥ�(BCGˡ)(�ʾ塤��ưʬ������7150������Ω�����)���ʥȥꥦ�प��ӥ��ꥦ��(�ʾ塤�������ˡ����ư������ٷ�480���������˥�)����������(����ũ��ˡ�������饤�ɥ�����CL-6M��ʿ�»���)��A/G��(��������֥ߥ��껻��)�ʤ�Ӥ�����ʬ��(��������������ơ������ŵ���ưˡ������ư�ŵ���ư����CTE-150�����)��¬�ꤷ����
6)��˶������Ӵﴱ����¬��
��¸��ˤĤ��Ƥ���Ϳ28������Ӳ���14���������ˡ����Τ����˻�������ˤĤ��Ƥ��˻����ˡ��γ�ɽ��ѻ����������ƥ���첼�Ǻη�������व��˶���������ޤ���Ǿ�������Ρ��������þ���(���龮�δޤ�)���١���¡����¡����¡���¡�����ա����㤪�������ν��̤�¬�ꤹ��ȤȤ�ˡ����н��̤�˶���������νŤǽ���100��褸�����н��̤Ф�����
7)�������ȿ��ظ���
����ˤĤ��ƴ�¡����¡���¡����¡���١�Ǿ(��Ǿ����Ǿ)�������Ρ����ա��þ��������龮�Ρ�������IJ��������ᡤ�¡���塤���ܥ����ᡤ�ܲ������岼���������������������桤������������ܹ�(�����ޤ�)���Կ�(����)�����ʶ�(��¦����)��������ư̮����Ƭ�����ɡ����ɻ١���ƻ����(���ߡ�����)�������IJ����IJ����IJ����IJ����IJ��ľIJ���������ǹ(�Ÿ�����ޤ�)����Ω�������㡤�ҵܡ�紤���Ӻ������Ф�10 %�����˾ץۥ�ޥ��դǡ����㤪���������Τ�֥���դǡ���太��ӥϡ���������ǥӥåɥ���դǸ��ꤷ����������Ŧ�дﴱ���ȿ����ˡ�ˤ������äƥѥ�ե�����������ڤ����إޥȥ�����������������������������������
5.�����ײ���
�νš��ν������̤�����ν�����Ψ���ݱ��̡�Ǣ����������Ū���ܡ���ճظ�������������ظ������ﴱ�����н��̤�������н��̤η�̤ˤĤ���Bartlett�θ���ˡ��Ԥ�����ʬ��������Ϥ�������ʬ���ξ��ϰ층����ʬ��ʬ��ˡ�ˤ����Ϥ�������ʬ���ξ���Kruskal-Wallis�θ���ˡ�Dz��Ϥ�����Kruskal-Wallisˡ�β��Ϥη�̡�ͭ�պ���ǧ���줿���ˤϡ�Mann-Whitney��U-����ˡ�Dz��Ϥ�����
Ǣ��Ť����Ǣ����������Ū���ܤη�̤ˤĤ��Ƥϡ�Kruskal-Wallis�θ���ˡ�Dz��Ϥ���ͭ�պ���ǧ���줿���ϡ�Mann-Whitney��U-����ˡ���Ѥ��Ʋ��Ϥ�����
������оȷ����︳ʪ����Ϳ���Ȥδ֤θ���ˤ����Ƥϡ��������ͭ�տ���5 %�Ȥ�����
���
1.�����̾���
��Ϳ���֤ˤϡ���ͺ�Ȥ�˰۾��ǧ����ʤ��ä���
�������֤ˤϡ�ͺ���оȷ���1��Dz���13���˿�夬ǧ���줿���ᡤ�˻�����˶����Ԥä��Ȥ�����ɡ���˹��ޤ�ǧ���졤��Ǣ�˻��Ѥ�����ե�������Ǥλ��Τˤ���ǽ�����ͤ���줿����Ǥϰ۾��ǧ����ʤ��ä���
2.���ν�
��ͺ�Ȥ���оȷ��Ȥδ֤˺���ǧ����ʤ��ä���
3.���ݱ���
��Ϳ���֤ˤϡ�ͺ�Ǥ��оȷ��Ȥδ֤˺���ǧ����ʤ��ä�����Ǥϡ�1000 mg/kg������Ϳ2�����ݱ��̤ι��ͤ�ǧ���줿������������Ѳ��Ǥ��ꡤ7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�Ȥδ�Ϣ�Ϥʤ���Τȹͤ���줿��
�������֤ˤϡ���ͺ�Ȥ���оȷ��Ȥδ֤˺���ǧ����ʤ��ä���
4.��Ǣ����
��Ϳ���ֺǽ����ˤϡ�ͺ��300��1000 mg/kg���ʤ�Ӥ˻��1000 mg/kg���ǥ��ꥦ�������̤ι��ͤ�ǧ���줿���ޤ���ͺ��1000 mg/kg���ǥʥȥꥦ�������̤����ͤ�ǧ���줿��
�������ֺǽ����ˤϡ����1000 mg/kg���ǥ��륷���������̤ι��ͤ���Ӱ����̤ι��ͤ�ǧ���줿������������Ϳ���ֽ�λ����Ʊ�ͤ��Ѳ���ǧ����Ƥ��ʤ����ȡ��������ֽ�λ���η�������ظ�������������ȿ��ظ������õ����٤��Ѳ���ǧ����ʤ��ä����Ȥ��顤��ȯŪ���Ѳ��ȹͤ���줿��
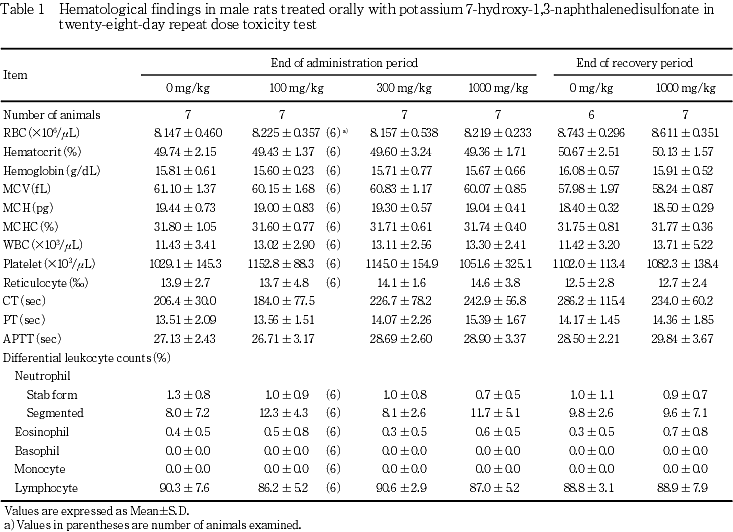
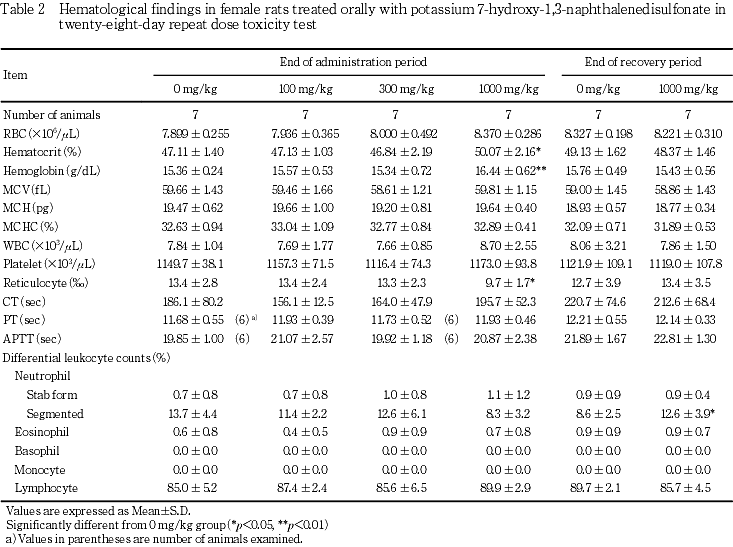
5.����ճظ���(Table 1, 2)
��Ϳ���ֽ�λ���ˤϡ�ͺ�Ǥϡ��оȷ��Ȥδ֤˺���ǧ����ʤ��ä�����Ǥϡ�1000 mg/kg���ǥإޥȥ���å��ͤ���ӥإ⥰���ӥ��̤ι��͡��ַ����ι��ͷ����ʤ�Ӥ����ַ��Ψ�����ͤ�ǧ���줿��
�������ֽ�λ���ˤϡ�ͺ�Ǥ��оȷ��Ȥδ֤˺���ǧ����ʤ��ä�����Ǥϡ�1000 mg/kg����ʬ�ճ˹����Ψ�ι��ͤ�ǧ���줿������������ư������������������Ѳ��ʤɤ�ǧ����ʤ��ä����Ȥ��顤��ȯŪ���Ѳ��ȹͤ���줿��
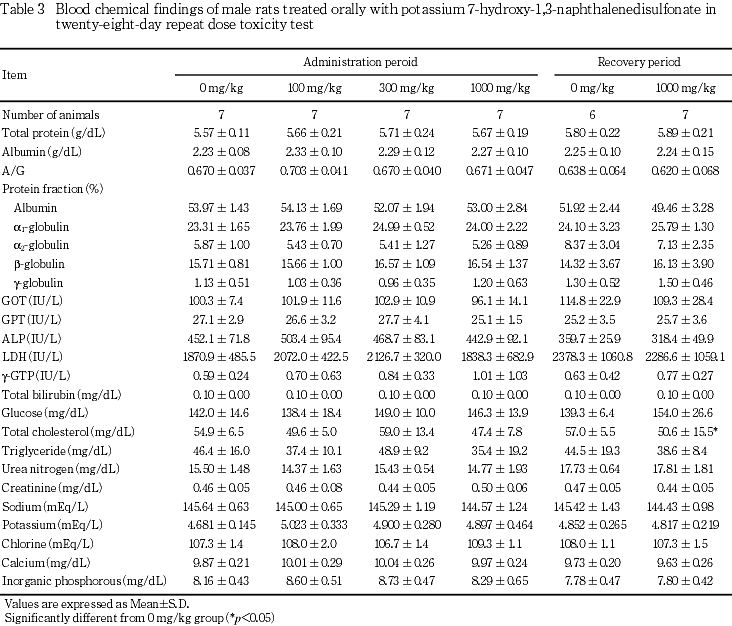
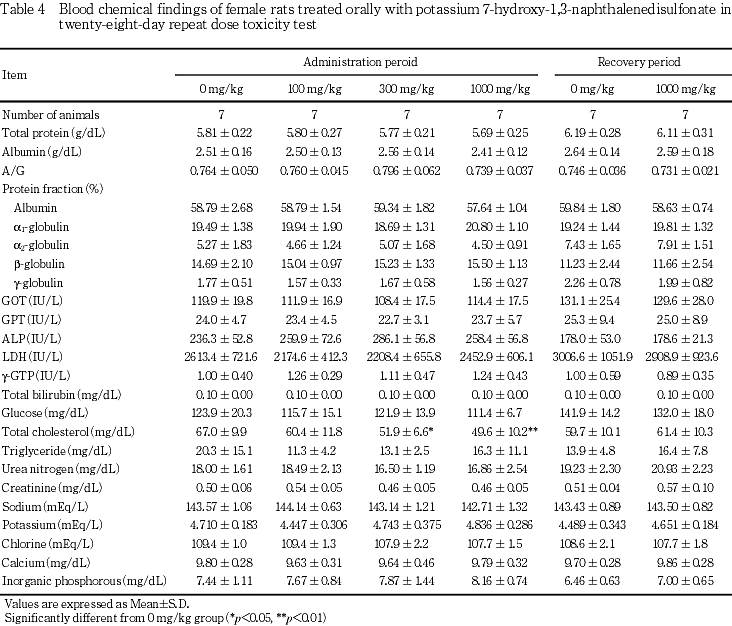
6.����������ظ���(Table 3, 4)
��Ϳ���ֽ�λ���ˤϡ����300�����1000 mg/kg���������쥹�ƥ���������ͤ�ǧ���줿��
�������ֽ�λ���ˤϡ�ͺ�� 1000 mg/kg���������쥹�ƥ���������ͤ�ǧ���줿������Ϳ���ֽ�λ���ˤ����Ѳ���ǧ���줺��7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�Ȥδ�Ϣ�����餫�ǤϤʤ��ä�����Ǥϡ��оȷ��Ȥδ֤˺���ǧ����ʤ��ä���
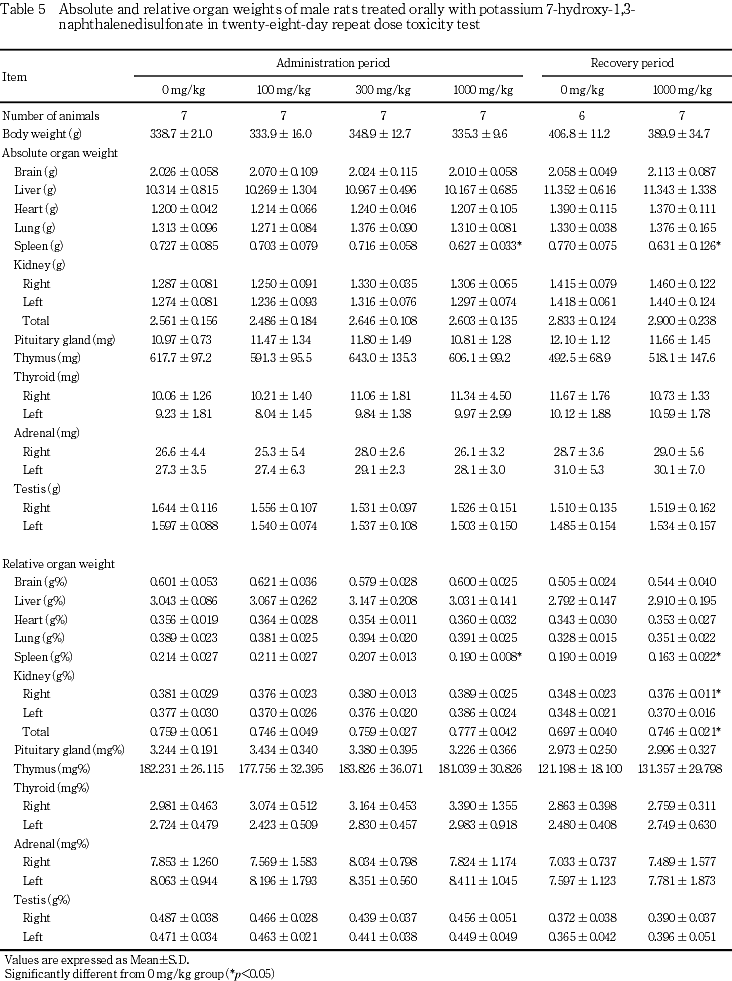
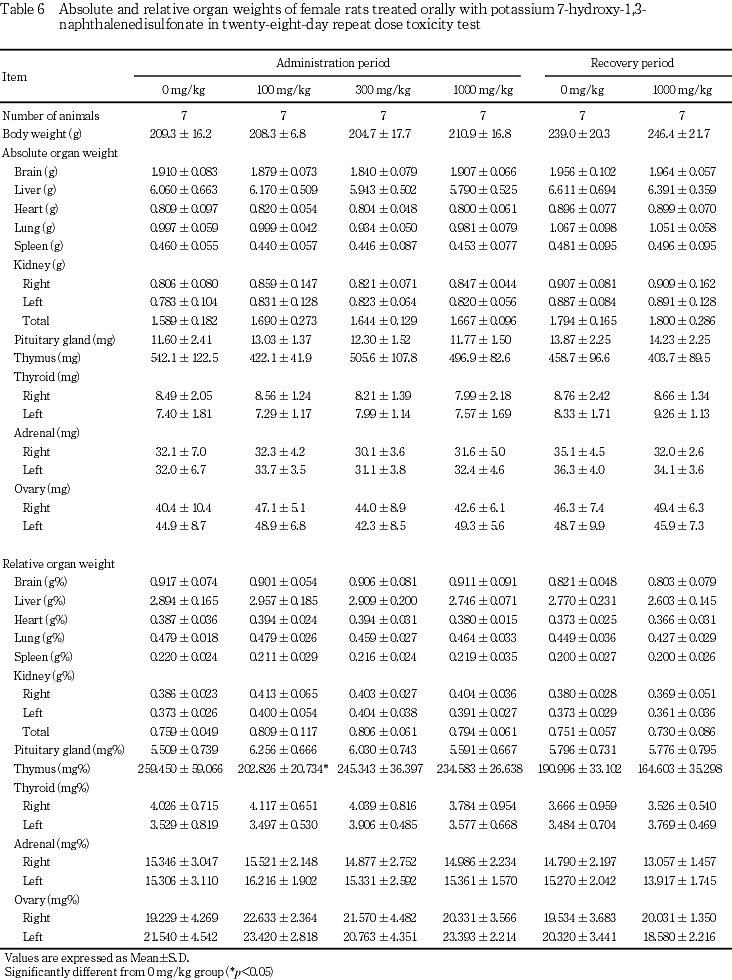
7.���ﴱ����(Table 5��6)
��Ϳ���ֽ�λ���ˤ�ͺ��1000 mg/kg�����¡�����н��̤�������н��̤����ͤ�ǧ���줿����Ǥϡ�100 mg/kg���Ƕ��������н��̤����ͤ�ǧ���줿����300�����1000 mg/kg���Ǥ�ǧ����ʤ��ä���
�������ֽ�λ���ˤ�ͺ��1000 mg/kg�����¡�����н��̤�������н��̤����ͤ�ǧ���줿���ޤ�����¡�����н��̤ι��ͤ�ǧ���줿������Ϳ���ֽ�λ���ˤ����Ѳ���ǧ���줺��7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ��αƶ��ȤϹͤ��ʤ��ä�����Ǥ��оȷ��Ȥδ֤˺���ǧ����ʤ��ä���
8.��˶��
��Ϳ���ֽ�λ������Ӳ������ֽ�λ���ˤϡ���ͺ�Ȥ��7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�ȴ�Ϣ����긫��ǧ����ʤ��ä���
9.�������ȿ��ظ���
��ͺ�Ȥ��7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�ȴ�Ϣ����긫��ǧ����ʤ��ä���
�ͻ�
7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ���0(1 %�����������ʥȥꥦ����ϱ�)��100��300�����1000 mg/kg��1���������ͺ��7���뤤��14ɤ��Crj:CD(SD)��åȤ�28����ȿ���и���Ϳ����������Ƥ���������0�����1000 mg/kg���λ�ͺ��7ɤ���Ѥ���14���֤β�������ʻ���Ƹ�Ƥ������
���̾��֡��νš��ݱ��̡�˶������������ȿ��ظ����Ǥϡ�7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�ˤ���Ѳ���ǧ����ʤ��ä���
Ǣ�����Ǥϡ���Ϳ4���˥��ꥦ�������̤ι��ͤ�ͺ��300�����1000 mg/kg���ʤ�Ӥ˻��1000 mg/kg����ǧ���줿�����ꥦ�������̤ι��ͤϷи���Ϳ���줿7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Υ��ꥦ�बǢ����������줿���Ȥ˵��������Ѳ��Ǥ���ȿ仡���졤����Ū���Ѳ��ȤϹͤ����ʤ��ä����ޤ������楫�ꥦ��ǻ�٤��Ѳ���ǧ����ʤ��ä����Ȥ��顤���ꥦ���������®�䤫�Ǥ��ä��ȹͤ���줿��ͺ��1000 mg/kg���Ǥ���Ϳ4���˥ʥȥꥦ�������̤����ͤ�ǧ���졤���ꥦ�������̤����ä��Ф���ʥȥꥦ��κƵۼ�ж�ʤβ�ǽ����ͤ���줿�������������ꥦ�������̤ι��ͤ��ߤ�줿ͺ��300 mg/kg������ӻ��1000 mg/kg���ǤϤ��Τ褦�ʷ������ߤ�줺���ʥȥꥦ�������̤��Ѳ�������Ū����ư�ϰ���Ǥ��ꡤ����¾�οյ�ǽ�ѥ������뤤�Ͽ�¡�������ȿ��ظ����Ǥ�7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�ˤ��ȹͤ������Ѳ���ǧ����ʤ��ä����Ȥ�������Ū���Ѳ��ȤϹͤ����ʤ��ä���
��ճظ����Ǥϡ���Ϳ���ֽ�λ���˻��1000 mg/kg���ǥإޥȥ���å��͡��إ⥰���ӥ��̤�����ַ��ι��ͤ��뤤�Ϲ��ͷ����ʤ�Ӥ����ַ��Ψ�����ͤ�ǧ���졤7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�αƶ��ȹͤ���줿����������¤���Ϥ������ȿ��ظ����Ǥϰ۾��ǧ���줺�����ε��������餫�ˤʤ�ʤ��ä�����������ظ����Ǥϡ���Ϳ���ֽ�λ���˻��300�����1000 mg/kg���������쥹�ƥ���������ͤ�ǧ���졤7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ����Ϳ�αƶ��ȹͤ���줿������������¡���������ȿ��ظ����Ǥϰ۾��ǧ���줺�����ε��������餫�ˤʤ�ʤ��ä����ʤ����������ֽ�λ���η�ճظ�������ӷ�������ظ����ǤϤ������Ѳ���ǧ���줺���������ĵ�Ū���Ѳ��ȹͤ���줿��
�ﴱ���̤Ǥϡ�ͺ��1000 mg/kg������Ϳ���ֽ�λ������Ӳ������ֽ�λ�����¡�����н��̤�������н��̤����ͤ�ǧ���줿�������ε��������餫�ˤʤ�ʤ��ä���
�ʾ�Τ��Ȥ��顤�ܻ�ˤ�����7-�ҥɥ�����-1,3-�ʥե������ۥ�����ꥦ���̵�ƶ���(NOEL)�ϡ�ͺ��300 mg/kg/day�����100 mg/kg/day�Ǥ���ȹͤ���줿��
| Ϣ���� |
| ���Ǥ�ԡ� | ��¼���� |
| �ô���ԡ� | ����ѡ�Ĺë�߰졤�������ҡ���¼����Ϻ�����Ĥߤ�� |
| (��)����ʪ����������� |
| ��004-0839�����ڻ����Ķ迿��363��24 |
| Tel 011-885-5031�� | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Hiroyuki Yoshimura(Study director)
Hitoshi Shigeno, Junichi Nagaya, Masatoshi Furukawa, Kotaro Kawamura, Miyoko Takeda |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo, Hokkaido, 004-0839, Japan |
| Tel +81-11-885-5031�� | Fax +81-11-885-5313 | |

 nwald-Giemsa����)��¬�ꤷ��������̮����μ褷��̵������դ��Ѥ��ƶŸǻ���(ή��Ǵ���Ѳ��ˤ�������¬��ˡ���ޥ�����������������������饤�ʡ�)��¬�ꤷ��������ˡ�ʢ����ư̮���μ褷����դ�����ʥȥꥦ��ǽ��������塤3000��ž/ʬ��10ʬ�ֱ�ʬΥ��������줿�������Ѥ��ơ��ץ��ȥ���ӥ����(�ȥ���ܥץ饹����ˡ)����ӳ�������ʬ�ȥ���ܥץ饹�������(���饸���ˡ)(�ʾ塤��նŸǼ�ư¬�����֥�����KC-10A���Х�������)��¬�ꤷ����
nwald-Giemsa����)��¬�ꤷ��������̮����μ褷��̵������դ��Ѥ��ƶŸǻ���(ή��Ǵ���Ѳ��ˤ�������¬��ˡ���ޥ�����������������������饤�ʡ�)��¬�ꤷ��������ˡ�ʢ����ư̮���μ褷����դ�����ʥȥꥦ��ǽ��������塤3000��ž/ʬ��10ʬ�ֱ�ʬΥ��������줿�������Ѥ��ơ��ץ��ȥ���ӥ����(�ȥ���ܥץ饹����ˡ)����ӳ�������ʬ�ȥ���ܥץ饹�������(���饸���ˡ)(�ʾ塤��նŸǼ�ư¬�����֥�����KC-10A���Х�������)��¬�ꤷ����
 blewski & La Dueˡ)����-GTP(����L-��-���륿�ߥ�-��-�˥ȥ����˥�ɴ��ˡ)�����륳����(�إ������ʡ���ˡ)�������쥹�ƥ�����(����ˡ)���ȥꥰ�ꥻ���(ͷΥ���ꥻ������õ�ˡ)�����ӥ��ӥ�(�����ӥ��ӥ�ˡ)��Ǣ������(���쥢����������ɥե��Ρ���ˡ)�����쥢���˥�(Jaff
blewski & La Dueˡ)����-GTP(����L-��-���륿�ߥ�-��-�˥ȥ����˥�ɴ��ˡ)�����륳����(�إ������ʡ���ˡ)�������쥹�ƥ�����(����ˡ)���ȥꥰ�ꥻ���(ͷΥ���ꥻ������õ�ˡ)�����ӥ��ӥ�(�����ӥ��ӥ�ˡ)��Ǣ������(���쥢����������ɥե��Ρ���ˡ)�����쥢���˥�(Jaff ˡ)�����륷����(OCPCˡ)��̵�����(Fiske-SubbaRowˡ)��������(�ӥ���å�ˡ)����ӥ���֥ߥ�(BCGˡ)(�ʾ塤��ưʬ������7150������Ω�����)���ʥȥꥦ�प��ӥ��ꥦ��(�ʾ塤�������ˡ����ư������ٷ�480���������˥�)����������(����ũ��ˡ�������饤�ɥ�����CL-6M��ʿ�»���)��A/G��(��������֥ߥ��껻��)�ʤ�Ӥ�����ʬ��(��������������ơ������ŵ���ưˡ������ư�ŵ���ư����CTE-150�����)��¬�ꤷ����
ˡ)�����륷����(OCPCˡ)��̵�����(Fiske-SubbaRowˡ)��������(�ӥ���å�ˡ)����ӥ���֥ߥ�(BCGˡ)(�ʾ塤��ưʬ������7150������Ω�����)���ʥȥꥦ�प��ӥ��ꥦ��(�ʾ塤�������ˡ����ư������ٷ�480���������˥�)����������(����ũ��ˡ�������饤�ɥ�����CL-6M��ʿ�»���)��A/G��(��������֥ߥ��껻��)�ʤ�Ӥ�����ʬ��(��������������ơ������ŵ���ưˡ������ư�ŵ���ư����CTE-150�����)��¬�ꤷ����





