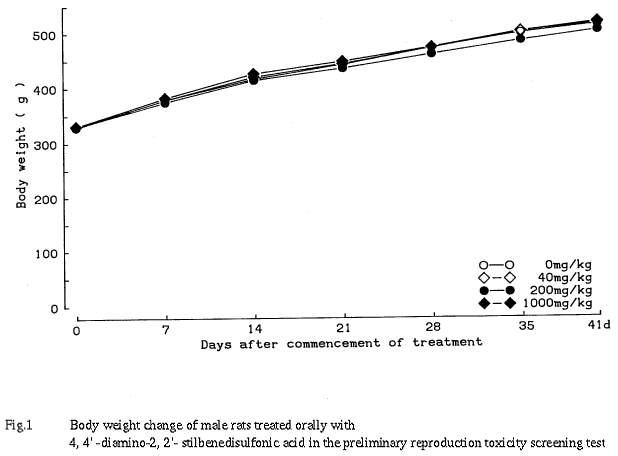
以上の結果から,本試験条件下における4,4'-ジアミノ-2,2'-スチルベンジスルホン酸の反復投与毒性および生殖発生毒性に関する無影響量はともに1000 mg/kgと考えられる.
検疫・馴化期間を含めた全飼育期間中,温度20〜25℃,湿度40〜70%R.H., 換気約12回/時,照明12時間/日(7:00〜19:00)に自動調節された飼育室を使用した.動物は実験動物用床敷(ペータチップ:日本チャールス・リバー)を敷いたポリカーボネート製ケージに,1ケージ当り投与開始後は1匹,交配期間中は雌雄各1匹,哺育期間は1腹で収容し飼育した.
動物には,オートクレーブ滅菌した実験動物用固型飼料(CRF-1:オリエンタル酵母工業)および5 μmのフィルター濾過後,紫外線照射した水道水をそれぞれ自由摂取させた.
雌雄のSD系ラットを用いて8日間の反復投与予備試験(用量:0,100,300,1000 mg/kg)を行った結果,技術的投与限界量の1000 mg/kg群でも体重および剖検ともに変化は認められなかった.従って,本試験では高用量を1000 mg/kgとし,以下公比5で中用量を200 mg/kg,低用量を40 mg/kgとした.さらに溶媒のみを投与する対照群を設けた.
投与期間は,雌雄とも交配前14日間,交配期間中,および雄は計画殺前日までの計41日間,雌は交尾成立後分娩を経て哺育3日までとし,0.5% CMC-Na水溶液に懸濁させた被験物質を,胃ゾンデを用いて1日1回,午前中に強制経口投与した.投与液量は10 ml/kgとし,至近測定日の体重を基に算出した.
投与液は褐色瓶に入れて冷暗所保存した.また,投与開始前に均一性,安定性および濃度を確認した.
雄の対照および1000 mg/kg群の精巣および精巣上体について,常法に従いへマトキシリン・エオジン染色標本を作製し鏡検した.また,未交尾および非妊娠雌の卵巣,剖検時に肉眼的な異常が認められた40 mg/kg群の1例の精巣についても同様に検査した.
哺育4日の解剖時に卵巣,子宮を摘出して黄体数および着床数を検査した.交尾確認後25日を経ても分娩しない雌は剖検し,肉眼的に着床が認められない動物の子宮については,2% KOH水溶液に浸漬し,着床の有無を確認した.これらの結果から,妊娠期間(妊娠0日から出産が確認された日までの期間),出産率([生児出産雌数/妊娠雌数]×100),着床率([着床数/黄体数]×100),分娩率([総出産児数/着床数]×100)を算出した.
 法またはScheff
法またはScheff 型の多重比較検定を行った.ただし,下記*印の項目については,Kruskal-Wallisの検定から行った.計数データはFisherの直接確率法により検定した.有意水準は5%以下とした.新生児に関するデータについては,各母動物毎に算出した平均値を統計単位とした.以下に検定の対象となる項目を示す.
型の多重比較検定を行った.ただし,下記*印の項目については,Kruskal-Wallisの検定から行った.計数データはFisherの直接確率法により検定した.有意水準は5%以下とした.新生児に関するデータについては,各母動物毎に算出した平均値を統計単位とした.以下に検定の対象となる項目を示す.

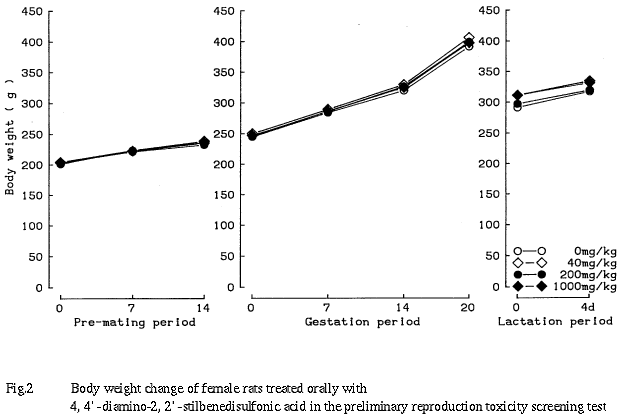
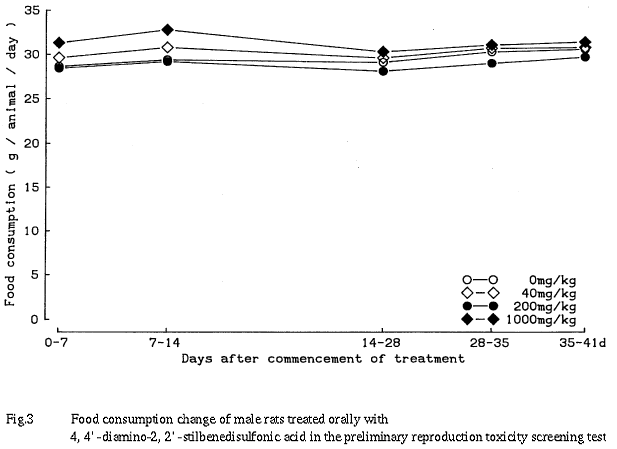
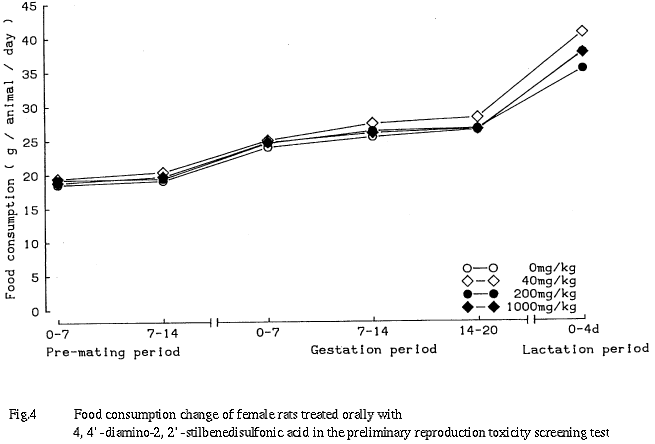

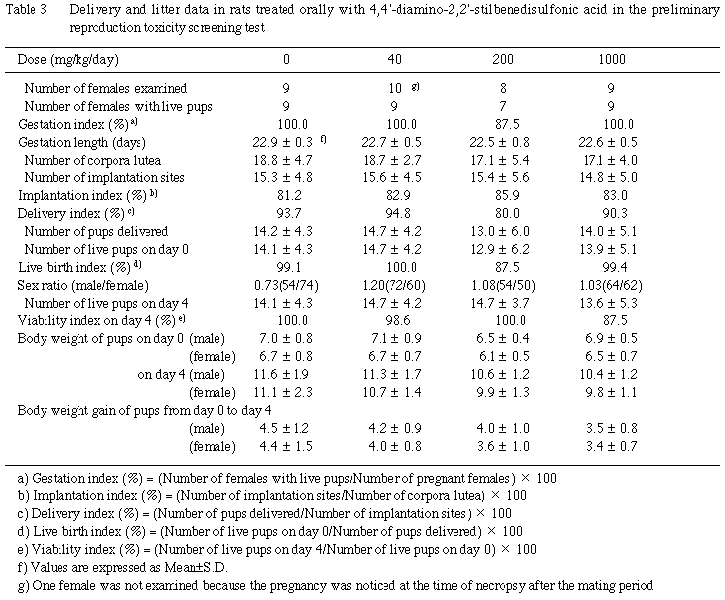
各群で死産児および出生後の死亡が少数例観察されたが,出産児数,出産生児数,性比,出生率および新生児生存率のいずれにも対照群と被験物質投与群との間に有意な差は認められなかった.なお,200 mg/kg群の出生率および1000 mg/kg群の新生児生存率が他の群に比べやや低い値を示したが,出産児数が1例のみの腹の死亡率が100%を示したことが反映した見掛け上の変化である.
(2)新生児の観察
一般状態に被験物質に起因する異常は認められなかった.また,外表異常については痕跡尾が200 mg/kg群の1例に認められたのみであった.
(3)体重(Table 3)
雌雄とも哺育0日および4日の体重,ならびにその間の体重増加量に対照群と被験物質投与群との間に有意な差は認められなかった.
(4)剖検
生存動物および死亡動物ともに異常は認められなかった.
生殖発生毒性について,生殖機能検査の結果,交尾率,受胎率に被験物質の影響は認められなかった.交配中の膣垢検査では,1000 mg/kg群でもほとんどの雌に交配開始後4日以内に発情期が観察され,被験物質による性周期への影響を疑わせる変化は認められなかった.また,妊娠期間,黄体数,着床数,着床率,出産率および分娩率に被験物質の影響は認められなかった.さらに,分娩後の母動物の哺育行動,新生児の一般状態,出産児数,出産生児数,性比,出生率,新生児生存率,体重および剖検においても被験物質に起因する変化は認められなかった.
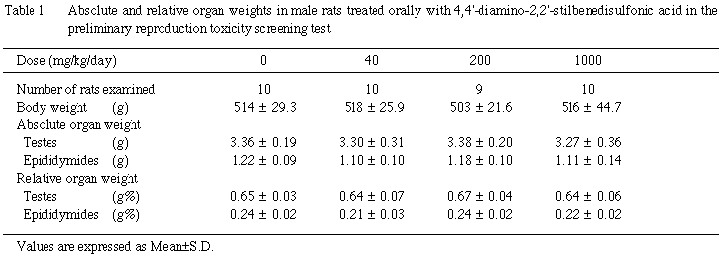
被験物質は合成エストロジェン剤のジエチルスチルベストロール(DES)と構造が類似し,弱いエストロジェン様作用を有している1).DESやエストロジェン剤は,反復投与による影響として,精巣の萎縮性変化あるいはライデッヒ細胞の増生,精巣上体の組織変化,子宮内膜の増生など,生殖器に障害を起こすことが知られている2).しかし,被験物質のナトリウム塩である4,4'-ジアミノ-2,2'-スチルベンジスルホン酸・ジナトリウムについては,混餌法による長期毒性試験が実施されており,13週間投与試験では100000 ppm投与においてもマウスおよびラットともに精巣には病理組織学的変化は認められなかったことが報告されている3).さらに13週間投与試験においては,マウスで子宮内膜の増生が認められたが,ラットではこのような変化は認められなかったこと,および2年間投与試験においてはマウス,ラットともに生殖器も含めてエストロジェン様作用による影響を示唆する変化は認められなかったことが報告されている3).本試験の結果も同様に,技術的投与限界用量である1000 mg/kg群においても精巣および精巣上体ともに被験物質投与の影響は認められなかった.また,生殖・発生への影響に関しては,DESあるいはエストロジェン剤は繁殖障害,性周期の変化,着床阻害,妊娠期間延長,胚の死亡および発育抑制などを起こすことが知られている4-8).しかし,本試験においては親動物および児動物ともに被験物質による生殖・発生への影響を示唆する変化は認められなかった.
以上のように,本試験では技術的投与限界用量である1000 mg/kg群においても反復投与による一般毒性学的影響は認められず,また生殖・発生に及ぼす影響も認められなかった.したがって,本試験条件下における反復投与毒性および生殖発生毒性に関する無影響量はともにl000 mg/kgと考えられる.
| l) | E.R. Smith, M.M. Quinn, J.Toxicol.Environ.Health, 36, 13-25(1992). |
| 2) | 宮蔦宏彰, "毒性病理学, 毒性試験講座5(前川昭彦,林裕造編)," 地人書館, 東京, 1991, pp. 387-407. |
| 3) | National Toxicology Program(NTP)Technical Report Series No.412.(l992), NIH Publication No.92-3143.U.S.Department of Health and Human Services, Public Health Service, National Institutes of Health, Research Triangle Park, NC U.S.A. |
| 4) | 鈴木勝士, トキシコロジーフォーラム, 7, 572-576(1984). |
| 5) | 高橋日出彦, "くすりの毒性," 南江堂, 東京, 1974, pp. 276-3l2. |
| 6) | T.H. Shepard, "Catalog of teratogenic agents," 6th ed., The Johns Hopkins University Press, Baltimore, 1989, pp. 217-220. |
| 7) | 清藤英一, "催奇形性等発生毒性に関する薬品情報(西村秀雄監修)," 東洋書店, 東京, 1977, pp. 497-505. |
| 8) | J.L. Schardein, "Chemical induced birth defects, " 2nd ed., Marcel Dekker, New York, 1993, pp. 271-339. |
| 連絡先 | |||
| 試験責任者 | :松浦郁夫 | ||
| 試験担当者 | :岡部恵美,土谷 稔,涌生ゆみ | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 314-02 茨城県鹿島郡波崎町砂山14 | |||
| Te1 0479-46-287l | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Ikuo Matsuura(Study director) Emi 0kabe, Minoru Tsuchitani,Yumi Wako | |||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | ||||
| 14 Sunayama ,Hasaki-machi, Kashima-gun,Ibaraki, 314-02 Japan | ||||
| Te1 +81-479-46-287l | Fax +81-479-46-2874 | |||