C.I.ピグメントイエロー53のラットを用いる反復経口投与毒性・生殖発生毒性併合試験
Combined Repeat Dose and Reproductive/Developmental Toxicity Screening Test
of C.I. Pigment Yellow 53 by Oral Administration in Rats
要約
C.I.ピグメントイエロー53は,チタン,アンチモン,ニッケルの複合酸化物であり,各種塗料,印刷インキ,絵具等に使用されている1).C.I.ピグメントイエロー53を1 %カルメロースナトリウム水溶液に懸濁し,0(対照群),250,500および1000 mg/kgの投与量で,1群雌雄各12匹のCrj:CD(SD)IGSラットに,雄ラットに対しては交配前,交配期間および交配後を含む計46日間,雌ラットに対しては交配前,交配および妊娠期間,ならびに哺育4日までの期間,反復経口投与し,雌雄動物への反復投与による影響,雌雄動物の生殖および新生児の発生に及ぼす影響について検討し,以下の成績を得た.
1. 反復投与毒性
一般状態の変化として500 および1000 mg/kg群で,雌雄とも糞便の黄色または黄褐色化,剖検所見として盲腸の内容物黄緑色化が観察された.しかし,これらの変化は,被験物質が消化管の内容物を着色したものであり,投与による毒性学的な変化とは考えられなかった.体重推移,摂餌量,尿検査,血液学検査,血液生化学検査,剖検所見および器官重量のいずれの指標にも,各投与群の雌雄とも投与による影響は認められなかった.1000 mg/kg群の病理組織学検査の結果,雌雄とも投与による影響は認められなかった.
以上のことから,各投与群の雌雄ともC.I.ピグメントイエロー53の反復投与による影響は認められなかった.したがって,本試験条件下におけるC.I.ピグメントイエロー53の無影響量(NOEL)は雌雄とも1000 mg/kg/day以上であると考えられた.
2. 生殖発生毒性
生殖能検査では,各投与群の雌雄とも異常は認められず,新生児にも投与による影響は認められなかった.
したがって,本試験条件下におけるC.I.ピグメントイエロー53の反復投与による親動物の生殖に対する無影響量(NOEL)ならびに新生児の発生に対する無影響量(NOEL)は1000 mg/kg/day以上と考えられた.
方法
1. 被験物質および投与液の調製
C.I.ピグメントイエロー53(純度:100 %,Lot No. 4879,石原産業(株),大阪)は,黄色の粉末である.入手後の被験物質は遮光気密容器に入れて冷所で保存した.残余被験物質を提供者が分析し,投与期間中の被験物質の安定性を確認した.投与液は,投与量ごとに被験物質を精秤し,所定の濃度となるように溶媒である1 %カルメロースナトリウム水溶液(丸石製薬(株))を加えて懸濁し,超音波を用いて分散させて調製した.投与に先立って,10および200 mg/mLの濃度の調製液について,室温で24時間,冷所保存条件下で7日間の安定性および均一性を確認した.調製液は,調製後速やかに遮光気密容器に入れて冷所保存し,調製後7日以内に使用した.投与に用いた初回および最終調製時の各濃度の調製液について被験物質の濃度を分析した結果,含有率は設定値の98.3〜101.7 %であり,調製液は規定の濃度を含有することを確認した.
2. 試験動物および飼育条件
日本チャールス・リバー(株)よりSprague-Dawley系ラット(Crj:CD(SD)IGS)の雌雄を8週齢で購入し,14日間の検疫および馴化を行い,雌については10日間の性周期検査も併せて行った後,雌雄各48匹の健康な動物を選択して10週齢で試験に供した.投与開始日の体重は雄が345〜401 g,雌が207〜261 gであった.動物は,温度20〜24 ℃,湿度45〜66 %,換気回数10〜15回/時間および照明時間12時間(8:00から20:00まで点灯)に制御されたバリアシステムの飼育室で,ブラケット式金属製金網床ケージに,群分け前は1ケージあたり雌雄別に3匹以内を収容し,群分け後は1匹,交配中は雌雄各1匹,妊娠期間中は1母動物,哺育期間中は1腹を収容した.雌は,妊娠17日から哺育4日まで金網床のかわりに実験動物用床敷(ホワイトフレーク,日本チャールス・リバー(株))を敷いたステンレス製受皿を使用した.飼料はg線照射固型飼料(CRF-1,オリエンタル酵母工業(株))を金属製給餌器を用いて,飲料水は札幌市水道水を自動給水装置を用いてそれぞれ自由に摂取させた.
3. 投与量および投与方法
投与量設定試験では0,500,1000および2000 mg/kgの用量で1群雌雄各5匹のSD系ラットに1日1回,14日間投与した結果,全ての被験物質投与群の雌雄で,一般状態の変化として糞便の黄色または黄褐色化,剖検所見として盲腸内容の黄色または黄緑色化が観察された.しかし,これらの変化は,被験物質が消化管の内容物を着色したものと考えられ,他の検査項目には異常が認められなかったことから,投与による影響とは考えられなかった.したがって,本試験の投与量は高用量をOECD試験法ガイドライン(422)で規定された限度量である1000 mg/kgとし,以下,公比2で除して500および250 mg/kgを雌雄ともに設定した.そのほかに溶媒である1 %カルメロースナトリウム水溶液のみを同様の方法で投与する対照群を設けた.1群の動物数は雌雄とも12匹とし,投与前々日の体重に基づいて層化無作為抽出法により群分けを行った.
投与に際しては,ラット用胃ゾンデを用いて1日1回強制的に胃内に投与した.投与期間は,雄については交配前14日間および交配期間を含む46日間,雌については交配前14日間および交尾成立までの交配期間,さらに交尾成立例は妊娠期間および哺育4日までの期間,交尾不成立例は交配期間終了後23日までの期間とした.投与容量を10 mL/kgとし,各動物の投与液量は投与日に最も近い測定日の体重に基づいて算出した.
4. 検査項目
1) 一般状態観察
雌雄全例について,試験期間中1日1回の頻度で,視診および触診により行動,外観などを観察した.
2) 体重測定
投与開始日を投与1日として起算し,交配前は雌雄全例について,投与1,2,3,5,7,10および14日に測定した.交配開始後は,雄については投与21,28,35,42,46日(最終投与日)および剖検日(最終投与日の翌日)に,雌の交尾成立例は妊娠0,1,3,5,7,10,14,17および20日,哺育0,1および4日ならびに剖検日(哺育4日の翌日)に,交尾不成立例は投与28,35,42および49日ならびに剖検日(投与51日の翌日)に測定した.体重増加量および体重増加率を,雄については投与1から46日,雌については投与1から14日,妊娠0から20日および哺育0から4日について算出した.
3) 摂餌量測定
雌雄全例について,交配期間および剖検日を除き,体重測定と同じ日に,各ケージの給与量または残量を測定した.飼料消費量を給与日数で除し,各測定日間の1匹当りの1日の平均摂餌量(g/rat/day)を算出した.
4) 尿検査
雄の各群6例について投与期間の最終週(投与44〜45日)に,代謝ケージに収容して非絶食下で採尿を行い,同時に採尿中の飲水量(重量)も測定した.約3時間の蓄尿についてpH,蛋白,糖,ケトン体,ウロビリノーゲン,ビリルビン,潜血反応(以上,マルティスティックス,バイエル メディカル(株))および色調(肉眼観察)ならびに沈渣(鏡検)を検査し,21時間蓄尿について尿量(容量)および比重(屈折計法,アタゴ)を測定した.
5) 血液学検査
雄の全例および雌の哺育母動物各群6例について,剖検日の前日から16〜22時間絶食させ,剖検日にエーテル麻酔下で腹部大動脈より採血し,EDTA・2Kで処理した血液を用いて赤血球数,ヘマトクリット値,血小板数,白血球数(以上,電気抵抗法),ヘモグロビン量(シアンメトヘモグロビン法),平均赤血球容積(赤血球数,ヘマトクリット値より算出),平均赤血球ヘモグロビン量(赤血球数,ヘモグロビン量より算出),平均赤血球ヘモグロビン濃度(ヘマトクリット値,ヘモグロビン量より算出)(以上,自動血球計数装置F-820,シスメックス),網赤血球数(Brecher法)および白血球百分比(May-Gr殤wald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 回転/分で10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
6) 血液生化学検査
雄の全例および血液学検査で用いた同じ各群6例の雌について血液学検査と同時期に,腹部大動脈より採血し,ヘパリン処理した後,3000 回転/分で10分間遠心分離して得られた血漿を用いてGOT(IFCC法)およびグルコース(ヘキソキナーゼ法)を測定し,無処理血液を3000 回転/分で10分間遠心分離して得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),コリンエステラーゼ(ヨウ化ブチリルチオコリン基質法),総コレステロール,リン脂質(以上,酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff 法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
7) 剖検および器官重量測定
雄は全例投与46日の翌日に,雌の分娩例は哺育4日の翌日に,交尾不成立例は交配期間終了後24日に,妊娠25日まで分娩が認められない交尾成立例は妊娠26日に,いずれも最終投与日の翌日に,体外表を観察し,エーテル麻酔下で採血後,放血により安楽死させて剖検した.また,脳,心臓,肝臓,腎臓,脾臓,副腎,胸腺,精巣,精巣上体および卵巣の重量を測定した.さらに,絶対重量を剖検当日の体重で除し100を乗じて相対重量を算出した.
8) 病理組織学検査
全例について,脳(大脳・小脳),下垂体,胸腺,甲状腺,上皮小体,副腎,脾臓,心臓,胸部大動脈,舌,食道,胃(前胃および腺胃),肝臓,膵臓,十二指腸,空腸,回腸(パイエル板を含む),盲腸,結腸,直腸,喉頭,気管,肺(気管支含む),腎臓,膀胱,前立腺,精嚢(凝固腺含む),卵巣,子宮(角部および頸部),膣,乳腺(腹部,雌のみ),皮膚(腹部),胸骨(骨髄含む),大腿骨(骨髄含む),脊髄(頸部),骨格筋(大腿部),腸間膜リンパ節,下顎リンパ節,顎下腺,舌下腺,耳下腺,坐骨神経ならびに肉眼的異常部位を10 %中性緩衝ホルマリン液で固定・保存した.左肺については注入固定を行った.眼球およびハーダー腺はデビッドソン液で固定・保存し,精巣および精巣上体はブアン液で固定後70 %エタノールに保存した.これらの器官・組織を常法に従ってパラフィン包埋後,薄切してヘマトキシリン・エオジン染色標本を作製し,対照群および最高用量群の雌雄全例を鏡検した.
9) 生殖能検査
雌全例について,投与開始日の10日前から交尾までの連日,ギムザ染色による膣垢塗抹標本を作製し,光学顕微鏡下で性周期段階(発情前期,発情期,発情後期および発情休止期)の判定を行い,性周期の各段階を4日から5日の間隔で2回以上繰り返すものを正常と判定した.発情休止期あるいは発情期が7日以上継続してみられる場合に性周期の異常と判定した.各雌動物の発情期間隔を算出した.投与14日の夕方から,同試験群内の雌雄を1対1(無作為組合わせ)で14日間を限度として同居させた.交尾の成立は,膣内または受皿上に落下した膣栓,あるいは膣垢スメア標本中の精子が確認された場合とし,いずれかが認められた日を妊娠0日とした.妊娠成立の確認を,分娩の有無および剖検時に子宮内の着床痕の有無を調べることによって行った.交尾率[(交尾動物数/同居動物数)×100]および受胎率[(受胎動物数/交尾動物数)×100]を算出した.
10) 分娩および哺育状態観察
交尾確認雌動物は全例自然分娩させた.分娩状態を,妊娠21日から25日まで観察した.9:00に分娩終了を確認した場合,その日を哺育0日とした.剖検時に各雌の卵巣の黄体数および子宮内の着床数を肉眼的に数えて記録した.これらの結果から,妊娠期間[妊娠0日から哺育0日までの日数],出産率[(生児出産雌数/妊娠雌数)× 100],着床率[(着床数/黄体数)×100],分娩率[(出産児数/着床数)×100]および哺育4日の哺育率[(哺育4日に生存児の認められる雌数/生児出産雌数)×100]を算出した.
11) 新生児の一般状態観察および生存率
哺育0日に,腹毎に生存児数および死亡児数を数え,哺育状態,出産児の性別および外表を観察した.生存児数および死亡児数の合計を出産児数とした.児動物の性は,肛門と生殖突起の間の長さで判定した.哺育1日から哺育4日までは,1日1回,哺育児の生存および死亡を確認し,一般状態および外表について観察した.これらの観察結果から,出生率[(出産生児数/出産児数)×100],性比[雄出産児数/雌出産児数]および新生児の4日の生存率[(哺育4日生児数/出産生児数)×100]を1腹を単位として算出した.ただし,喰殺あるいは行方不明となった新生児は死亡例として扱った.
12) 新生児の体重測定
全例について,哺育0,1および4日に個体毎に測定し,腹毎に雌雄別の平均体重を求めた.
13) 新生児の剖検
死亡例は発見後速やかに剖検した.生存例については,哺育4日に体外表(口腔内を含む)を観察後,二酸化炭素吸入法により安楽死させ,全身の器官・組織を肉眼的に観察した.
5. 統計解析
正常性周期出現率,交尾率,受胎率,出産率,哺育4日の哺育率,ならびに病理組織学検査結果のうち1段階の陽性グレードがみられた所見については多試料χ2-検定を行い,その結果,有意差がみられた場合は2試料χ2-検定で解析した.ただし,これらの検定に不適合の場合はFisherの正確確率検定法を用いた.
尿検査の定性的項目,尿比重および病理組織学検査結果のうち2段階以上の陽性グレードがみられた所見についてはKruskal-Wallisの検定法で解析し,有意差がみられた場合は,Mann-WhitneyのU-検定法を用いて解析した.
その他の項目について,Bartlettの検定法によって等分散性を解析し,等分散の場合は,一元配置分散分析法で解析し,有意差がみられた場合は,Dunnettの検定法により解析した.不等分散の場合は,Kruskal-Wallis法で解析し,有意差がみられた場合は,Mann-WhitneyのU-検定法を用いて解析した.なお,新生児の出生率,性比,4日の生存率および雌雄別体重は,1腹を標本単位として処理した.
これら対照群と被験物質投与群との間の検定においては,いずれも有意水準を5 %とした.
結果
1. 反復投与毒性
1) 一般状態
投与2日以降剖検日まで500 mg/kg群で黄褐色便が雌雄とも12例全例に,1000 mg/kg群で黄色または黄褐色便が雌雄とも12例全例に観察された.しかし,便のその他の性状には異常はなかった.その他に,雄の250 mg/kg群で切歯破折が投与42日に1例観察されたが,ケージ内の事故によるものと考えられた.雌では,対照群の1例に脱毛が妊娠12日以降剖検日まで認められた.250 mg/kg群で背部痂皮形成および500 mg/kg群で下眼瞼の外傷および痂皮形成がそれぞれ1例みられたが,投与による影響ではないと考えられた.
2) 体重(Fig. 1)
雌雄とも対照群と比較して有意な差は認められなかった.
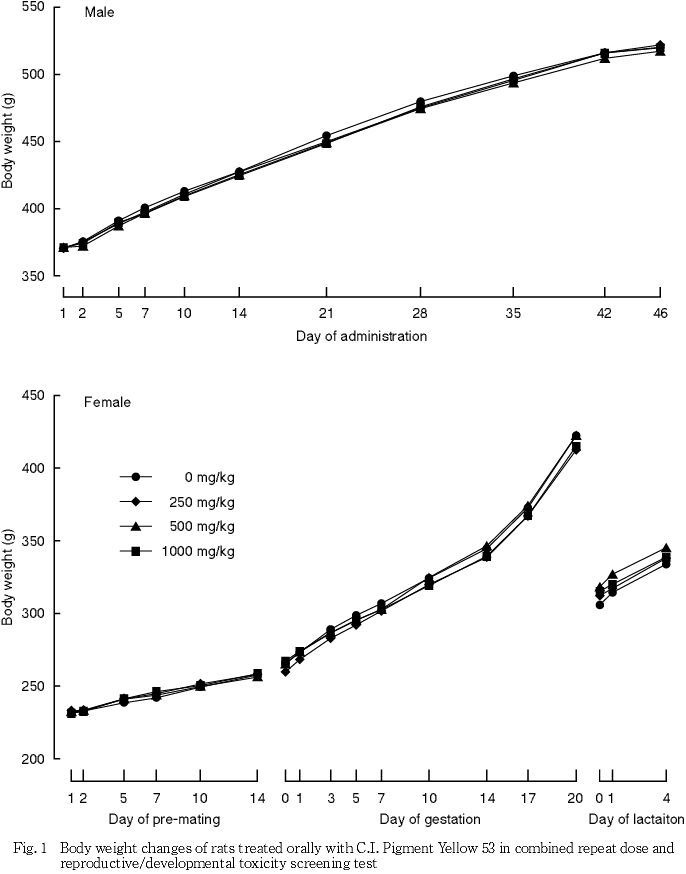
3) 摂餌量(Fig. 2)
雌雄とも対照群と比較して有意な差は認められなかった.

4) 尿検査
雄の250 mg/kg群で尿比重の有意な上昇がみられたが,500 mg/kg以上の投与群ではみられない変化であった.その他の各検査項目には,各投与群と対照群との間に有意差は認められなかった.
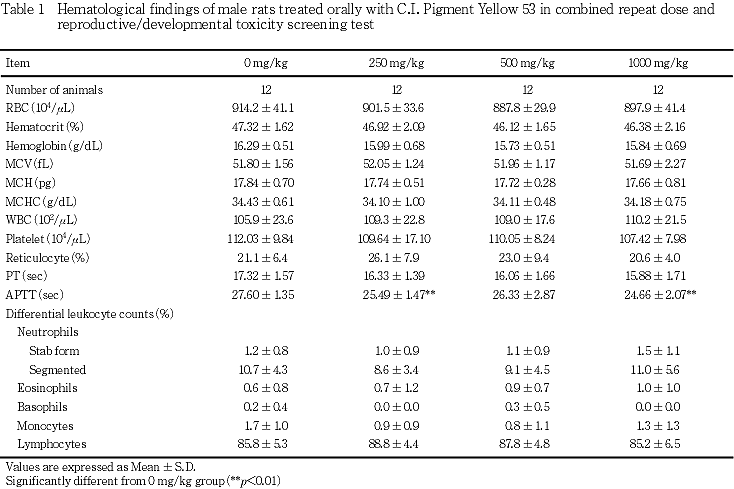
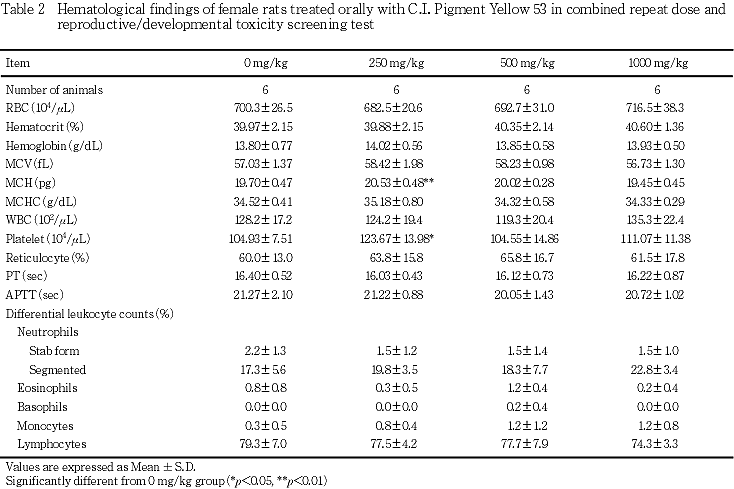
5) 血液学検査(Table 1, 2)
雄では,250および1000 mg/kg群で活性化部分トロンボプラスチン時間(APTT)の有意な短縮が認められた.
雌では,250 mg/kg群で平均赤血球ヘモグロビン量(MCH)および血小板の有意な高値が認められたが,500 mg/kg以上の投与群ではみられない変化であった.
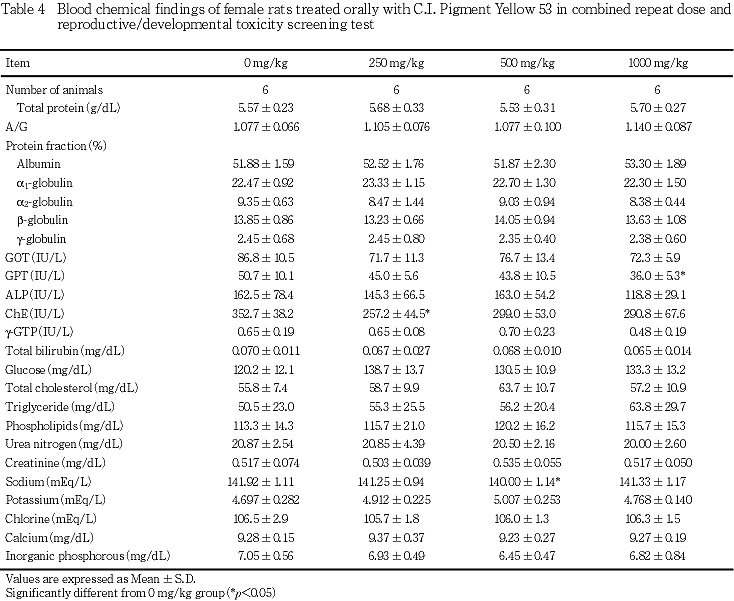
6) 血液生化学検査(Table 3, 4)
雄では,1000 mg/kg群でカリウムの有意な低値が認められたが,毒性学的意義がないと考えられた.
雌では,250 mg/kg群でコリンエステラーゼの有意な低値,500 mg/kg群でナトリウムの有意な低値,1000 mg/kg群でGPTの有意な低値が認められたが,いずれも関連項目に変化がみられないため,投与との関連性はないものと考えられた.

7) 剖検
雄では,盲腸の内容物黄緑色化が,500 mg/kg群で1例,1000 mg/kg群で12例全例に認められた.その他には異常は認められなかった.
雌では,対照群では腎盂拡張と脱毛が各1例観察された.500 mg/kg群では盲腸の内容物黄緑色化が4例観察された.1000 mg/kg群では,胃および盲腸の内容物黄色化が1例,盲腸の内容物黄緑色化が8例認められた.胃および盲腸の内容物黄色化がみられた例は,妊娠の証拠が得られなかった動物で,子宮に黄白色液体貯留ならびに膣閉鎖および黄白色液体貯留も観察された.
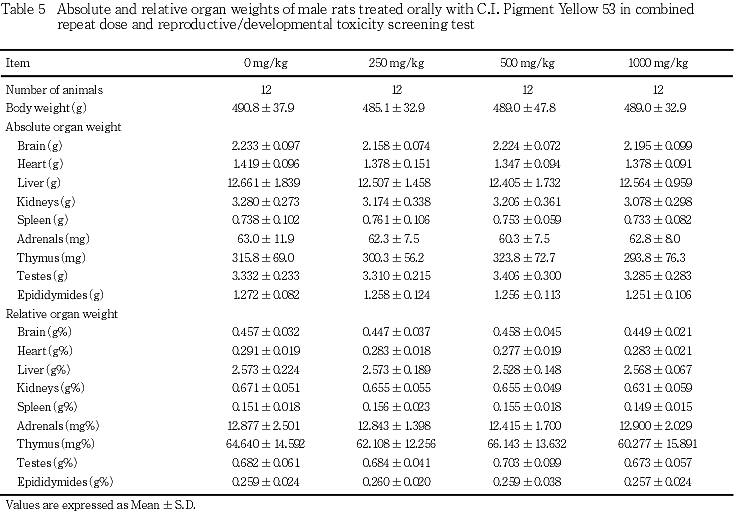
8) 器官重量(Table 5, 6)
雌雄とも,測定したいずれの器官にも対照群と各投与群の間に有意な差はみられなかった.

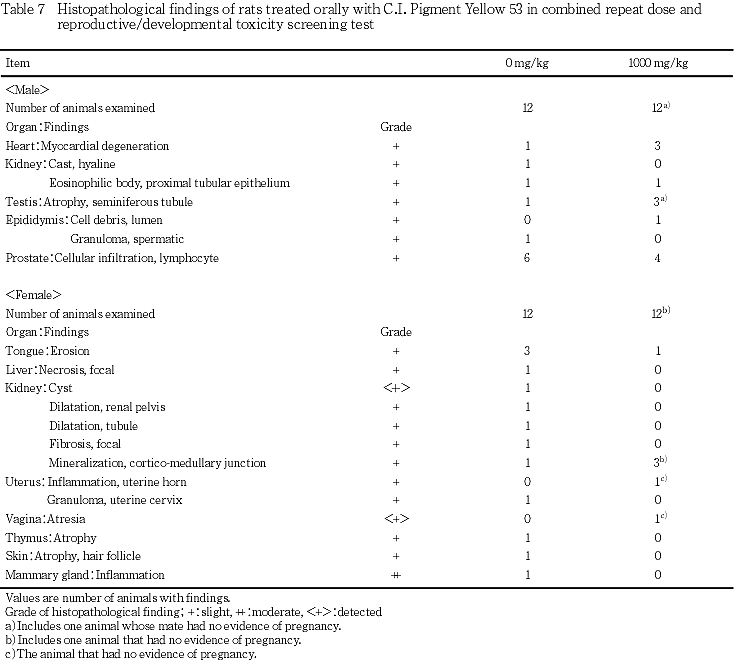
9) 病理組織学検査(Table 7)
雄では,対照群で,心臓の心筋変性,腎臓の硝子円柱,近位尿細管上皮の好酸性小体,精巣の精細管の萎縮および精巣上体の精子肉芽腫が各1例,ならびに前立腺のリンパ球浸潤が6例みられた.1000 mg/kg群では,心臓の心筋変性が3例,腎臓の近位尿細管上皮の好酸性小体が1例,精巣の精細管の萎縮が3例,精巣上体の管腔内細胞残屑が1例および前立腺のリンパ球浸潤が4例みられた.
雌では,対照群では舌のびらんが3例,ならびに肝臓の限局性壊死,腎臓の嚢胞,腎盂拡張,尿細管の拡張,腎臓の限局性線維化,腎臓の皮髄境界部における鉱質沈着,子宮頸部の肉芽腫,胸腺の萎縮,皮膚毛嚢の萎縮および乳腺の炎症が各1例みられた.1000 mg/kg群では,舌のびらんが1例および腎臓の皮髄境界部における鉱質沈着が3例観察された.また,剖検で膣の閉鎖がみられた1例(不妊例)に,膣の閉鎖および子宮角部の炎症が観察され,膣の閉鎖については先天的な異常であり,不妊の原因と考えられた.
以上の変化はいずれもその出現頻度に対照群と比較して有意な差は認められなかった.
2. 生殖発生毒性
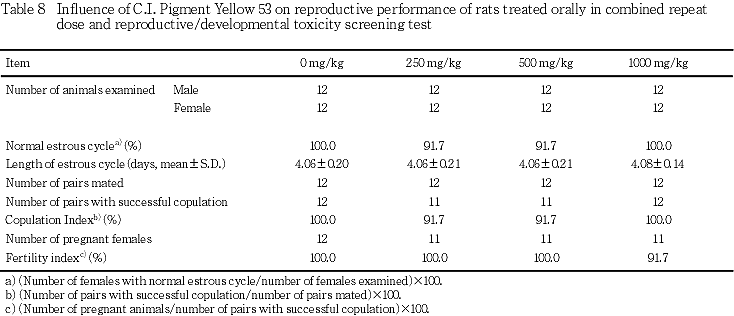
1) 生殖能検査(Table 8)
正常性周期出現率,発情期間隔,交尾率,受胎率,出産率,妊娠期間および哺育4日時哺育率には各投与群とも対照群と比較して有意差は認められなかった.交尾不成立が250および500 mg/kg群でそれぞれ1組に認められた.これらの組の雌の性周期検査で交配中に発情休止期の連続が認められたが,1000 mg/kg群ではみられなかったことから,投与による影響とは考えられなかった.不妊例は1000 mg/kg群で1例認められた.この例は,病理学検査で先天的な異常である膣の閉鎖が観察され,不妊の原因であると考えられた.
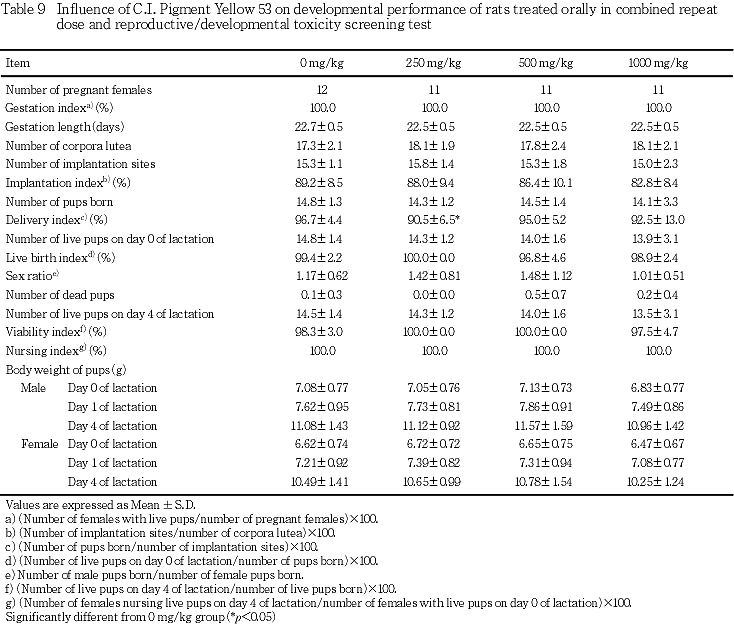
2) 分娩および哺育状態観察(Table 9)
難産などの分娩異常はいずれの動物にもみられなかった.黄体数,着床数,着床率,総出産児数,出産児の性比,哺育0日の生存児数,出生率,哺育4日の生存児数,新生児の4日の生存率には,各投与群とも対照群と比較して有意差は認められなかった.分娩率が250 mg/kg群で有意に低下したが,500 mg/kg以上の投与群では有意な差がみられなかったことから,偶発的な変動と考えられた.
3) 新生児の生存率(Table 9)
各投与群とも対照群と比較して有意な差は認められなかった.
4) 新生児の一般状態
分娩終了確認時の死亡児が対照群で雌1例,500 mg/kg群で雄2例,雌3例,1000 mg/kg群で雄2例に認められた.哺育4日までの期間の死亡あるいは不明例が対照群で雄2例,雌1例,1000 mg/kg群で雄3例,雌1例に認められた.生存例では腹部外傷が500 mg/kg群で雌1例に認められたのみであった.
5) 新生児の体重推移(Table 9)
各投与群とも対照群と比較して有意な差は認められなかった.
6) 新生児の剖検
死亡例では痂皮が1000 mg/kg群の雄1例にみられた他は,いずれの例にも異常は認められなかった.
哺育4日の剖検では,肝臓の黄白色部が250 mg/kg群の雌1例および1000 mg/kg群の雄1例,一般状態観察でみられた500 mg/kg群の外傷が雌1例に認められたが,その他に異常は認められなかった.
考察
1. 反復投与毒性
500 および1000 mg/kg群で,雌雄とも一般状態の変化として糞便の黄色または黄褐色化,剖検所見として盲腸の内容物黄緑色化が観察された.しかし,これらの変化は,性状が黄色である被験物質の大量投与により,消化管の内容物を着色したものであり,投与による消化器等への器質的または機能的影響によるものではないと考えられた.
体重推移,摂餌量および尿検査では,雌雄ともいずれの投与群においても投与による影響は認められなかった.
血液学検査および血液生化学検査では,1000 mg/kg群において雄で活性化部分トロンボプラスチン時間(APTT)の有意な短縮,雌でGPTの有意な低値がみられた.しかし,APTTの短縮については,臨床的意義が乏しいこと,肝機能あるいは血小板に異常なく凝固系因子の活性化を示唆するような所見はみられないことから,毒性学的意義のない変化と考えられた.一方,GPTの低値についてもその臨床的意義が乏しいこと,雄に変化はなく被験物質の測定系への干渉による低下は考えられないことから,偶発的変化であり,被験物質の投与による影響とは考えられなかった.
器官重量には,雌雄ともいずれの投与群においても投与による影響は認められなかった.
病理組織学検査の結果,雌雄ともいずれの投与群においても投与による影響は認められなかった.
以上のことから,各投与群の雌雄ともC.I.ピグメントイエロー53の反復投与による影響は認められなかった.したがって,本試験条件下におけるC.I.ピグメントイエロー53の無影響量(NOEL)は雌雄とも1000 mg/kg/day以上であると考えられた.
2. 生殖発生毒性
生殖能検査では,各投与群とも雌の性周期,雌雄の交尾率,受胎率,出産率,妊娠期間および哺育4日時哺育率に変化はみられず,生殖器(精巣,精巣上体および卵巣)および内分泌器官(副腎)の重量ならびに剖検に変化は認められなかった.また,1000 mg/kg群の生殖器の病理組織学検査でも異常は認められなかった.
母動物の黄体数,着床数,着床率,総出産児数,出産児の性比,哺育0日の生存児数,出生率,哺育4日の生存児数,新生児の4日の生存率には,被験物質の投与による影響は認められなかった.
新生児の一般状態,体重および剖検では,各投与群とも影響は認められなかった.
以上のことから,雌雄の生殖および新生児に各投与群ともC.I.ピグメントイエロー53の投与による影響は認められなかった.したがって,本試験条件下におけるC.I.ピグメントイエロー53の反復投与による親動物の生殖に対する無影響量(NOEL)ならびに新生児の発生に対する無影響量(NOEL)は1000 mg/kg/day以上と考えられた.
文献
| 1) | 化学工業日報社編,"13398の化学商品,"化学工業日報社,東京,1998,pp.1165-1166. |
| 連絡先 |
| 試験責任者: | 藤井咲子 |
| 試験担当者: | 木口雅夫,咲間正志,平田真理子,古川正敏 |
| (株)化合物安全性研究所 |
| 〒004-0839 札幌市清田区真栄363番24 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Sakiko Fujii(Study director)
Masao Kiguchi, Masashi Sakuma, Mariko Hirata, Masatoshi Furukawa |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo, Hokkaido, 004-0839, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |

 法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,自動炎光光度計480型,コーニング),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.










