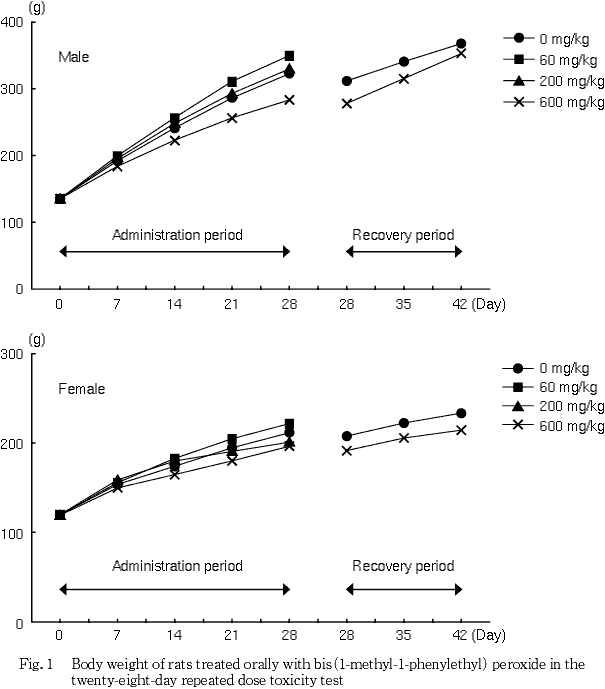
雌雄の200および600 mg/kg群で流涎が観察されたが,対照群を含むいずれの群にも死亡例はみられなかった.体重では雌雄の600 mg/kg群で低値を示し,増加抑制が認められた.摂餌量は,雌雄とも各投与群で投与期間中に継続性のある変化はみられなかった.
血液学検査の結果,雄の200および600 mg/kg群で好中球比率の高値がみられた.血液凝固能検査の結果,雌雄いずれの投与群とも被験物質に起因すると考えられる変化は認められなかった.
血液生化学検査の結果,雌雄の600 mg/kg群でγ-GTPが高値を示し,雄の600 mg/kg群ではALTの高値も認められた.
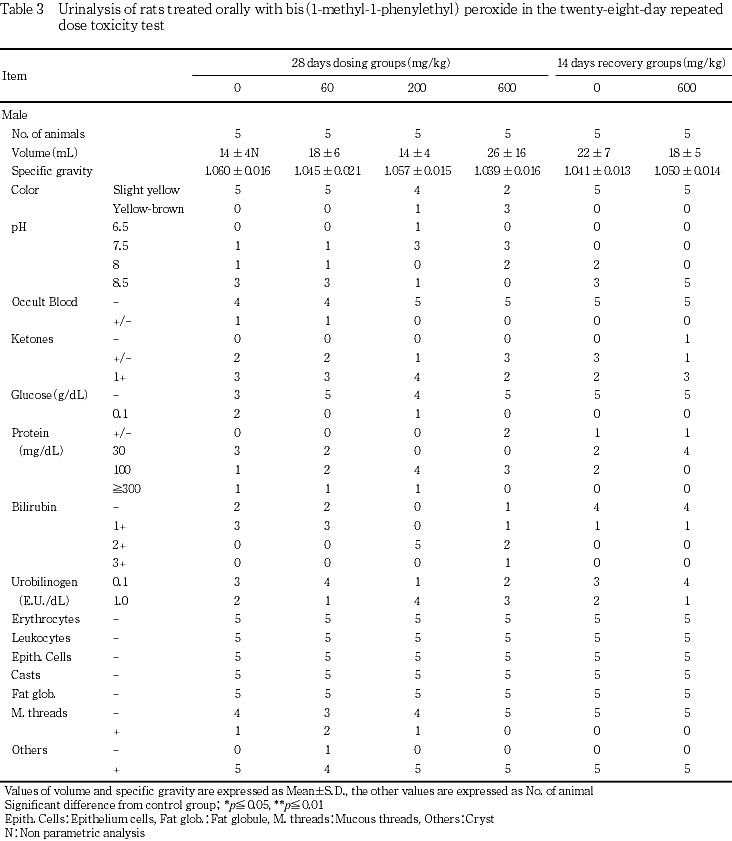
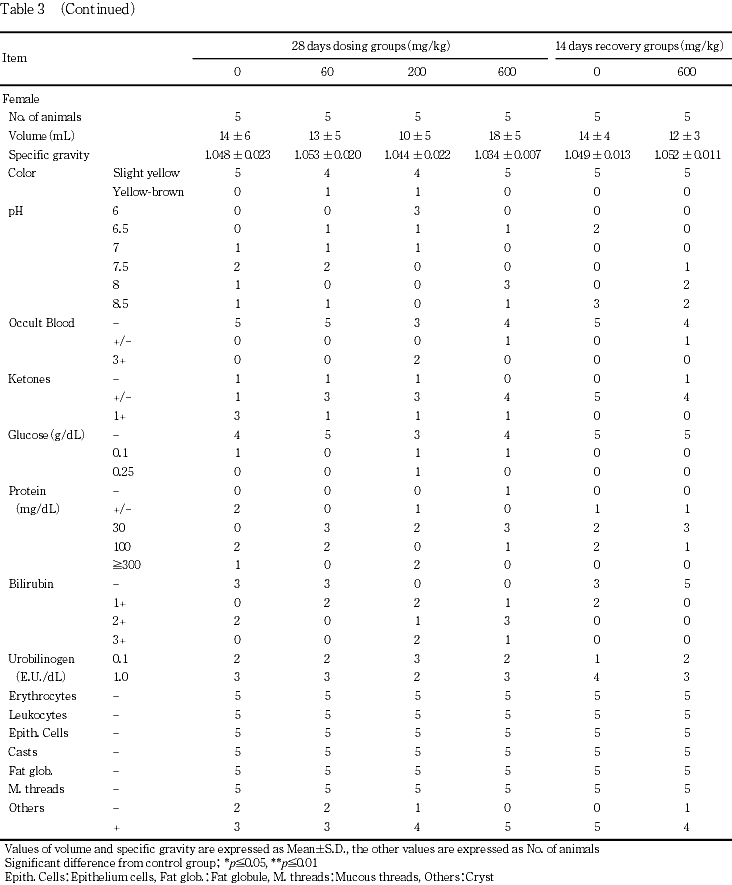
蛋白電気泳動検査および尿検査の結果,被験物質に起因すると考えられる変化は認められなかった.
器官重量測定の結果,雌雄の600 mg/kg群で肝臓の実重量および相対重量の高値が,雌の200 mg/kg群では肝臓相対重量の高値が認められた.また,雌雄の600 mg/kg群では胸腺の実重量および相対重量の低値が認められた.いずれの変化も回復が認められた.
病理学検査の結果,剖検所見では肝臓の肥大が雌の600 mg/kg群に認められ,組織所見としては,肝細胞の肥大(小葉中心性)が200および600 mg/kg群,肝細胞の変性が雌雄の600 mg/kg群に観察された.これら肝臓の病変は回復期間終了時の剖検および組織所見では認められなかった.
以上の結果,本試験条件下におけるビス(1-メチル-1-フェニルエチル)ペルオキシドの無影響量は雌雄とも60 mg/kg/dayと判断された.
[用量設定理由]
投与用量設定のための2週間反復投与試験を0,100,300および1000 mg/kgの4用量で実施した結果,1000 mg/kg群で雌雄とも2例が死亡した.一般状態の変化では雌雄の1000 mg/kg群で流涎および痩削が観察された.器官重量測定の結果,雌雄の300 mg/kg以上の群で肝臓実重量および相対重量の高値が認められた.従って,28日間反復投与毒性試験の最高用量を600 mg/kgとし,以下公比約3で除し,中用量を200 mg/kg,低用量を60 mg/kgと設定した.
器官重量は脳,肝臓,腎臓,副腎,胸腺,脾臓,精巣,精巣上体および卵巣について測定した.器官重量/体重比(相対重量)は投与28日または回復14日の測定体重および器官重量から算出した.また,脳(大脳,小脳,橋を含む),脊髄,下垂体,眼球,唾液腺(顎下腺,舌下腺),甲状腺,上皮小体,心臓,胸腺,肺(気管支を含む),気管,肝臓,腎臓,脾臓,副腎,胃,小腸(パイエル氏板を含む),大腸,精巣,精巣上体,精嚢,前立腺,卵巣,子宮,腟,膀胱,末梢神経(坐骨神経),リンパ節(下顎リンパ節,腸間膜リンパ節),骨髄(大腿骨),大動脈および皮膚は十分な量の10 %中性緩衝ホルマリン液で固定した.但し,精巣および精巣上体はブアン液で前固定した後,10 %中性緩衝ホルマリン液で固定した.
病理組織学検査は固定した器官・組織のうち,投与期間終了時に解剖した対照群および高用量群の胸腺,心臓,胃,小腸,大腸,肝臓,脾臓,腎臓,副腎,精巣,精巣上体,子宮,卵巣,骨髄(大腿骨)について実施した.器官重量,肉眼観察,組織学検査の結果,肝臓に変化が認められたため,他の用量群および回復群の肝臓についても組織学検査を行った.組織標本は,常法に従ってパラフィン包埋,薄切後,ヘマトキシリン・エオジン染色を施した.鏡検では,病変の種類および程度を含む各所見について記録した.
回復期間では体重の回復がみられ,対照群に比較して雄の600 mg/kg群で体重増加量が高値を示した.

雄では,対照群に比較して200および600 mg/kg群で好中球比率が高値を示した.また,600 mg/kg群ではMCHおよびリンパ球比率の低値が認められたが,いずれも軽微な変化であった.
雌では,対照群に比較して200および600 mg/kg群でヘマトクリット値が,600 mg/kg群ではヘモグロビン量が低値を示した.その他,600 mg/kg群でリンパ球比率が低値を示したが,軽微な変化であった.
[回復期間終了時の検査結果]
雄では,対照群と比較して600 mg/kg群でヘマトクリット値が僅かな低値を,また雌では,対照群と比較して600 mg/kg群でMCHCが僅かな低値を示したが,これらの変化は雌雄いずれも軽微なものであった.
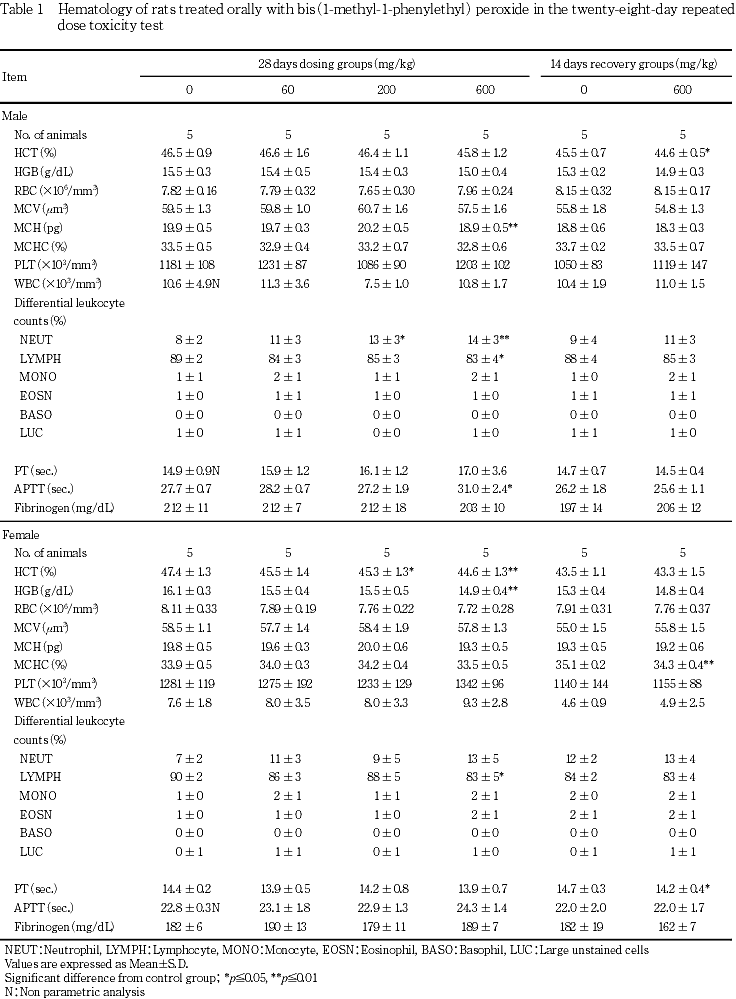
雄では対照群と比較して600 mg/kg群でAPTTが延長を示した.
[回復期間終了時の検査結果]
雌では対照群と比較して600 mg/kg群でPTが短縮を示したが,軽微な変化であった.
雄では,対照群に比較して200および600 mg/kg群で総コレステロールが低値を示した.600 mg/kg群ではALTおよびγ-GTPが高値,ASTが低値を示した.その他,60 mg/kg群でASTが僅かに低値を示し,200 mg/kg群ではBUNが高値を示したが,用量に対応しない変化であった.
雌では,対照群に比較して60,200および600 mg/kg群でカルシウムが高値を示した.200および600 mg/kg群では総蛋白が高値を示した.600 mg/kg群ではアルブミンおよびγ-GTPが高値を示した.
[回復期間終了時の検査結果]
雄では,対照群に比較して600 mg/kg群でALTが高値を示した.雌では,対照群に比較して600 mg/kg群で総コレステロール,総ビリルビンおよびカルシウムが高値を示した.しかし,雌雄のいずれも軽微な変化であった.
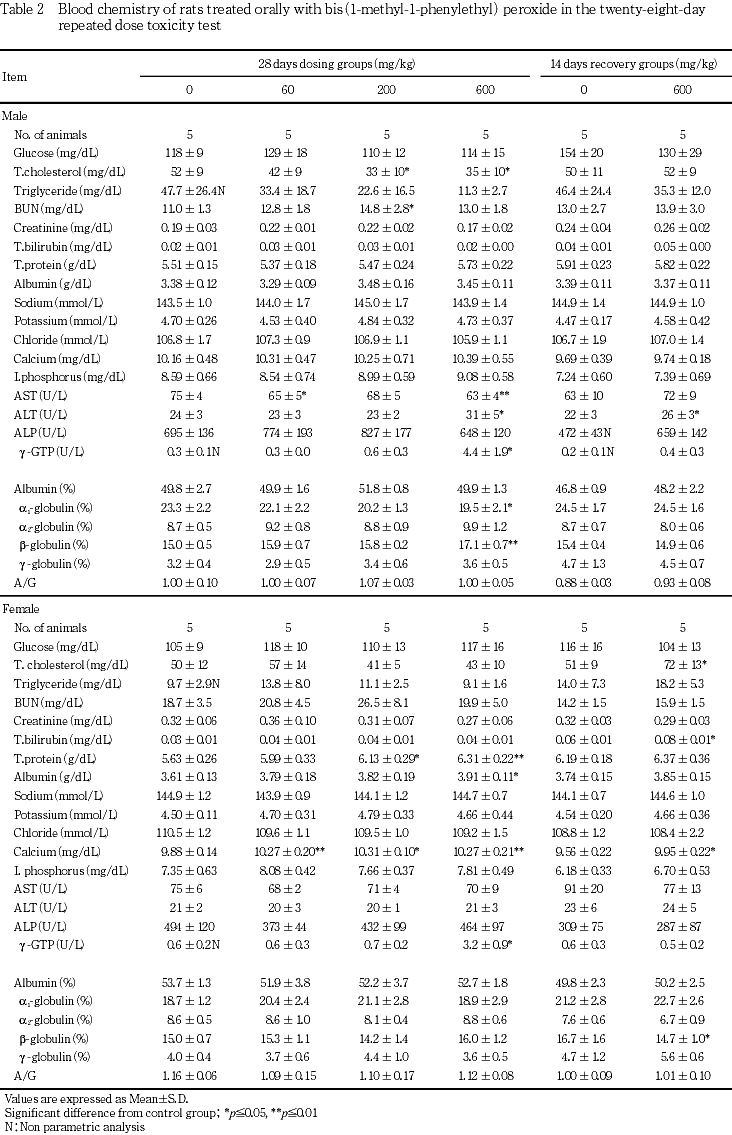
雄では,対照群に比較して600 mg/kg群でa1グロブリン比率が低値およびbグロブリン比率が高値を示した.
[回復期間終了時の検査結果]
雌では,対照群に比較して600 mg/kg群でbグロブリン比率が低値を示した.しかし,投与期間終了時の結果においてみられなかった変化であった.
雄では,200 mg/kg群でビリルビン2+が5例中5例,600 mg/kg群で2+が2例,3+が1例認められた.雌では200 mg/kg群で2+が5例中1例,3+が2例,600 mg/kg群で2+が5例中3例,3+が1例それぞれ認められた.
[回復期間終了時の検査結果]
雌雄とも,対照群に比較して600 mg/kg群では差が認められなかった.
雌雄とも,対照群に比較して600 mg/kg群で肝臓重量が高値および胸腺重量が低値を示した.
[回復期間終了時の検査結果]
雌では,対照群に比較して600 mg/kg群で脾臓重量が低値を示したが,軽微な変化であった.
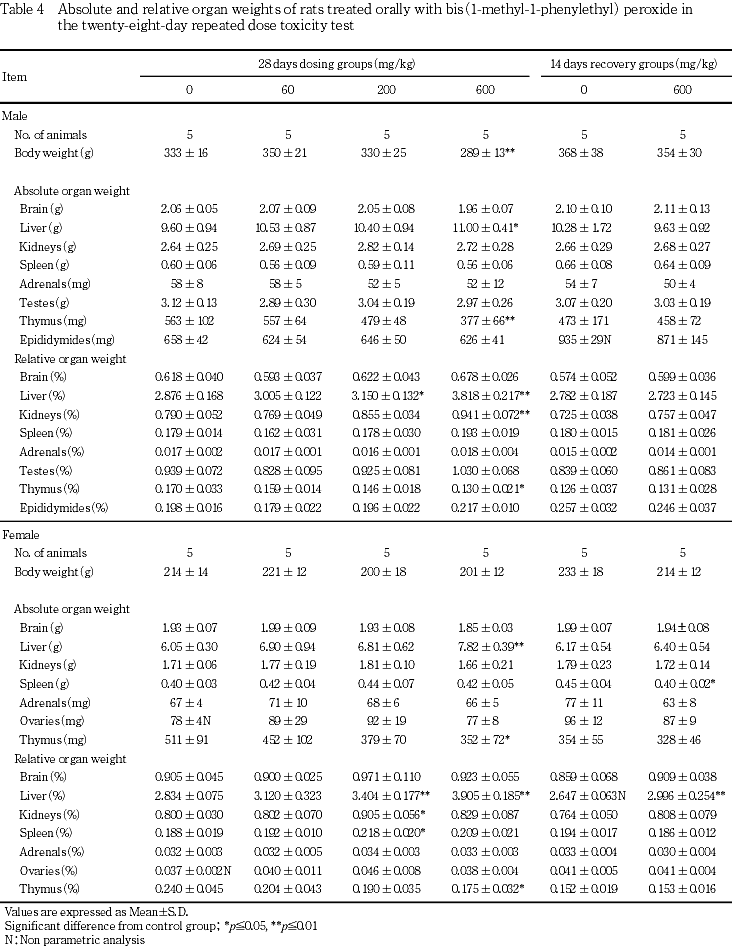
対照群に比較して雌雄の200および600 mg/kg群で肝臓相対重量が高値を示した.また,雌雄の600 mg/kg群で胸腺相対重量が低値を示した.雄の600 mg/kg群および雌の200 mg/kg群で腎臓相対重量が高値を示した.
[回復期間終了時の検査結果]
雌では,対照群に比較して600 mg/kg群で肝臓相対重量が高値を示したが,投与終了時に比較すると軽微であった.
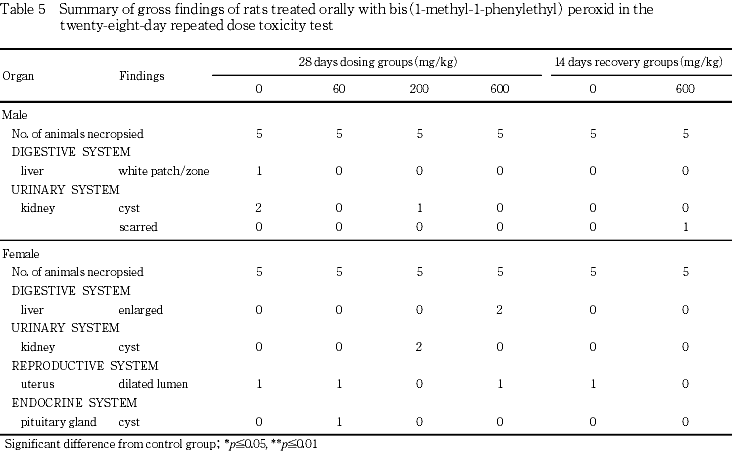
600 mg/kg群のみに肝臓の肥大が雌の2例に観察された.その他,肝臓の白色斑/区域,腎臓の嚢胞,子宮の内腔拡張,下垂体の嚢胞が投与群に少数例または単発性の病変として観察された.いずれの所見も統計学的に有意な差は認められなかった.
[回復期間終了時の検査結果]
投与期間終了時に観察された肝臓の肥大は認められなかった.その他,腎臓の瘢痕,子宮の内腔拡張が単発性の病変として観察された.いずれの所見も統計学的に有意な差は認められなかった.
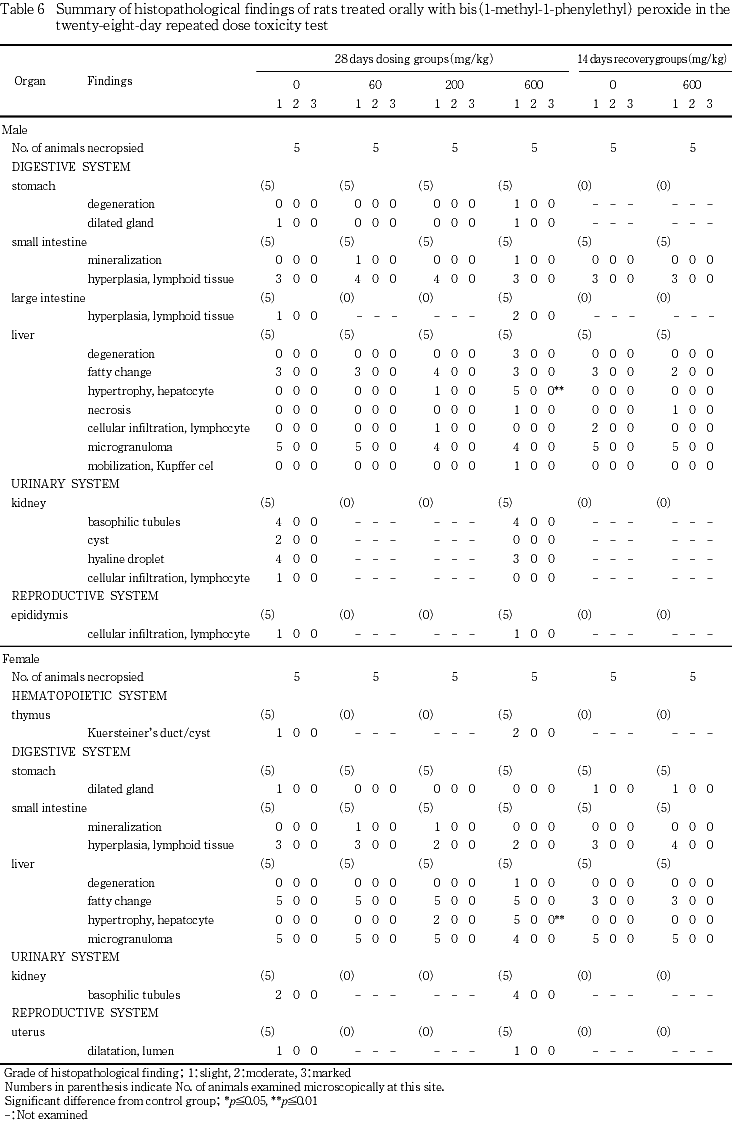
対照群に比較して被験物質投与群において統計学的に有意に増加した病変として,肝細胞の肥大(小葉中心性)が雄の200 mg/kg群で1例,600 mg/kg群で全例,雌の200 mg/kg群で2例,600 mg/kg群で全例に認められた.被験物質投与群に多く発生した所見として,肝細胞の変性が600 mg/kg群で雄の3例,雌の1例に認められ,クッパー細胞動員も肝細胞の変性の認められた雄の600 mg/kg群の1例に見られた.また,600 mg/kg群の雌雄で肝細胞の脂肪化,小肉芽腫,雄で腎臓の尿細管好塩基化,硝子滴変性が観察されたが,その他の所見を含めていずれも散発性または単発性のものであった.
[回復期間終了時の検査結果]
投与終了時に観察された肝細胞の肥大(小葉中心性),変性およびクッパー細胞動員は認められなかった.600 mg/kg群の雌雄で肝細胞の小肉芽腫および脂肪化が観察されたが,いずれも所見は散発性または単発性のものであり,統計学的に有意な差は認められなかった.
一般状態の変化では,投与期間中に雌雄の200および600 mg/kg群で流涎が認められ被験物質の影響と考えられた.
体重では,雌雄の600 mg/kg群で低値を示した週がみられ,投与4週間の体重増加量も低値を示し,この群での体重増加抑制が認められた.なお,回復期間においては順調な体重増加が認められ,雄では体重増加量が有意な高値を示した.
摂餌量は,雌雄とも各投与群で投与期間中に継続性のある変化は認められなかった.
血液学検査では,雌の200および600 mg/kg群でヘマトクリット値が,600 mg/kg群ではヘモグロビン量がそれぞれ統計学的に低値を示した.しかし,ヘマトクリット値およびへモグロビン量の背景値は,それぞれ43.5 ± 2.0 %(n=60),14.9 ± 0.6 g/dL(n=60)であることから,ヘマトクリット値およびヘモグロビン量の低値は対照群の値が高値であったことによると考えられた.
血液凝固能検査では雄の600 mg/kg群でAPTTが延長を示し,被験物質による変化と考えられた.
血液生化学検査では,雌雄の600 mg/kg群でγ-GTPが高値を示し,さらに,雄の同群で認められたALTの高値および総コレステロールの低値をも含めて被験物質の肝臓への影響が示唆された.回復期間終了時には,雄の600 mg/kg群でALTの高値が認められたが,投与終了時の結果と比較すると上昇の程度は僅かであり,これらの変化は回復期間中に回復したと考えられた.雌の200および600 mg/kg群で総蛋白の高値や雄の600 mg/kg群でアルブミンの高値が認められたため,蛋白電気泳動検査を行った.しかし,雌雄の各投与群のA/Gについては対照群と比較して変化は認められなかったことから,被験物質の影響とは考えられなかった.雌の各投与群のカルシウムが高値を示したが,発現の機序については不明であった.
尿検査では,雌雄の200および600 mg/kg群でビリルビン2+および3+の動物が観察されたが,血液中のビリルビン濃度は高値を示していないことから毒性学的に意義のない変化と考えられた.
器官重量測定では,雌雄の600 mg/kg群で肝臓重量および相対重量,雌の200 mg/kg群では肝臓相対重量が高値を示した.それぞれ後述する肝臓肥大および肝細胞肥大(小葉中心性)の病理組織学変化に対応した変化であると考えられた.雌雄の600 mg/kg群では胸腺重量および相対重量が低値を示した.なお,これらの変化は回復期間に回復が認められた.
病理学検査では,被験物質によると思われる病変が肝臓に観察された.剖検所見では肝臓の肥大が雌の200 mg/kg群,組織所見では肝細胞の肥大(小葉中心性)が雌雄の200および600 mg/kg群,肝細胞の変性が雌雄の600 mg/kg群,クッパー細胞動員が雄の600 mg/kg群に観察され,いずれも被験物質の肝臓に対する影響が示唆された.なお,本病変は回復群においては観察されなかったことから,可逆性の変化と考えられた.器官重量で胸腺の実重量と相対重量の低下が見られたが,組織学的に異常病変は観察されなかった.その他,観察された所見は散発性または単発性の発生であり,明らかな用量に対応した変化でないことから,自然発生病変と考えられた.
これらの結果から,本試験におけるビス(1-メチル-1-フェニルエチル)ペルオキシドの無影響量は雌雄とも60 mg/kg/dayと判断された.
| 1) | 佐野正樹,岡山佳弘,医薬安全性研究会会報,32, 21-44(1990). |
| 2) | M. Yoshida,J. Japanese Soc. Comp. Stat. 1, 111(1988). |
| 3) | 倍味繁,稲葉太一,医薬安全性研究会会報,40, 33(1994). |
| 連絡先 | |||
| 試験責任者: | 渡修 明 | ||
| 試験担当者: | 各務 進,伊賀達也,向井大輔,細井理代,大橋信之 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Nobuaki Watari(Study director) Susumu Kakamu, Tatsuya Iga, Daisuke Mukai, Rumiko Miyajima, Nobuyuki Oohashi | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | ||||
| 582-2 Arahama, Shioshinden, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||