投与期間中1000 mg/kgの雄2例が死亡したが,盲腸を中心とする腸管の出血が死因と推定された.生存動物の一般状態では,投与期間の後半に1000 mg/kg群の雌で腹部膨満がみられた.
体重では,200 mg/kg群の雌および1000 mg/kg群の雌雄で増加抑制が認められ,これらの群では摂餌量の低値も観察された.
血液学検査では,1000 mg/kg群の雌雄で赤血球数,ヘモグロビン量およびヘマトクリット値の減少がみられ,雌では平均赤血球血色素濃度の減少も認められた.
血液生化学検査では,1000 mg/kg群の雌雄で総コレステロールの減少,雄でアルカリホスファターゼの増加,また,雌で総たん白質およびアルブミンの増加がみられた.
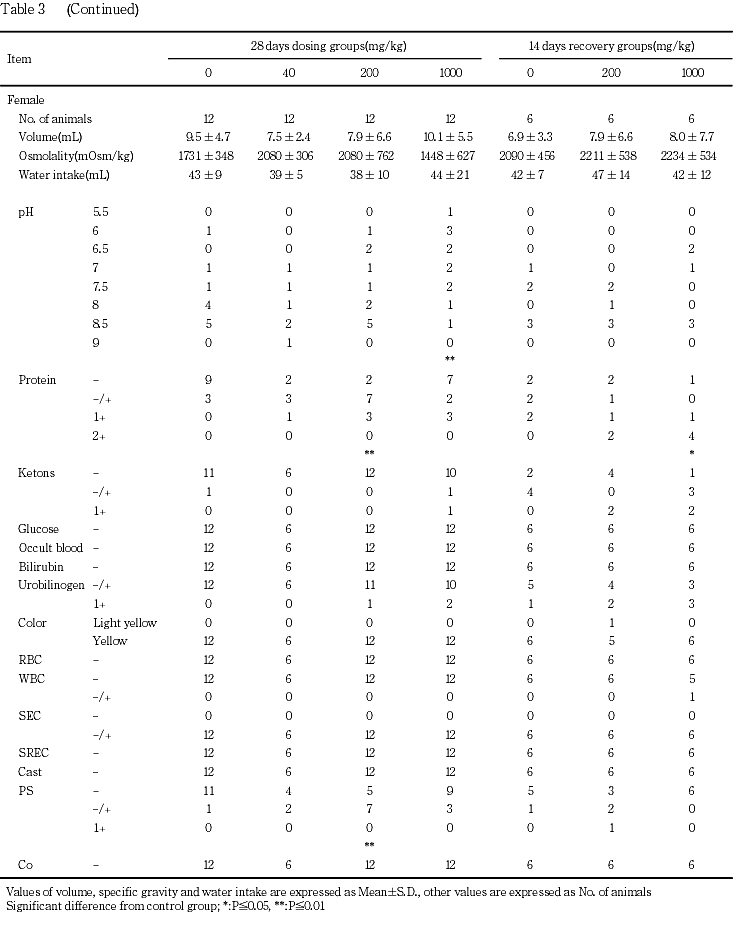
尿検査では,尿たん白陽性例の増加が200および1000 mg/kg群の雌雄,pHの低下が200 mg/kg群の雄と1000 mg/kg群の雌雄,ウロビリノーゲンの増加が200および1000 mg/kg群の雄にみられた.
病理学検査では,盲腸,肝臓,胸腺,副腎,脾臓,骨髄(大腿骨),骨(大腿骨)および腎臓に変化がみられた.盲腸では,1000 mg/kg群の雌雄で肉眼的な拡張がみられ,組織学的には200および1000 mg/kg群の雌雄で粘膜の過形成および粘膜上皮の単細胞壊死がみられた.肝臓では,1000 mg/kg群の雌雄で重量増加,組織学的には小葉中心性の肝細胞肥大がみられたほか,髄外造血が認められた.胸腺では,1000 mg/kg群の雌雄で重量の減少と肉眼的および組織学的な萎縮がみられた.副腎では,1000 mg/kg群の雄で重量増加,組織学的に皮質束状帯細胞の肥大が観察された.また,脾臓における髄外造血の亢進および骨髄(大腿骨)における造血の亢進が1000 mg/kg群の雄にみられた.骨(大腿骨)では,海綿骨の増加が1000 mg/kg群の雌雄にみられた.腎臓では,200および1000 mg/kg群の雄で重量の増加がみられた.
回復群では,上記の変化のほとんどは消失または軽減され,回復性が認められた.ただし,200および1000 mg/kg群の雌雄における尿たん白陽性例および腎臓重量の増加は投与終了時剖検群と同程度であり,腎臓への影響については回復性が明らかではなかった.
以上の結果から,本試験条件下における4,4'-スルホニルジフェノールの無影響量は,雌雄ともに40 mg/kg/dayと考えられた.
投与容量が10 mL/kg体重となるよう,0.5 w/v%メチルセルロース水溶液に懸濁して4,20および100 mg/mL懸濁液を調製した.また,投与開始前および投与終了週の2回,投与に使用する各濃度液について当施設で測定した結果,いずれも濃度は適正でかつ均一であった.
動物は,群分け当日の体重に基づいて層別化し,各群平均体重がほぼ均等となるよう,コンピュータを用いて各群に割り付けた.
動物は,温度23±3℃,相対湿度50±20 %,換気回数1時間当たり10〜15回,照明1日12時間の飼育室で,金属製網ケージに1匹ずつ収容し,固形飼料(放射線滅菌CRF-1,オリエンタル酵母工業(株))および飲料水(水道水)を自由に摂取させ飼育した.
被験液の投与容量は10 mL/kg体重とし,金属製胃ゾンデを用いて1日1回28日間強制経口投与した.対照群には溶媒(0.5 %メチルセルロース水溶液)を同様に投与した.投与液量は最新の体重を基準に算出した.回復期間は14日間とした.
 法),ナトリウム,カリウムおよび塩素(イオン選択電極法),カルシウム(OCPC法),無機リン(モリブデン酸法),総たん白質(Biuret法),アルブミン(BCG法)およびA/G比(総たん白質およびアルブミンから算出)を測定した.また,ヘパリンを加えた容器に採血し,遠心分離(3000rpm,10分間)により得られた血漿を用いてGOT,GPT,LDH(UV-rate法)およびγ-GTP(γ-グルタミル-3-カルボキシ-4-ニトロアニリド法) (以上いずれも全自動分析装置Monarch,Instrumentation Laboratory)を測定した.
法),ナトリウム,カリウムおよび塩素(イオン選択電極法),カルシウム(OCPC法),無機リン(モリブデン酸法),総たん白質(Biuret法),アルブミン(BCG法)およびA/G比(総たん白質およびアルブミンから算出)を測定した.また,ヘパリンを加えた容器に採血し,遠心分離(3000rpm,10分間)により得られた血漿を用いてGOT,GPT,LDH(UV-rate法)およびγ-GTP(γ-グルタミル-3-カルボキシ-4-ニトロアニリド法) (以上いずれも全自動分析装置Monarch,Instrumentation Laboratory)を測定した.
脳,胸腺,心臓,肺(気管支を含む),肝臓,脾臓,腎臓,副腎,精巣,卵巣
脳,脊髄,坐骨神経,心臓,気管,肺(気管支を含む),胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,肝臓,甲状腺(上皮小体を含む),副腎,胸腺,脾臓,腸間膜リンパ節,顎下リンパ節,腎臓,膀胱,精巣,前立腺,卵巣,子宮,骨および骨髄(胸骨・大腿骨),大腿部骨格筋,肉眼的異常部位
投与期間中,1000 mg/kg群の雄の主群および回復群の各1例が死亡した.いずれも死亡前の一般状態に異常はみられなかった.
生存動物では,雄で投与直後の流涎が1000 mg/kg群の1例で投与20日にみられた.雌では,腹部膨満が1000 mg/kg群で投与15日に1例にみられ,その後例数が増加して投与28日には12例中5例に認められた.また,投与直後の流涎が1000 mg/kg群の1例で投与18日にみられた.
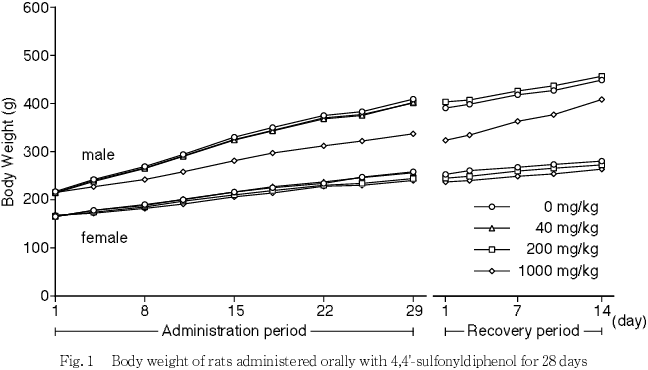
雌では,各投与群と対照群の間に有意な差は認められなかった.しかし,200および1000 mg/kg群の体重は投与24日以降低値傾向を示し,投与期間中の体重増加量は対照群に比べて有意に低かった.
雌では,各投与群と対照群の体重は,同様に推移した.
雌では,200 mg/kg群で投与4日,1000 mg/kg群で投与4,21および24日に対照群に比べて有意な低値がみられた.
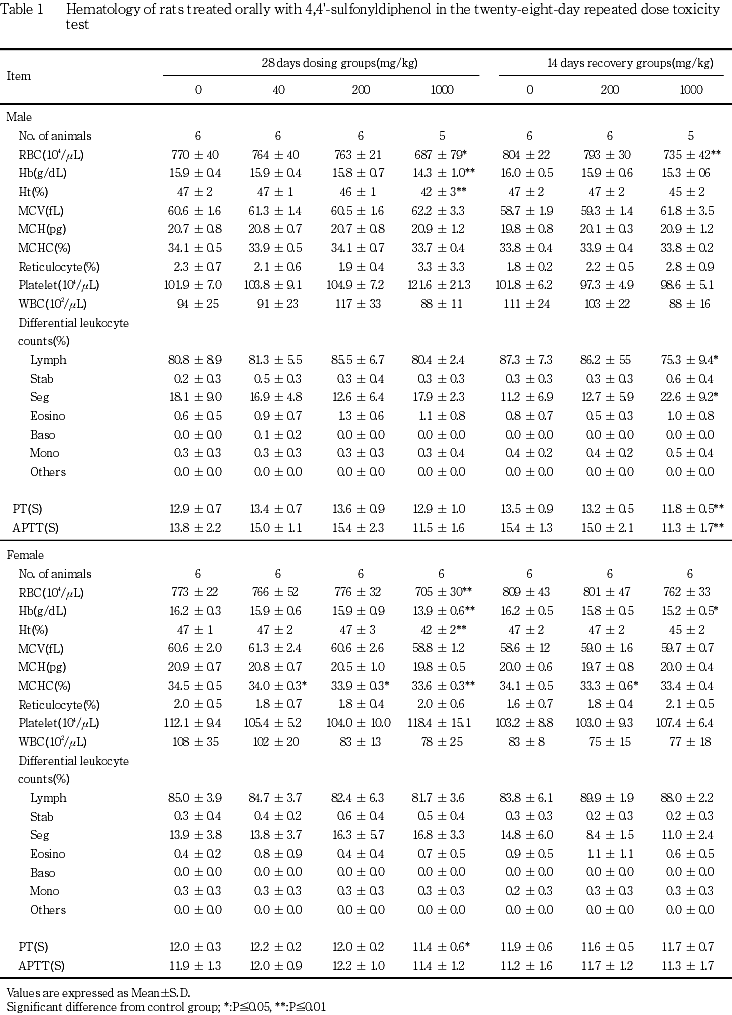
雌では,全ての被験物質投与群で平均赤血球血色素濃度の有意な減少がみられた.1000 mg/kg群では,これに加えて赤血球数,ヘモグロビン量およびヘマトクリット値の有意な減少ならびにプロトロンビン時間の有意な短縮がみられた.
雌では,1000 mg/kg群でヘモグロビン量の有意な減少がみられた.なお,200 mg/kg群で平均赤血球血色素濃度の有意な減少がみられたが,用量に応じた変化ではなかった.
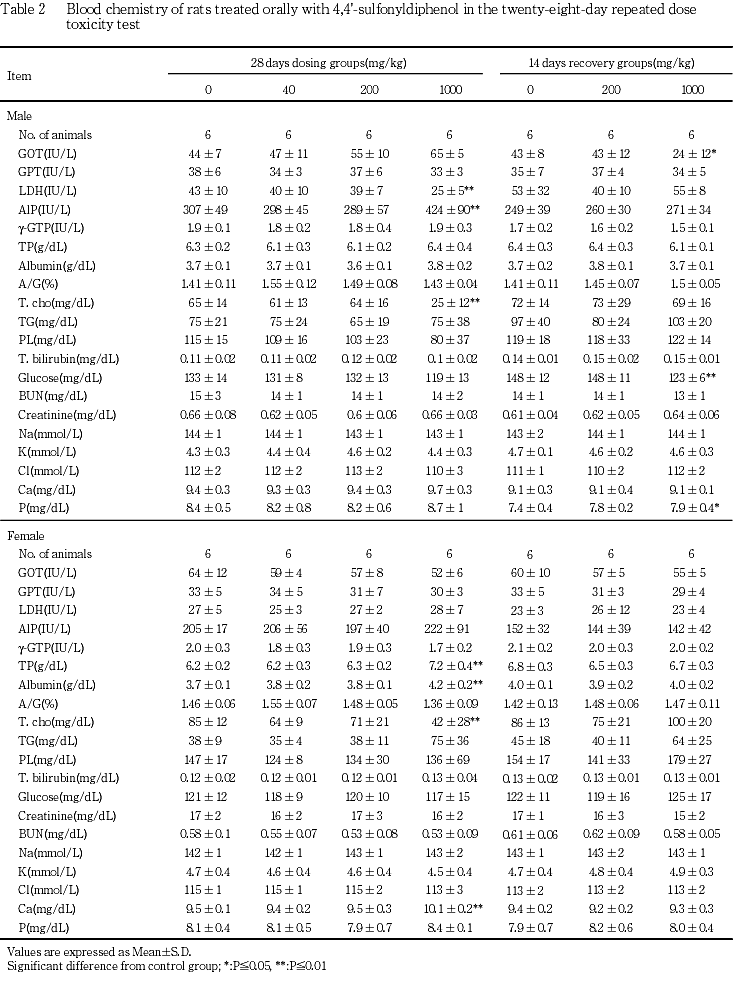
雌では,1000 mg/kg群で総たん白質,アルブミンおよびカルシウムの有意な増加と総コレステロールの有意な減少がみられた.
雌では,被験物質投与による変化は認められなかった.
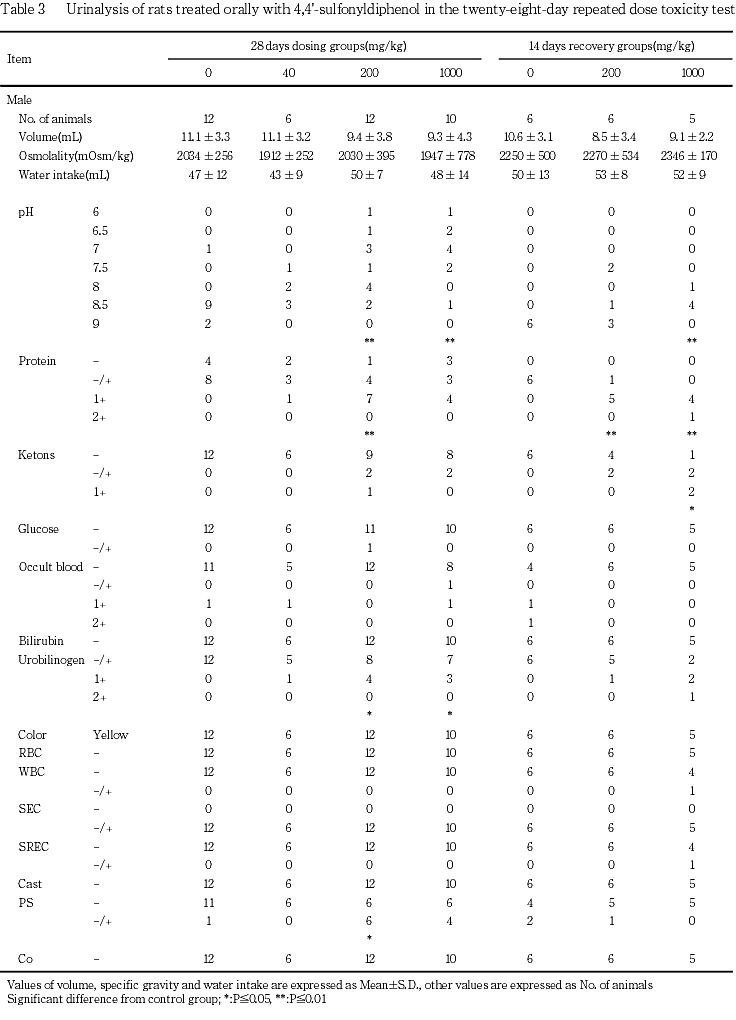

雌では,尿たん白陽性例の有意な増加が200 mg/kg群に,増加傾向が1000 mg/kg群にみられ,1000 mg/kg群ではpHの有意な低下もみられた.なお,尿沈渣中のリン酸塩結晶の有意な増加が200 mg/kg群にみられたが,用量に応じた変化ではなかった.
雌では,200 mg/kg群で尿たん白陽性例の増加傾向がみられ,1000 mg/kg群で尿たん白陽性例の有意な増加,pHの低下傾向およびケトン体陽性例の増加傾向がみられた.
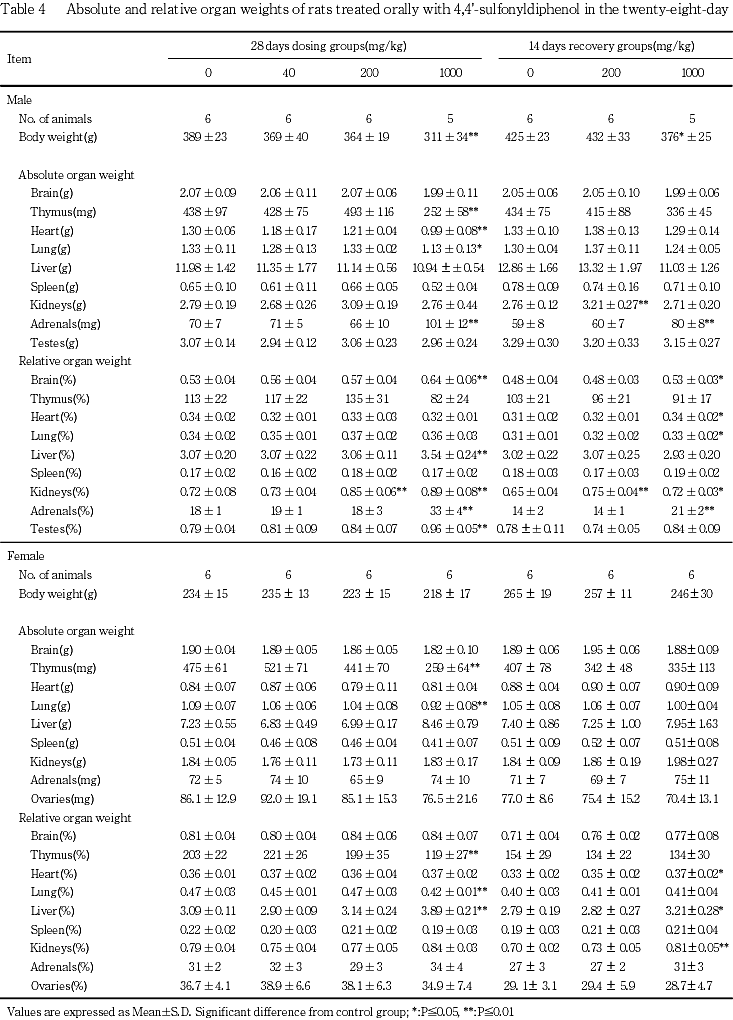
雌では,1000 mg/kg群で胸腺の絶対および相対重量の有意な減少,肺の絶対および相対重量の有意な減少および肝臓の相対重量の有意な増加がみられた.
他に,1000 mg/kg群の雄の心臓,肺,脳および精巣において,絶対重量の有意な減少あるいは相対重量の有意な増加がみられたが,いずれも剖検時の体重の低値に起因する変化と考えられた.
雌では,1000 mg/kg群で心臓,肝臓および腎臓の相対重量の有意な増加がみられた.
他に,1000 mg/kg群の雄の心臓,脳および肺の相対重量の有意な増加がみられたが,いずれも剖検時の体重の低値に起因する変化と考えられた.

他に,雌で対照群の1例に回腸の憩室,200 mg/kg群の1例に空腸の憩室がみられたが,偶発所見と考えられた.
雌では,腺胃の暗赤色点が200および1000 mg/kg群の各2例にみられた.
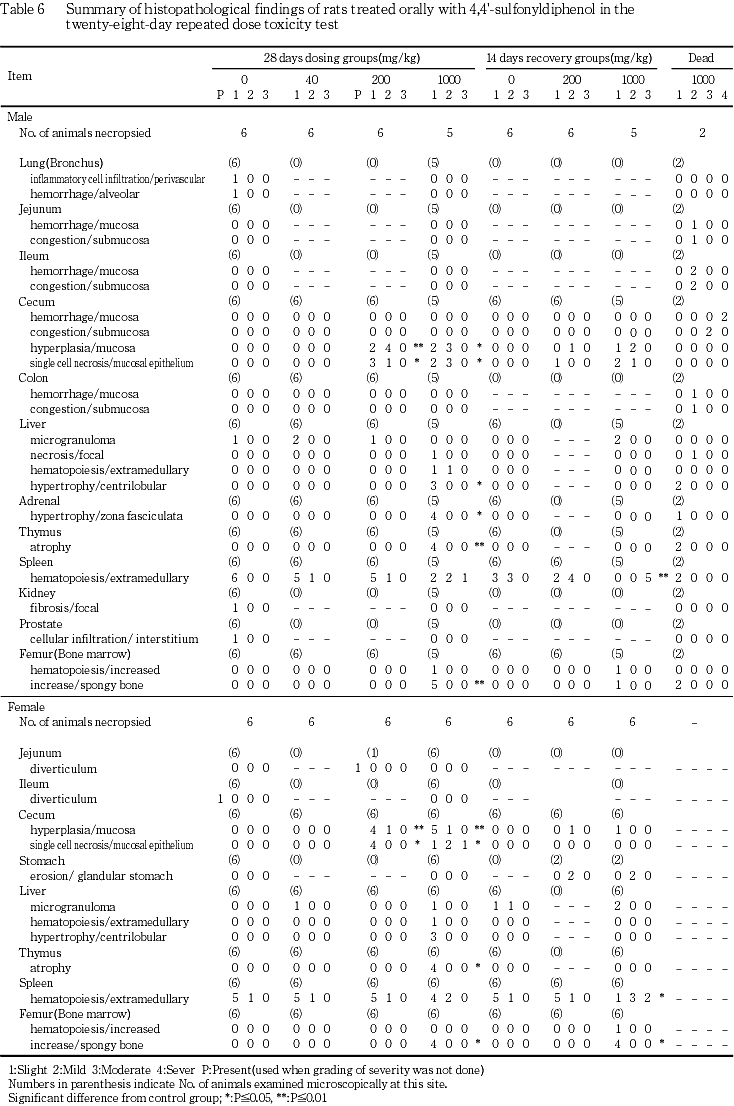
盲腸:ごく軽度あるいは軽度の粘膜の過形成が200 mg/kg群の雄全例と雌5例および1000 mg/kg群の雌雄全例に,ごく軽度〜中等度の粘膜上皮の単細胞壊死が,200 mg/kg群の雌雄各4例および1000 mg/kg群の雄全例と雌4例にみられた.
肝臓:ごく軽度の小葉中心性の肝細胞肥大が1000 mg/kg群の雌雄各3例に,ごく軽度あるいは軽度の髄外造血が1000 mg/kg群の雄2例と雌1例にみられた.
副腎:ごく軽度の皮質束状帯細胞の肥大が1000 mg/kg群の雄4例にみられた.
胸腺:ごく軽度の萎縮が1000 mg/kg群の雌雄各4例にみられた.
脾臓:髄外造血が,雄では対照群で全例がごく軽度なのに対し,40および200 mg/kg群ではそれぞれごく軽度5例と軽度1例,1000 mg/kg群ではごく軽度および軽度各2例と中等度1例であり,1000 mg/kg群では髄外造血の亢進傾向がみられた.一方,雌では対照群,40および200 mg/kg群でそれぞれごく軽度5例と軽度1例,1000 mg/kg群でごく軽度4例と軽度2例であり,髄外造血の亢進は明らかではなかった.
骨髄(大腿骨):ごく軽度の造血の亢進が1000 mg/kg群の雄1例にみられた.
骨(大腿骨):ごく軽度の海綿骨の増加が1000 mg/kg群の雄全例と雌4例にみられた.
上記以外の所見は出現状況とその病理学的性状からいずれも偶発所見と判断した.
盲腸:ごく軽度あるいは軽度の粘膜の過形成が200 mg/kg群の雌雄各1例と1000 mg/kg群の雄3例と雌1例に,ごく軽度あるいは軽度の粘膜上皮の単細胞壊死が200 mg/kg群の雄1例と1000 mg/kg群の雄3例にみられた.
脾臓:髄外造血が,雄では対照群でごく軽度と軽度が各3例なのに対し,200 mg/kg群ではごく軽度2例と軽度4例,1000 mg/kg群では全例が中等度,雌では対照群および200 mg/kg群でそれぞれごく軽度5例と軽度1例なのに対し,1000 mg/kg群ではごく軽度1例,軽度3例および中等度2例であり,1000 mg/kg群の雌雄で髄外造血の有意な亢進がみられた.
骨髄(大腿骨):ごく軽度の造血の亢進が1000 mg/kg群の雌雄各1例にみられた.
骨(大腿骨):ごく軽度の海綿骨の増加が1000 mg/kg群の雄1例と雌4例にみられた.
上記以外の所見は出現状況とその病理学的性状からいずれも偶発所見と判断した.
生存動物の一般状態では,1000 mg/kg群の雌において腹部膨満が投与期間の後半にみられたが,これは剖検時にみられた盲腸の拡張を反映した変化であった.また,投与直後の流涎が1000 mg/kg群の雌雄各1例にそれぞれ1回みられた.本所見は苦味などの刺激がある被験液を強制経口投与したときにしばしばみられるものであるが,今回の試験では発現頻度が非常に低く,毒性学的意義に乏しい変化であった.
体重では,200 mg/kg群の雌および1000 mg/kg群の雌雄で増加抑制が認められ,特に1000 mg/kg群の雄では影響が比較的強かった.また,これらの群では摂餌量の低値も観察された.
血液学検査では,1000 mg/kg群の雌雄において赤血球数,ヘモグロビン量およびヘマトクリット値の減少がみられたが,摂餌量の低下および盲腸の拡張による低栄養状態がもたらした二次的変化であろうと推定された.なお,雌の全ての投与群で平均赤血球血色素濃度の減少がみられたが,当施設における背景資料(32.7〜38.8 %)と比較すると,いずれも生理的変動の範囲内とみなせる程度の僅かな変化であることから,他の赤血球パラメーターに変化がみられなかった40および200 mg/kg群については,偶発的な変化と考えられた.なお,1000 mg/kg群の雌でみられたプロトロンビン時間の変化は,延長ではなく短縮であるため,毒性学的意義は乏しいと判断した.
血液生化学検査では,1000 mg/kg群でAlPの増加が雄に,総コレステロールの減少が雌雄にみられ,前者は後述の大腿骨における海綿骨の増加,後者は被験物質投与による低栄養状態あるいは肝臓障害に関連した変化と考えられた.その他として,1000 mg/kg群の雄にみられたLDH活性の変化は増加ではないことから毒性学的意義のある変化ではなかった.また,同群の雌でみられた総たん白質およびアルブミンの増加は被験物質投与による変化と考えられたがその機序は不明であった.なお,カルシウムの増加はアルブミンが増加したことによる「みかけ上のカルシウム高値」2)であり,毒性変化ではなかった.
尿検査では,200 mg/kg群の雄と1000 mg/kg群の雌雄でpHの低下,200および1000 mg/kg群の雌雄で尿たん白の増加と雄でウロビリノーゲンの増加がみられた.これらの変化の機序は明らかではないが,被験物質が腎臓に対して何らかの影響を及ぼすことが示唆された.
病理学検査では,盲腸,副腎,肝臓,胸腺,脾臓,骨髄(大腿骨),骨(大腿骨)および腎臓に変化がみられた.盲腸では,1000 mg/kg群の雌雄で肉眼的拡張がみられ,組織学的には200および1000 mg/kg群の雌雄で粘膜の過形成および粘膜上皮の単細胞壊死がみられた.盲腸の拡張は,ラットに抗生剤等の腸内細菌叢に変動をきたす物質や腸管内に水分を引き込む作用を有する高分子化合物を投与した際によくみられる.本被験物質は低分子物質であることから,今回みられた盲腸の拡張は,被験物質が腸内細菌叢に影響した結果引き起こされた可能性が示唆された.粘膜の過形成は盲腸が拡張したことに対する適応性の変化と考えられた.また,粘膜上皮の単細胞壊死は抗生剤等を投与した場合にはみられない変化であり,被験物質が盲腸粘膜に直接障害性に作用した可能性が示唆された.
肝臓では,1000 mg/kg群の雌雄で重量増加,組織学的には小葉中心性の肝細胞肥大が観察され,被験物質の肝臓に対する影響が示唆された.また,1000 mg/kg群の雌雄で髄外造血がみられたが,貧血に対する反応性の変化と考えられた.
胸腺では,1000 mg/kg群の雌雄で重量の減少と肉眼的および組織学的萎縮がみられ,被験物質投与によりもたらされた低栄養状態を反映した変化と考えられた.
副腎では,1000 mg/kg群の雄で重量増加,組織学的に皮質束状帯細胞の肥大が観察された.副腎は種々のストレスにより束状帯および網状体が肥大することが知られており,本試験では被験物質投与による低栄養状態や盲腸の拡張に伴う腸管の水分バランスの乱れがストレスの原因となり上記の変化を引き起こしたと考えられた.
脾臓における髄外造血の亢進および骨髄(大腿骨)における造血の亢進が1000 mg/kg群の雄にみられたが,いずれも肝臓の髄外造血と同様,貧血に対する反応性の変化と考えられた.
骨(大腿骨)では,海綿骨の増加が1000 mg/kg群の雌雄にみられたが,本変化の機序は明らかではなかった.
腎臓では,200および1000 mg/kg群の雄で重量の増加がみられたが,組織学検査では何ら異常は認められなかった.しかし,尿検査で尿たん白陽性例が200および1000 mg/kg群の雌雄にみられており,重量および尿たん白陽性例の変化は回復群にも主群と同程度にみられていることから,被験物質が腎臓に何らかの影響を及ぼしているものと考えられた.
その他として,肺の器官重量の増加が1000 mg/kg群の雌にみられたが,組織学的には何ら変化が認められず,偶発的な変化と考えられた.
休薬により,上記の変化のほとんどは消失または軽減され,回復性が認められた.ただし,200および1000 mg/kg群の雌雄では尿たん白陽性例および腎臓重量の増加が投与終了時剖検群と同程度にみられ,被験物質の腎臓への影響については回復性が明らかではなかった.なお,1000 mg/kg群の雌雄でみられた摂餌量の増加は,低栄養状態の回復期におけるリバウンド現象であり,脾臓の髄外造血および骨髄(大腿骨)の造血の亢進は,貧血の回復期におけるリバウンド現象と考えられた.更に,尿検査,血液学検査,血液生化学検査および器官重量において回復期間に新たに変化を生じた項目がみられたが,いずれも毒性学的意義に乏しいか毒性学的意義を持たない変化であった.
以上の如く,4,4'-スルホニルジフェノールをラットに28日間反復投与した結果,主な変化として200および1000 mg/kg群では盲腸における粘膜の過形成と粘膜上皮の単細胞壊死および尿蛋白陽性例の増加が雌雄に,腎臓の重量増加が雄にみられた.1000 mg/kg群ではこれに加えて盲腸の肉眼的拡張,赤血球数,ヘモグロビン量,ヘマトクリット値ならびに総コレステロールの減少,胸腺の肉眼的および組織学的な萎縮ならびに重量減少,肝臓の重量増加,小葉中心性の肝細胞肥大ならびに髄外造血および大腿骨における海綿骨の増加が雌雄に,副腎の重量増加と皮質束状帯細胞の肥大,脾臓の髄外造血の亢進,骨髄(大腿骨)における造血の亢進およびアルカリホスファターゼの増加が雄にみられた.一方40 mg/kg群の雌雄では変化は認められなかった.
これらの結果から,本試験における4,4'-スルホニルジフェノールの無影響量は雌雄ともに40 mg/kg/dayと推定された.
| 1) | S. C. Gad and C. S. Weil, "Principles and Methods of Toxicology," 2, ed. by A. W. Hayes, Raven Press Ltd., New York, 1989, pp. 435-483. |
| 2) | 藤田拓男,日本臨床(秋季増刊),532, 456(1985). |
| 連絡先 | |||
| 試験責任者: | 榎並倫宣 | ||
| 試験担当者: | 高須正生,畠山和久,田村一利,津田敏治,勝亦倶慶 | ||
| (株)ボゾリサーチセンター 御殿場研究所 | |||
| 〒412-0039 静岡県御殿場市かまど1284 | |||
| Tel 0550-82-2000 | Fax 0550-82-2379 | ||
| Correspondence | ||||
| Authors: | Tomonori Enami (Study director) Masao Takasu, Kazuhisa Hatayama, Kazutoshi Tamura, Toshiharu Tsuda, Toyohisa Katsumata | |||
| Gotemba Laboratory, Bozo Research Center Inc. | ||||
| 1284 Kamado, Gotemba-shi, Shizuoka, 412-0039, Japan | ||||
| Tel +81-550-82-2000 | Fax +81-550-82-2379 | |||