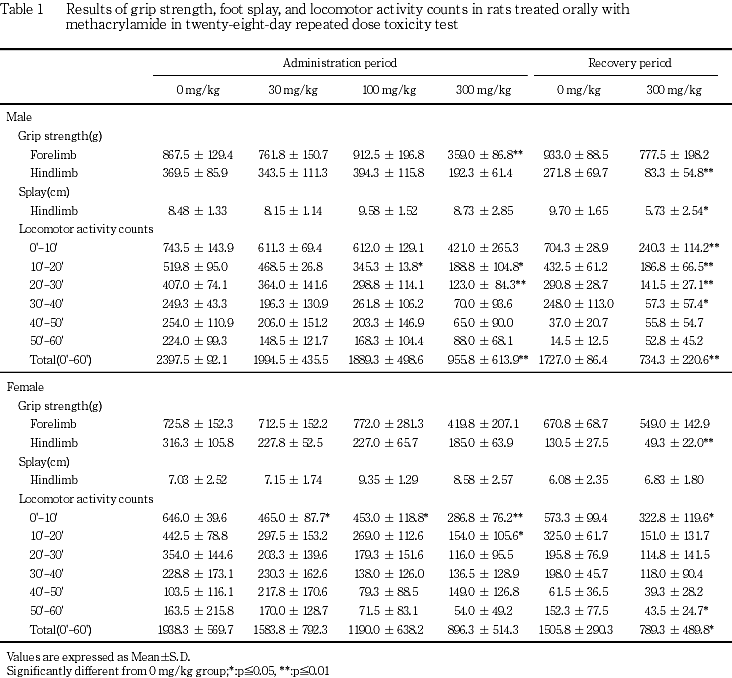
一般状態では,雌雄の300 mg/kg群でよろめき歩行ならびに後肢の反転を伴う例が認められ,この症状は回復期間の14日間を通して認められた.行動機能観察では300 mg/kg群に投与21あるいは28日に雌雄で筋緊張の低下,歩行失調,雄で前肢の握力の低下がみられ,100および300 mg/kg群の雌雄ならびに30 mg/kg群の雌で自発運動量の低下が認められた.回復期間にも,300 mg/kg群の雌雄で筋緊張の低下,歩行失調,後肢の握力および自発運動量の低下がみられ,雄では後肢の着地開脚幅の低下も認められた.この変化は,投与期間および回復終了時の病理組織学検査において,300 mg/kg群の雌雄の全例で坐骨神経に神経線維の変性,また小脳に小脳脚における軸索膨化(1〜2例)がみられたことから,メタクリルアミドによる神経毒性に起因するものであった.この神経毒性に関連して,投与終了時の剖検時に300 mg/kg群の雌雄の1〜3例に膀胱の内腔拡張も認められた.
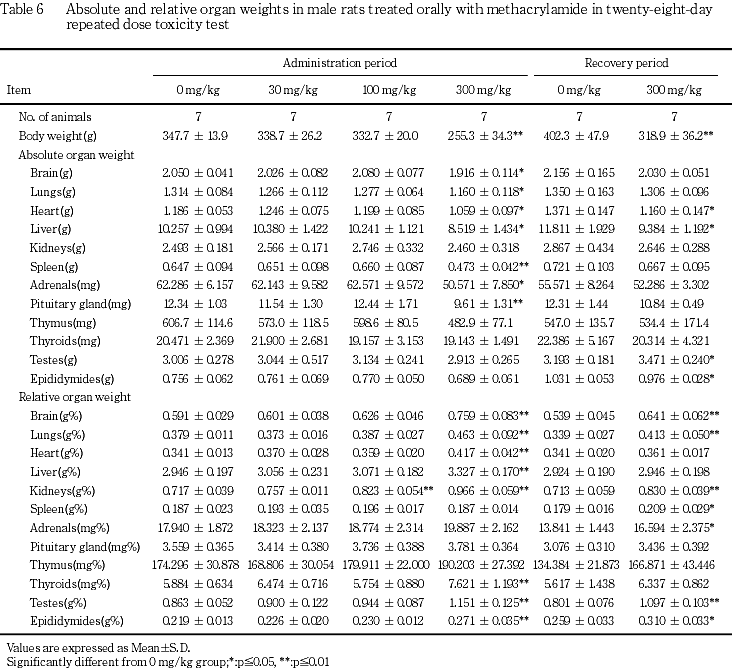
一方,回復終了時の病理組織学検査で1例のみの変化ではあるが,雄の300 mg/kg群にステージIX,Xにおけるステップ19精子細胞のretentionがみられ,軽度な精巣毒性も認められた.この変化との関連は明らかでなかったが,回復終了時に300 mg/kg群の雄の精巣の器官重量および器官体重重量比の増加も認められた.
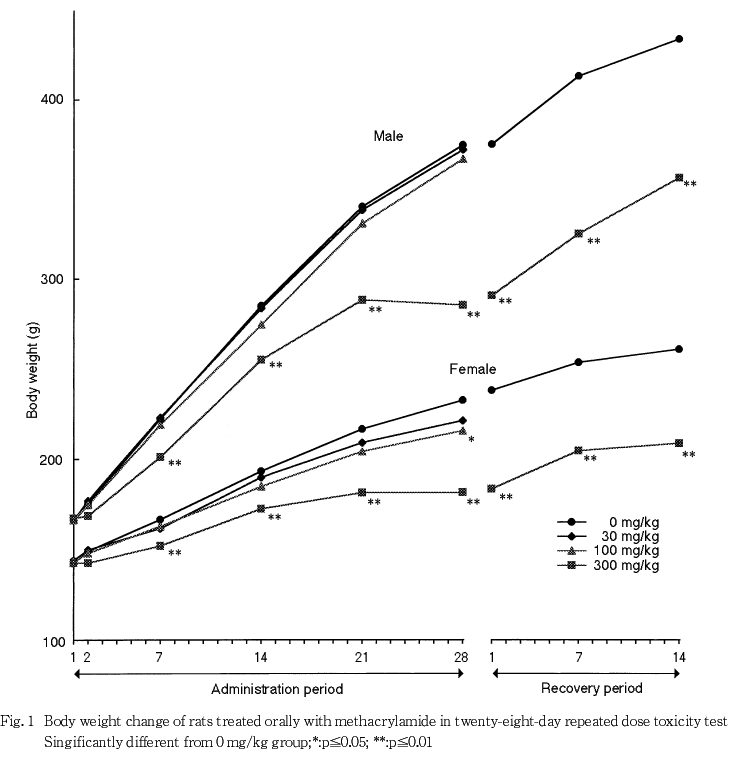
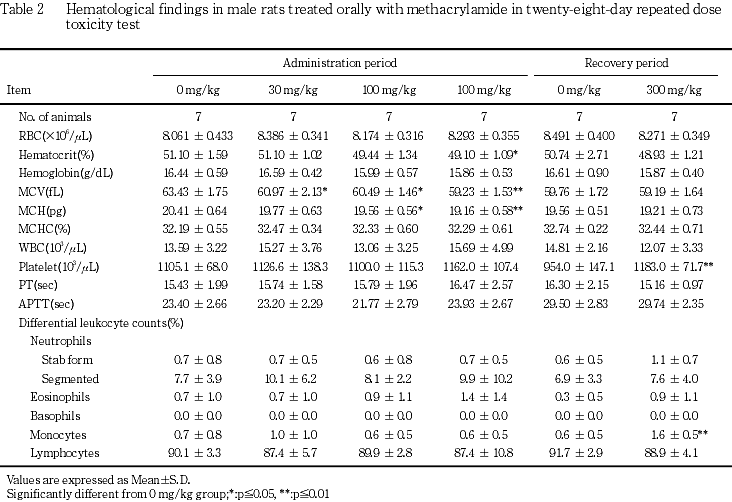
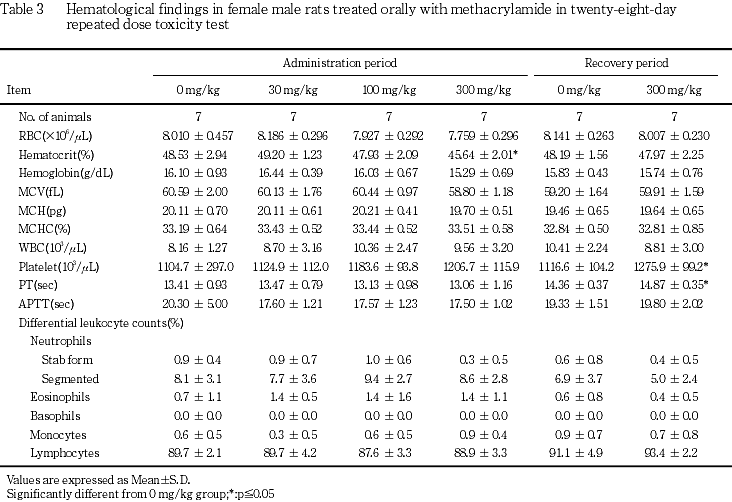
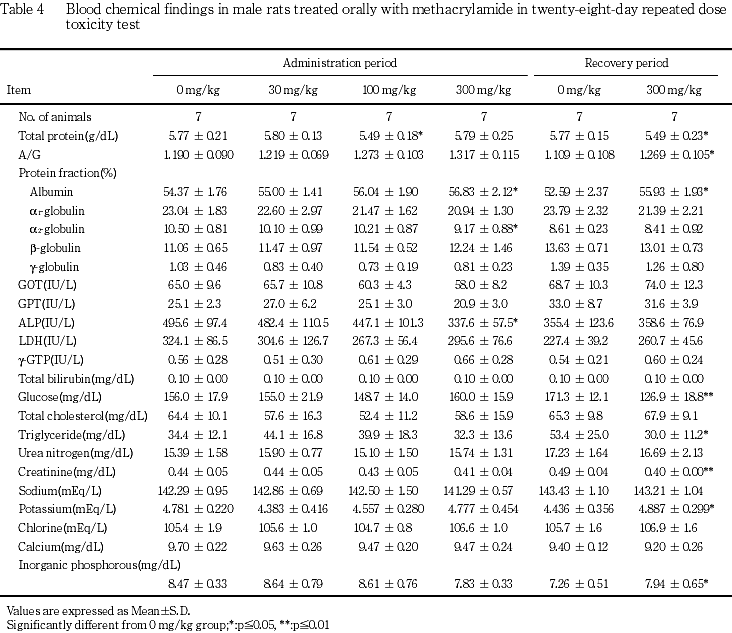
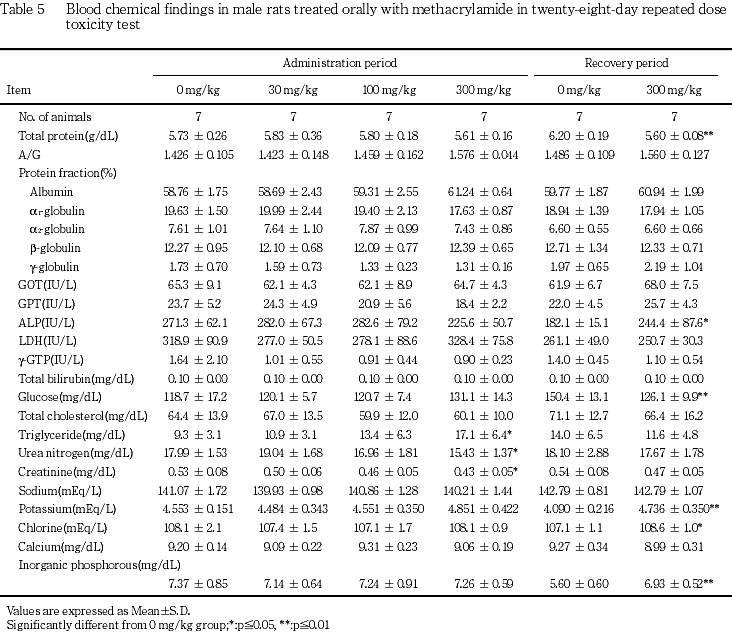
その他にも,体重では,300 mg/kg群の雌雄で投与2日から体重増加抑制が認められ,投与7日以降にも低く推移し,この体重増加抑制は回復期間中にも認められた.また,投与28日には100 mg/kg群の雌でも認められた.摂餌量では,300 mg/kg群の雌雄で摂餌量の低下が投与2日以降に散見されたが,この摂餌量の低下は回復期間の後半には回復した.また投与4週に300 mg/kg群の雌雄で飲水量の低下がみられ,雌では回復2週にも認められた.血液学検査では,300 mg/kg群の雌雄および100 mg/kg群の雄で貧血傾向が認められたが,回復終了時には雄で血小板数の増加が,雌で血小板数の増加およびプロトロンビン時間の延長が認められたのみであった.血液生化学検査では,300 mg/kg群の雌雄でアルブミンの増加,α1-グロブリンおよびアルカリホスファターゼの低下がみられ,雄でα2-グロブリンの低下,雌でトリグリセリドの増加,尿素窒素およびクレアチニンの低下が認められた.回復終了時では,300 mg/kg群の雄でA/G比,アルブミン,カリウムおよび無機リンの増加,総蛋白,グルコースおよびトリグリセリドの低下,雌でアルカリホスファターゼ,カリウム,クロールおよび無機リンの増加,総蛋白およびグルコースの低下が認められた.これらの変化はメタクリルアミドの直接の毒性あるいはメタクリルアミドによる神経毒性に関連した変化と考えられた.
以上のことから,本試験条件下での無影響量(NOEL)は雄で30 mg/kg/day,雌で30 mg/kg/day未満と考えられた.
動物は,投与日に一番近い測定日の体重に基づいて5 mL/kgの容量でラット用胃ゾンデを用いて1日1回,28日間の計28回,強制的に胃内に投与した.
 nwald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 rpmで10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
nwald-Giemsa染色)を測定した.また,3.8 %クエン酸ナトリウムで処理した後,3000 rpmで10分間遠心分離して得られた血漿を用いて,プロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,血液凝固自動測定装置アメルングKC-10A,バクスター)を測定した.
 blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,また,無処理血液を3000 rpmで10分間の遠心分離で得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff
blewski & La Due法)およびグルコース(ヘキソキナーゼ法)を測定し,また,無処理血液を3000 rpmで10分間の遠心分離で得られた血清を用いてGPT(IFCC法),アルカリホスファターゼ(Bessey-Lowry法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(Jaff 法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,コーニング480型炎光光度計),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
法),カルシウム(OCPC法),無機リン(Fiske-SubbaRow法),総蛋白(ビウレット法)(以上,自動分析装置7150形,日立製作所),ナトリウム,カリウム(以上,炎光光度法,コーニング480型炎光光度計),クロール(電量滴定法,クロライドカウンターCL-6M,平沼産業),蛋白分画およびA/G比(以上,セルロースアセテート膜電気泳動法,全自動電気泳動装置CTE-150,常光)を測定した.
回復期間中は,300 mg/kg群で,雌雄とも回復7および14日に筋緊張の低下および歩行失調がみられ,そのスコアに有意差が認められた.また,回復2週に雌雄とも後肢に有意な握力の低下がみられ,また自発運動量では,雄で0〜10,10〜20,20〜30および30〜40分ならびに60分間のカウント数,雌で0〜10および50〜60分のカウント数ならびに60分間のカウント数に有意な低下が認められた.雄ではさらに後肢に有意な着地開脚幅の低下も認められた.

回復期間中も,雌雄の300 mg/kg群で体重が低く推移したが,体重増加量および体重増加率は対照群を上回り回復傾向が認められた.
回復期間中は,雌雄の300 mg/kg群で回復1あるいは7日まで有意な低下がみられたが,回復14日には有意差はみられなかった.
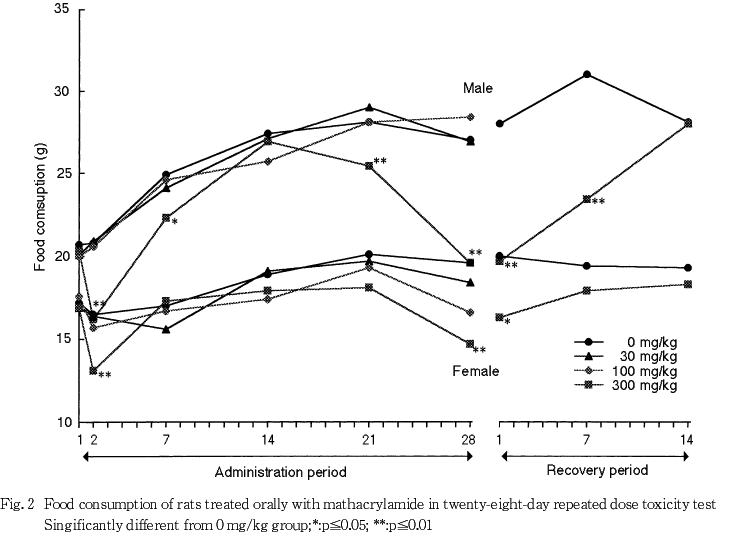
飲水量では,投与4週に雌雄の300 mg/kg群で対照群と比較して有意な低下あるいは低下傾向が認められ,回復2週にも雌で有意な低下が認められた.
回復終了時に,雌雄の300 mg/kg群で血小板数に有意な増加がみられ,雌でプロトロンビン時間に有意な延長が認められた.また,雄で単球に有意な増加がみられたが,正常範囲内の数値であった.
回復終了時に,300 mg/kg群の雄でA/G比,アルブミン,カリウムおよび無機リンの有意な増加,総蛋白,グルコースおよびトリグリセリドの有意な低下が認められた.また,雌ではアルカリホスファターゼ,カリウム,クロールおよび無機リンの有意な増加,総蛋白およびグルコースの有意な低下が認められた.一方,雄でクレアチニンに有意な低下が認められたが,対照群の変動範囲内の値であった.
回復終了時に,300 mg/kg群の雄の1例で肺の右中間葉および左肺に白色斑が認められ,また雌の1例で右腎臓に腎盂拡張および子宮に嚢胞が認められた.
回復終了時には,300 mg/kg群の雌雄ともに3〜5例で小脳脚における軸索膨化が軽度に認められ,また全例で坐骨神経に軽度〜中等度な神経線維の変性が認められた.さらに,雄の1例で精巣にステージIX,Xにおけるステップ19精子細胞の軽度なretentionが認められた.
対照群および300 mg/kg群で投与終了時および回復終了時にみられたその他の変化にはメタクリルアミド投与との関連性は認められなかった。
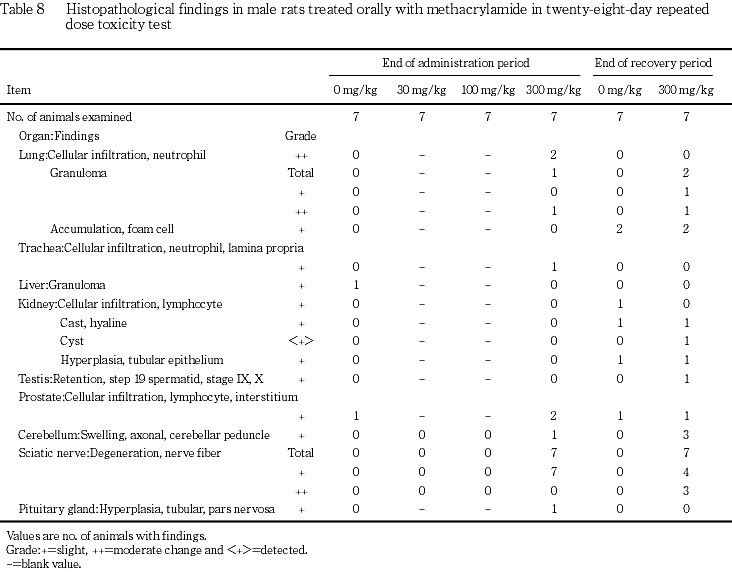
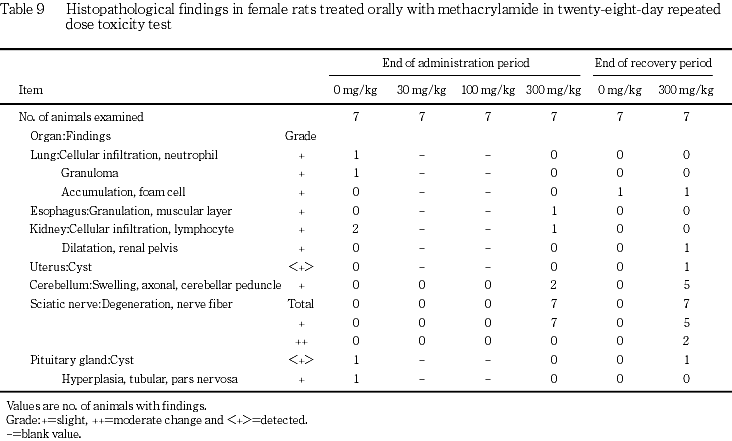
一般状態では,300 mg/kg群で投与3〜4週から雌雄いずれにもよろめき歩行がみられ,後肢の反転を伴う例も認められ,これらの神経症状は回復期間中にも継続して観察された.よろめき歩行および後肢の反転はアクリルアミドにおいて報告されている後肢の麻痺3)と類似した症状と考えられ,メタクリルアミドではマウスに神経毒性が報告1)されていることから,これらの歩行異常はメタクリルアミドの末梢神経に対する毒性により,後肢が麻痺した結果と推察された.
行動機能観察では,投与期間中に300 mg/kg群の雌雄で筋緊張の低下,歩行失調,握力の低下,雄で自発運動量の低下が認められた.この変化はいずれも末梢神経に対する神経毒性を示唆する前述の一般状態の変化とともに認められた.後肢の着地開脚幅の低下については回復期間に認められており,自発運動量の低下についても雌雄とも回復期間中の方がより高頻度に認められた.このことは末梢神経に対する神経毒性が,投与期間終了後にも進行したものと推察された.握力の低下については,アクリルアミドの30 mg/kgを5週間投与した試験4)でも報告されていることから,この変化はメタクリルアミドの影響と考えられた.後肢の握力の低下に関連する病変として病理組織学所見で坐骨神経に神経線維の変性が確認された.前肢の握力の低下については,病理組織学検査で認められた小脳の小脳脚における軸索膨化との関連が考えられた.雌の30および300 mg/kg群,雌雄の100 mg/kg群では,自発運動量の測定開始後0〜10あるいは10〜20分に有意な低下が認められた.対照群の動物では測定開始後の自発運動量が時間の経過とともに減少していく傾向がみられており,これは周囲の状況に馴れるに従って運動量が低下していくものと推察された.したがって,60分間の自発運動量に変化がみられないこと,各投与群の自発運動量の低下がいずれも測定開始後の初期にみられたことから,対照群に比較して周囲の状況の変化に対して鈍感であった可能性,あるいは運動活性が低下していた可能性が考えられた.このことは,60分間の自発運動量に有意差がみられている300 mg/kg群でも,測定開始後の初期に対照群と比較して有意差がみられる場合が多いことから,測定開始後の初期に認められた自発運動量の低下は,メタクリルアミドの影響によるものと推察された.なお,雌雄の30および100 mg/kg群では,一般状態,病理組織学検査において変化はみられなかった.
剖検では,300 mg/kg群で雌雄とも1〜3例と少数例ではあるが膀胱に内腔拡張が認められた.この変化は,600 mg/kgを10〜13日間投与した予備試験における死亡例にも認められ,メタクリルアミドとの関連が示唆された.また,この変化は,前述の後肢の麻痺に関連して,末梢神経の障害に起因した排尿困難による可能性も考えられた.
病理組織学検査では,300 mg/kg群の雌雄の全例で,坐骨神経に軽度な神経線維の変性が認められ,メタクリルアミドの神経毒性と考えられた.この変化は回復終了時ではその程度を増強し,前述と同様に末梢神経に対する神経毒性が,回復期間にも進行した可能性が推察された.アクリルアミドの50 mg/kgの週3回投与を4週間行った試験では,投与終了後40日には後肢の麻痺が回復し,末梢神経線維の再生像も認められている3)ことから,本試験において認められた神経線維の変性は,14日間の回復期間では回復するまでには至らなかったものと考えられた.また,300 mg/kg群の雌雄の小脳に散見された小脳脚における軸索膨化については,アクリルアミドの50 mg/kgの10日間投与においても認められている5).なお,30および100 mg/kg群では,これらの神経毒性を示唆する変化は認められなかった.
一方,300 mg/kg群の1例の精巣で回復終了時に認められたステージIX,Xにおけるステップ19精子細胞のretentionについては,セルトリ細胞の障害に起因するものと考えられている6).メタクリルアミドの急性経口投与毒性試験2)においても精巣毒性が示唆され,精母細胞および精子細胞に変化が認められたが,本試験で認められた所見とは異なり,またセルトリ細胞に障害がみられないことから,神経毒性の発現により体重および摂餌量の低下が継続したことに起因して,前述の精子細胞のretentionが起きた可能性も考えられた.しかし,精子細胞のretentionについては,特定のステージにのみ認められていることから精巣毒性の可能性を否定することはできなかった.
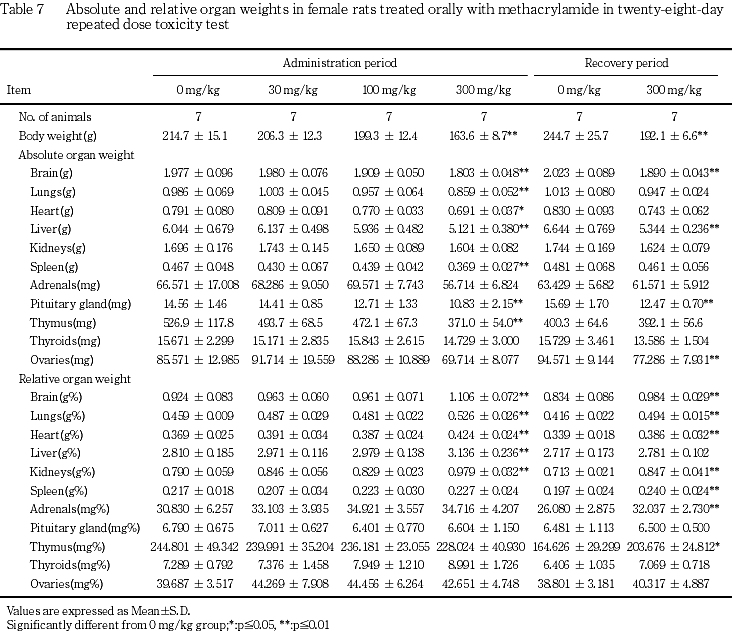
体重では,300 mg/kg群で雌雄とも投与初期から体重増加抑制が認められ,投与7日以降,回復終了時まで体重が低く推移した.また100 mg/kg群の雌でも投与28日に有意な体重増加抑制が認められた.回復期間には体重増加が認められたが,対照群と同等までの回復には至らなかった.
摂餌量では,300 mg/kgで雌雄とも摂餌量の低下が,投与初期から回復期間の前半まで継続したが,回復期間終了の時点では対照群とほぼ同等まで回復した.
血液学検査では,雌雄の300 mg/kg群でヘマトクリット値およびヘモグロビン量の低下あるいは低下傾向が認められ,雄の100 mg/kg群でもヘマトクリット値およびヘモグロビン量に低下傾向が認められた.また,雄の100および300 mg/kg群では平均赤血球容積および平均赤血球ヘモグロビン量にも低下が認められた.この貧血傾向は,雌雄の300 mg/kg群において神経症状が継続して認められたこと,体重の低下が投与7日以降継続して認められ,投与28日には減少あるいは停滞したこと,ならびに摂餌量の低下が継続的に認められたことに関連した二次的な変化と考えられた.しかし,骨髄あるいは脾臓に毒性を示唆する変化は認められず,回復期間には,これら貧血傾向を示唆する変化は認められなかった.また,雌雄の300 mg/kg群に血小板数の増加,雌のプロトロンビン時間の延長が認められ,この変化も,神経症状ならびに体重と摂餌量の低下が継続した影響によるものと考えられた.
血液生化学検査では,投与終了時に雌雄の300 mg/kg群でα1-グロブリンに低下傾向およびアルカリホスファターゼに低下あるいは低下傾向がみられ,雄ではα2-グロブリンに低下,雌ではトリグリセリドに増加もみられた.この変化も血液学検査の場合と同様に,神経症状ならびに体重および摂餌量の低下が継続したことに起因するものと推察された.雌雄の300 mg/kg群でアルブミンに増加あるいは増加傾向が認められ,回復終了時に雄ではA/G比に増加も認められた.雌の300 mg/kg群では,尿素窒素およびクレアチニンに低下が認められたが,腎臓に病理組織学的な異常は認められなかった.
回復期間に雌雄いずれも総蛋白,グルコースに低下およびカリウム,無機リン等の電解質に増加が認められたが,この変化は,神経症状ならびに体重と摂餌量の低下が継続した影響が回復していないことに起因するか,あるいは神経毒性が進行したことから神経組織からの逸脱に起因する等の可能性が考えられた.
器官重量および器官体重重量比では,回復終了時の300 mg/kg群で精巣の器官重量および器官体重重量比に増加が認められたが,精子細胞のretentionが認められたのは1例のみであり,その原因について病理組織学所見から明らかにすることは出来なかった.
以上,メタクリルアミドをラットに28日間反復経口投与した場合,雌雄いずれも300 mg/kg投与で神経症状および体重増加抑制が認められ,病理組織学的には神経毒性が認められた.14日間の回復終了後に,この神経毒性には回復性が認められなかった.また,100 mg/kg投与でも,雌雄いずれにも自発運動量の低下,さらに雄で貧血傾向および腎臓の器官体重重量比の増加が,雌で体重増加抑制が認められた.30 mg/kg投与では,雌で自発運動量の低下が認められた.
これらのことから,本試験条件下での無毒性量(NOEL)は雄で30 mg/kg/day,雌で30 mg/kg/day未満と考えられた.
| 1) | K. Hashimoto, J. Sakamoto, and H. Tanii, Arch. Toxicol., 47, 179(1981). |
| 2) | 厚生省生活衛生局企画課生活化学安全対策室監修,"化学物質毒性試験報告,"Vol. 7,化学物質点検推進連絡協議会,東京,1999, p. 41. |
| 3) | B. Veronesi, K. Jones, S. Gupta, J. Pringle and C. Mezei, Neurotoxicology, 12, 715(1991). |
| 4) | G. E. Schulze and B. G. Boysen, Fund. Appl. Toxicol., 16, 602(1991). |
| 5) | D. J. O'Shaughnessy and G. J. Losos, Toxicol. Pathol., 14, 389(1986). |
| 6) | D. M. Creasy, Toxicol. Pathol., 25, 119(1997). |
| 連絡先 | |||
| 試験責任者: | 須永昌男 | ||
| 試験担当者: | 吉田文子,皆川英俊,平田真理子,古川正敏,山本美代子 | ||
| (株)化合物安全性研究所 | |||
| 〒004-0839 札幌市清田区真栄363番24 | |||
| Tel 011-885-5031 | Fax 011-885-5313 | ||
| Correspondence | ||||
| Authors: | Masao Sunaga (Study director) Ayako Yoshida, Hidetoshi Minagawa, Mariko Hirata, Masatoshi Hurukawa, Miyoko Yamamoto | |||
| Safety Research Institute for Chemical Compounds Co., Ltd. | ||||
| 363-24 Shin-ei, Kiyota-ku, Sapporo, Hokkaido, 004-0839, Japan | ||||
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |||