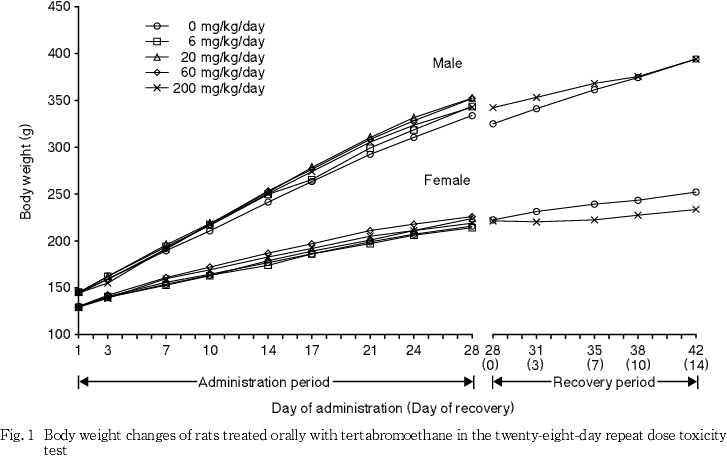
今回,四臭化エタンについて,SD系[Crj:CD(SD)IGS]ラットを用い,0(溶媒),6,20,60および200 mg/kg用量で,28日間反復経口投与毒性試験を実施した.動物数は1群雌雄各5匹とし,投与期間終了後屠殺群の5群,ならびに14日間回復群として対照および200 mg/kgの2群を設定した.
その結果,200 mg/kg群で雌雄に一過性の軟便が認められた.尿検査においては,200 mg/kg群で雄にpHの低下が認められた.血液学検査においては,200 mg/kg群で雌に血小板数の減少が認められた.血液生化学検査においては,20および60 mg/kg群で雌にアルブミンおよび総タンパクの増加,雄に塩素の減少,60 mg/kg群で雄にカリウムの減少,雌にA/G比およびカルシウムの増加が認められ,200 mg/kg群ではこれらの変化および総コレステロールの増加が雌雄に,γ-GTPの増加および総ビリルビンの減少が雄に認められた.剖検においては,20 mg/kg以上の群で雌雄に肝臓の大型化が認められ,肝臓重量は,20 mg/kg群の雄で相対重量,60および200 mg/kg群の雌雄で絶対および相対重量の増加が認められた.また,200 mg/kg群で腎臓の雄では相対重量,雌では絶対および相対重量の増加が認められた.病理組織学検査においては,肝臓に小葉中心性肝細胞肥大が20 mg/kg以上の群で雌雄に,甲状腺の濾胞上皮肥大が60および200 mg/kg群で雌雄に認められた.腎臓には変化は認められなかった.
回復群では,肝臓の病理組織学的変化およびこれと関連する血液生化学的変化は残るものの回復傾向にあり,その他の変化はいずれも回復することが確認された.
以上の結果から,四臭化エタンのラットへの28日間反復投与による主な毒性は,肝臓および甲状腺に対する影響で,腎臓,電解質,血液などに対する影響も認められた.無影響量は,雌雄とも6 mg/kg/dayと推定された.
 法),GOT,GPT,γ-GTP,ALP(以上,JSCC法),LDH(SFBC法),コリンエステラーゼ(BTC-DTNB法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-132]により,ナトリウムおよびカリウムを測定した.塩素は高速液体クロマトグラフシステム[島津製作所(株),LC-10Aイナーイト]を用いてイオンクロマトグラフ法で測定した.
法),GOT,GPT,γ-GTP,ALP(以上,JSCC法),LDH(SFBC法),コリンエステラーゼ(BTC-DTNB法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-132]により,ナトリウムおよびカリウムを測定した.塩素は高速液体クロマトグラフシステム[島津製作所(株),LC-10Aイナーイト]を用いてイオンクロマトグラフ法で測定した.
 群間で標本数が異なる場合)の方法により対照群に対する各群の比較検定を行った.カテゴリカルデータにはFisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.
群間で標本数が異なる場合)の方法により対照群に対する各群の比較検定を行った.カテゴリカルデータにはFisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.

回復期間において,雌の200 mg/kg群の摂餌量が低値傾向にあったものの,有意な変化ではなかった.
回復期間中の検査において,各検査項目に変化は認められなかった.
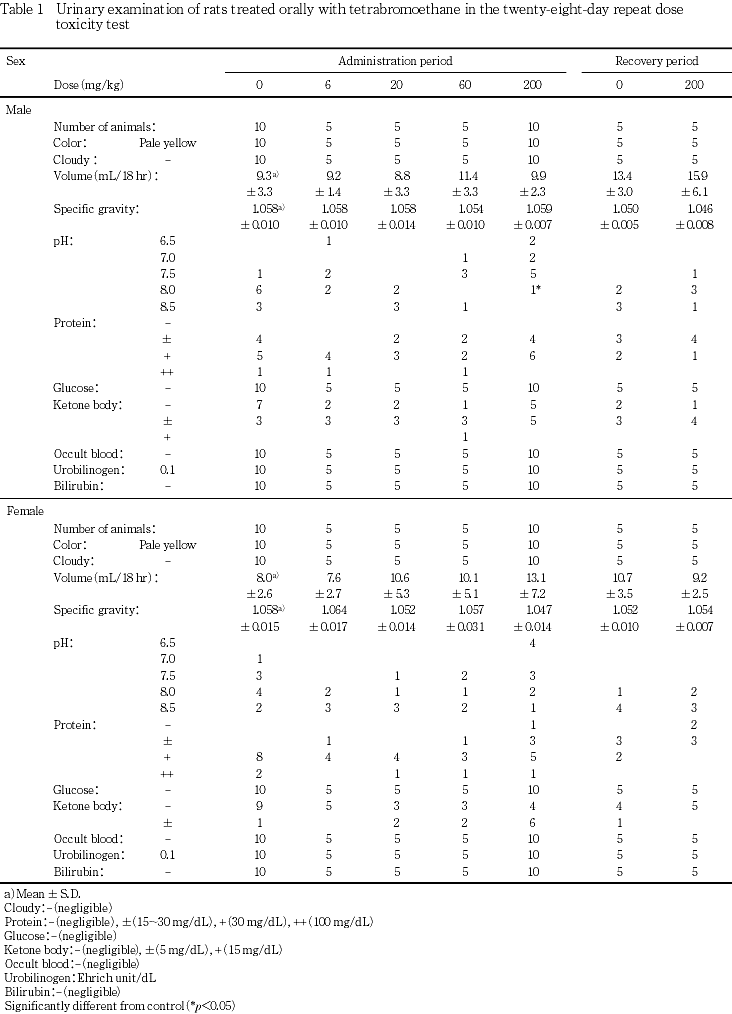
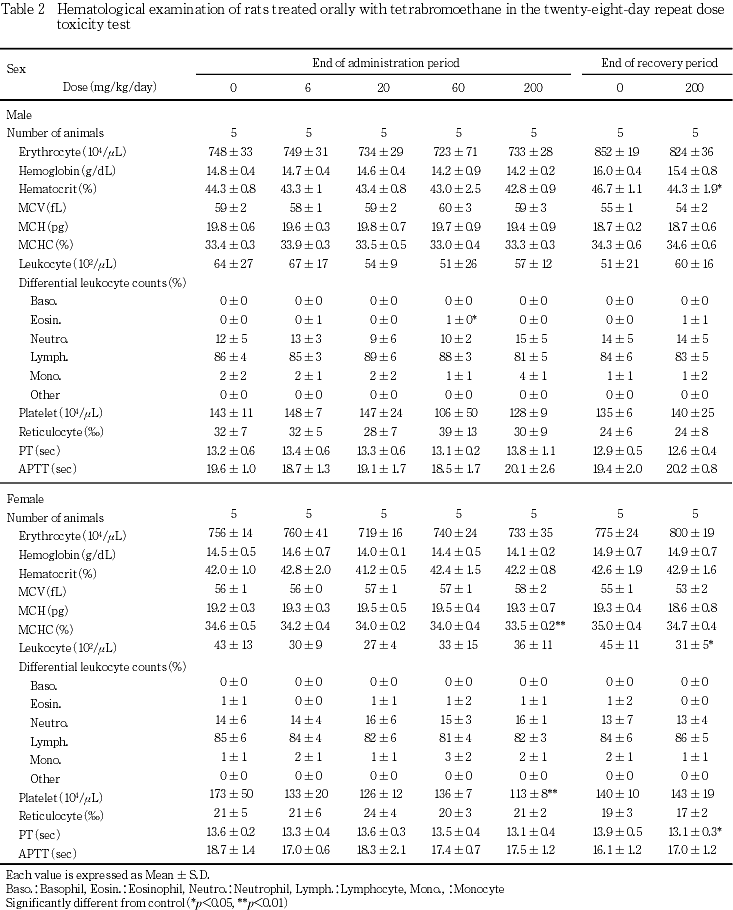
回復期間終了時の検査において,雄にヘマトクリット値の減少,雌に白血球数の減少およびプロトロンビン時間の短縮が認められたが,これらはいずれも投与期間終了時の検査では認められなかった変化であり,偶発的な所見と判断された.
回復期間終了時の検査において,雌雄の総タンパクの増加,雄の総ビリルビンの減少および雌の総コレステロールの増加に有意差が残るものの,総タンパクおよび総コレステロールの変化は軽減する傾向にあった.雌雄のγ-GTPは有意な減少および雄のカリウムは有意な増加を示したが,これは投与期間終了時とは逆の変化であった.

回復期間終了時においては,肝臓の大型化が雄の3匹,雌の2匹に認められた.
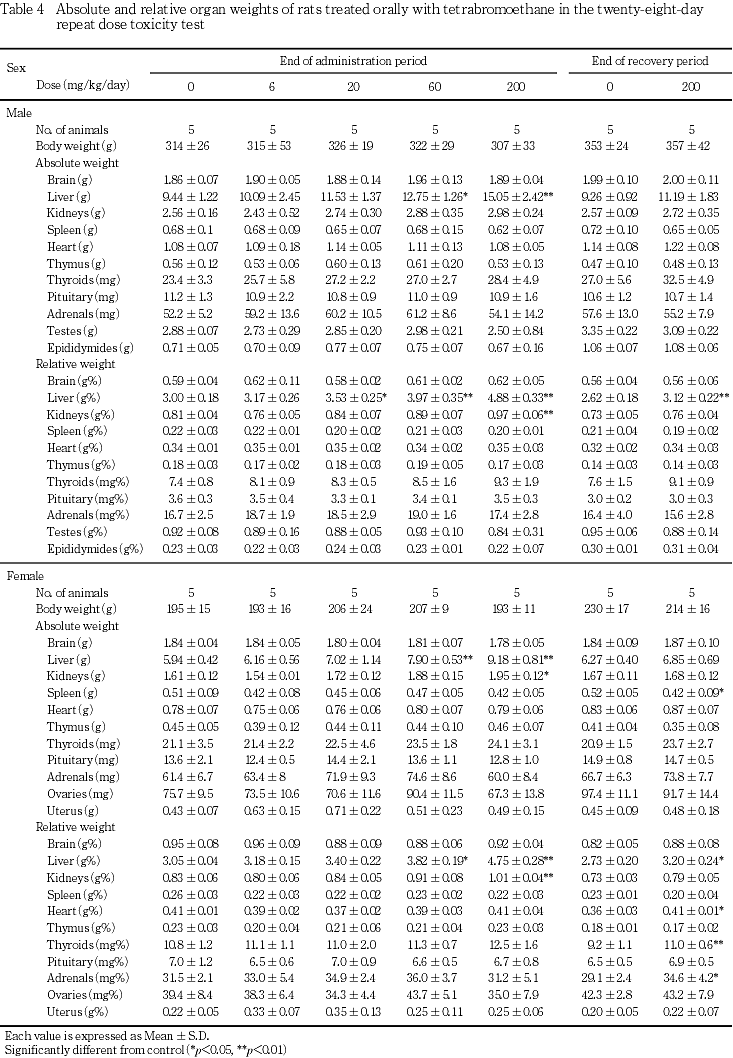
回復期間終了時の検査では,投与期間終了時で認められた変化のうち,肝臓は雌雄とも相対重量に有意差が残るものの変化の程度は軽減する傾向にあり,腎臓には有意な変化は認められなかった.雌雄の甲状腺の絶対および相対重量の増加傾向は回復群においても残存し,雌の相対重量には有意差が認められた.
なお,回復群において,雌で最終体重の低値傾向がみられ,あわせて脾臓の絶対重量の有意な減少ならびに心臓および副腎の相対重量の有意な増加が認められた.
回復期間終了時において,200 mg/kg群で肝臓の肝細胞肥大が雄の3匹および雌の2匹に認められたが,投与期間終了時と比べて,発現率および変化の程度は軽減する傾向にあった.
以上の変化以外にも,投与期間終了時屠殺動物の検査した各器官に変化が認められたが,散発的あるいは用量相関の認められない所見であった.


肝臓に対する影響としては,肝臓重量の増加傾向が20 mg/kg以上の群の雌雄に用量相関的に認められ,病理組織学的には小葉中心性の肝細胞肥大が認められた.肝機能と関連する血液生化学的変化として,20 mg/kg以上の群の雌および200 mg/kg群の雄にアルブミンの増加が認められ,総タンパクおよびA/G比は高値を示した.200 mg/kg群でみられた雌雄の総コレステロールの有意な増加,雄のγ-GTPの有意な増加についても,肝臓に対する影響と関連した変化である可能性が考えられる.なお,肝臓の巣状壊死が雄の各群に認められ,200 mg/kg群では増加傾向にあり,雌では200 mg/kg群にのみ1例の発現が認められた.しかしながら,この変化はラットの肝臓に自然発生病変として一般的に認められる変化で,対照群の発現率との間に統計学的有意差が認められないことから,被験物質の投与による変化ではないと判断された.したがって,四臭化エタンの肝臓に対する影響は,主にアルブミンの増加を伴った肝細胞の肥大で,酵素誘導を惹起する物質の投与により発現する機能亢進性の変化1)と同質のものと考えられた.四臭化エタンの毒性について,ラットへの106日間反復吸入投与により,肝臓重量の増加が認められたとの報告2)があるが,経口投与による本試験においても,肝臓に対する影響が確認された.
甲状腺に対する影響について,病理組織学的検査で濾胞上皮の軽度な肥大が雌雄の60 mg/kg以上の群で認められ,200 mg/kg群の雌雄の甲状腺重量は増加傾向を示した.化学物質の投与による濾胞上皮の肥大はほとんどが循環血中の甲状腺ホルモンの低下によるnegative-feedback機構が関与した,持続性の濾胞上皮の刺激が原因となり,その作用機序として肝臓での甲状腺ホルモンの代謝・分解の亢進が報告3, 4)されている.したがって,本物質による甲状腺の変化は,肝臓に対する影響と関連した変化である可能性も考えられる.
腎臓に対する影響について,200 mg/kg群の雌雄で腎臓相対重量の増加が認められ,雌では絶対重量も高値を示した.しかしながら,腎臓の病理組織学的変化は認められず,また,腎機能と関連した血液生化学的変化も認められなかった.したがって,本物質の腎臓に対する影響は軽度なものと考えられる.
電解質に対する影響について,塩素の減少が20と60 mg/kg群の雄および200 mg/kg群の雌雄,カリウムの減少が60 mg/kg群の雄および200 mg/kg群の雌雄,ならびにカルシウムの増加が60 mg/kg群の雌および200 mg/kg群の雌雄に認められ,塩素の変化は顕著なものであった.臭素化合物を投与した動物の塩素について,これを一般的なイオン電極法で測定すると,生体内で解離した臭素イオンが加算されて測定されるため塩素は高値を示すことが多く5, 6),本物質についてもイオン電極法を用いて測定した14日間の投与量設定試験の結果では塩素は用量相関的に高値を示し,被験物質に由来する臭素イオンの存在が示唆された.一方,本試験では,特異性の高いイオンクロマトグラフ法で測定した結果,塩素の低値が認められた.腎臓の尿細管における物質の再吸収において,塩素イオンと臭素イオンは競合し,血中に臭素イオンが増加すると塩素イオンの排泄が促進され,塩素イオンは減少することが知られている7).したがって,塩素の低値は,被験物質の腎臓に対する毒性影響と関連した変化ではないと判断された.
血液に対する影響について,200 mg/kg群で雌に血小板数の減少が認められた.しかしながら,骨髄および脾臓の造血細胞に病理組織学的変化が認められなかった.
回復群においては,被験物質の投与と関連した変化のうち,肝臓における重量変化および病理組織学的変化ならびに肝機能と関連すると思われるアルブミンの変化は雌雄に,総コレステロールの変化は雌に残存していたが,変化の程度は軽減し,回復傾向が認められた.雌で甲状腺の相対重量の増加が認められたが,関連する病理組織学的変化は認められなかった.
以上の結果から,四臭化エタンのラットへの28日間反復投与による主な毒性として,肝臓,甲状腺,腎臓,電解質,血液に対する影響が認められた.無影響量は雌雄とも6 mg/kg/dayと推定された.
| 1) | T. Wakabayashi, et al., Exp. Mol. Pathol., 31, 387(1979). |
| 2) | R. L. Hollingsworth, et al., Am. Ind. Hyg. Assoc. J., 24, 28(1963). |
| 3) | C. C. Capen, et al., Toxicol. Pathol., 17, 266(1989). |
| 4) | P. F. Smith, et al., Toxicol. Pathol., 19, 197(1991). |
| 5) | Y. Ito, et al., Tox. Test. Rep. Envilon. Chem., 2, 357(1995). |
| 6) | H. Hiratuka et al., Tox. Test. Rep. Envilon. Chem., 4, 81(1996). |
| 7) | 上條一也,大森義仁,高木敬次郎,藤原元始,吉利和監訳,"Goodman Gilman薬理書(上)薬物治療の基礎と臨床,第5版,"廣川書店,東京,1980, p.151. |
| 連絡先 | |||
| 試験責任者: | 伊藤義彦 | ||
| 試験担当者: | 野田 篤,山口真樹子,伊藤雅也,赤木 博 | ||
| (財)畜産生物科学安全研究所 | |||
| 〒229-1132 神奈川県相模原市橋本台3-7-11 | |||
| Tel 042-762-2775 | Fax 042-762-7979 | ||
| Correspondence | ||||
| Authors: | Yoshihiko Ito(Study director) Atushi Noda, Makiko Yamaguchi, Masaya Ito, Hiroshi Akagi | |||
| Research Institute for Animal Science in Biochemistry and Toxicology | ||||
| 3-7-11 Hashimotodai, Sagamihara-shi, Kanagawa, 229-1132, Japan | ||||
| Tel +81-042-762-2775 | Fax +81-042-762-7979 | |||