以上の結果から,本試験条件下では,1,1,2-トリクロロエタンはマウスの骨髄細胞において染色体異常誘発作用あるいは紡錘体形成阻害作用を示さないが,骨髄細胞に対する増殖抑制作用を示すと考えられる.
媒体は,被験物質が水に不溶のため,オリブ油を選択した.投与検体は,投与前日に被験物質を秤量し,日局オリブ油(製造番号:1110,丸石製薬(株))に溶解して調製し,室温,遮光条件で気密容器に保管した後,投与に用いた.6および0.2 %の調製検体については,室温,遮光条件下で2日間の安定性が確認された.なお,各濃度の投与検体について被験物質の含量を測定した結果,平均含量が調製指示値の90.0〜110 %の範囲内にあることが確認された.
動物は,全飼育期間を通じて,許容温度:21.0〜25.0 ℃,許容湿度:40.0〜75.0 %,換気回数:約15回/時間,照明12時間(7時〜19時)に設定された飼育室内で,床敷として木製チップ(ホワイトフレーク,日本チャールス・リバー(株))を入れたTPX樹脂製ケージに1匹ずつ収容し,固型飼料(CE-2,日本クレア(株))と水道水(秦野市水道局給水)を自由摂取させて飼育した.
陰性対照群と陽性対照群の小核出現頻度が,背景データのばらつきの範囲内(平均値 ± 3 × 標準偏差)にあるか否かを調べた.
小核出現頻度については,陰性対照群と被験物質投与群の間および陰性対照群と陽性対照群の間で,Fisherの正確確率検定法5)(片側検定)により有意差検定を行った.なお,検定にあたっては,多重性を考慮してBonferroniの補正6)を行った.また,小核出現頻度の用量(対数値)依存性について,Cochran-Armitageの傾向検定7)(片側検定)を行った.
(赤血球中に占める幼若赤血球の比率)
骨髄細胞の増殖抑制の指標としての幼若赤血球の比率について,まずBartlett検定5)により陽性対照群を除く各群の分散の一様性の検定を行った.その結果,いずれも等分散であったことからDunnett検定8)を用いて陰性対照群と各被験物質投与群との平均値の差の検定を行った.陰性対照群と陽性対照群との比較については,F検定5)により分散の一様性の検定を行い,等分散であったことからStudentのt検定5)を行った.
(判定)
被験物質が骨髄細胞において,染色体異常誘発作用または紡錘体形成阻害作用を示すか否かの判定は,統計解析の結果をもとに,用量反応性および陰性対照の背景データ,骨髄細胞増殖への影響等を参考にして総合的に行った.
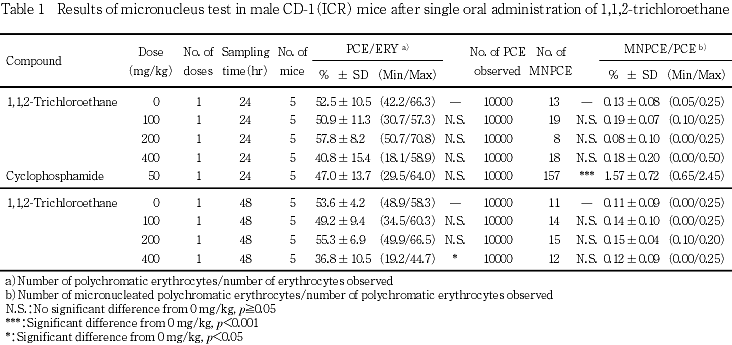
小核出現頻度および赤血球中に占める幼若赤血球の比率をTable 1に示した.陰性対照群および陽性対照群の小核出現頻度は,いずれも背景データのばらつきの範囲内であったことから,本試験系の有効性が確認された.被験物質投与群の小核出現頻度は,いずれの標本作製時期においても陰性対照群との間に有意差は認められず,用量に依存して増加する傾向も認められなかった.一方,CPAを投与した陽性対照群では,0.1 %水準で有意な小核出現頻度の増加が確認された.
赤血球中に占める幼若赤血球の比率は,いずれの標本作製時期においても400 mg/kg投与群で低下し,投与後48時間に標本を作製した400 mg/kg投与群では有意差が認められた.200 mg/kg以下の被験物質投与群および陽性対照群においては,陰性対照群との間に有意差は認められなかった.

以上の結果から,本試験条件下では,1,1,2-トリクロロエタンはマウスの骨髄細胞において染色体異常誘発作用あるいは紡錘体形成阻害作用を示さないが,400 mg/kgの用量で骨髄細胞に対する増殖抑制作用を示すと考えられた.
| 1) | K. L. White, et al., Drug. Chem. Toxicol., 8, 333(1985). |
| 2) | W. Schmid, Mutat. Res., 31, 9(1975). |
| 3) | W. Schmid, "Chemical Mutagens," Vol. 4, ed. by A. Hollaender, Plenum Press, N. Y. -London, 1976, pp. 76-78. |
| 4) | M. Hayashi, T. Sofuni, M. Jr. Ishidate, Mutat. Res., 120, 241(1983). |
| 5) | G. W. Snedecor, W. G. Cochran, "Statistical methods," 7, Iowa State University Press, 1980. |
| 6) | B. H. Margolin, M. A. Resnick, J. Y. Rimpo, P. Archer, S. M. Galloway, A. D. Bloom, E. Zeiger, Environ. Mutagen., 8, 183(1986). |
| 7) | B. H. Margolin, K. J. Risko, "Evaluation of Short-Term Tests for Carcinogens," eds. by J. Ashby, et al., Cambridge Univ. Press, 1988, pp. 1.29-1.42. |
| 8) | C. W. Dunnet, J. Am. Statist. Assoc., 50, 1096(1955). |
| 9) | J. Ashby, R. W. Tennant, Mutat. Res., 257, 229(1991). |
| 10) | J. C. Mirsalis, et al., Environ. Mol. Mutagen., 14, 155(1989). |
| 11) | M. Tafazoli, M. Kirsch-Volders, Mutat. Res., 371, 185(1996). |
| 12) | E. Gocke, M. -T. King, K. Eckhardt, D. Wild, Mutat. Res., 90, 91(1981). |
| 連絡先 | |||
| 試験責任者: | 原 巧 | ||
| 試験担当者: | 太田 亮,松本浩孝,関 剛幸,堀内伸二,稲田浩子,三枝克彦,安生孝子 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Takumi Hara(Study director) Ryo Ohta, Hirotaka Matsumoto, Takayuki Seki, Shinji Horiuchi, Hiroko Inada, Katsuhiko Saegusa, Takako Anjo | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||