被験物質を注射用水に溶解して,0,1,3,10および30 mg/kgに相当する量を毎日1回,4週間反復経口投与し,一般状態の観察,体重測定,摂餌量測定,血液学検査,血液凝固能検査,血液生化学検査,尿検査,器官重量測定および病理学検査を行った.なお,回復期間は2週間とし,投与終了時と同様の検査を実施した.
投与期間および回復期間を通して対照群および各投与群で死亡例は認められなかった.
一般状態観察では,30 mg/kg群の雌雄で削痩,立毛および流涎,雌で鼻端の汚れがそれぞれ観察された.回復期間では一般状態に変化は観察されなかった.
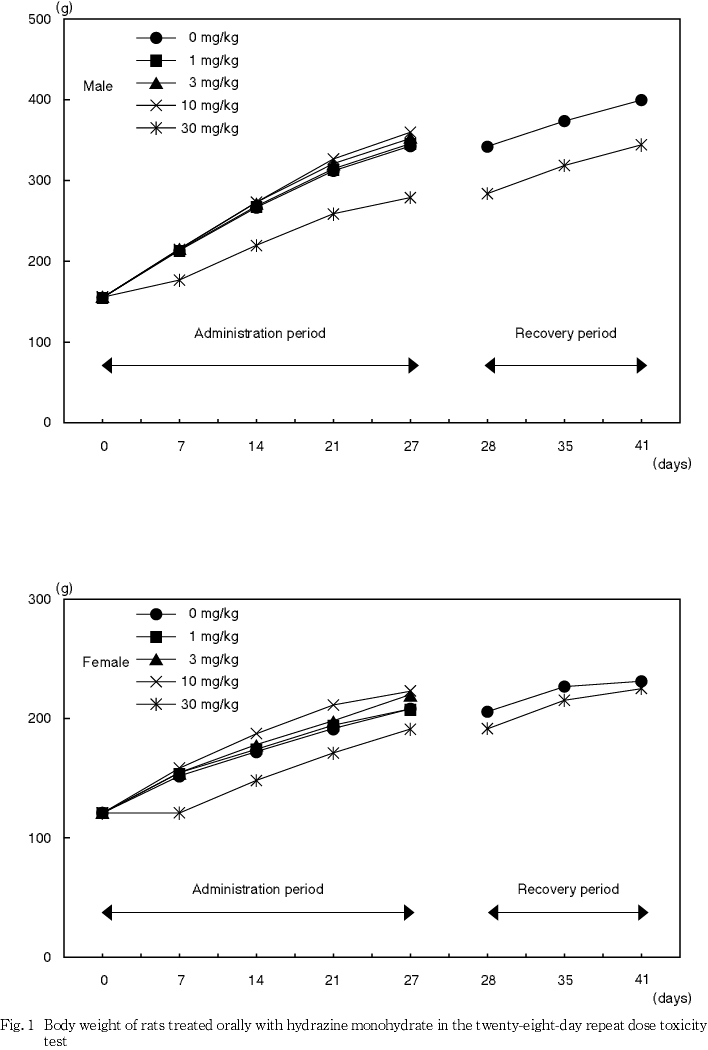
体重は,30 mg/kg群の雌雄で低値を示し,体重増加量も減少してこの群での体重増加抑制が認められた.なお,休薬により体重の回復が認められた.
摂餌量は,30 mg/kg群の雌雄で投与7日に低値を示した.しかし,投与14日以降は差がみられなかった.30 mg/kg群の雄では飼料効率も低下し,この群での体重増加抑制が原因と考えられた.30 mg/kg群の雌では投与7日に著しい飼料効率の低下が認められたが,その後は回復した.
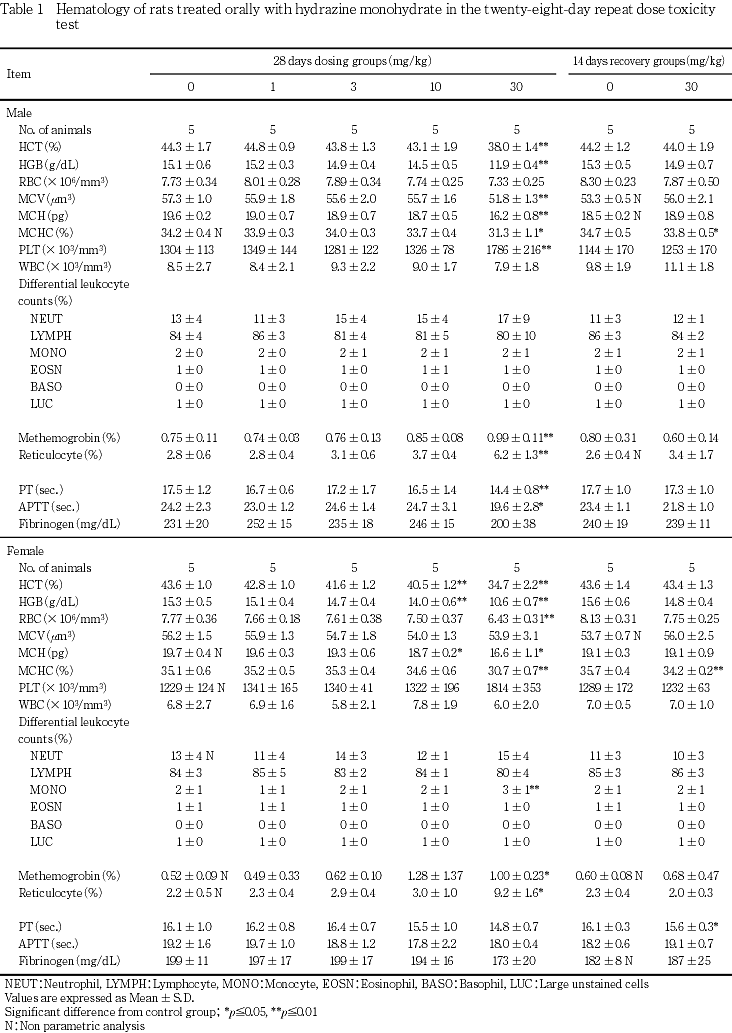
血液学検査では,30 mg/kg群の雌雄でヘマトクリット値,ヘモグロビン量,MCHおよびMCHCが低値および網赤血球比率が高値,30 mg/kg群の雄ではMCVが低値,30 mg/kg群の雌では赤血球数が低値,さらに10 mg/kg群の雌ではヘマトクリット値,ヘモグロビン量およびMCHが低値を示した.30 mg/kg群の雌雄および10 mg/kg群の雌では,メトヘモグロビン比率が高値および高値傾向を示した.
血液生化学検査では,30 mg/kg群の雌雄で総ビリルビン濃度,A/G比および無機リン濃度が高値,血糖値および塩素濃度が低値を示し,さらに,30 mg/kg群の雄で尿素窒素およびアルブミンの濃度が高値,30 mg/kg群の雌でカルシウム濃度が高値を示した.
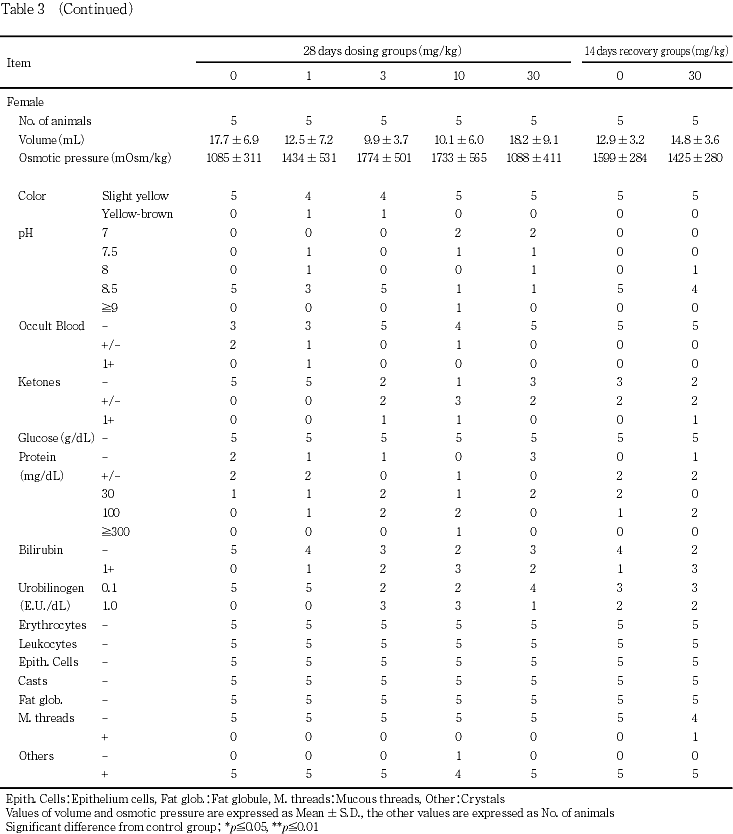
尿検査の結果,各投与群において変化が認められなかった.
器官重量では,10および30 mg/kg群の雌雄で腎臓および肝臓の絶対重量または相対重量が高値あるいは高値傾向を示した.30 mg/kg群の雌雄では脾臓の絶対重量または相対重量が高値を示した.
解剖所見として,30 mg/kg群の雌雄で肝臓の淡色化が観察された.病理組織所見として,肝臓の小葉辺縁性の肝細胞の脂肪化が10および30 mg/kg群の雄で,対照群,1,3,10および30 mg/kg群の雌に観察された.なお,回復期間終了時では雌雄ともに対照群と比較して差は認められなかった.脾臓では色素沈着が30 mg/kg群の雌雄で,髄外造血が30 mg/kg群の雌雄および10 mg/kg群の雄に観察され,溶血性貧血に対する反応と考えられた.回復期間終了時では,脾臓の色素沈着が30 mg/kg群の雌雄で全例に観察され,溶血性貧血に伴う二次的変化と考えられた.
以上のように,10 mg/kg群の雄で腎臓絶対重量の高値傾向,肝臓および腎臓相対重量の高値あるいは高値傾向があり,雌ではヘマトクリット値,ヘモグロビン量およびMCHの低値,肝臓および腎臓の絶対重量の高値と相対重量の高値あるいは高値傾向が認められたことから本試験条件下におけるヒドラジン一水和物のラットに対する無影響量は,雌雄とも3 mg/kg/dayと判断された.
投与液は,被験物質を注射用水((株)大塚製薬工場)に溶解して0.1,0.3,1.0および3.0 mg/mLの濃度となるように調製した.なお,注射用水中のヒドラジン一水和物は冷蔵保存条件下で7日間安定であることから,投与液の調製は毎週1回実施し,1日分ずつ小分けして投与まで冷蔵庫に保管した.全ての試験群の投与液について適切に調製されていることを確認するため,初回および最終調製時の各投与液の一部を分取し,被験物質濃度分析を行った.初回調製時は設定濃度の91.8〜97.5 %および最終調製時は93.2〜100.3 %であり,適切に調製されていることが確認された.
動物は,温度21.4〜25.9 ℃,湿度51〜75 %,換気回数1時間20回,照明12時間(午前7時点灯,午後7時消灯)に設定されたバリアシステム飼育室で飼育した.アルミ製前面・床ステンレス網目飼育ケージに動物を1匹ずつ収容し,オリエンタル酵母工業(株)製造の放射線滅菌したラット,マウス飼料CRF-1(Lot No. 010406)および水道水を自由に摂取させた.飼育ケージは隔週1回,給餌器は週1回取り換えた.
投与液量は体重100 g当たり1.0 mLとし,個体別に測定した体重に基づいて投与液量を算出し,1日1回胃ゾンデを用いて強制経口投与した.対照群には注射用水のみを同様に投与した.なお,回復期間は14日間とした.
採取した血液の一部にEDTA-2Kを添加し,白血球数(WBC:フローサイトメトリー),赤血球数(RBC:暗視野板法),ヘモグロビン量(HGB:シアンメトヘモグロビン法),ヘマトクリット値(HCT:RBC,MCVより算出),平均赤血球容積(MCV:暗視野板法),平均赤血球血色素量(MCH:HGB,RBCより算出),平均赤血球血色素濃度(MCHC:HGB,HCTより算出),血小板数(PLT:暗視野板法),白血球百分率(フローサイトメトリー)および網赤血球率(Reticulocyte:RNA染色法)を総合血液学検査装置ADVIA120(バイエル社)を用いて測定した.また,上述の血液を用いてメトヘモグロビン比率(Methemoglobin:松原法)を測定した.さらに,3.13 %クエン酸ナトリウム水溶液添加血液の血漿を用いて,プロトロンビン時間(PT:Quick1段法),活性化部分トロンボプラスチン時間(APTT:クロット法)およびフィブリノーゲン量(Fibrinogen:トロンビン時間法)を血液凝固自動測定装置KC-40(独国Amelung社)により測定した.
器官重量は脳,心臓,肝臓,腎臓,副腎,胸腺,脾臓,精巣,精巣上体および卵巣について測定した.器官重量/体重比(相対重量)は投与27日または回復13日の測定体重および器官重量から算出した.また,リンパ節(腸間膜,下顎),骨髄(大腿骨),胸腺,気管,肺(気管支を含む),心臓,甲状腺,上皮小体,胃,十二指腸,空腸,回腸(パイエル氏板を含む),盲腸,結腸,直腸,肝臓,脾臓,膵臓,腎臓,副腎,膀胱,精嚢,前立腺,精巣,精巣上体,卵巣,子宮,腟,眼球,脳,下垂体,脊髄(頸部,胸部,腰部),骨格筋(大腿部)および坐骨神経を10 %中性緩衝ホルマリン液で固定した.なお,精巣および精巣上体はホルマリン酢酸液(FA液)で前固定した後,10 %中性緩衝ホルマリン液で固定した.病理組織学検査は対照群および最高用量群の上記器官および組織について実施した.また,最高用量群の肝臓および脾臓で被験物質の影響と考えられる変化が認められたため,他の用量群および回復群についても実施した.組織標本の作製は,常法に従ってパラフィン包埋,薄切後,ヘマトキシリン・エオジン染色を施した.鏡検では,病変の種類および程度を含む各所見について記録した.

雄では,対照群に比較して30 mg/kg群でヘマトク リット値,ヘモグロビン量,MCV,MCHおよびMCHCが低値,血小板数,メトヘモグロビン比率および網赤血球比率が高値を示した.雌では,対照群に比較して10および30 mg/kg群でヘマトクリット値,ヘモグロビン量,MCHが低値,30 mg/kg群で赤血球数およびMCHCが低値を示した.また,30 mg/kg群で単球比率,メトヘモグロビン比率および網赤血球比率が高値を示した.血液凝固能検査では,対照群に比較して30 mg/kg群の雄でPTおよびAPTTが短縮を示した.
[回復期間終了時]
対照群に比較して30 mg/kg群の雌雄でMCHCが低値を示したが軽微な変化であった.血液凝固能検査では,対照群に比較して30 mg/kg群の雌でPTが短縮を示した.
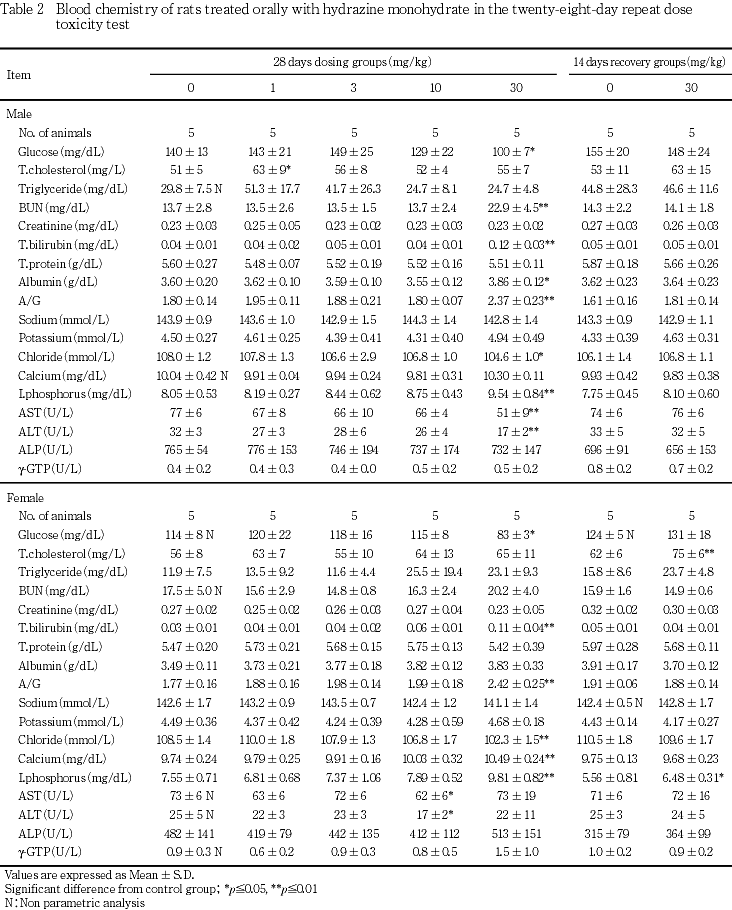
対照群に比較して30 mg/kg群の雌雄で総ビリルビン濃度,A/G比および無機リン濃度が高値,血糖値および塩素濃度が低値を示した.30 mg/kg群の雄で尿素窒素およびアルブミンの濃度が高値,ASTおよびALTの活性が低値を示した.30 mg/kg群の雌でカルシウム濃度が高値を示した.その他,1 mg/kg群の雄で総コレステロール濃度が高値,10 mg/kg群の雌でASTおよびALTの活性が低値を示したが用量に依存した変化ではなかった.
[回復期間終了時]
対照群に比較して30 mg/kg群の雌で無機リンおよび総コレステロールの濃度が高値を示した.
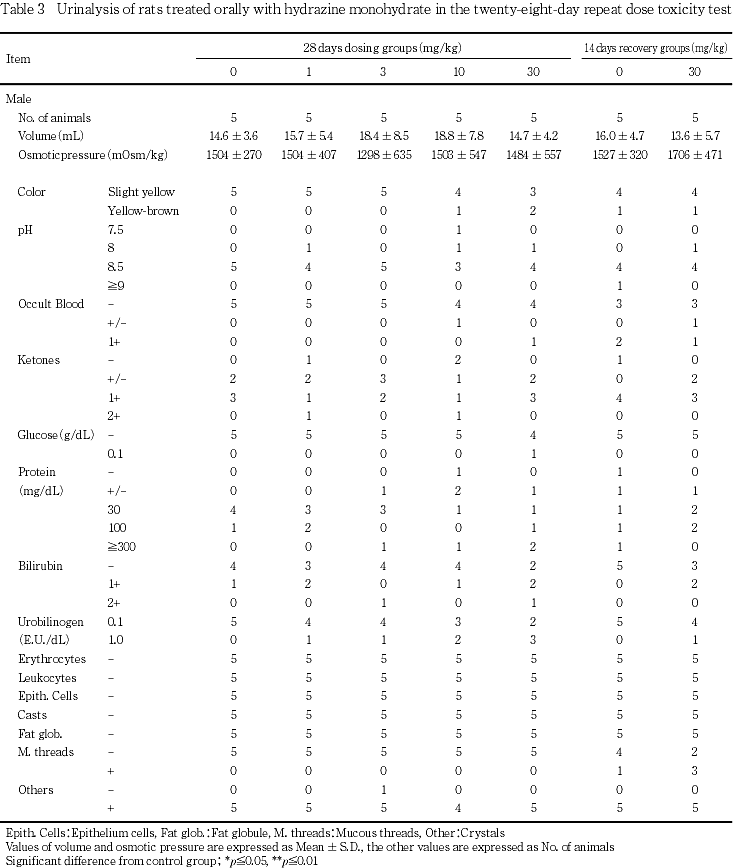
対照群に比較して各投与群の雌雄において検査したいずれの項目においても変化が認められなかった.
[回復期間終了時]
対照群に比較して30 mg/kg群の雌雄において検査したいずれの項目においても変化が認められなかった.
対照群に比較して10および30 mg/kg群の雌雄で腎臓絶対重量が高値あるいは高値傾向を示した.10および30 mg/kg群の雌では肝臓絶対重量が,30 mg/kg群の雌では脾臓絶対重量が高値を示した.その他,30 mg/kg群の雄で脳および精巣上体の絶対重量が低値を示した.
器官重量/体重比では,対照群に比較して10および30 mg/kg群の雌雄で肝臓および腎臓の相対重量が高値あるいは高値傾向を示した.30 mg/kg群の雌雄で脾臓相対重量が高値を示した.また,30 mg/kg群の雄で脳相対重量および雌で心臓相対重量が高値を示した.
[回復期間終了時]
対照群に比較して30 mg/kg群の雄で脳および心臓の絶対重量が低値を示した.
器官重量/体重比では対照群に比較して30 mg/kg群の雄で胸腺相対重量,雌で肝臓および腎臓の相対重量が高値を示した.

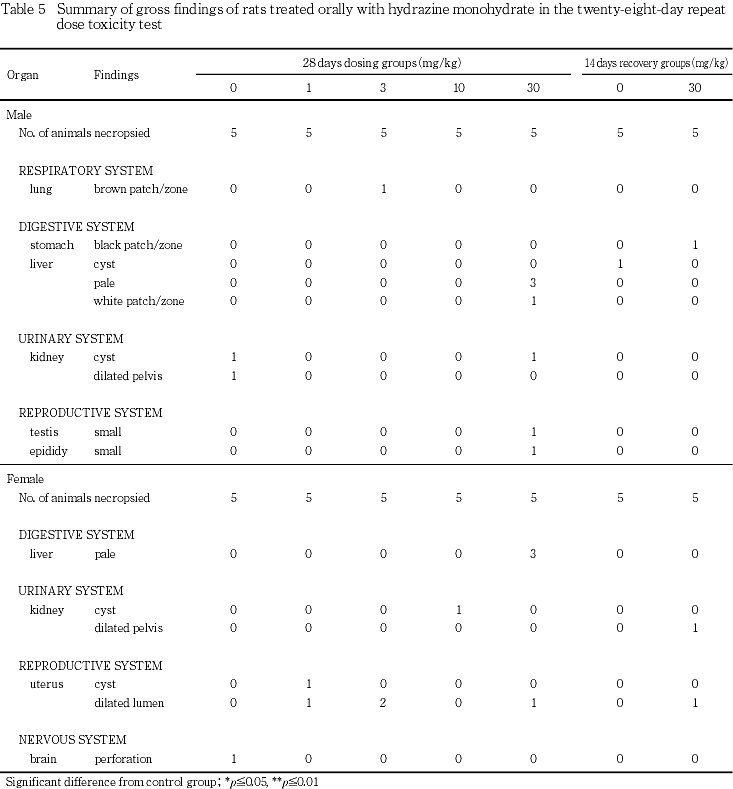
30 mg/kg群に認められた所見として肝臓の淡色化が雌雄の各3例に観察された.その他,肺の褐色斑/区域,肝臓の白色斑/区域,腎臓の嚢胞,子宮の嚢胞および内腔拡張,精巣および精巣上体の小型化がそれぞれ単発性,散発性もしくは用量に依存しない発生を示した.
[回復期間終了時]
胃の黒色斑/区域,腎臓の腎盂拡張および子宮の内腔拡張がそれぞれ単発性に発生した.
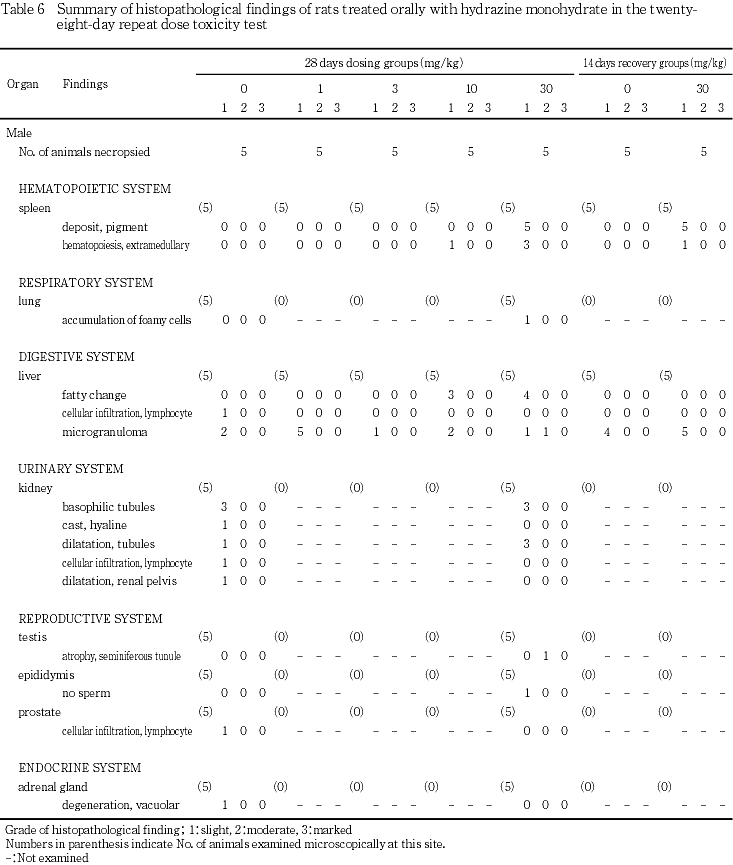
対照群に比較して投与群において有意に増加した所見として,肝臓の肝細胞の脂肪化が10および30 mg/kg群の雄でそれぞれ3および4例に認められた.雌では対照群,1,3,10および30 mg/kg群でそれぞれ4,4,3,4および5例に観察された.これらの脂肪化は主に小葉辺縁性に認められた.脾臓の色素沈着が30 mg/kg群の雌雄でそれぞれ5および4例に観察された.さらに,髄外造血が10および30 mg/kg群の雄で1および3例,30 mg/kg群の雌で4例に観察された.
その他,肺の泡沫細胞集簇,肝臓の小肉芽腫,腎臓の尿細管好塩基化および尿細管拡張,精巣の中等度精細管萎縮および精巣上体の無精子,子宮の内腔拡張および甲状腺の鰓後体遺残が単発性あるいは対照群にも認められた.
[回復期間終了時]
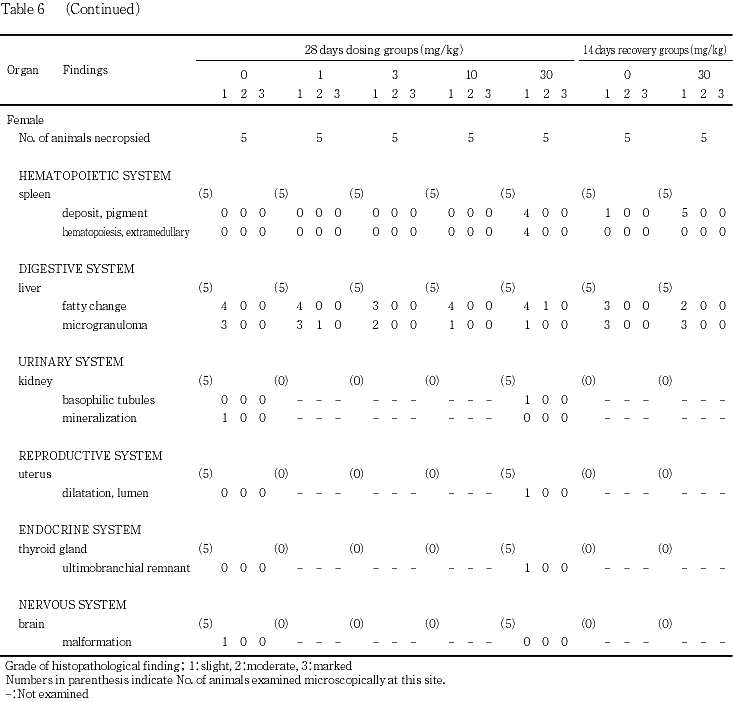
脾臓の色素沈着が対照群の雌の1例および30 mg/kg群の雌雄の全例に観察され,雌雄とも有意な発生数の増加が認められた.
また,肝臓の脂肪化が対照群および30 mg/kg群の雌でそれぞれ3および2例に観察された.その他,肝臓の小肉芽腫が雌雄とも対照群と同様に認められた.
投与期間および回復期間を通して対照群および各投与群で死亡例は認められなかった.一般状態の観察では,30 mg/kg群の雌雄で削痩,立毛および流涎,雌で鼻端の汚れがそれぞれ認められた.なお,これらの所見は回復期間で消失した.
体重は30 mg/kg群の雌雄で低値を示し,体重増加量も減少し,この群での体重増加抑制が認められた.なお,休薬により体重の回復が認められた.
摂餌量は30 mg/kg群の雌雄で投与7日に低値を示したが投与14日以降は差がなかった.飼料効率は30 mg/kg群の雌雄で低値を示し,特に雌では投与7日に著しい低値を示した.いずれもこの群での体重増加抑制に起因するものと考えられた.なお,休薬により30 mg/kg群の雌雄で回復が認められた.
血液学検査では,30 mg/kg群の雌雄でヘマトクリット値,ヘモグロビン量,MCHおよびMCHCが低値,網赤血球比率が高値を示し,30 mg/kg群の雄ではMCVが低値,雌では赤血球数が低値を示した.さらに,10 mg/kg群の雌ではヘマトクリット値,ヘモグロビン量およびMCHが低値を示した.これに伴って30 mg/kg群では総ビリルビン濃度の高値があり,後述のごとく脾臓の髄外造血亢進および脾臓の色素沈着が認められたことから,本試験で認められた貧血は溶血性貧血であると判断された.なお,回復期間終了時に貧血は回復傾向を示した.さらに30 mg/kg群の雌雄および10 mg/kg群の雌では,メトヘモグロビン比率が高値および高値傾向を示したが,ヒドラジンを投与したラットにおいてメトヘモグロビン血症の発現することがすでに報告されている4).
血液凝固能検査では,30 mg/kg群の雄でPTおよびAPTTが短縮を示し,回復期間終了時では30 mg/kg群の雌でPTが短縮を示した.いずれも短縮方向への変化であり毒性学的意義のない変化と考えられた.
血液生化学検査では,30 mg/kg群の雌雄で総ビリルビン濃度,A/G比および無機リン濃度が高値,血糖値および塩素濃度が低値,雄で尿素窒素およびアルブミンの濃度が高値を示し,いずれも被験物質の影響と考えられた.また,30 mg/kg群の雌でカルシウム濃度が高値を示した.その他,30 mg/kg群の雄でASTおよびALTの活性が低値を示したがいずれも減少方向の変化であり毒性学的意義のない変化と考えられた.回復期間終了時では30 mg/kg群の雌で無機リン濃度が高値を示したが,軽微な変化であった.また,総コレステロール濃度が高値を示したが,投与終了時においては認められなかった変化であった.
尿検査では各投与群において変化が認められなかった.
器官重量では,10および30 mg/kg群の雌雄で腎臓の絶対重量および相対重量が高値および高値傾向を示した.また,10および30 mg/kg群の雌で肝臓絶対重量が高値,10および30 mg/kg群の雌雄で肝臓相対重量が高値を示した.組織所見における小葉辺縁性の肝細胞の脂肪化の発生数とも相関しており被験物質の影響と考えられた.30 mg/kg群の雌で脾臓絶対重量が高値,30 mg/kg群の雌雄では脾臓相対重量が高値を示し,組織所見における脾臓の髄外造血の発生数と相関しており被験物質の影響と考えられた.その他,30 mg/kg群の雄で脳および精巣上体の絶対重量が低値を示し,30 mg/kg群の雌雄で脳および心臓の相対重量が高値あるいは高値傾向を示したが,いずれもこの群の体重増加抑制に伴う二次的変化と考えられた.回復期間終了時,30 mg/kg群の雌で肝臓および腎臓の相対重量が高値を示した.そこで脳重量比を算出して比較した結果,肝臓(対照群:327.54 %,30 mg/kg群:362.86 %)および腎臓(対照群:90.29 %,30 mg/kg群:96.90 %)とも大差は認められなかった.30 mg/kg群の雄で脳および心臓の絶対重量が低値,胸腺相対重量が高値を示したが,いずれもこの群の体重の低値に起因すると考えられた.
病理組織所見として,肝臓の淡色化に相当する組織所見の肝細胞の脂肪化が10および30 mg/kg群の雄で増加し,被験物質投与との関連が示唆された.しかし,回復期間終了時で認められず回復性を有すると考えられた.一方,雌では投与終了時および回復期間終了時のいずれにおいても対照群を含む各群にほぼ同様に認められた.雌雄の脾臓に観察された髄外造血は溶血性貧血に対する反応性変化と考えられた.髄外造血の発生数は回復期間終了時では1例のみであり血液学検査の結果からも貧血が回復したと考えられた.なお,脾臓の色素沈着は回復期間終了時においても雌雄の全例に観察され,溶血性貧血による二次的変化と考えられた.その他,観察された所見は単発性あるいは散発性もしくは用量に依存しない発現であることから,いずれも自然発生性病変と考えられた.
以上のように,10 mg/kg群の雄で腎臓絶対重量の高値傾向,肝臓および腎臓相対重量の高値あるいは高値傾向があり,雌ではヘマトクリット値,ヘモグロビン量およびMCHの低値,肝臓および腎臓の絶対重量の高値と相対重量の高値あるいは高値傾向が認められたことから,本試験条件下におけるヒドラジン一水和物のラットに対する無影響量は雌雄とも3 mg/kg/dayと判断された.
| 1) | 佐野正樹,岡山佳弘,医薬安全性研究会会報,32, 21(1990). |
| 2) | M. Yoshida, J. Jap. Soc. Comp. Stat., 1, 111(1988). |
| 3) | 倍味繁,稲葉太一,医薬安全性研究会会報,40, 33 (1994). |
| 4) | S. J. Moloney, R. Prough, Reviews in Biochemical Toxicology, 5, 313(1983). |
| 連絡先 | |||
| 試験責任者: | 渡 修明 | ||
| 試験担当者: | 各務 進,田代 淳,杉山 豊,木原 亨,大橋信之 | ||
| (財)食品農医薬品安全性評価センター | |||
| 〒437-1213 静岡県磐田郡福田町塩新田字荒浜582-2 | |||
| Tel 0538-58-1266 | Fax 0538-58-1393 | ||
| Correspondence | ||||
| Authors: | Nobuaki Watari(Study director), Susumu Kakamu, Jun Tashiro, Yutaka Sugiyama, Tohru Kihara, Nobuyuki Ohashi | |||
| Biosafety Research Center, Foods, Drugs and Pesticides(An-pyo Center) | ||||
| 582-2 Arahama, Shioshinden, Fukude-cho, Iwata-gun, Shizuoka, 437-1213, Japan | ||||
| Tel +81-538-58-1266 | Fax +81-538-58-1393 | |||