なお、本試験はOECDガイドライン「反復投与毒性・生殖発生毒性併合試験(1990年)」に従って実施した。また、化審法(1984年)およびOECD(1981年)のGLP基準を満足している。
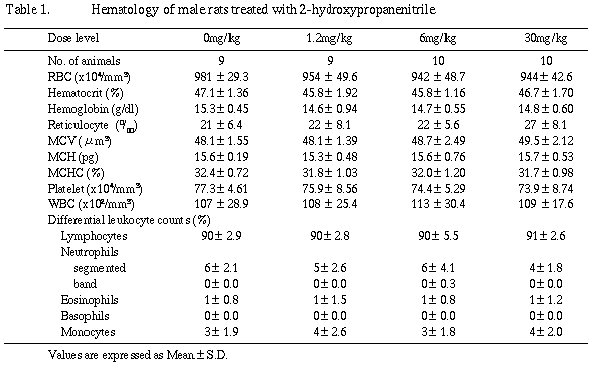
6 mg/kg以下の群では被験物質投与に起因する変化は認められなかった。
以上の結果より、本試験条件下における2−ヒドロキシプロパンニトリルの反復投与毒性に関する無影響量は雌雄とも6mg/kg、生殖・発生毒性に関する無影響量は親動物の雌雄および児動物ともに30mg/kgと考えられる。
今回、OECDによる既存化学物質の安全性点検に係わる毒性調査事業の一環として、ラットを用いて2−ヒドロキシプロパンニトリルの反復投与毒性・生殖発生毒性併合試験を実施し、生体への一般毒性学的影響および生殖・発生に及ぼす影響について検討したので報告する。
動物入荷後6日間馴化し、健康状態が良好なことを確認した後、雌雄とも8週齢で投与を開始した。
投与開始前日に動物を体重別層化無作為抽出法により群分けした後、イヤーパンチを用いて群および個体を識別した。投与開始時の体重範囲は、雄が299〜336g、雌が187〜215gであった。
実験動物用床敷(ベータチップ:日本チャールス・リバー株式会社)を敷いたポリカーボネート製ケージ(265W×426D×200Hmm)に1ケージあたり馴化・検疫期間中は2匹(同性)、交配前投与期間中は1匹、交配期間中は雌雄各1匹、哺育期間は1腹で収容し、スチール製架台上で飼育した。ステンレス製の固型飼料用給餌器およびポリカーボネート製の給水瓶(700 ml)を用いた。
ケージ(含床敷)、給餌器および給水瓶は、週1回の頻度でオートクレーブ滅菌したものと交換した。

| a) | 赤血球数 | レーザー光散乱法 |
| b) | 白血球数 | 同上 |
| c) | 血小板数 | 同上 |
| d) | ヘモグロビン濃度 | シアンメトヘモグロビン法 |
| e) | ヘマトクリット値 | ミクロヘマトクリット法 |
| f) | 白血球百分率 | ライト染色塗抹標本について測定 |
| g) | 網状赤血球数 | ニューメチレンブルー染色後ライト染色した塗抹標本について測定 |
| h) | 平均赤血球容積(MCV) | a)、e)より算出 |
| i) | 平均赤血球血色素量(MCH) | a)、d)より算出 |
| j) | 平均赤血球血色素濃度(MCHC) | d)、e)より算 |
a)〜d)は自動血液分析装置(ELT-8/ds:オルソインスツルメンツ社)、e)はヘマトクリット用遠心機(MC-201:株式会社日立製作所)、f)、g)は血液細胞自動分析装置(MICROXHEG-70A:立石電機株会社)により測定した。
| a) | GOT(AST) | UV-Rate法(SSCC改良法) |
| b) | GPT(ALT) | UV-Rate法(SSCC改良法) |
| c) | ALP | p−ニトロフェニルリン酸基質法(GSCC改良法) |
| d) | γ- GTP | γ−グルタミル・p−ニトロアニリド基質法(SSCC改良法) |
| e) | 尿素窒素 | 酵素−UV法(Urease-GLDH法) |
| f) | グルコース | 酵素−UV法(GK-G6PDH法) |
| g) | 総コレステロール | 酵素法(CES-CO-POD法) |
| h) | トリグリセライド | 酵素法(LPL-GK-G3PO-POD法) |
| i) | クレアチニン | Jaffe法 |
| j) | 総ビリルビン | Jendrassik改良法 |
| k) | 総蛋白 | Biuret法 |
| l) | アルブミン | BCG法 |
| m) | A/G 比 | k)およびl)より算出 |
| n) | カルシウム | O-CPC法 |
| o) | 無機リン | UV法 |
| p) | ナトリウム | イオン選択電極法 |
| q) | カリウム | イオン選択電極法 |
| r) | クロライド | イオン選択電極法 |
雄は投与43日、雌は哺育4日(投与40〜45日)に、全生存動物について、ペントバルビタールナトリウムの腹腔内投与による麻酔下で腹大動脈切断により放血致死させ剖検した。
(2) 器官重量
全生存動物について、剖検後に以下の器官の重量を測定した。測定には電子上皿天秤(ED-H60:株式会社島津製作所)を用いた。さらに、解剖日の体重を基に対体重比についても算出した。なお未交尾の雌のデータについては、解剖日が異なるため集計から除外した。
胸腺、肝臓、腎臓、精巣および精巣上体
(3) 病理組織学的検査
全生存動物について以下の器官を採取し、10%リン酸緩衝中性ホルマリン液(精巣および精巣上体はブアン液)にて固定後保存した。
雌雄とも対照および高用量群の器官について、常法に従いヘマトキシリン・エオジン染色標本を作製し鏡検した。この結果、雄の肝臓で被験物質の影響が認められたため低および中用量群の雄の肝臓についても検査した。この他、剖検時に異常の認められた中用量群の雄1例の肺についても検査した。一部の動物の肝臓については、PAS染色およびOil red O染色を施した。
脳、心臓、肝臓、脾臓、腎臓、副腎、精巣、精巣上体、卵巣(非妊娠動物のみ)
7日間の交配で対照群および中用量群の各1対を除き他は全例に交尾が認められたため、交尾能に被験物質の影響はないと判断し以後の交配は行わなかった。この間に交尾しなかった雌については、交配期間終了後14日(投与35日)に剖検し、卵巣を保存した。
交配結果ならびに雌の妊娠状況から次の項目を算出した。
a)交尾所要日数
b)交尾が成立するまでに逸した発情期の回数
c)交尾率(%):(交尾動物数/同居動物数)×100
d)受胎率(%):(妊娠動物数/交尾動物数)×100
哺育4日の解剖時に卵巣、子宮を摘出して黄体数および着床数を検査した。これらの検査結果から次の項目を算出した。
a)妊娠期間:妊娠0日から出産が確認された朝の前日までの期間
b)出産率(%):(生存児出産雌数/妊娠雌数)×100
c)着床率(%):(着床数/黄体数)×100
d)分娩率(%):(総出産児数/着床数)×100
哺育1日に生存児数、死亡児数、性別および外表異常の有無を検査した後、一般状態、死亡の有無を毎日観察した。哺育1および4日の生存児数から、次の項目を算出した。
a)出生率(%):(出産確認時生存児数/総出産児数)×100
b)新生児生存率(%):(哺育4日生存児数/出産確認時生存児数)×100
(2) 体重
哺育1日および4日に1腹毎に雌雄単位でまとめて測定し、それぞれの平均値を算出した。
(3) 剖検
全ての生存児について哺育4日に口腔を含む外表を検査した後、ペントバルビタールの腹腔内投与による麻酔下で開腹し、腹大動脈切断により放血致死させ剖検した。
 の方法により平均値あるいは順位の多重比較検定を行った。ただし、一部の項目については、はじめにKruskal-Wallisの検定を行い、有意差が認められた場合に順位の多重比較検定を行った(下記*印)。
の方法により平均値あるいは順位の多重比較検定を行った。ただし、一部の項目については、はじめにKruskal-Wallisの検定を行い、有意差が認められた場合に順位の多重比較検定を行った(下記*印)。
計数データについてはFisherの直接確率法により検定した。有意水準は5%以下とした。新生児に関するデータについては、各母動物毎に算出した平均値を統計単位とした。以下に検定の対象となる項目を示す。
この他に対照群の雄1例が投与23日に死亡したが、剖検の結果、肺に出血および水腫が認められたことから投与過誤によるものと判断した。

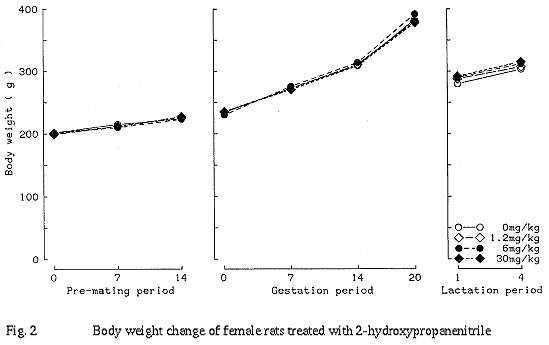

この他、偶発的な変化として、肺の小黒色斑が1.2 mg/kg群で1例、また、30 mg/kg群で片側腎臓の小のう胞が1例、片側精巣および精巣上体の萎縮が1例に認められた。
雌において、生存動物の剖検ではいずれの動物にも異常は認められなかった。30 mg/kg群の死亡動物の剖検の結果、両側性の腎臓の腫大・褪色、透明胸水の貯留、胸腺萎縮、脾臓の褪色、肺の各葉辺縁部の貧血、両側副腎の腫大および膣からの出血が認められた。
その他に、限局性の心筋変性、肺の限局性炎症性変化、肝臓の微小肉芽腫、片側腎臓の軽微な腎症と尿細管の限局性好塩基性変化、両側腎臓の尿細管における好酸性小体の形成と皮髄境界部尿細管ののう胞状拡張、片側精巣の精細管の萎縮およびこの変化に伴う片側精巣上体の萎縮が散発的に認められた。これらの変化は、本系統のラットではしばしば自然発生病変として認められものであり、しかも少数例でしかみられなかったことから、被験物質投与とは関連はないものと考えられる。
雌では被験物質に起因すると考えられる変化は認められなかったが、脾臓における造血細胞の軽度の増数と副腎束状帯のび漫性肥大が、未交尾動物を除くほぼ全例に群差なく認められた。未交尾動物では両側卵巣で排卵黄体とは異なる黄体内で黄体細胞の増生が認められた。このほか肝臓での肝細胞内グリコーゲンの増量が対照群および30mg/kg群の各1例で認められた。
30 mg/kg群の雌の死亡動物では、両側腎臓で動・静脈および糸球体毛細管内の多発性の血栓と腎全域に及ぶ壊死が認められ、これが直接の死因と考えられた。この動物には他に肝臓類洞内の繊維素血栓、両側副腎皮質の楔状壊死、肺辺縁部の貧血、心臓の心筋変性によるミネラル沈着巣、脾ろ胞の萎縮および髄外造血、胸腺の急性退縮と子宮および膣腔内の凝血塊が認められた。以上の所見からこの動物では播種性血管内凝固(DIC)が惹起されていたものと考えられた。
30 mg/kg群の交尾所要日数が有意に短かったが、各群とも交尾確認ができなかった動物を除き、全ての動物は初回の発情期に交尾が認められた。
なお、6 mg/kg群の雌1例は膣垢の検査では交尾が確認されなかったが、後の観察で妊娠が確認されたため、交尾率および受胎率はこの動物も含めて算出した。しかし、妊娠日が不明のためこの動物の交配以後のデータについては集計から除外した。



妊娠期間、黄体数、着床数、着床率および分娩率に対照群と被験物質投与群との間に有意な差はなかった。
30 mg/kg群の哺育2日に死亡した母動物に全新生児死亡が観察された他は、各群ともに哺育1日から4日までに少数例の死亡が観察されたのみであった。
出産児数、生存児数および性比、また出生率および新生児生存率ともに対照群と被験物質投与群との間に有意な差は認められなかった。
(2) 新生児の観察
分娩あるいは哺育行動に異常が認められた1.2および30 mg/kg群の各1例の母動物の新生児が未授乳のため衰弱し死亡した。その他には各群とも1〜2例に皮下出血が観察されたのみで、被験物質投与に起因すると考えられる所見は認められなかった。
外表異常として、30 mg/kg群の1例に無尾が認められたが、その他の新生児には異常は認められなかった。
(3) 体重
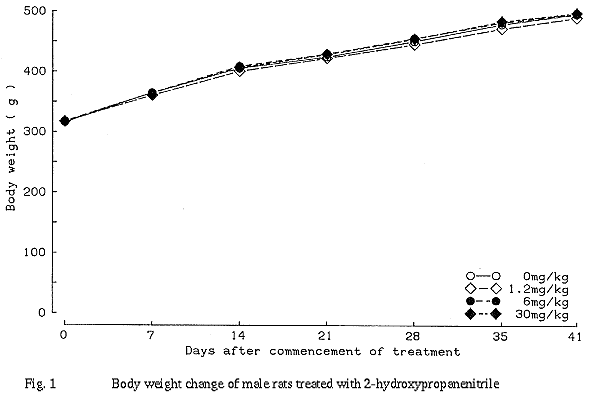
雄雌とも哺育1日および4日の体重ならびにその間の体重増加量に対照群と被験物質投与群との間に有意な差は認められなかった。
(4) 剖検
哺育4日の全生存動物の剖検の結果、胸腺頚部残留が対照群より順次3、7、8および7例、6 mg/kg群で横隔膜ヘルニアが1例、左臍動脈が2例に認められた。いずれも用量依存性がないか、または少数例の発現であることから、被験物質投与に起因するものではないと考えられる。
死亡動物の剖検では、30 mg/kg群の哺育2日に死亡した母動物の出産児にのみ胸腺頚部残留が1例、腎盂拡張が7例に認められた。

剖検および器官重量において、雄の30 mg/kg群で肝臓の腫大が認められ、病理組織学的検査の結果、小葉中心性の肝細胞肥大および脂肪化が認められた。
肝細胞肥大は種々の薬剤によって引き起こされる変化である5-7)。適応性肥大を起こした肝細胞では細胞質内小器官の量的変動がみられ、光顕的に細胞質は擦りガラス状を呈してみえる。今回認められた肝臓の変化はそれと同質の所見であり、生体の適応性変化を示唆するものであった。
一方、肝細胞の脂肪化はラットを用いた毒性試験では非特異的にしばしば認められる変化8)であるが、今回の場合肥大した肝細胞領域で形成されていたことから、肝細胞肥大と脂肪化は一連の変化であり、脂肪化は退行性の脂肪変性と考えられる。
nitrileの主な代謝部位は肝臓と考えられていることから1-4)、今回認められた肝細胞の脂肪化は、被験物質の影響が肝臓での適応範囲を越えて、細胞障害が惹起されたものと推察される。しかし、肝細胞の脂肪化は小葉中心性の肝細胞肥大を示した7例中1例で、且つ軽度に認められるのみであり、さらに雄の6 mg/kg以下の群および雌では肝細胞肥大も認められなかった。また、体重、摂餌量および血液学的検査においても異常は認められなかったことから、被験物質の毒性学的影響は軽度のものと考えられる。
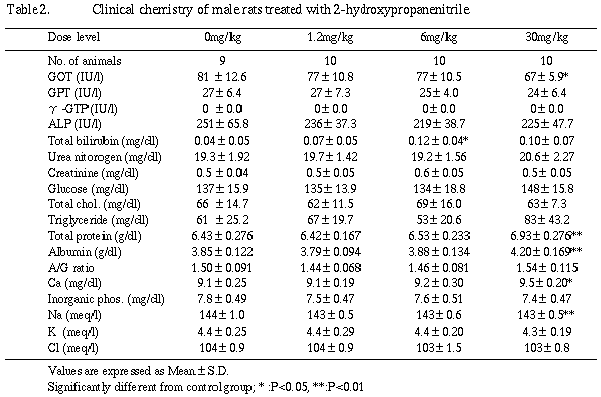
雄の臨床化学検査で30 mg/kg群で認められた総蛋白およびアルブミンの増加は生体における適応反応としての肝細胞肥大に伴った蛋白合成亢進が反映した結果と考えられる。同様にカルシウムの増加についても、アルブミン増加に伴った変化と推察される。なお、GOTの低下については、通常の肝障害でみられる変化とは逆の方向への変動であり、その毒性学的意義は不明である。
雌で多数例に認められた脾臓の増血細胞の増数は分娩時の出血に対する反応であり、副腎束状帯細胞の肥大は泌乳・哺育等に伴う内分泌性9)あるいはストレス性10)の変化と考えられる。分娩後に貧血を呈し死亡した30 mg/kgの母動物には全身に播種性血管内凝固(DIC)によると思われる変化が認められた。DICは全身諸臓器の微小循環における線維素血栓の形成と続発する組織障害をみる病態であり、様々な原因による二次性ショックによってもひきおこされる11)。臨床経過を考慮すると、この動物では分娩時の何らかのショックにより偶発的に本病態が惹起されたものと推察され、被験物質投与との関連はないと考えられる。
30 mg/kg群で交尾所要日数の短縮がみられたが、各群全例が初回の発情期に交尾しており、発情期招来のずれによる偶発的なものと考えられる。また、30 mg/kg群の死亡した母動物の全出産児死亡については、上述のDICに起因した母動物の衰弱によるもので、被験物質の分娩・哺育機能への影響とは考えられられない。
黄体数、着床数、着床率、出産率、分娩率、出産児数、生存児数の検査からも排卵、着床およびその後の胚の発育に対する被験物質の影響を示唆する変化は認められなかった。
新生児の検査において、外表、生存率、出生時体重および生後の体重増加のいずれにも異常は認められなかった。剖検で胸腺頚部残留および腎盂拡張が各群で散見されたが、これらの所見は胎生末期の胎児でしばしば自然発生的に認められる所見であり12)、発現頻度にも用量との相関はなかった。
被験物質のparent nitrileであるpropionitrileのラットの器官形成期投与では催奇形性作用がないことが報告されている13)。本試験の結果、propionitrileのα位に水酸基を付加した場合でも胚毒性および発生毒性を示唆する変化は認められなかった。
以上のように、本試験では30 mg/kg群で親動物に雌雄ともに軽度の毒性兆候が認められたが、交尾、妊娠、分娩、哺育等の生殖機能および新生児には被験物質の影響は認められなかった。したがって、本試験条件下における反復投与毒性に関する無影響量は雌雄ともに6mg/kg、生殖・発生毒性に関する無影響量は親動物の雌雄および児動物ともに30 mg/kgと考えられる。
| 1) | C.C. Willhite and R.P. Smith, Tox. Appl. Pharmacol., 59, 589 (1981). |
| 2) | P.V. Kaplita, and R.P. Smith, Tox. Appl. Pharmacol., 84, 533 (1986). |
| 3) | F.R. Johannsen, and G.J. Levinskas, Fund. Appl.Toxicol., 7, 690 (1986). |
| 4) | H. Tanii and K.Hashimoto, Arch. Toxicol., 55, 47 (1984). |
| 5) | H.W. Altmann, "Drug-induced Pathology : Drug-induced liver action : A morphological approach. II. Adaptative phenomena," (E. Grundmann, ed.), Springer-Verlag, Berlin, 1980, pp.71-76. |
| 6) | Gopinath,C., Pretice,D.E. and Lewis,D.J. "Hypertrophy (The liver), Atlas of Experimental toxicological pathology," MTP Press Limited, Lancaster, 1987, p.53 . |
| 7) | P. Greaves,"Hepatocellular hypertrophy and hyperplasia (Liver), Histopathology of Preclinical toxicity Studies," Elsevier, Amsterdam, 1990, pp.403-406 |
| 8) | 榎本眞, "毒性試験講座5, 毒性病理学," 前川昭彦, 林裕造編, 地人書館, 東京 , 1991, pp. 136-165. |
| 9) | 水野秀夫, 横山昭, "畜産大辞典 泌乳とホルモン," 養賢堂, 東京, 1978, pp.316-325 , |
| 10) | 笹野公伸,笹野伸明,"現代病理学体系 17(B)巻 副甲状腺 副腎 胃腸膵内分泌系 副腎皮質,6.変性・壊死・炎症・ストレスに伴う変化," 飯島宗一ら編, 中山書店, 東京, 1991, pp.139-154 |
| 11) | 菊地浩吉,"新病理学総論 , 6. 循環障害, H.ショック, " 相沢幹, 菊地浩吉編, 南山堂, 東京, 1987, pp.162-167. |
| 12) | H.Morita, F.Ariyuki, N. Inomata, K. Nishimura, Y. Hasegawa, M. Miyamoto and T.Watanabe, : Cong. Anom., 27, 147 (1987). |
| 13) | P.E. Berteau, J.G. Levinskas and D.E. Podwell, : Toxicologist, 2, 118 (1982). |
| 連絡先: | |||
| 試験責任者 | 松浦郁夫 | ||
| (株)三菱化成安全科学研究所鹿島研究所 | |||
| 〒314-02 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence: | |||
| Matsuura, Ikuo | |||
| Mitsubishi-Kasei Institute of Toxicological and Environmental Sciences, Japan | |||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-02, Japan | |||
| Tel 81-479-46-2871 | Fax 81-479-46-2874 | ||