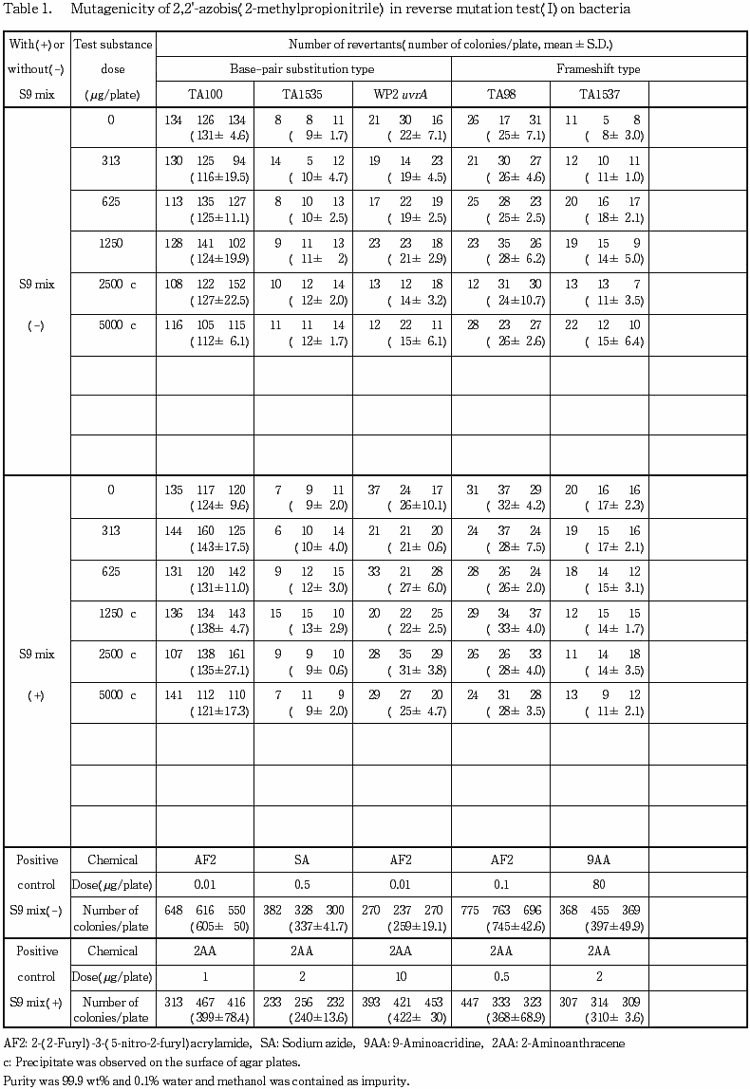
検定菌として,Salmonella typhimurium TA100,TA1535,TA98,TA1537 1)および Escherichia coli WP2 uvrA 2,3)の5菌株を用い,S9 mix 無添加および添加試験のいずれも用量設定試験において,すべての検定菌において抗菌性は認められなかったことから,本試験では S9 mix 無添加試験および添加試験を 313〜5000 μg/プレートの範囲で用量を設定して実施した.
その結果,TA1537 の S9 mix 添加試験およびその他の検定菌においては,溶媒対照値の2倍以上となる変異コロニー数の増加は認められなかった.TA1537の S9 mix 無添加試験では,2回の本試験でともに変異コロニー数が溶媒対照値の2倍以上となる用量が認められたが,変異コロニー数の偶発的な増加の可能性が考えられたため,等差により 225〜625 μg/プレートの範囲で再現性試験を実施したが,溶媒対照値の2倍以上となる変異コロニー数の増加は認められなかった.
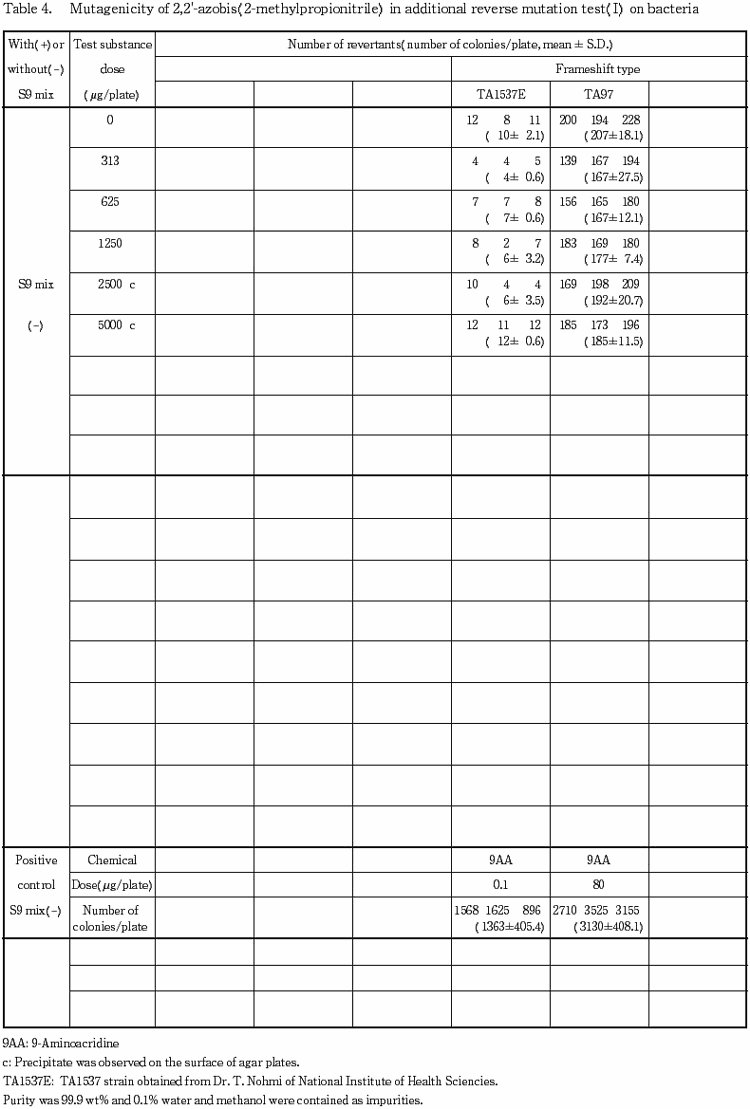
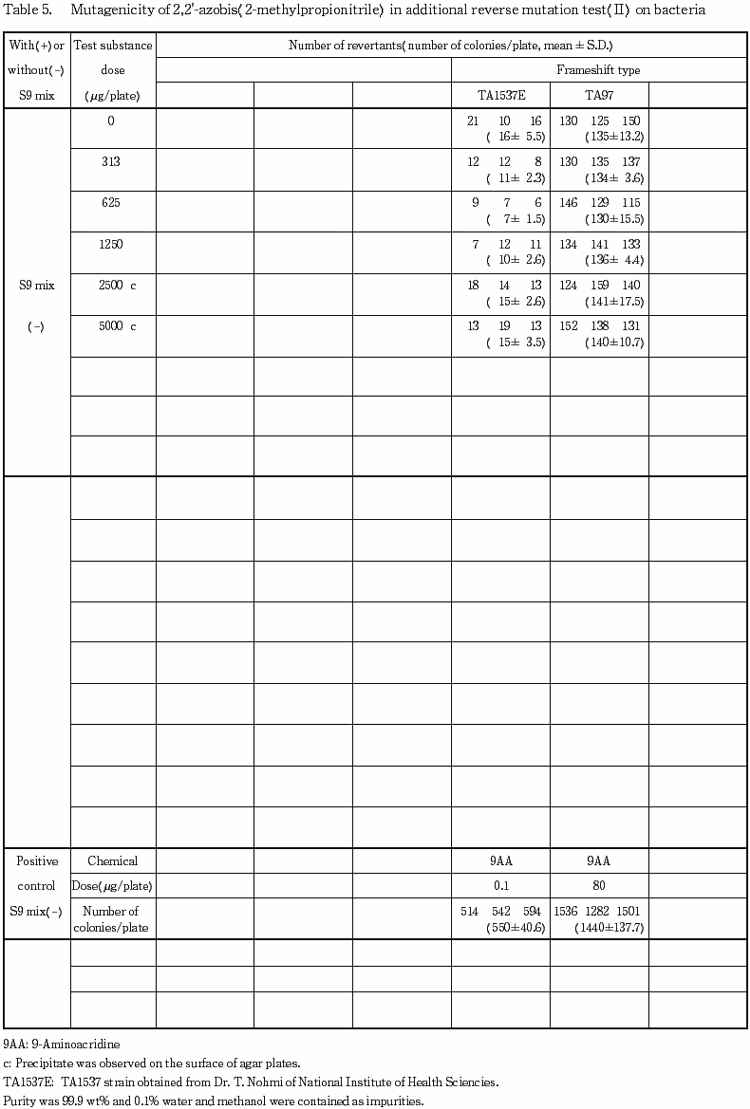
TA1537 の S9 mix 無添加試験では,明確な結論が得られなかったため, TA1537 および TA97 を国立衛生試験所から分与を受けて,313〜5000 μg/プレートの範囲で用量を設定して2回の追加試験を行った.その結果,いずれの検定菌においても溶媒対照値の2倍以上となる変異コロニー数の増加は認められなかった.これらのことから,TA1537 のS9 mix 無添加試験においては変異原性が認められないものと考えられる.
以上の結果から,2,2'-アゾビス(2-メチルプロピオニトリル)は,用いた試験系において変異原性を有しない(陰性)と判定された.
S. typhimurium の4菌株は1975年10月31日にアメリカ合衆国,カリフォルニア大学のB.N. Ames 博士から分与を受けた.
E. coli WP2 uvrA 株は1979年5月9日に国立遺伝学研究所の賀田恒夫博士から分与を受けた.
ただし,TA1537 の S9 mix 無添加試験では,明確な結論が得られなかったため,TA1537(以下 TA1537E)および TA1537 と検出し得る変異原物質が類似している S. typhimurium の TA97 を,1996年9月25日に国立衛生試験所の能美健彦博士から分与を受けて追加試験を行った.
検定菌は-80℃以下で凍結保存したものを用い,各菌株の特性確認は,凍結保存菌の調製時に,アミノ酸要求性,UV感受性,および膜変異(rfa)とアンピシリン耐性因子 pKM 101(プラスミド)の有無について調べ,特性が維持されていることを確認した.試験に際して,ニュートリエントブロスNo. 2(Oxoid)を入れたL字型試験管に解凍した種菌を一定量接種し,37℃で10時間〜12時間10分往復振とう培養したものを検定菌液とした.
2,2'-アゾビス(2-メチルプロピオニトリル)は,ジメチルスルホキシド(DMSO,ロット番号:ESK4546,和光純薬工業(株))に溶解して最高濃度の調製液を調製した後,同溶媒で公比約3ないし2で希釈し,速やかに試験に用いた.ただし,再現性試験においては,等差になるように希釈を行った.
| AF2 | : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド(上野製薬(株)) |
| SA | : | アジ化ナトリウム(和光純薬工業(株)) |
| 9AA | : | 9-アミノアクリジン(Sigma Chem. Co.) |
| 2AA | : | 2-アミノアントラセン(和光純薬工業(株)) |
下記の水溶液(A)および(B)を容量比 10:1 の割合で混合した.
| (A) | バクトアガー(Difco) | 0.6 % |
| 塩化ナトリウム | 0.5 % | |
| (B)* | L-ヒスチジン | 0.5 mM |
| D-ビオチン | 0.5 mM |
| *: | WP2 uvrA 用には,0.5 mM L-トリプトファン水溶液を用いた. |
培地は,極東製薬工業(株)製の最少寒天培地を用いた.なお,培地1 l あたりの組成は下記のとおりである.
| 硫酸マグネシウム・7水和物 | 0.2 g |
| クエン酸・1水和物 | 2 g |
| リン酸水素二カリウム | 10 g |
| リン酸一アンモニウム | 1.92 g |
| 水酸化ナトリウム | 0.66 g |
| グルコース | 20 g |
| バクトアガー(Difco) | 15 g |
| **: | HY2101 では,大洋寒天(清水食品)を使用. |
1 ml中下記の成分を含む
| S9*** | 0.1 ml |
| 塩化マグネシウム | 8 μmol |
| 塩化カリウム | 33 μmol |
| グルコース-6-リン酸 | 5 μmol |
| NADH | 4 μmol |
| NADPH | 4 μmol |
| ナトリウム-リン酸緩衝液(pH 7.4) | 100 μmol |
| ***: | 7週齢の Sprague-Dawley 系雄ラットをフェノバルビタール(PB)および 5, 6-ベンゾフラボン(BF)の併用投与で酵素誘導して作製したS9を用いた. |
プレインキュベーション法 4)により,S9 mix 無添加試験および S9 mix 添加試験を行った.
小試験管中に,被験物質調製液 0.1 ml,リン酸緩衝液 0.5 ml(S9 mix 添加試験においては S9 mix 0.5 ml),検定菌液 0.1 ml を混合し,37℃で20分間往復振とう培養したのち,トップアガー2 mlを加えて混和し,合成培地平板上に流して固めた.また,対照群として被験物質調製液の代わりに使用溶媒,または数種の陽性対照物質溶液を用いた.各検定菌ごとの陽性対照物質の名称および用量は各Table 中に示した.なお,溶媒および陽性対照群は,同時に実施した他の試験と共通とした.培養は37℃で48時間行い,生じた変異コロニー数を算定した.抗菌性の有無については,肉眼的あるいは実体顕微鏡下で,寒天表面の菌膜の状態から判断した.用いた平板は用量設定試験においては,溶媒および陽性対照群では3枚ずつ,各用量については1枚ずつとした.また,本試験および再現性試験においては,両対照群および各用量につき,3枚ずつを用い,それぞれその平均値と標準偏差を求めた.用量設定試験は1回,本試験は同一用量について2回実施し,結果の再現性の確認を行った.また,TA1537 の S9 mix 無添加試験については,変異コロニー数増加の再現性と用量依存性を確認するために,再現性試験を行った.更に,追加試験として,TA1537E と TA97 の S9 mix 無添加試験について,1回の用量設定試験と2回の本試験を実施した.
したがって,本試験における最高用量は,S9 mix 無添加試験および添加試験とも 5000 μg/プレートとした.

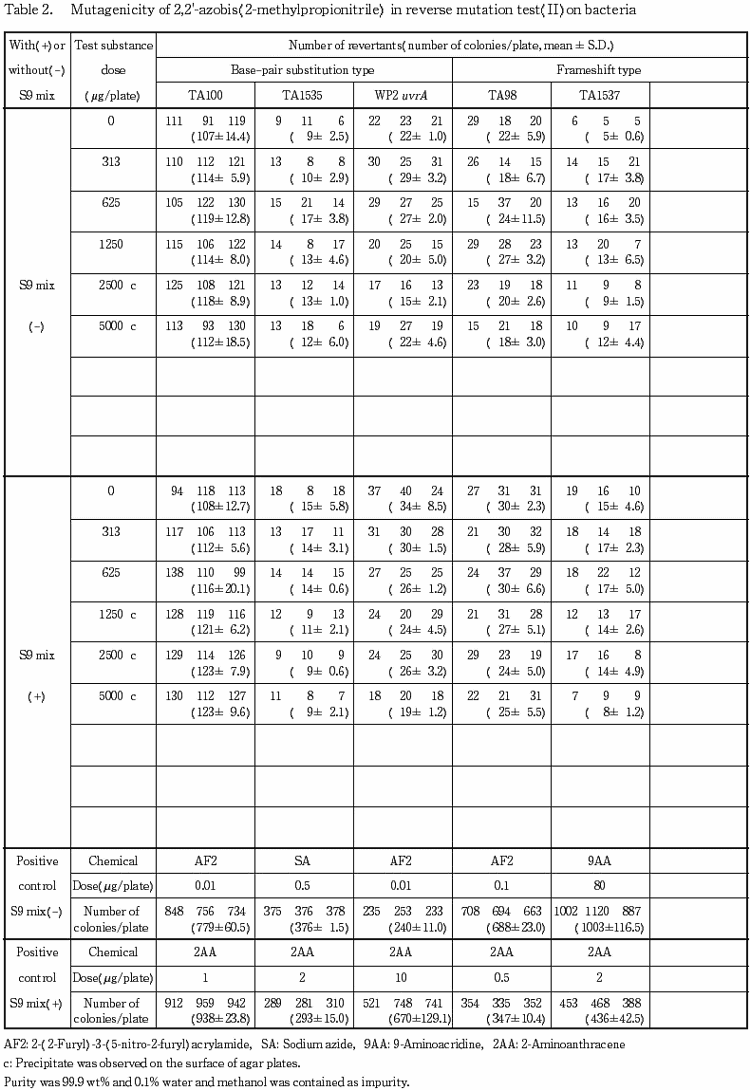
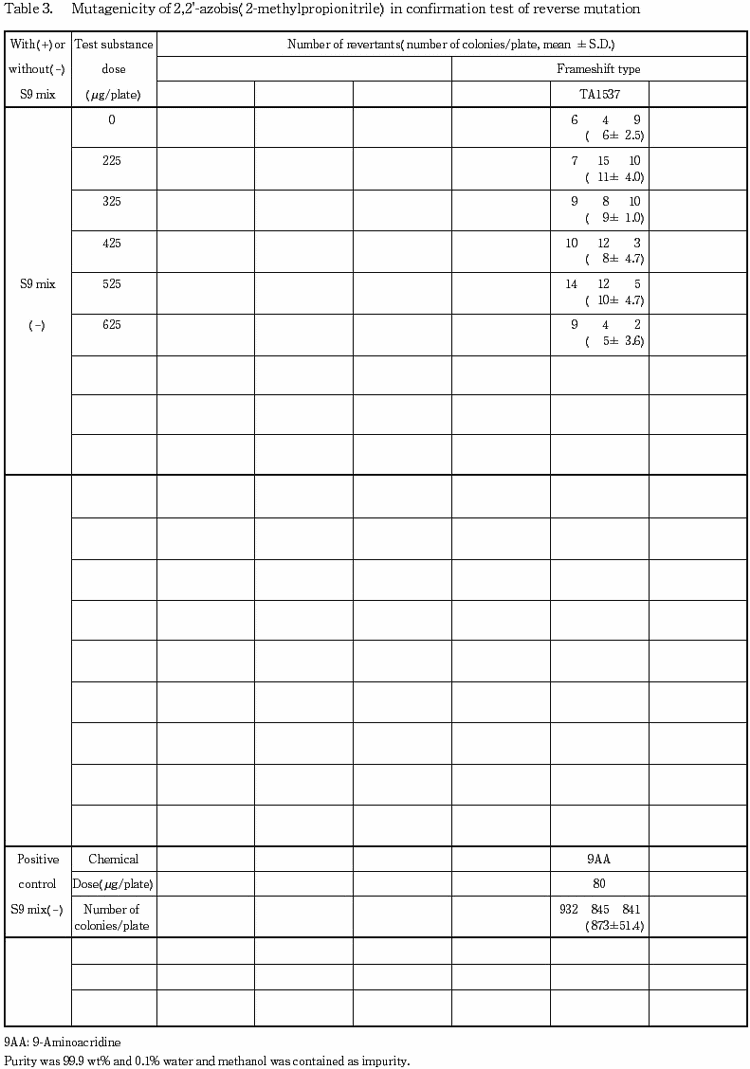
以上の結果に基づき,2,2'-アゾビス(2-メチルプロピオニトリル)は,用いた試験系において変異原性を有しないもの(陰性)と判定した.
| 1) | D.M. Maron, B.N. Ames, Mutat. Res., 113, 173(1983). |
| 2) | S. Venitt, C. Crofton-Sleigh, "Evaluation of Short-Term Tests for Carcinogens," eds. by F.J. de Serres, J. Ashby, Elsevier/North-Holland, New York, 1981, pp. 351-360. |
| 3) | M.H.L. Green, "Handbook of Mutagenicity Test Procedures," eds. by B.J. Kilbey, M. Legator, W. Nichols, C. Ramel, Elsevier, Amsterdam, New York, Oxford, 1984, pp.161-187. |
| 4) | T. Matsushima, T. Sugimura, M. Nagao, T. Yahagi, A. Shirai, M. Sawamura, "Short-Term Test Systems for Detecting Carcinogens," eds. by K.H. Norpoth, R.C. Garner, Springer, Berlin, Heidelberg, New York, 1980, pp. 273-285. |
| 連絡先: | |||
| 試験責任者 | 澁谷 徹 | ||
| 試験担当者 | 原 巧,坂本京子,堀谷尚古, 川上久美子,笠間菊子,宮田美穂子 | ||
| (財)食品薬品安全センター 秦野研究所 | |||
| 〒257 神奈川県秦野市落合 729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Tohru Shibuya(Study Director) Takumi Hara, Kyoko Sakamoto, Naoko Horiya, Kumiko Kawakami, Kikuko Kasama, Mihoko, Miyata | |||
| Hatano Research Institute,Food and Drug Safety Center | ||||
| 729-5 Ochiai,Hadano-shi,Kanagawa 257 Japan | ||||
| Tel +81-463-82-4751 | FAX +81-463-82-9627 | |||