リン酸トリス(2-ブトキシエチル)エステルのラットを用いる
28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of
Tris(2-butoxyethyl) phosphate in Rats
要約
リン酸トリス(2-ブトキシエチル)エステルの28日間反復経口投与毒性試験(回復14日間)を雌雄の Sprague-Dawley 系(Crj:CD)ラットを用いて実施した.投与量は,雌雄とも0(溶媒対照群),100,300 および 1000 mg/kg とした.雌雄とも溶媒対照群および1000 mg/kg 投与群では1群10匹,100 および 300 mg/kg 投与群では1群5匹を使用し,このうち溶媒対照群および 1000 mg/kg 投与群の雌雄各5匹について14日間の回復試験を行った.その結果,以下の成績を得た.
投与期間中および回復試験期間中に,溶媒対照群および被験物質投与群において死亡例は認められなかった.
一般状態の変化として,1000 mg/kg 投与群の雌において,初回投与時に,脱力,うつ伏せ状態,粗大呼吸が数例で認められたが,数時間後には回復した.また,雌雄とも被験物質投与群の全例で,投与直後に被験物質の刺激性に起因したと考えられる一過性の流涎が観察され,1000 mg/kg 投与群の雌では投与第16,17,23および25日に保定時から流涎が認められる例もあった.回復試験群では休薬によりこれらの変化はすみやかに消失した.
体重および摂餌量については,溶媒対照群と被験物質投与群との間に有意差は認められなかった.
投与期間終了時の尿検査,血液学検査において,被験物質投与に起因すると考えられる変化は認められなかった.
投与期間終了時の血液生化学検査では,雌雄において血漿中のコリンエステラーゼ活性が用量依存的に低下する傾向があり,1000 mg/kg 投与群の雌雄で有意差が認められた.しかし,赤血球中のコリンエステラーゼ活性に有意差は認められなかった.その他に,被験物質投与に起因すると考えられる変化は認められなかった.一方,回復試験期間終了時の検査では,雌雄ともに血漿中および赤血球中のコリンエステラーゼ活性を含む各検査項目において,溶媒対照群と被験物質投与群との間で差は認められなかった.
投与期間終了時屠殺剖検例の 1000 mg/kg 投与群の雌雄および 300 mg/kg 投与群の雌において,肝臓の絶対重量および相対重量が有意に増加した.回復試験期間終了時屠殺剖検例では,1000 mg/kg 投与群の雌の腎臓で絶対重量が有意に低下した.
投与期間終了時屠殺剖検例の病理学検査において,肝臓の小肉芽腫が雌では 300 mg/kg投与群で変化の程度が有意に増強した.また,300 mg/kg 以上の投与群では,小葉周辺帯の肝細胞の微細空胞化の発生頻度および程度がともに増強する傾向にあり,雌の 1000mg/kg 投与群では,統計学的に有意な差が認められた.一方,回復試験期間終了時の屠殺剖検例では,被験物質投与に起因すると思われる変化は認められなかった.
以上の結果,本試験条件下におけるリン酸トリス(2-ブトキシエチル)エステルの無影響量(NOEL)は,雌雄とも 100 mg/kg/day であると考えられる.また,被験物質投与に起因すると考えられる上記の変化は,14日間の休薬によりいずれも回復することが明らかとなった.
方法
1.被験物質および投与検体の調製
被験物質として,大八化学工業(株)より提供されたリン酸トリス(2-ブトキシエチル)エステル〔ロット番号:K70702,無色透明,刺激性を有する液体,比重:1.019,純度:98.2%〕を使用した.
被験物質を20%(w/v)の濃度になるようコーンオイル〔ロット番号:V5P5523,ナカライテスク(株)〕に溶解し,さらに,この20%溶液を6および2%(w/v)濃度となるように段階希釈して投与検体を調製した.投与検体の調製は3〜7日間に1回の頻度で行った.なお,リン酸トリス(2-ブトキシエチル)エステルの安定性試験および含量試験を実施した結果,0.2および 20.0%(w/v)コーンオイル溶液中の被験物質は,室温下で8日間は安定であり,また,投与検体中の被験物質の含量は,所定濃度の96.7〜100%であることが確認された.
2.動物および飼育方法
生後4週で購入した雌雄の Sprague-Dawley 系ラット(Crj:CD;SPF,日本チャールス・リバー(株),厚木飼育センター生産)を8日間にわたり予備飼育した後,一般状態に異常の認められなかった雌雄各30匹を試験に供した.動物は,全飼育期間を通じて,温度24±1℃,湿度50〜65%,換気回数約15回/時間,照明時間12時間(7〜19時点灯)に制御された飼育室内で,金属製金網床ケージ(220×270×190 mm)に1匹ずつ収容し,固型飼料(CE-2,日本クレア(株))および水道水(秦野市水道局給水)を自由に摂取させて飼育した.
3.群および群分け
本試験における投与量は,本試験開始前に秦野研究所で実施したリン酸トリス(2-ブトキシエチル)エステルのラットにおける7日間反復経口投与毒性試験の成績を参考にして決定した.即ち,雄の Sprague-Dawley 系ラットにリン酸トリス(2-ブトキシエチル)エステルを 1000 mg/kg,300 mg/kg および 100 mg/kg の用量で7日間反復投与した結果,死亡例はなく,投与直後に一過性の流涎が観察されたほかには一般状態に変化が認められなかった.また,8日目に行った剖検においても,被験物質投与に起因すると思われる異常所見は認められなかった.従って,本試験では,化審法ガイドライン「ほ乳類を用いる28日間の反復投与毒性試験」に従って,雌雄とも最高投与用量を 1000 mg/kg とし,以下 300および 100 mg/kg 投与群を設定した.なお,雌雄とも1群を溶媒対照群としてコーンオイルのみを経口投与した.
群分けは,投与開始前日の体重に基づいて,体重別層化無作為抽出法により行った.各群の匹数および動物番号を以下に示した.
| 群 (投与液の濃度) |
匹数(動物番号) |
| 雌 | 雄 |
| 溶媒対照群(コーンオイル) | 10(1〜10) | 10(31〜40) |
| 被験物質 100 mg/kg 投与群(2%,w/v) | 5(11〜15) | 5(41〜45) |
| 被験物質 300 mg/kg 投与群(6%,w/v) | 5(16〜20) | 5(46〜50) |
| 被験物質 1000 mg/kg 投与群(20%,w/v) | 10(21〜30) | 10(51〜60) |
4.投与方法
本試験の投与経路は,化審法ガイドライン「ほ乳類を用いる28日間の反復投与毒性試験」に従い経口投与とした.
投与は,1日1回,28日間,ラット用胃管を用いて強制的に行い,投与液量は,雌雄とも5ml/kg として,各投与時に最も近い時点で測定された体重値を基準にして個別に算出した.なお,雌雄とも溶媒対照群および 1000 mg/kg 投与群の各5匹を投与期間終了後,14日間の回復試験に用いた.
5.検査項目
1) 一般状態の観察
投与期間および回復試験期間を通じて,死亡例の有無を調べたほか,生存例全例について,一般状態を投与期間中は毎日投与前および投与後の2回(回復試験期間中は1回)観察した.
2) 体重および摂餌量の測定
投与開始週では,投与開始直前と投与第4日,第2週以降の投与期間および回復試験期間中は,生存例全例について1週に2回の頻度で体重を測定し,投与期間あるいは回復試験期間終了日および剖検日にも体重の測定を行った.また,投与開始週では,投与開始日に,第2週以降の投与期間および回復試験期間中は,生存例全例について1週に1回の頻度で1日当たりの摂餌量の測定を行った.
3) 尿検査
投与期間終了週(投与第23日)に各群とも動物番号の若い方から5匹を選択し,また回復試験期間終了週(回復第9日)には回復試験例全例をいずれも,約24時間代謝ケージ(夏目製作所製)に収容して採尿し,尿量〔天秤で計量(尿重量を比重で除す)〕,色調および混濁(視診),比重〔重量法,天秤(AE200)〕について検査した.なお,pH,潜血,蛋白質,糖,ケトン体,ビリルビン,ウロビリノーゲンおよび沈渣の検査は,代謝ケージに収容して約4時間以内に採取した尿について,試験紙法〔マルティスティックス/クリニテック200(マイルス三共)〕および鏡検(光学顕微鏡)によって実施した.
4) 血液学検査
投与期間終了時および回復試験期間終了時の剖検に先立ち,全例について,約18ないし24時間絶食させたのち,ペントバルビタール麻酔下で腹部後大静脈より EDTA 2K を抗凝固剤として採血し,Coulter Counter Model S-PLUS IV(コールターエレクトロニクス社)により赤血球数(電気抵抗法),白血球数(電気抵抗法),血色素量(吸光度法),平均赤血球容積(電気抵抗法),および血小板数(電気抵抗法)を測定し,これらを基に平均赤血球血色素量,平均赤血球血色素濃度およびヘマトクリット値を算出した.また,血液の一部は塗抹標本とし,白血球分類(Wright-Giemsa 染色)および網状赤血球比率(Brecher 法)を求めた.なお,プロトロンビン時間および活性部分トロンボプラスチン時間については,クエン酸ナトリウムを抗凝固剤として採血した血液を用いて,CA-3000〔光散乱検出法(東亜医用電子)〕 により測定した.
5) 血液生化学検査
前述の血液学検査のための採血に引き続き,ヘパリンを抗凝固剤として採血し,それぞれ血漿を分離して遠心方式生化学自動分析装置(COBAS-FARA,ロッシュ社)により,総蛋白濃度(ビウレット法),アルブミン濃度(BCG 法),総コレステロール濃度(COD・DAOS 法),ブドウ糖濃度(グルコキナーゼ・G6PDH 法),尿素窒素濃度(ウレアーゼ・GlDH法),クレアチニン濃度(Jaff 法),アルカリフォスファターゼ活性(ρ-ニトロフェニルリン酸基質法),GOT 活性(SSCC 法),GPT 活性(SSCC 法),LDH 活性(Wroblews-LaDue 法),コリンエステラーゼ活性(DTNB 法),カルシウム濃度(OCPC 法),無機リ濃度(モリブデン酸直接法),トリグリセライド濃度(GPO・DAOS 法),γ-GTP(γ-グタミル-3-カルボキシ-ρ-ニトロアニリド基質法),A/G 比(総蛋白濃度およびアルブミン濃度より算出)を測定した.なお,赤血球のコリンエステラーゼ活性の測定は,血液生化学検査用に採血した血液を使用し,Pilz の方法を参考にして,まず,全血 0.25 ml を 0.9% NaCl 10 ml で3回洗い,洗浄した赤血球に精製水 5 ml を加え溶血させ遠心後,上清についてコリンエステラーゼ活性およびヘモグロビン濃度を測定した.赤血球のコリンエステラーゼ活性は,ヘモグロビンあたりの活性として表示した.また,全自動電解質分析装置 EA05(A&T)により,ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法)を測定した.
法),アルカリフォスファターゼ活性(ρ-ニトロフェニルリン酸基質法),GOT 活性(SSCC 法),GPT 活性(SSCC 法),LDH 活性(Wroblews-LaDue 法),コリンエステラーゼ活性(DTNB 法),カルシウム濃度(OCPC 法),無機リ濃度(モリブデン酸直接法),トリグリセライド濃度(GPO・DAOS 法),γ-GTP(γ-グタミル-3-カルボキシ-ρ-ニトロアニリド基質法),A/G 比(総蛋白濃度およびアルブミン濃度より算出)を測定した.なお,赤血球のコリンエステラーゼ活性の測定は,血液生化学検査用に採血した血液を使用し,Pilz の方法を参考にして,まず,全血 0.25 ml を 0.9% NaCl 10 ml で3回洗い,洗浄した赤血球に精製水 5 ml を加え溶血させ遠心後,上清についてコリンエステラーゼ活性およびヘモグロビン濃度を測定した.赤血球のコリンエステラーゼ活性は,ヘモグロビンあたりの活性として表示した.また,全自動電解質分析装置 EA05(A&T)により,ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法)を測定した.
6) 病理学検査
上記の採血に引き続き,必要に応じて腋窩動脈を切断して放血屠殺したのち,器官および組織の肉眼的観察を行った.また,各動物の脳,肝臓,腎臓,副腎,卵巣または精巣の重量測定を行い,各器官重量を剖検日の体重で除して,それぞれの相対重量を算出した.さらに,脳,頸髄,下垂体,眼球,甲状腺(上皮小体を含む),顎下腺(舌下腺を含む),心臓,肺,肝臓,腎臓,脾臓,膵臓,副腎,胃,十二指腸,空腸,回腸,結腸,直腸,卵巣または精巣,膀胱,大腿骨骨髄,坐骨神経は,0.1 M リン酸緩衝10%ホルマリン液(pH7.2)で固定した.脳,頸髄,顎下腺(舌下腺を含む),心臓,肝臓,腎臓,脾臓,膵臓,副腎,坐骨神経のほか,剖検時に肉眼的変化の認められた一部の例の胃,胸腺,肺,直腸,皮膚をパラフィン包埋後,ヘマトキシリン・エオジン染色標本を作製し,病理組織学検査を実施した.
6.統計処理法
体重,摂餌量,尿検査(半定量検査を除く),血液学検査,血液生化学検査ならびに器官重量で得られた実測値をもとにして,各群ごとに平均値および標準偏差を求めた.また,試験群の構成が溶媒対照群を含め3群以上ある場合は,Bartlett の方法による分散の一様性の検定(有意水準:5%)を行い,ついで,分散が一様な場合は,一元配置型の分散分析を行い,有意(有意水準:5%)の時は Dunnett あるいは Scheff の方法で多重比較を行った.一方,分散が一様でない場合は Kruskal-Wallis の順位検定を行い,有意(有意水準:5%)ならば Dunnett 型あるいは Scheff
の方法で多重比較を行った.一方,分散が一様でない場合は Kruskal-Wallis の順位検定を行い,有意(有意水準:5%)ならば Dunnett 型あるいは Scheff 型の方法で多重比較を行った.また,試験群が溶媒対照群を含め2群となる場合には,溶媒対照群と被験物質投与群の各平均値の差の検定は,等分散であれば Student のt検定,不等分散であれば Aspin-Welch 検定を行った.病理組織検査所見中,溶媒対照群および被験物質投与群の双方に共通してみられ,被験物質投与群で頻度,程度が増強している所見については,Mann- Whitney U test および Fisher exact test を行った.
型の方法で多重比較を行った.また,試験群が溶媒対照群を含め2群となる場合には,溶媒対照群と被験物質投与群の各平均値の差の検定は,等分散であれば Student のt検定,不等分散であれば Aspin-Welch 検定を行った.病理組織検査所見中,溶媒対照群および被験物質投与群の双方に共通してみられ,被験物質投与群で頻度,程度が増強している所見については,Mann- Whitney U test および Fisher exact test を行った.
結果
1.一般状態
一般状態の変化として,1000 mg/kg 投与群の雌において初回投与30分後に2例で全身または両後肢の脱力が認められ,うつ伏せ状態となりこのうちの1例で軟便の排泄も認められ,さらに30分後にはうずくまり,呼吸も荒くなった.この2例の症状は投与後2〜3時間には回復した.また,他の1例においても投与後3時間に両後肢の脱力が認められたが,30分後に回復した.さらに,被験物質投与群の全例で,投与直後に一過性の流涎が観察され,その多くは投与第2日以降に発現し,投与を重ねるに従って流涎のみられる例数が増加する傾向にあった.特に 1000 mg/kg 投与群では雌雄ともに全例で,投与第2日からほぼ毎日一過性の流涎が認められるようになり,投与第16,17,23および25日には投与時に保定するだけで流涎が観察された例も雌で認められた.また,投与期間中頸部または頬の皮膚に痂皮形成が雌の溶媒対照群および 1000 mg/kg 投与群で各1例,雄の溶媒対照群および 100 mg/kg 投与群で各1例,300 mg/kg 投与群で2例認められた.投与期間中に痂皮の一部が脱落して潰瘍を形成する例も認められたが,その後,潰瘍あるいは痂皮は次第に縮小し,投与期間終了時の屠殺剖検では,1000 mg/kg 投与群の雌および 300 mg/kg投与群の雄の各1例に痂皮が認められたのみであった.その他に,被験物質投与群において投与直後に摂食行動が多くの例で認められたが,用量に依存した変化ではなかった.
2.体重(Fig.1)
雌雄共に,投与期間および回復試験期間を通して,溶媒対照群と被験物質投与群との間で平均体重に有意差は認められなかった.
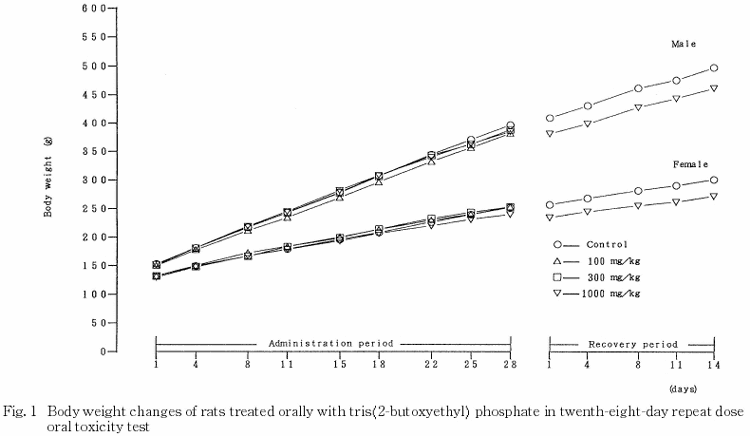
3.摂餌量(Fig.2)
雌雄共に,投与期間および回復試験期間を通して,溶媒対照群と被験物質投与群との間で平均摂餌量に有意差は認められなかった.
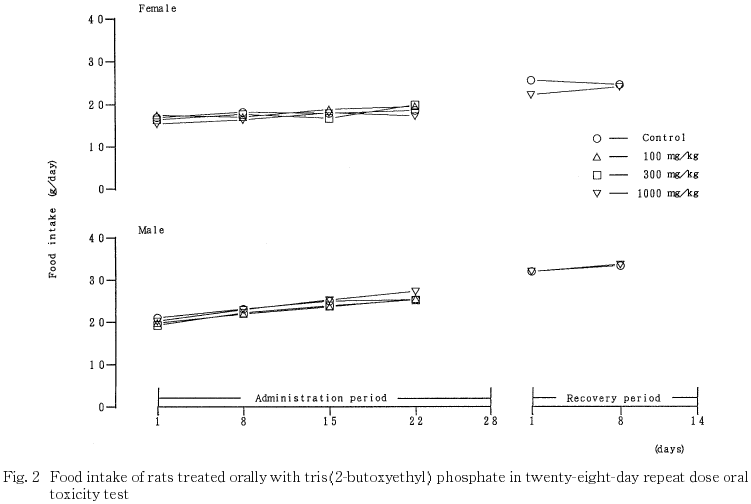
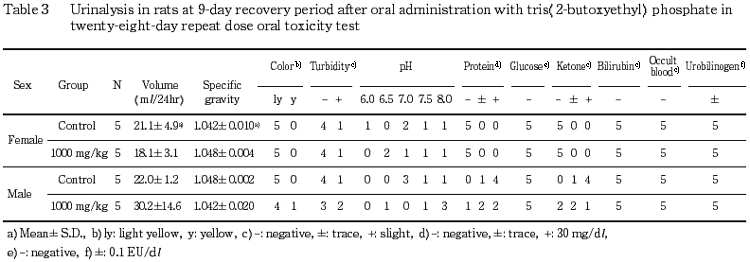
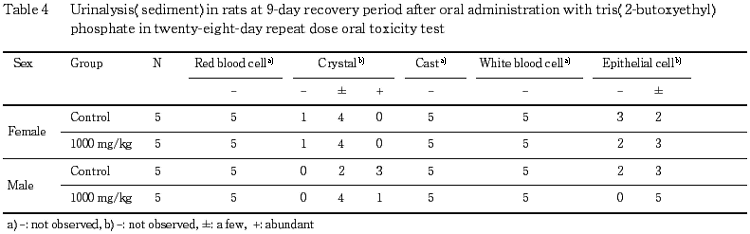
4.尿検査(Table 1〜4)
投与期間終了週の検査では,1000 mg/kg 投与群の雌雄において,尿量の増加傾向が認められた.また,300 mg/kg 投与群の雄の1例において,ビリルビンが陽性であった.その他,一部で蛋白質,ケトン体が陽性または疑陽性となる例があり,尿沈渣中に上皮細胞または結晶が観察される例もあったが,いずれも,その出現例数あるいは程度に用量依存性は認められなかった.なお,その他の検査項目については,溶媒対照群と被験物質投与群との間に差は認められなかった.また,回復試験期間終了週の検査では,いずれの検査項目にも溶媒対照群と 1000 mg/kg 投与群との間で差は認められなかった.
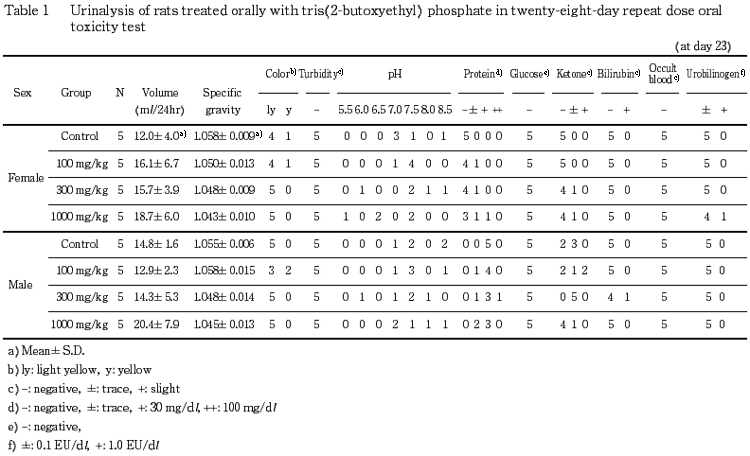
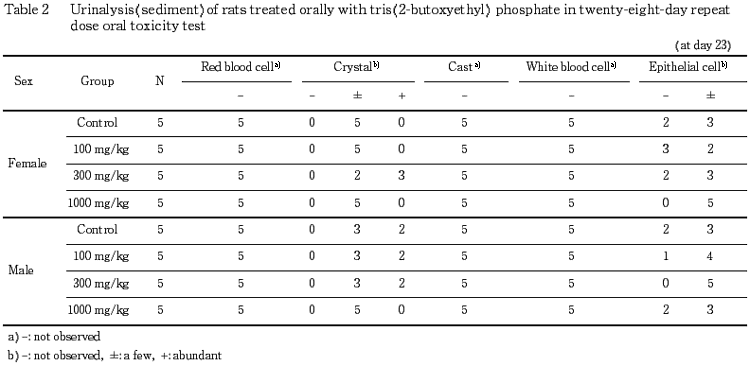
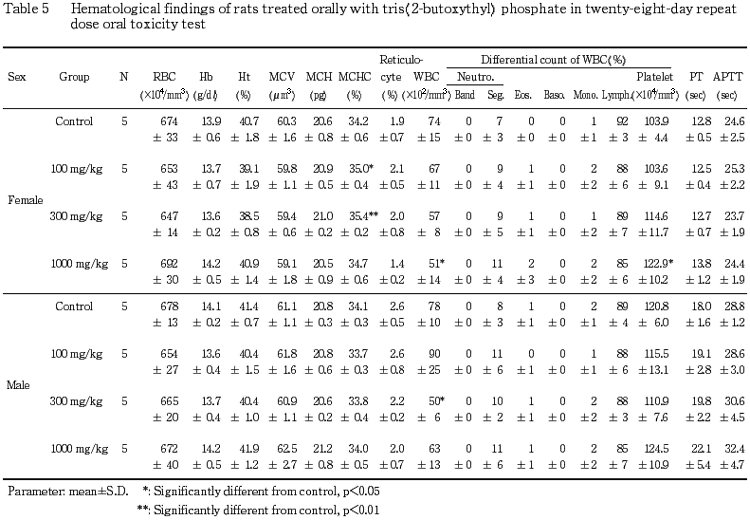
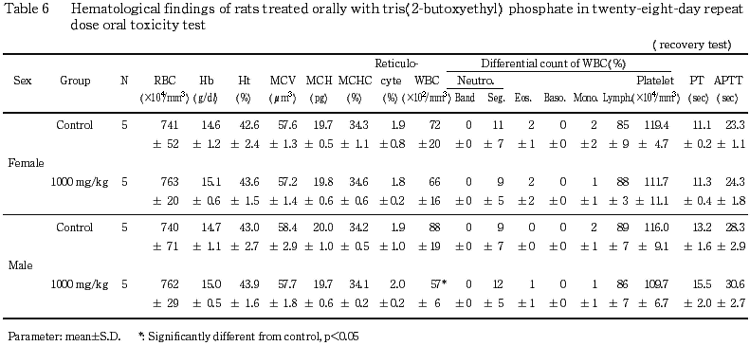
5.血液学検査(Table 5,6)
投与期間終了時の検査では,1000 mg/kg 投与群の雌および 300 mg/kg 投与群の雄において,白血球数の有意な減少が認められ,300 mg/kg 投与群の雌および 1000 mg/kg 投与群の雄でも白血球数の減少傾向が認められた.その他の検査項目では,雌において100および 300 mg/kg 投与群の平均赤血球血色素濃度と1000 mg/kg 投与群の血小板数が有意に増加した.
回復試験期間終了時の検査では,1000 mg/kg 投与群の雄において白血球数の有意な減少が認められた.
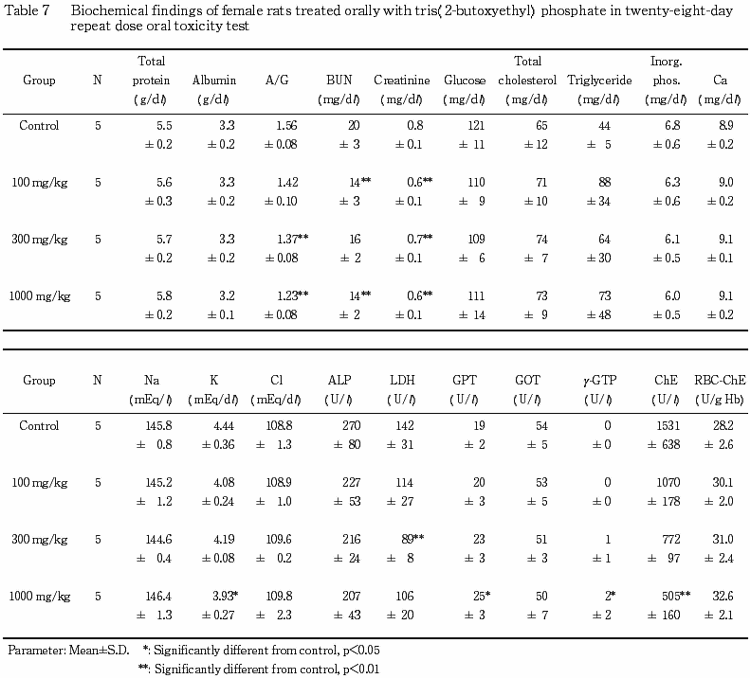
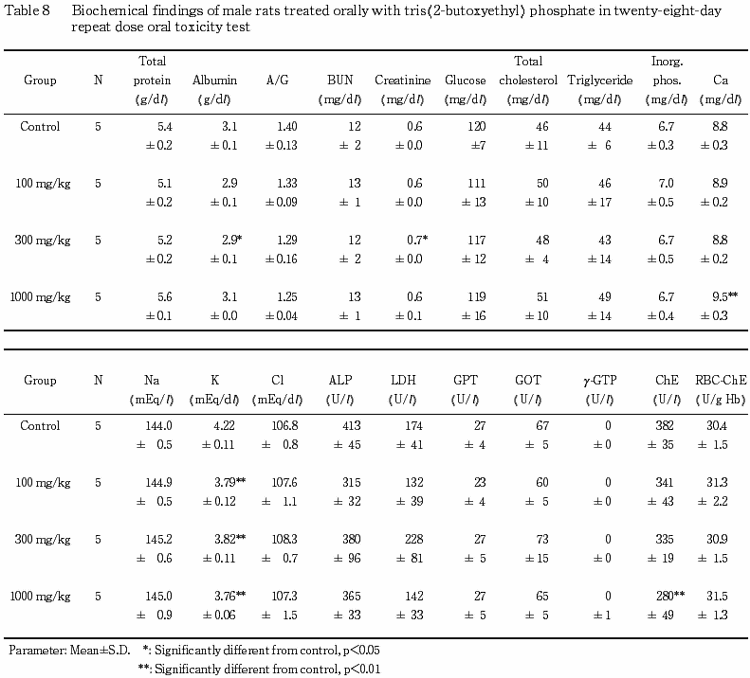
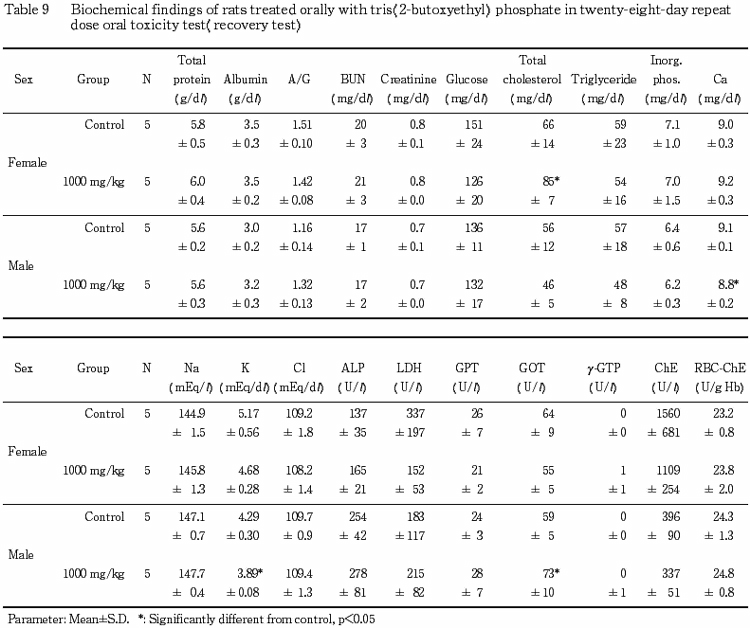
6.血液生化学検査(Table 7〜9)
投与期間終了時の検査では,雌雄において血漿中のコリンエステラーゼ活性が用量依存的に低下する傾向にあり,1000 mg/kg 投与群の雌雄で有意差が認められた.しかし,赤血球中のコリンエステラーゼ活性に変化は認められなかった.その他,統計学的に有意差のみられた変化として,雌では,300 および 1000 mg/kg 投与群において A/G 比の低下,100 および 1000 mg/kg 投与群において尿素窒素濃度が低下し,各被験物質投与群でクレアチニン濃度の低下が認められた.さらに,300 mg/kg 投与群で LDH 活性の低下,1000 mg/kg 投与群でカリウム濃度の低下,GPT およびγ- GTP 活性の上昇が認められた.一方,雄では,各被験物質投与群でカリウム濃度の低下が認められたほか,300 mg/kg 投与群でアルブミン濃度の低下およびクレアチニン濃度の上昇が認められた.しかし,これらの変化には,いずれも用量依存性は認められなかった.また,雄の 1000 mg/kg 投与群でカルシウム濃度の上昇が認められた.その他の検査項目では,溶媒対照群と被験物質投与群との間に有意差は認められなかった.
回復試験期間終了時の検査では,1000 mg/kg 投与群において雌で総コレステロール濃度,雄で GOT 活性がそれぞれ有意に上昇し,さらに雄ではカルシウム濃度およびカリウム濃度が有意に低下した.
7.病理学検査
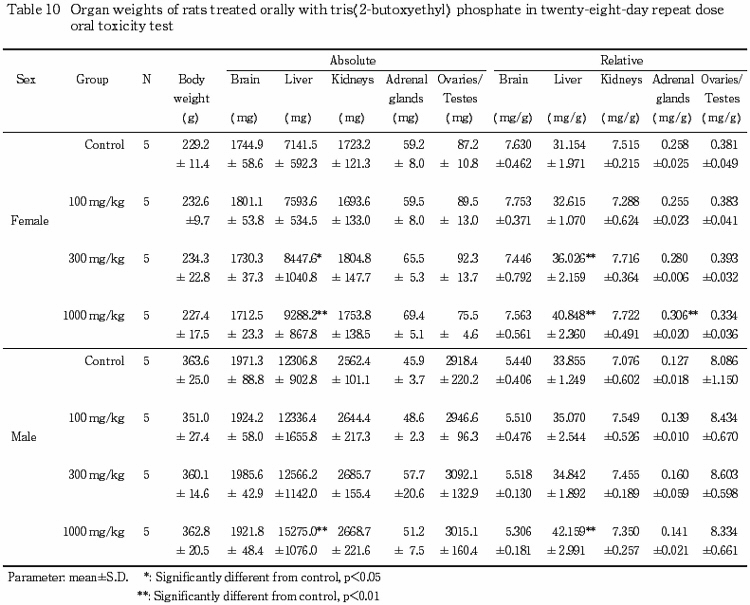
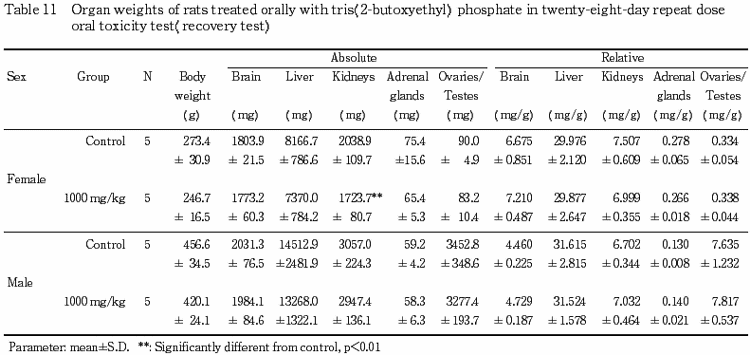
1) 器官重量(Table 10〜11)
投与期間終了時屠殺剖検例では,1000 mg/kg 投与群の雌雄において,肝臓の絶対重量および相対重量が有意に増加した.また,300 mg/kg 投与群の雌においても肝臓の絶対重量および相対重量が有意に増加した.さらに,1000 mg/kg 投与群の雌において副腎の相対重量が有意に増加したが,その他には溶媒対照群と被験物質投与群との間に有意差は認められなかった.
回復試験期間終了時屠殺剖検例では,1000 mg/kg 投与群の雌の腎臓で絶対重量が有意に低下した.
2) 剖検所見
投与期間終了時屠殺剖検例では,肝臓に 1000 mg/kg 投与群の雌5例,雄4例,300 mg/kg 投与群の雌3例,および 100 mg/kg 投与群の雄1例に小葉像の明瞭化が認められ,1000 mg/kg 投与群の雌1例に腫大が認められた.また,1000 mg/kg 投与群の雌2例,雄1例および 300 mg/kg 投与群の雌雄各1例に黄色化が,1000 mg/kg 投与群の雄1例,300 mg/kg 投与群の雌1例に褐色化が,1000 および 300 mg/kg 投与群の雌雄各1例に暗色化が観察された.その他,対照群あるいは被験物質投与群の1部の例で肺に暗色点あるいは赤色点が,胃に暗色あるいは赤色点,陥凹部,ヘマチン様物質の付着,胸腺に赤色点,皮膚の脱毛あるいは痂皮が観察されたが,いずれも散発性で用量に依存した変化ではなかった.
回復試験期間終了時屠殺剖検例では,用量に依存した異常所見は認められなかった.
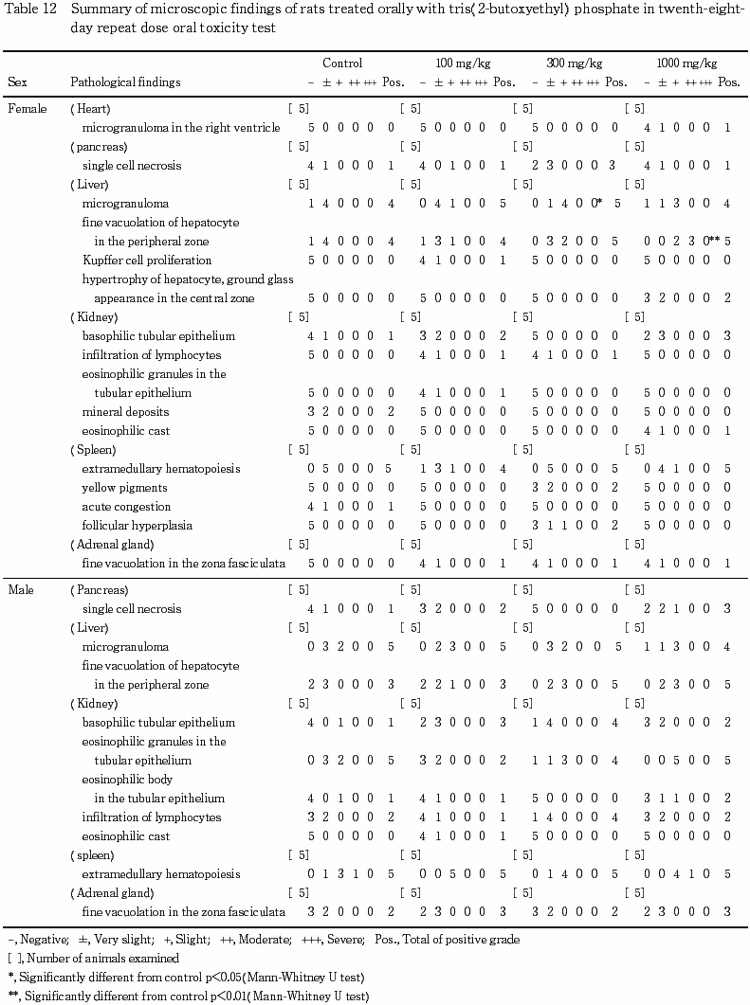
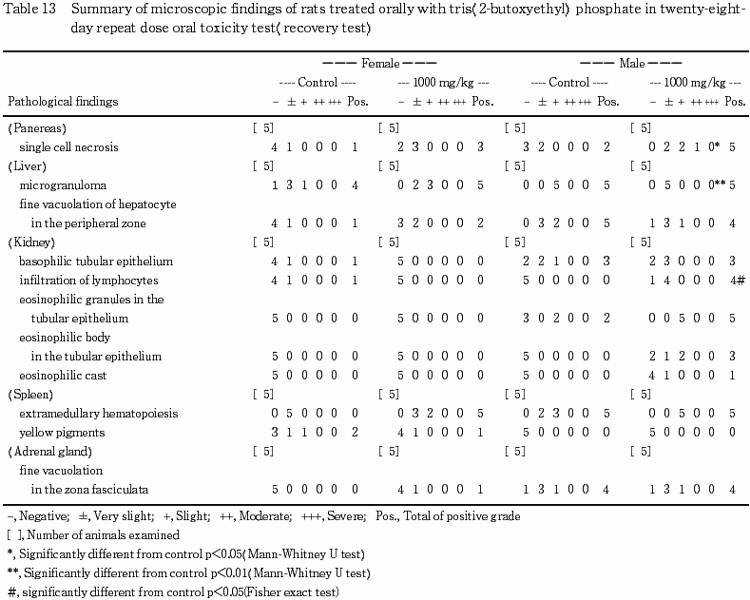
3) 病理組織学所見(Table 12〜13)
投与期間終了時屠殺剖検例では,雌雄の溶媒対照群を含む各被験物質投与群の肝臓に小肉芽腫が観察され,雌では 300 mg/kg 投与群で変化の程度が有意に増強した,雄では溶媒対照群と被験物質投与群との間に発生頻度および病変の程度に差は見られなかった.また,溶媒対照群および各被験物質投与群の雌雄に小葉周辺帯に微細空胞を持つ肝細胞が観察され,1000 mg/kg 投与群の雌で,その発生頻度あるいは程度が有意に増強した.その他に,1000 mg/kg 投与群の雌の2例に軽微な細胞質のスリガラス状変化を伴った軽微な小葉中心性肝細胞の肥大が観察された.
腎臓では,その他,好塩基性尿細管上皮,尿細管上皮に好酸性微細顆粒あるいは eosinophilic body が観察され,好酸性円柱も認められたほか,膵臓では,単細胞壊死が,副腎では,束状帯の微細空胞化が,心臓では,右心室に小肉芽腫が観察されたが,いずれもその発生は散発的であり用量依存性も認められなかった.
回復試験期間終了時屠殺剖検例では,肝臓において,小肉芽腫が,小葉周辺帯の肝細胞の空胞化が,腎臓では,尿細管上皮に好酸性微細顆粒,eosinophilic body,軽微なリンパ球浸潤が,膵臓では,単細胞壊死が,副腎では,束状帯の空胞化が観察されたが,いずれも用量に依存した変化ではなかった.なお,脾臓では,溶媒対照群および 1000 mg/kg投与群の雌雄全例に軽微から軽度の髄外造血が観察され,1000 mg/kg 投与群の雌雄ともに変化の程度が強くなる傾向が見られた.
この他,投与期間終了時あるいは回復試験期間終了時の屠殺剖検では,腎臓の鉱質沈着,脾臓の鬱血,腺胃のびらん等が観察されたが,いずれも用量に依存した変化ではなかった.
考察
プラスチックあるいは合成ゴムの可塑剤,難燃剤,床磨き剤の添加剤等として家庭用品に広く使用されているリン酸トリス(2-ブトキシエチル)エステルの100,300 および1000 mg/kg を,雌雄の Sprague-Dawley 系(Crj:CD)ラットに1日1回,28日間にわたって反復経口投与した.その結果,一般状態の変化として,1000 mg/kg 投与群の雌において,初回投与時に脱力,うずくまり,軟便等の急性症状が認められたが,3時間前後で回復し,それ以後の投与時には認められなかった.さらに,雌雄とも被験物質投与群の全例で,投与直後に一過性の流涎が観察されたが,その多くは投与第2日以降に発現し,投与を重ねるに従って流涎のみられる例数が増加する傾向にあり,特に,1000 mg/kg 投与群の雌では,投与の保定時から認められることもあった.リン酸トリス(2-ブトキシエチル)エステルは,粘膜に対して刺激性を有することが明らかにされていることから,本試験で観察された流涎は,被験物質の粘膜刺激性に対する反応であり,連続投与により条件反射が成立したものと考えられる.
血液生化学検査では,投与期間終了時の雌雄ともに血漿中のコリンエステラーゼ活性が用量依存的に低下する傾向が認められ,1000 mg/kg 投与群の雌雄で有意差が認められた.リン酸トリス(2-ブトキシエチル)エステルは,いわゆる有機燐剤の一つであり,ある種の有機燐剤は,コリンエステラーゼ活性阻害作用を有しており,神経接合部でのコリンエステラーゼ活性を阻害することにより神経障害を惹起することが明らかにされている2).津田ら2)はリン酸トリス(2-ブトキシエチル)エステルの Wistar 系ラットにおける14週間反復経口(混餌)投与毒性試験において血清中のコリンエステラーゼ活性が約50%低下するが,明らかな神経症状はみられないと報告している.従って,リン酸トリス(2-ブトキシエチル)エステルがコリンエステラーゼ活性阻害作用を有している可能性が示唆されるが,本試験においてもコリンエステラーゼ活性阻害により惹起される特徴的な急性の神経症状は無く,赤血球中のコリンエステラーゼ活性にも差が認められなかったことから,その作用は非常に弱いものであると判断される.その他いくつかの検査項目で溶媒対照群と比べ有意差が認められたが,用量依存性がみられないことから,被験物質投与に起因した変化ではないと判断した.また,これらの血液生化学変化に対応した病理形態学的変化も認められなかった.
病理学検査では,投与期間終了時剖検屠殺例の肝臓において,1000 mg/kg 投与群の雌雄で絶対重量および相対重量の増加が,300 mg/kg 投与群の雌でも絶対重量および相対重量の増加が認められ,雌雄ともに,300 mg/kg 以上の投与群で小葉周辺帯の肝細胞の空胞性変化の発生頻度あるいは程度が増強する傾向が認められた.1000 mg/kg 投与群の雌の2例に軽微な小葉中心性の肝細胞の肥大が認められたが,細胞質がスリガラス状を呈していることから薬物代謝酵素が誘導されている可能性が示唆された.前述の Wistar 系ラットを用いた津田らの報告においてもリン酸トリス(2-ブトキシエチル)エステル3%混餌投与群で小葉周辺帯の肝細胞の腫大が認められることを明らかにしていることから,リン酸トリス(2-ブトキシエチル)エステルは,肝細胞を標的臓器としている可能性が高いが,本試験からその作用機序を明らかにすることは出来なかった.なお,肝細胞の小肉芽腫は,通常のSD系ラットにもみられる変化であるが,雌のリン酸トリス(2-ブトキシエチル)エステル 300 mg/kg 以上の投与群で,変化の程度が増強されていることから,小葉周辺帯の肝細胞の空胞変性のみならず,壊死,脱落が加わっている可能性が高い.その他の器官においても,変化が認められたが,発生頻度も少なく,用量依存性も認められなかったことから,被験物質投与に起因した変化ではないと判断した.
尿検査では,投与期間終了週において,1000 mg/kg 投与群の雌雄で尿量の増加傾向が認められたが,生理的変動の範囲内であった.また,300 mg/kg 投与群の雄の1例にビリルビン陽性が見られたが,出現頻度も少なく,被験物質投与に起因した変化ではないと判断した.
血液学検査では,投与期間終了時の検査で,1000 mg/kg 投与群の雌および300 mg/kg投与群の雄において,白血球数の減少が認められ,回復試験期間終了時の検査においても1000 mg/kg 投与群の雄において白血球数の減少が認められた.しかし,これらはいずれも生理的変動範囲内の変化であり,これに伴う白血球百分比の変化がみられないことから偶発的な所見である可能性が高いと考えられる.また,その他の検査項目においても有意差が認められたが,いずれも,生理的変動範囲内を超えるものではなかった.
なお,リン酸トリス(2-ブトキシエチル)エステル投与により発現したと考えられる上記の変化は,14日間の休薬した例では観察されなかったことから,休薬後すみやかに回復し得る変化であると考えられる.
以上のことから,本試験条件下におけるリン酸トリス(2-ブトキシエチル)エステルの無影響量は,雌雄とも 100 mg/kg であると考えられる.
文献
| 1) | W. Pilz, "Methods of Enzymatic Analysis," 2nd ed., vol. 2, Academic Press, New York, 1974, p. 844. |
| 2) | M. Tsuda, M. Saitoh, T. Umemura, J. Toxicol., 18, 421(1993). |
| 連絡先 |
| 試験責任者: | 今井 清 |
| 試験担当者: | 関 剛幸,加藤博康,小島幸一,稲田浩子,中尾美津男,畔上二郎,永田伴子,三枝克彦 |
| (財)食品薬品安全センター 秦野研究所 |
| 〒257 秦野市落合 729-5 |
| Tel 0463-82-4751 | Fax 0463-82-9627 | |
| Correspondence |
| Authors: | Kiyosi Imai(Study Director)
Takayuki Seki,Hiroyasu Katoh, Kohichi Kojima,
Hiroko Inada,Mitsuo Nakao,Jiro Azegami,
Tomoko Nagata,Katsuhiko Saegusa |
| Hatano Research Institute,Food and Drug Safety Center |
| 729-5 Ochiai,Hadano-shi,Kanagawa 257 Japan |
| Tel +81-463-82-4751 | FAX +81-463-82-9627 | |

 法),アルカリフォスファターゼ活性(ρ-ニトロフェニルリン酸基質法),GOT 活性(SSCC 法),GPT 活性(SSCC 法),LDH 活性(Wroblews-LaDue 法),コリンエステラーゼ活性(DTNB 法),カルシウム濃度(OCPC 法),無機リ濃度(モリブデン酸直接法),トリグリセライド濃度(GPO・DAOS 法),γ-GTP(γ-グタミル-3-カルボキシ-ρ-ニトロアニリド基質法),A/G 比(総蛋白濃度およびアルブミン濃度より算出)を測定した.なお,赤血球のコリンエステラーゼ活性の測定は,血液生化学検査用に採血した血液を使用し,Pilz の方法を参考にして,まず,全血 0.25 ml を 0.9% NaCl 10 ml で3回洗い,洗浄した赤血球に精製水 5 ml を加え溶血させ遠心後,上清についてコリンエステラーゼ活性およびヘモグロビン濃度を測定した.赤血球のコリンエステラーゼ活性は,ヘモグロビンあたりの活性として表示した.また,全自動電解質分析装置 EA05(A&T)により,ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法)を測定した.
法),アルカリフォスファターゼ活性(ρ-ニトロフェニルリン酸基質法),GOT 活性(SSCC 法),GPT 活性(SSCC 法),LDH 活性(Wroblews-LaDue 法),コリンエステラーゼ活性(DTNB 法),カルシウム濃度(OCPC 法),無機リ濃度(モリブデン酸直接法),トリグリセライド濃度(GPO・DAOS 法),γ-GTP(γ-グタミル-3-カルボキシ-ρ-ニトロアニリド基質法),A/G 比(総蛋白濃度およびアルブミン濃度より算出)を測定した.なお,赤血球のコリンエステラーゼ活性の測定は,血液生化学検査用に採血した血液を使用し,Pilz の方法を参考にして,まず,全血 0.25 ml を 0.9% NaCl 10 ml で3回洗い,洗浄した赤血球に精製水 5 ml を加え溶血させ遠心後,上清についてコリンエステラーゼ活性およびヘモグロビン濃度を測定した.赤血球のコリンエステラーゼ活性は,ヘモグロビンあたりの活性として表示した.また,全自動電解質分析装置 EA05(A&T)により,ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(イオン電極法)を測定した.
 の方法で多重比較を行った.一方,分散が一様でない場合は Kruskal-Wallis の順位検定を行い,有意(有意水準:5%)ならば Dunnett 型あるいは Scheff
の方法で多重比較を行った.一方,分散が一様でない場合は Kruskal-Wallis の順位検定を行い,有意(有意水準:5%)ならば Dunnett 型あるいは Scheff 型の方法で多重比較を行った.また,試験群が溶媒対照群を含め2群となる場合には,溶媒対照群と被験物質投与群の各平均値の差の検定は,等分散であれば Student のt検定,不等分散であれば Aspin-Welch 検定を行った.病理組織検査所見中,溶媒対照群および被験物質投与群の双方に共通してみられ,被験物質投与群で頻度,程度が増強している所見については,Mann- Whitney U test および Fisher exact test を行った.
型の方法で多重比較を行った.また,試験群が溶媒対照群を含め2群となる場合には,溶媒対照群と被験物質投与群の各平均値の差の検定は,等分散であれば Student のt検定,不等分散であれば Aspin-Welch 検定を行った.病理組織検査所見中,溶媒対照群および被験物質投与群の双方に共通してみられ,被験物質投与群で頻度,程度が増強している所見については,Mann- Whitney U test および Fisher exact test を行った.














