二クロム酸ナトリウム二水和物のラットを用いる単回経口投与毒性試験
Single Dose Oral Toxicity Test of Chromic acid disodium salt dihydrate in Rats
要約
OECD既存化学物質安全性点検に係わる毒性調査の一環として,二クロム酸ナトリウム二水和物を,1群雌雄各5匹のCrj:CD(SD)IGSのラットに,0(対照),100,130,180,240および330 mg/kgの用量で1回経口投与し,その急性期の毒性徴候および概略の致死量について検討した.
死亡は,雄で240 mg/kg以上の群,雌で130 mg/kg以上の群でみられ,LD50値(95 %信頼限界)は雄が252.4 mg/kg(193.3〜339.2 mg/kg),雌が181.0 mg/kg(146.1〜235.2 mg/kg)と推定された.
一般状態の観察では,生存例で自発運動の低下,緩徐呼吸,軟便,肛門周囲の汚れおよび腹部膨満が認められ,死亡例では前述の症状に加えて流涙,チアノーゼおよび腹臥位が認められた.
体重は,全ての被験物質投与群で増加抑制が認められ,240および330 mg/kg群では減少も認められた.
病理学検査では,死亡例で肉眼的にみられた腺胃粘膜の暗赤色化で組織的に潰瘍がみられた.また,肉眼的にみられた肺の暗赤色化で組織的に水腫またはうっ血が認められ,さらに肉眼的に気管内の泡沫状液体貯留および肺の収縮不全を伴っていた.生存例の雄では,肉眼的にみられた胃の境界縁の肥厚で組織学的に前胃および腺胃の潰瘍ならびに境界縁の扁平上皮細胞の過形成がみられた.生存例の雌ではいずれの器官においても肉眼的変化は認められなかった.
方法
1. 被験物質および媒体
二クロム酸ナトリウム二水和物(日本化学工業(株)(山口),ロット番号10205K1,純度100.07 wt%)は橙黄色の結晶性粉末である.被験物質は室温で保存し,試験期間中安定であったことを確認した.投与液の調製は投与6日前に行い,被験物質を日本薬局方 注射用水((株)大塚製薬工場(徳島),ロット番号1F77N)で溶解させ,投与日まで冷蔵,暗所下で保存した.なお,投与開始前に投与液の濃度が規定範囲内にあることを確認した.また,投与液は冷蔵,暗所下で8日間安定であることを確認した.
2. 使用動物および飼育条件
5週齢のCrj:CD(SD)IGSラット(日本チャールス・リバー(株))を6日間検疫馴化したのち,6週齢で試験に使用した.群分けは,投与前日に当日の体重を基に層別連続無作為化法で行った.投与日の体重は,雄が161.3〜187.9 g,雌が119.9〜137.8 gであった.
動物は,温度24 ± 2 ℃,湿度55 ± 10 %,照明12時間(午前7時〜午後7時)および換気回数13〜15回/時に設定したバリアーシステム飼育室で床敷(ホワイトフレーク,日本チャールスリバー(株))を入れたポリカーボネイト製ケージに,1ケージ当たり2〜3匹ずつ収容して飼育した.飼料は高圧蒸気滅菌処理した固型飼料(CRF-1,オリエンタル酵母工業(株))を,飲水は次亜塩素酸ナトリウムを添加(約2 ppm)した井戸水を給水瓶によりそれぞれ自由に摂取させた.
3. 投与量および投与方法
投与量は,予備試験(20,40,70,100,200および300 mg/kg,雌雄各3匹/群)の結果,300 mg/kg群の雌雄で自発運動の低下,緩徐呼吸などがみられ,雌雄全例が死亡した.また,200 mg/kg群の雌雄では自発運動の低下,緩徐呼吸などがみられ,雌雄各1例が死亡した.100 mg/kg以下の群には一般状態および体重ともに異常はみられなかった.したがって,本試験では明らかな毒性が発現すると予想される330 mg/kgを高用量とし,以下公比約1.35で除した240,180,130および100 mg/kgを設定した,媒体を投与する対照群を加えて計6群とし,1群当たりの動物数は各群とも雌雄各5匹とした.
投与経路は,経口とし,約18時間絶食させた動物に胃管を用いて1回強制投与した.投与容量は10 mL/kgとし,各動物の投与液量は投与日の体重を基に算出した.対照群には同容量の媒体を投与した.
4. 観察および検査
1) 一般状態観察
観察期間は投与後14日間とし,投与日(投与0日)は投与後8時間まで経時的に,投与後1日から13日は午前および午後の1日2回,投与後14日は午前中に1回,一般状態の観察および生死の確認を行った.
2) 体重測定
投与日の投与前(投与0日),ならびに投与後1,3,5,7,10および14日に測定した.
3) 病理学検査
投与日および観察期間中に死亡した動物は発見後速やかに,また,観察期間終了後の生存動物はエーテル麻酔下に放血致死させたのち剖検した.
肉眼的に異常が認められた肺,気管,胃および胸腺は摘出し,10 %中性緩衝ホリマリン溶液に固定した.さらに,肺,胃および胸腺については被験物質に起因した変化と判断し,代表例を常法に従ってパラフィン切片を作製し,ヘマトキシリン・エオジン(HE)染色を施して光学顕微鏡下で観察した.
5. 統計解析
投与後14日間の累積死亡動物数から,LD50値をProbit法により算出した.
体重は,各群ごとに平均値と標準偏差を求めた.なお,有意差検定は行わなかった.
結果
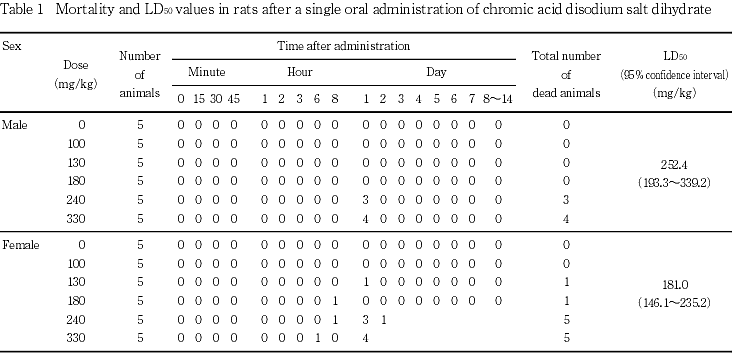
1. 死亡の発生状況およびLD50値(Table 1)
雄では240 mg/kg群で3例,330 mg/kg群で4例が投与後1日に死亡した.雌では130および180 mg/kg群で各1例,240および330 mg/kg群で各5例が投与後6時間から投与後2日に死亡した.LD50値(95 %信頼限界)は雄が252.4 mg/kg(193.3〜339.2 mg/kg),雌が181.0 mg/kg(146.1〜235.2 mg/kg)であった.
2. 一般状態
1) 死亡例
雄では,240 mg/kg群で投与後30分より自発運動の低下,緩徐呼吸,軟便および腹部膨満がみられ,330 mg/kg群では前述の症状に加えて肛門周囲の汚れ,チアノーゼおよび腹臥位が認められ,いずれも投与後1日に死亡した.
雌では,130 mg/kg群で投与後6時間より自発運動の低下が認められ,投与後1日に死亡した.180 mg/kgでは投与後30分より自発運動の低下,緩徐呼吸,軟便,肛門周囲の汚れ,流涙およびチアノーゼが認められ,投与後8時間に死亡した.240 mg/kg群では投与後30分より自発運動の低下,緩徐呼吸,軟便および肛門周囲の汚れが認められ,投与後8時間に1例,投与後1日に3例,ならびに投与後2日に1例が死亡した.330 mg/kg群では投与後15分より240 mg/kg群の症状に加えて腹部膨満が認められ,投与後6時間に1例,投与後1日に4例が死亡した.
2) 生存例
雄では,100 mg/kg群の1例および130 mg/kg群の2例で投与後45分より60分まで軟便が認められた.180 mg/kg群では全例で何ら異常は認められなかった.240 mg/kg群の1例では投与後30分より投与後8時間まで自発運動の低下がみられ,投与後6時間には緩徐呼吸も認められた.投与後1日には自発運動の低下および腹部膨満が認められ,自発運動の低下は投与後3日まで観察された.240 mg/kg群の他の1例では投与日および観察期間を通して何ら異常は認められなかった.330 mg/kg群では,投与後30分より投与後8時間まで自発運動の低下および緩徐呼吸がみられ,投与後30分に軟便,投与後45分より投与後2時間まで肛門周囲の汚れが認められた.投与後1日には自発運動の低下および腹部膨満が認められ,自発運動の低下は投与後4日まで観察された.
雌では,100 mg/kg群では1例で投与後30分に軟便が認められた.130 mg/kg群では1例で投与後30分に軟便,投与後45分に肛門周囲の汚れがみられ,投与後1日には自発運動の低下が認められたが,投与後2日以降は何ら異常は認められなかった.180 mg/kg群の1例では投与後1日に自発運動の低下が認められたが,投与後2日以降は何ら異常は認められなかった.また,他の2例では投与後30または45分に軟便が認められ,このうち1例では肛門周囲の汚れも認められた.
3. 体重
全ての被験物質投与群で投与後1日に増加抑制が認められた.100,130および180 mg/kg群では投与後3日以降は順調な増加を示した.240および330 mg/kg群の雄各1例では投与後3日に体重減少がみられたが,投与後5日以降は順調な増加推移を示した.
4. 剖検
1) 死亡例
雌雄全例で腺胃粘膜面の暗赤色化,330 mg/kg群の雄4/4例および雌3/5例,240 mg/kg群の雄1/3例および雌3/5例に胃の水様液による膨満が認められた.また,330 mg/kg群の雌1/5例,240 mg/kg群の雄1/3例および雌2/5例,130 mg/kg群の雌1/1例で肺の暗赤色化が認められた.さらに,330 mg/kg群の雄4/4例および雌2/5例,240 mg/kg群の雄1/3例および雌2/5例,180 mg/kg群の雌1/1,130 mg/kg群の雌1/1例で気管内の泡沫状液体の貯留がみられ,これらのうち330 mg/kg群の雄3/4例および雌2/5例,240 mg/kg群の雌2/5例,180 mg/kg群の雌1/1例に肺の収縮不全が認められた.その他,330 mg/kg群の雄2/4例,240 mg/kg群の雄3/3例および雌1/5例に胸腺の暗赤色点が認められた.
2) 生存例
330 mg/kgの雄1/1例および240 mg/kg群の雄1/2例に胃の境界縁の肥厚が認められた.雌では,いずれの動物においても変化は認められなかった.
5. 病理組織学的検査
1) 死亡例
肉眼的に腺胃粘膜面の暗赤色化がみられた130および180 mg/kg群の雌,ならびに240および330 mg/kg群の雌雄で腺胃に軽度の潰瘍が認められた.また,肉眼的に肺の暗赤色化がみられた130 mg/kg群の雌で肺に軽度の水腫がみられ,240 mg/kg群の雌雄および330 mg/kg群の雌で肺に軽度のうっ血が認められた.その他,肉眼的に胸腺に暗赤色点がみられた240 mg/kg群の雌雄および330 mg/kg群の雄で胸腺に軽度の出血が認められた.
2) 生存例
肉眼的に胃の境界縁の肥厚がみられた330 mg/kg群の雄で胃に重度の前胃および腺胃の潰瘍,軽度の境界縁の扁平上皮細胞の過形成がみられ,240 mg/kg群の雄で胃に中等度の腺胃の潰瘍,軽度の境界縁の扁平上皮細胞の過形成が認められた.
考察
Crj:CD(SD)IGSの雌雄ラットを用い,二クロム酸ナトリウム二水和物の経口投与による単回投与毒性試験を実施した.投与量は0(対照),100,130,240および330 mg/kgとした.
雄では,240 mg/kg群で3例,330 mg/kg群で4例が投与後1日に死亡した.雌では,130および180 mg/kg群で各1例,240および330 mg/kg群で全例が投与後6時間から投与後2日に死亡した.したがって,本試験条件下でのLD50値(95 %信頼限界)は,雄が252.4 mg/kg(193.3〜339.2 mg/kg),雌が181.0 mg/kg(146.1〜235.2 mg/kg)と推定された.
死亡例では,一般状態の観察において,雌雄で自発運動の低下,緩徐呼吸,軟便,肛門周囲の汚れ,流涙,チアノーゼ,腹部膨満および腹臥位が認められた.病理学検査では,130および180 mg/kg群の雌,ならびに240および330 mg/kg群の雌雄の胃で肉眼的に腺胃粘膜の暗赤色化,組織学的に潰瘍がみられ,本被験物質の胃粘膜への刺激性が認められた.また,130 mg/kg群の雌,240 mg/kg群の雌雄および330 mg/kg群の雌の肺で肉眼的に暗赤色化,組織学的に水腫またはうっ血が認められ,さらに肉眼的に気管内の泡沫状液体の貯留および肺の収縮不全を伴っていたことから,主な死亡原因は肺水腫に因る呼吸不全と考えられた.その他の変化として,240 mg/kg群の雌雄および330 mg/kg群の雄の胸腺で肉眼的に暗赤色点,組織学的に出血が認められた.この変化は死亡例においてしばしばみられる非特異的な変化であることから,死戦期による変化と考えられた.
生存例では,一般状態の観察において,投与日に雌雄で自発運動の低下,緩徐呼吸,軟便,肛門周囲の汚れおよび腹部膨満が認められ,もっとも遅いもので投与後4日まで観察された.また,病理学検査では,330 mg/kg群の雄で肉眼的に胃の境界縁の肥厚,組織学的に前胃および腺胃の潰瘍ならびに境界縁の扁平上皮細胞の過形成がみられ,死亡例と同様に本被験物質の刺激性が認められた.雌ではいずれの器官においても肉眼的変化は認められなかった.
| 連絡先 |
| 試験責任者: | 本田久美子 |
| 試験担当者: | 中岡靖雄,浜村政夫,平野光浩,和泉宏幸,鍬先恵美子 |
| (株)パナファーム・ラボラトリーズ安全性研究所 |
| 〒869-0425 熊本県宇土市栗崎町1285 |
| Tel 0964-23-5111 | Fax 0964-23-2282 | |
| Correspondence |
| Authors: | Kumiko Honda(Study Director)
Yasuo Nakaoka, Masao Hamamura, Mitsuhiro Hirano, Hiroyuki Izumi, Emiko Kuwasaki |
| Safety Assessment Laboratory, Panapharm Laboratories Co., Ltd. |
| 1285 Kurisaki-machi, Uto-shi, Kumamoto, 869-0425, Japan |
| Tel +81-964-23-5111 | Fax +81-964-23-2282 | |

