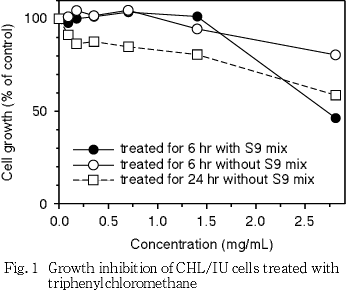
連続処理(24時間)および S9 mix 非存在下の短時間処理(6時間)では,2.8 mg/mL(10 mmol/L)の濃度においても50 %を越える細胞増殖抑制は認められなかった.S9 mix存在下の短時間処理における50 %細胞増殖抑制濃度は,2.7 mg/mLであった.従って,すべての処理群で2.8 mg/mL(10 mmol/L)を最高濃度とし,公比2で5濃度設定した.連続処理では,24時間処理後,短時間処理ではS9 mix非存在下および存在下で6時間処理し,新鮮培地で更に18時間培養後,標本を作製し,検鏡することにより染色体異常誘発性を検討した.染色体分析が可能な最高濃度は,すべての処理群において2.8 mg/mL(10 mmol/L)であったことから,これらの濃度を高濃度群として3濃度群を観察対象とした.
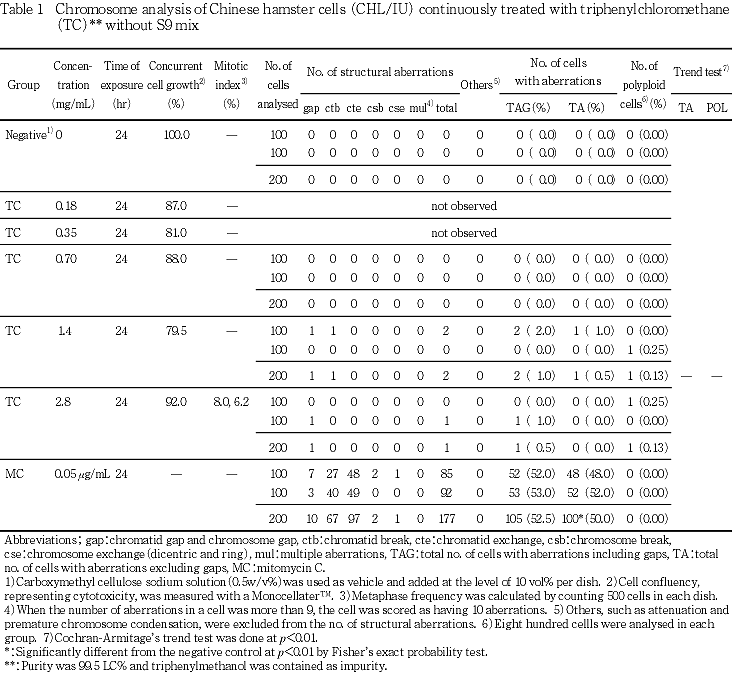
CHL/IU細胞を24時間連続処理した群では,いずれの処理群においても,染色体の構造異常および倍数性細胞の誘発作用は認められなかった.短時間処理では,S9 mix存在下および非存在下で6時間処理したいずれの処理群においても,染色体の構造異常や倍数性細胞の誘発作用は認められなかった.
以上の結果より,本試験条件下でトリフェニルクロロメタンは,染色体異常を誘発しない(陰性)と結論した.
その結果,連続処理およびS9 mix非存在下での短時間処理では,最高処理濃度の2.8 mg/mL(10 mmol/L)においても50 %を越える細胞増殖抑制作用は認められなかった.またS9 mix存在下の短時間処理における50 %細胞増殖抑制濃度は2.7 mg/mLであった(Fig. 1).

染色体異常試験において,溶媒対照群と処理群では1濃度あたり4枚のディッシュを用い,そのうちの2枚は染色体標本を作製し,別の2枚については単層培養細胞密度計により細胞増殖率を測定した.無処理対照群および陽性対照群については細胞増殖率測定は行わなかった.
また,細胞毒性増殖抑制試験において,被験物質処理時および終了時に培養液の黄色化が認められたことから,染色体異常試験において,処理開始時と終了時の処理液のpHを測定した.
作製したスライド標本のうち,1つのディッシュから得られた異なるスライドを,4名の観察者がそれぞれ処理条件が分からないようにコード化した状態で分析した.染色体の分析は,日本環境変異原学会・哺乳動物試験研究会(MMS)1)による分類法に基づいて行い,染色体型あるいは染色分体型のギャップ,切断,交換などの構造異常の有無と倍数性細胞(polyploid)の有無について観察した.また構造異常については1群200個,倍数性細胞については1群800個の分裂中期細胞を分析した.
染色体異常を有する細胞の出現頻度について,溶媒対照群と被験物質処理群および陽性対照群間でフィッシャーの直接確率法2)により,有意差検定を実施した(p<0.01).また,用量依存性に関してコクラン・アーミテッジの傾向性検定3)(p<0.01)を行った.これらの検定結果を参考とし,生物学的な観点からの判断を加味して染色体異常誘発性の評価を行った.
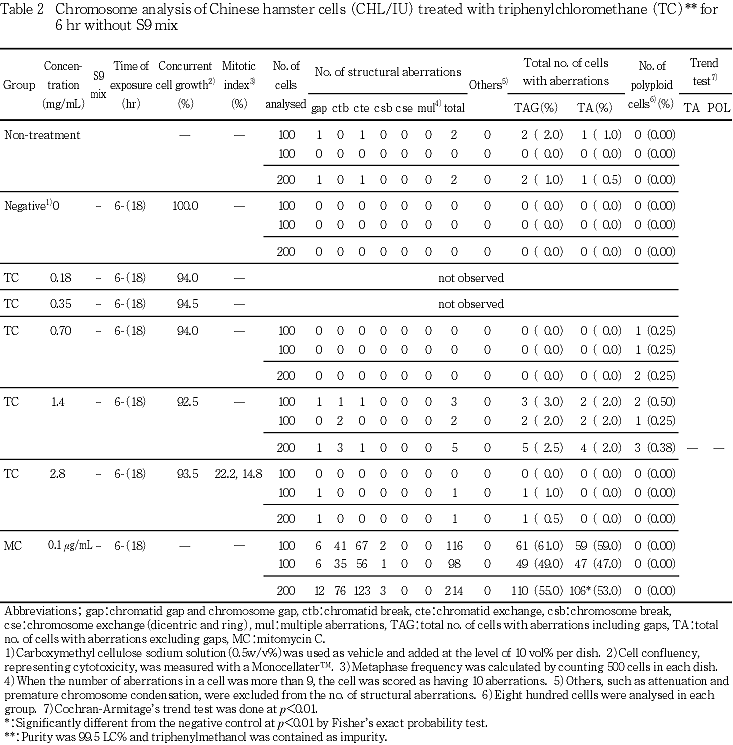
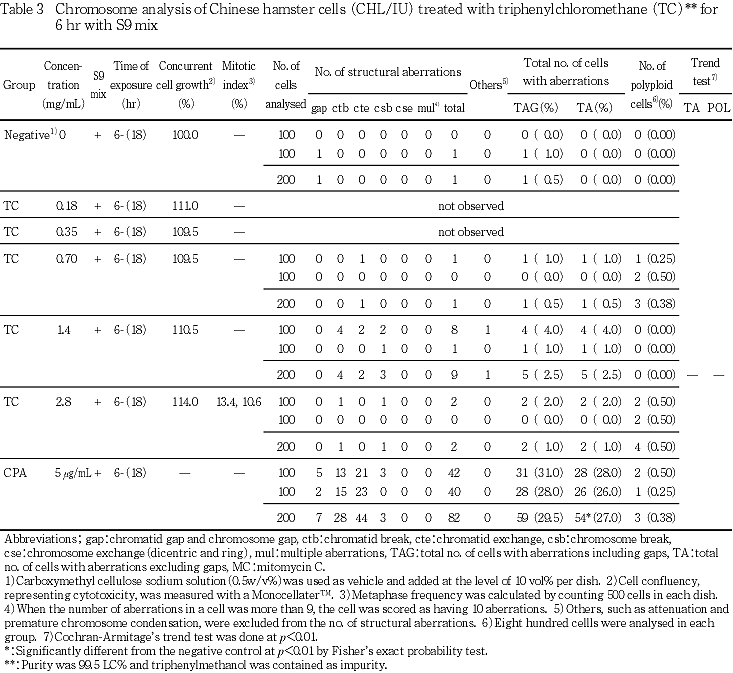
短時間処理による染色体分析の結果をTable 2, 3に示した.トリフェニルクロロメタンを加え,S9 mix非存在下および存在下で短時間処理したいずれの処理群においても,染色体の構造異常および倍数性細胞の誘発作用は認められなかった.また,処理開始時と処理終了時の処理液のpHは,6.50〜7.91であったことから,pHの影響はほとんどなかったと考えられる.
被験物質は,水,DMSOおよびアセトンのいずれにも不溶であったが,これらの溶媒を加えた場合,発熱・発泡や変色等の変化はなかった.また,水による分解は急激ではなく,数日後に分解が認められる程度であるとの提供元からの情報をもとに,被験物質を0.5 w/v% CMC Naに懸濁した場合においても安定であると判断した.しかし,化学分析により溶媒中での安定性を調べた結果,30.0 mg/mLの被験物質懸濁液の調製直後(被験物質に溶媒を加えてから測定までの時間は約30分)の含量は24.1 %,調製1時間後では13.1 %となった(data not shown).また,0.500 mg/mLの懸濁液では調製直後においても検出限界以下で,クロマトグラムよりその殆どが塩素が水酸基に置換したトリフェニールメタノールに変換したと考えられた.今回の試験では,懸濁状態で被験物質を添加していることから,細胞の一部は,被験物質と直接接触していると考えられる.従って,計算値よりも低い濃度ではあるが,未分解物の被験物質に細胞が暴露されていることから,今回の試験結果は,トリフェニルクロロメタンの染色体異常誘発性に関する活性を反映していると考えられる.
本物質に関しては,本試験と併行して細菌を用いる復帰突然変異試験が実施されており陰性の結果が得られていることから5),in vitroでの変異原活性はないものと考えられる.
陽性対照物質として用いたMCは,S9 mix非存在下で短時間処理および24時間連続処理した場合において染色体の構造異常を誘発し(Table 1, 2),CPAはS9 mix存在下で短時間処理した場合において染色体の構造異常を誘発した(Table 3).これらの陽性対照物質の結果より,本実験系の成立が確認された.
従って,トリフェニルクロロメタンは,上記の試験条件下で,試験管内のCHL/IU細胞に染色体異常を誘発しないと結論した.
| 1) | 日本環境変異原学会・哺乳動物試験分科会編,"化学物質による染色体異常アトラス,"朝倉書店,東京,1988, pp.16-37. |
| 2) | 吉村功編,"毒性・薬効データの統計解析,事例研究によるアプローチ,"サイエンティスト社,東京,1987, pp.76-78. |
| 3) | 吉村功,大橋端夫編,"毒性試験講座14,毒性試験データの統計解析,"知人書館,東京,1982, pp.42-43. |
| 4) | T. Morita et al., Mutat. Res., 268, 297(1992). |
| 5) | 原巧,化学物質毒性試験報告,9, 56(2002). |
| 連絡先 | |||
| 試験責任者: | 田中憲穂 | ||
| 試験担当者: | 山影康次,高橋俊孝,渡辺美香,橋本恵子,三枝克彦,加藤初美 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Noriho Tanaka (Study director) Kohji Yamakage, Toshitaka Takahasi, Mika Watanabe, Keiko Hashimoto, Katsuhiko Saegusa, Hatsumi Kato | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano, Kanagawa, 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||