80 mg/kg投与群の雌雄全例に常同行動が認められた他に被験物質投与に起因すると判断された一般状態の異常は認められなかった.体重増加および摂餌量は雌雄ともに80 mg/kg投与群において亢進が認められた.投与38日における雄の尿検査では,性状に異常は認められなかったが,20 mg/kg以上の投与群において比重が低下し,80 mg/kg投与群において尿量が増加してカリウム1日排泄量が増加した.投与31日における雌の新鮮尿の検査では,性状および比重のいずれにも投与の影響は認められなかった.
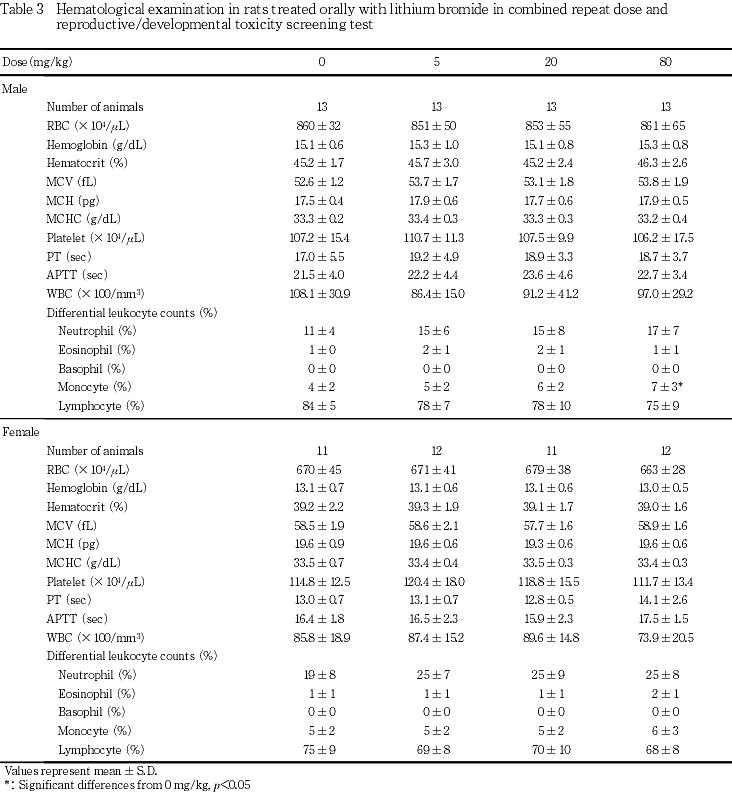
剖検時の血液学検査では,雄では80 mg/kg投与群において白血球百分比における単球の割合が増加した他に,血液凝固時間も含めて投与の影響は認められなかった.雌では血液凝固時間も含めて血液学検査の各項目には投与の影響は認められなかった.雄の血液生化学検査では,20 mg/kg以上の投与群においてクレアチニン濃度が僅かに上昇し,80 mg/kg投与群においてトリグリセリド濃度の上昇,ナトリウム濃度の軽微な低下および塩素濃度の低下が認められた.一方雌では,20 mg/kg以上の投与群においてアルブミン濃度が僅かに低下し,80 mg/kg投与群において尿素窒素濃度およびクレアチニン濃度の軽微な低下および塩素濃度の低下が認められた.器官重量は,雄では20 mg/kg以上の投与群において腎臓の相対重量が低下し,80 mg/kg投与群において下垂体の重量および相対重量が低下した.また,肝臓重量は80 mg/kg投与群において増加したが,雌では,対照群と被験物質投与群との間で有意差は認められなかった.病理学検査では雌雄ともに投与に起因した所見は認められなかった.
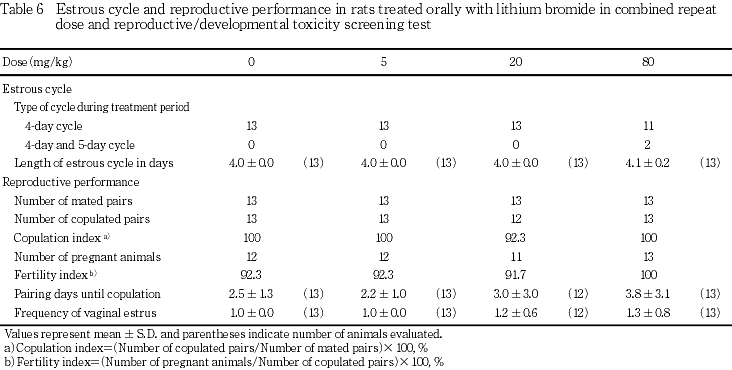
投与に起因すると考えられる分娩状態の異常は認められず,妊娠期間および出産率にも投与の影響は認められなかった.また,妊娠黄体数,着床数,着床率,産児数および分娩率といった出生までの胚および胎児の生存性,ならびに出産生児数,生児出産率,出生率,哺育4日における生存児数,哺育0日および4日における性比ならびに新生児生存率といった出生後の生存性のいずれにも投与の影響は認められなかった.出生児の体重にも投与の影響は認められず,投与に起因すると考えられる形態異常も認められなかった.
以上の試験成績から,本試験条件下における臭化リチウムの無作用量は,反復投与毒性および生殖発生毒性のいずれに関しても,雌雄ともに5 mg/kg/dayと推定され,出生児では80 mg/kg/dayであると推定された.
各濃度の投与検体は,入手物質を秤量して,媒体である日局注射用水(光製薬(株),製造番号:9912ST)で希釈して,いずれの用量においても投与液量が5 mL/kg体重になるように各濃度の投与検体を調製した.投与検体の安定性については,冷蔵,密封条件下における8日間の安定性を確認ているので,1週間に1回以上の頻度で調製し,調製後7日以内に使用した.投与検体中に含まれる被験物質の含量は秦野研究所において確認した.
各動物は,許容温湿度各21.0〜25.0 ℃,および40.0〜75.0 %,換気回数約15回/時間,照明12時間(7〜19時点灯)にそれぞれ制御された飼育室で,金属製金網床ケージに個別に収容し,固型飼料(CE-2,日本クレア(株))および飲料水(水道水,秦野市水道局給水)を自由に摂取させて飼育した.妊娠18日(腟栓あるいは精子発見日=妊娠0日)以後の母動物は,ラット用プラスチック製繁殖ケージに収容し,哺育5日(哺育0日=分娩日)まで紙パルプ製チップ(ペパークリーン,日本エスエルシー(株))を床敷として供給して飼育した.
 法によりクレアチニン濃度を測定し,全自動電解質分析装置EA05(A&T)を用いてイオン電極法によってナトリウムおよびカリウムの各濃度を測定した.また,イオン電極法では塩素濃度は被験物質に由来する臭素と弁別して測定するのが困難なので,イオンクロマト法を採用し,イオンクロマトグラフDX-320(DIONEX)を用いて対照群と高用量群について測定した.
法によりクレアチニン濃度を測定し,全自動電解質分析装置EA05(A&T)を用いてイオン電極法によってナトリウムおよびカリウムの各濃度を測定した.また,イオン電極法では塩素濃度は被験物質に由来する臭素と弁別して測定するのが困難なので,イオンクロマト法を採用し,イオンクロマトグラフDX-320(DIONEX)を用いて対照群と高用量群について測定した.
雌は投与31日に全例を代謝ケージに収容し,約4時間尿を採取して屈折計(ユリコン・アタゴ)を用いて屈折法により尿比重を測定し,雄と同様の方法で,pH,蛋白質,糖,ケトン体,ビリルビン,潜血およびウロビリノーゲンを調べた.
分娩を確認した全例について妊娠期間(妊娠0日〜分娩日の日数)を算定し,出産率[(生児出産雌数/受胎動物数)× 100,%]を各群について求めた.また,哺育1日から毎日,哺育状態を観察し,哺育5日の剖検において数えられた着床数および妊娠黄体数から着床率[(着床数/妊娠黄体数)× 100,%]を算出した.
出生児は,哺育0日に,雌雄別に産児数(生存児+死亡児)を調べ,分娩率[(産児数/着床痕数)× 100,%],生児出産率[(出産生児数/着床痕数)× 100,%]および出生率[(出産生児数/産児数)× 100,%]を算出した.生存児については外表奇形の有無を観察した.翌日(哺育1日)から哺育4日まで毎日一般状態を観察し,生児数と死亡児数を雌雄別に数えて新生児の4日の生存率[(哺育4日の生児数/哺育0日の生児数)× 100,%]を算出した.生存児については,哺育0および4日に個別の体重を測定し,各腹ごとに雌雄別の平均値を算出するとともに哺育0および4日における性比[(哺育0あるいは4日雄生児数/哺育0あるいは4日総生児数)× 100]を算出した.
投与42日に絶食を開始し,その18〜24時間後にペントバルビタールナトリウム麻酔下で腹部後大静脈から抗凝固剤としてクエン酸ナトリウムを用いて血液を採取し,プロトロンビン時間および活性部分トロンボプラスチン時間測定に用いた.次いで,腹部後大静脈から抗凝固剤としてEDTA-3Kを用いて採血し,その他の血液学検査に用いた.さらに,腹部後大静脈から抗凝固剤としてヘパリンを用いて採血し,血液生化学検査に用いた.動物は,採血終了後に放血致死させ解剖し,器官・組織の肉眼観察を行った.また,全例について,脳,下垂体,脊髄,甲状腺および上皮小体,心臓,気管,肝臓,腎臓,胸腺,脾臓,副腎,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,膀胱,下顎リンパ節,腸間膜リンパ節,坐骨神経,大腿骨および骨髄,精巣,精巣上体,前立腺腹葉,凝固腺を含む精嚢および病変部を採取し,脳,心臓,胸腺,肝臓,腎臓,脾臓,副腎,甲状腺,下垂体,精巣および精巣上体の重量を測定し,相対重量を算出した.
採取した器官および組織のうち,精巣ならびに精巣上体はブアン液(長期保存は0.1 Mリン酸緩衝10 %ホルマリン溶液を使用)に固定し,その他は0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.肺は,摘出前に0.1 Mリン酸緩衝10 %ホルマリン溶液を注入してから固定・保存した.
(2) 雌
交尾しなかった例は投与52日に,交尾したが分娩しなかった例については妊娠25日相当日に,また,分娩した例は哺育4日に絶食を開始し,いずれも絶食開始18〜24時間後にペントバルビタールナトリウム麻酔下で雄と同様に採血後,放血致死させ解剖し,器官・組織の肉眼観察を行った.また,全例について脳,下垂体,脊髄,甲状腺および上皮小体,心臓,気管,肝臓,腎臓,胸腺,脾臓,副腎,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,膀胱,下顎リンパ節,腸間膜リンパ節,坐骨神経,大腿骨および骨髄および病変部を採取し,脳,心臓,胸腺,肝臓,腎臓,脾臓,副腎,甲状腺および下垂体の重量を測定し,相対重量を算出した.子宮については着床数を数え,分娩した雌の卵巣については実体顕微鏡下で妊娠黄体数を数えた後,いずれも0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.肺は雄と同様に注入固定を行った.
(3) 出生児
死亡児は発見後速やかに剖検し,0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.生存児は全例を哺育4日にエーテル吸入により致死させ剖検し,0.1 Mリン酸緩衝10 %ホルマリン溶液に固定して保存した.
 法で,ブドウ糖濃度はグルコキナーゼG6PDH法で,総コレステロール濃度はCOD・DAOS法で,トリグリセライド濃度はGPO・DAOS法で,アルカリフォスファターゼ活性(ALP)はGSCC法で,GPTおよびGOT活性はIFCC法で,γ-GTP活性はγ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法で,総ビリルビン濃度はJendrassik/Grof法で,無機リン濃度はモリブデン酸直接法で,カルシウム濃度はOCPC法で測定し,A/G比は算出した.また,全自動電解質分析装置EA05(A&T)を用い,イオン電極法によって,ナトリウムおよびカリウムの各濃度を測定した.塩素濃度の測定は被験物質に由来する臭素イオンを分離して測定するために,イオンクロマトグラフDX-320(DIONEX)を用いてイオンクロマト法により測定した.
法で,ブドウ糖濃度はグルコキナーゼG6PDH法で,総コレステロール濃度はCOD・DAOS法で,トリグリセライド濃度はGPO・DAOS法で,アルカリフォスファターゼ活性(ALP)はGSCC法で,GPTおよびGOT活性はIFCC法で,γ-GTP活性はγ-グルタミル-3-カルボキシ-4-ニトロアニリド基質法で,総ビリルビン濃度はJendrassik/Grof法で,無機リン濃度はモリブデン酸直接法で,カルシウム濃度はOCPC法で測定し,A/G比は算出した.また,全自動電解質分析装置EA05(A&T)を用い,イオン電極法によって,ナトリウムおよびカリウムの各濃度を測定した.塩素濃度の測定は被験物質に由来する臭素イオンを分離して測定するために,イオンクロマトグラフDX-320(DIONEX)を用いてイオンクロマト法により測定した.
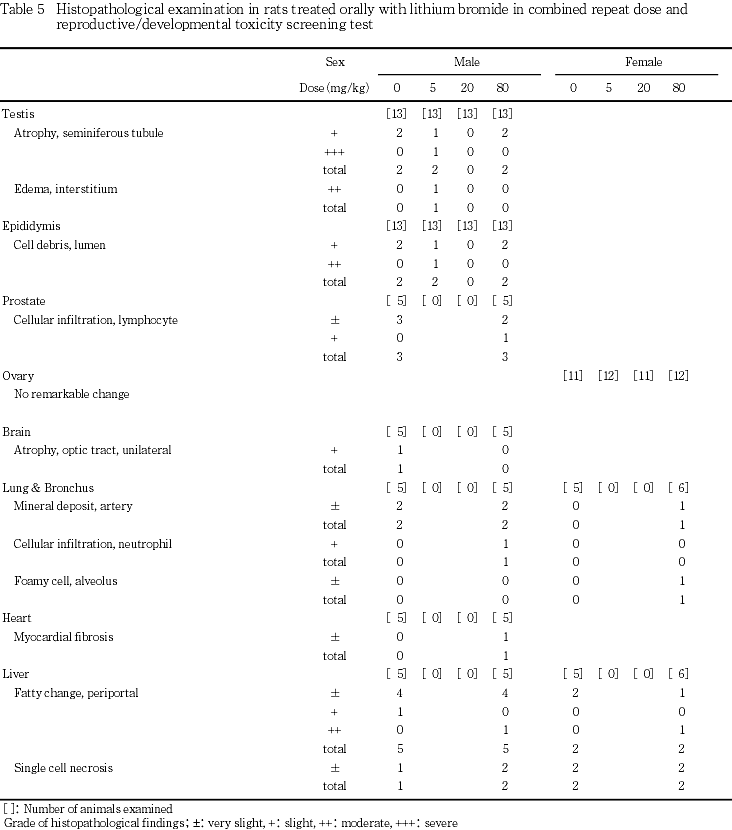
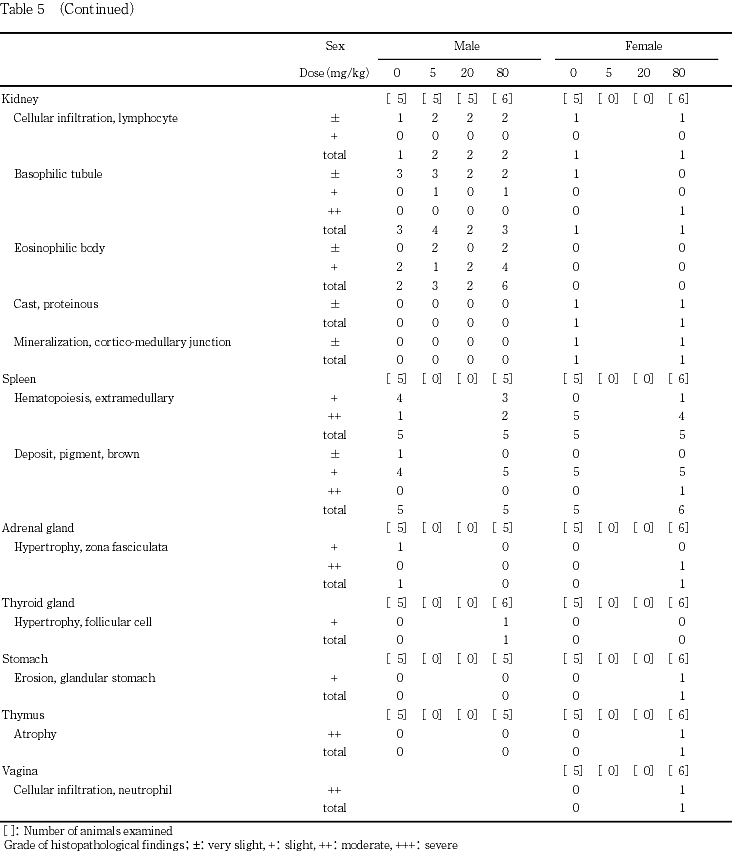
一般状態については,雌雄ともに80 mg/kg投与群において,投与15〜21日の週から,顎を飼育ケージの床に繰り返し摩り付けるという常同行動を示す例が認められるようになり,投与22〜35日の週をピークとして雄では全例に,雌では13例中12例に観察された.この他に,80 mg/kg投与群の雌の1例は,哺育1日に全出生児が死亡し,哺育2日から紅涙が観察されるようになり,翌日から削痩が認められた.哺育4日には排便が認められなくなり,自発運動の減少も認められた.さらに剖検日の哺育5日には自発運動の減少は鎮静へと進行した.本例は投与31日における尿検査では異常は認められなかったが,剖検時に実施した血液生化学検査では血漿中の尿素窒素濃度およびクレアチニン濃度が増加して,ナトリウム濃度およびカリウム濃度が増加し塩素濃度は低下していた.また,血液学検査ではヘマトクリット値が増加して血液の濃縮が認められ,腎臓の病理組織学検査では好塩基性尿細管が中等度に認められた.このほか,80 mg/kg投与群の雌に脱毛が観察された.
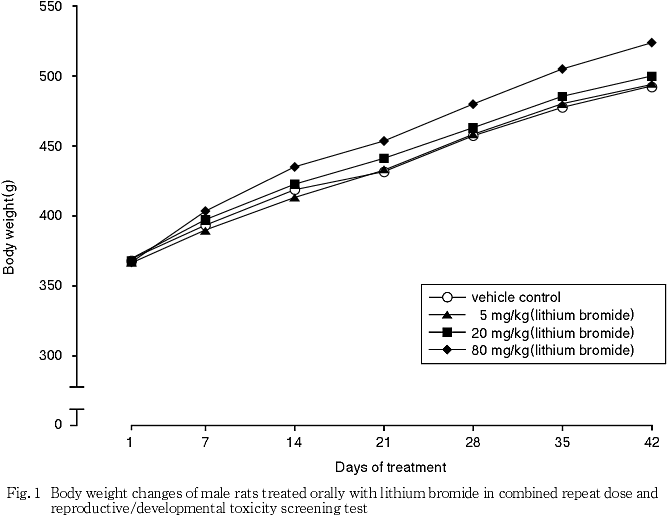
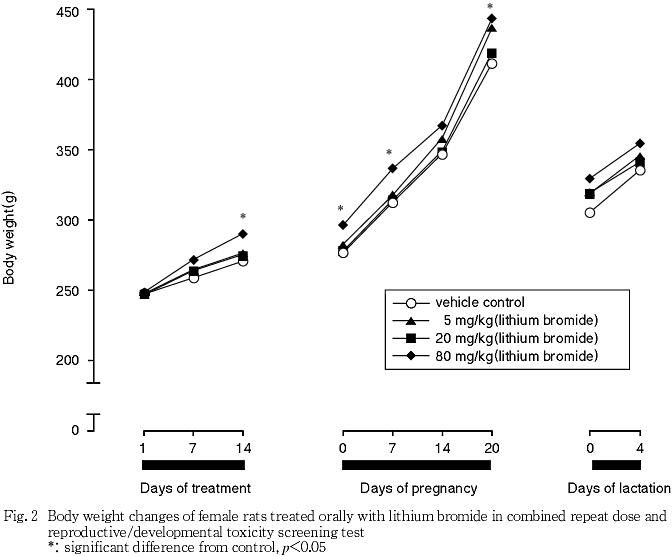
すなわち,雄では,実測値には対照群との間に有意差が認められなかったが,投与1〜7および7〜14日の体重増加量が対照群と比較して有意(p<0.05,p<0.01)な高値を示し,これにより投与期間のいずれの時点においても,累積増加量が対照群と比較して有意(p<0.01)な高値を示した.雌では,投与14日における体重,投与1〜7および7〜14日における増加量,ならびに投与7および14日の各時期までの累積増加量が対照群と比較して有意(p<0.05,p<0.01)に増加し,妊娠0,7および20日の実測値が対照群と比較して有意(p<0.05)な高値を示した.これらの他に,雄では投与14〜21日における体重増加量が全ての被験物質投与群において対照群と比較して有意(p<0.05)な高値を示した.また,雌では,5 mg/kg投与群における妊娠14〜20日の体重増加量および妊娠20までの累積増加量が対照群と比較して有意(p<0.05)な高値を示したが,これらは用量に依存した変化ではなく,被験物質投与に関連しない変化であると判断された.

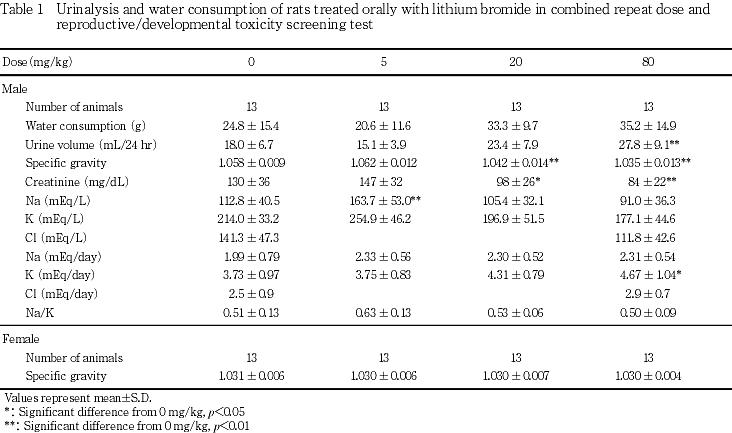
雄における24時間尿の検査では,対照群と比較して,20 mg/kg以上の投与群において尿比重の低下(p<0.01)が認められ,80 mg/kg投与群では尿量が増加した(p<0.01).尿量の増加傾向は20 mg/kg投与群においても認められたが,対照群との間に有意差はなかった.蓄尿の際に測定した飲水量は20 mg/kg以上の投与群において増加する傾向が認められたが,対照群との間に有意差は認められなかった.生化学検査では,20 mg/kg以上の投与群においてクレアチニン濃度の有意(p<0.05,p<0.01)な低下が認められた.電解質濃度については,20 mg/kg以上の投与群においてナトリウム濃度およびカリウム濃度の低下傾向が認められたが対照群との間に有意差はなかった.また,対照群と80 mg/kg投与群について測定した塩素濃度も,80 mg/kg投与群では低値の傾向を認めたが有意差はなかった.ナトリウム濃度は,20 mg/kg以上の投与群では低下する傾向が認められたが,5 mg/kg投与群では対照群と比較して有意(p<0.01)に増加した.尿量からクレアチニンおよび上記電解質の1日排泄量を算出した結果,80 mg/kg投与群においてカリウムの1日排泄量が対照群と比較して有意(p<0.05)に増加した他に対照群と被験物質各投与群との間に有意差は認められなかった.
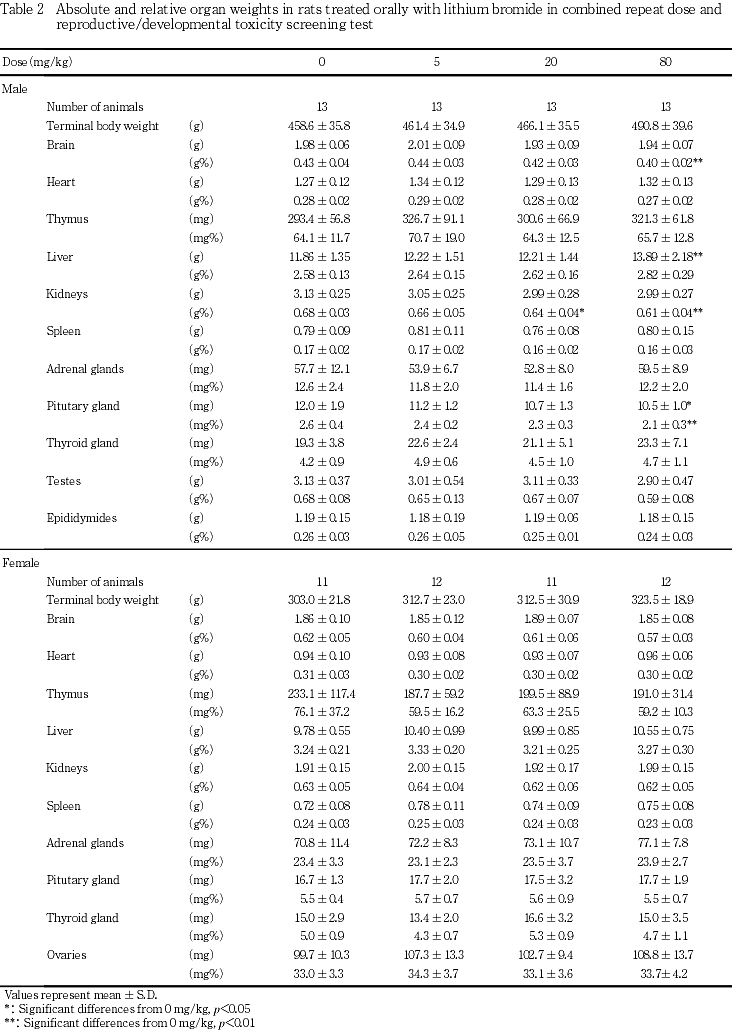
雄では,20 mg/kg以上の投与群において腎臓重量の相対重量が対照群と比較して有意(p<0.05,p<0.01)な低値を示したが,実測値に有意差は認められなかった.また,80 mg/kg投与群では,脳および下垂体の相対重量が対照群と比較して有意(p<0.05,p<0.01)な低値を示したが,実測値は下垂体のみ有意(p<0.05)な低下が認められた.この他,80 mg/kg投与群では肝臓重量が対照群と比較して有意(p<0.01)な高値を示したが,相対重量は対照群との間に差を認めなかった.その他の器官については,実測値および相対重量のいずれも対照群と被験物質投与群との間で有意差は認められなかった.
雌では,実測値および相対重量のいずれについても対照群と被験物質投与群との間に有意差の認められる器官はなかった.
雌では,いずれの検査項目についても対照群と被験物質投与群との間で有意差は認められなかった.
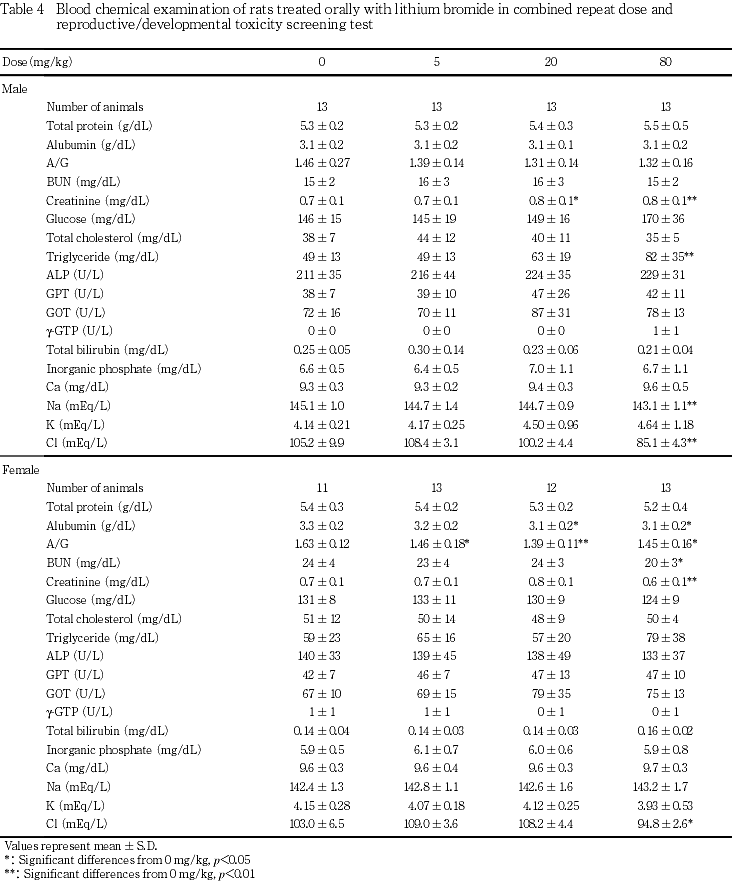
雌では,総蛋白濃度は対照群との間で有意差を認めなかったが,20 mg/kg以上の投与群においてアルブミン濃度が対照群と比較して有意(p<0.05)に低下し,全ての被験物質投与群においてA/G比が有意(p<0.05,p<0.01)な低値を示した.しかし,いずれの項目も変化は僅かであり,A/G比には明瞭な用量依存性は認められなかった.これらの変化の他に,80 mg/kg投与群では対照群と比較して,僅かではあるがクレアチニンおよび尿素窒素の各濃度が有意(p<0.05,p<0.01)に低下した.トリグリセリド濃度,ブドウ糖濃度,総コレステロール濃度および総ビリルビン濃度ならびにアルカリフォスファターゼ,GOT(AST),GPT(ALT),およびγ-GTPの各活性には対照群と被験物質投与群との間で有意差は認められなかった.血漿中電解質濃度については,80 mg/kg投与群において塩素濃度が対照群と比較して有意(p<0.05)に低下したが,無機リン,カルシウム,ナトリウムおよびカリウムの各濃度には対照群と被験物質投与群の間で有意差を認めなかった.
雌では,20 mg/kg 以下の投与群の動物に異常は認められなかった.80 mg/kg投与群では,分娩後に一般状態が不良となった例に肝臓の淡色化,腎臓の淡色域,前胃粘膜の白濁および肥厚,腟内に液体の貯留,胸腺の小型化ならびに副腎の腫大が認められ,別の1例に脱毛が認められた.
80 mg/kg投与群において全出生児の死亡後に全身状態が不良となった雌の例には,肺胞の泡沫細胞,肝臓における門脈周囲性脂肪化,腎臓における好塩基性尿細管,蛋白様円柱および皮髄境界部の鉱質沈着,脾臓における髄外造血および褐色色素の沈着,副腎束状帯の肥大,前胃の糜爛,胸腺の萎縮,ならびに腟の好中球浸潤が観察された.
哺育状態の不良はいずれの投与群の動物にも認められなかった.
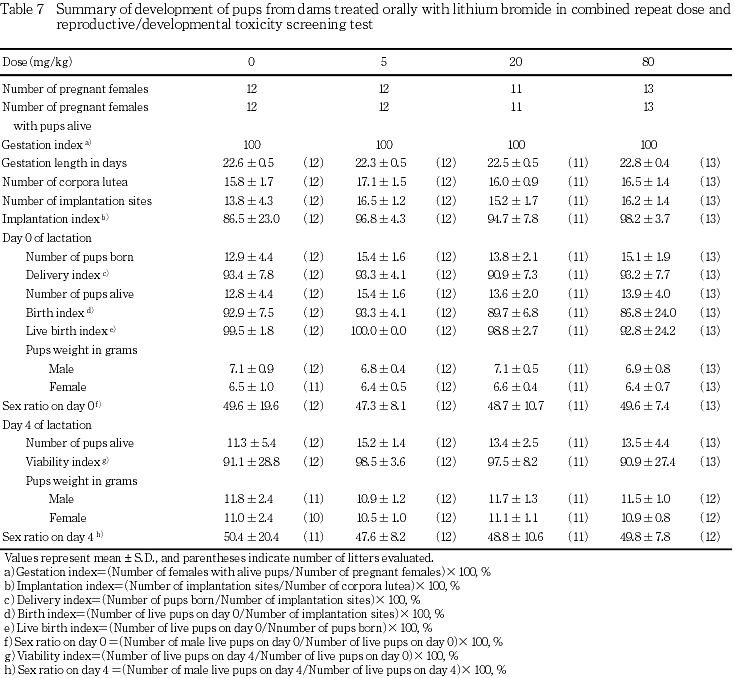
生存性についても,産児数,分娩率,生児出産率,出生率,新生児生存率のいずれにも対照群と被験物質投与群との間で有意差は認められなかった.また,哺育0日および哺育4日における性比にも対照群と被験物質投与群との間で有意差は認められなかった.
体重についても雌雄ともにいずれの時期も対照群と被験物質投与群との間で有意差は認められなかった.
生存産児の形態観察(表には示さず)では,20 mg/kg投与群の1例の出生児3例に,四肢および下腹部皮膚の皮下からの剥離が観察され,その内の1例は右後肢皮下の血腫を伴っていたが,その他の動物に異常は観察されなかった.死亡児の観察では,哺育0日に死亡が認められた20 mg/kg投与群の1例に全身浮腫および口蓋裂が認められた他に異常は観察されなかった.
哺育4日における剖検では,いずれの動物にも異常は観察されなかった.
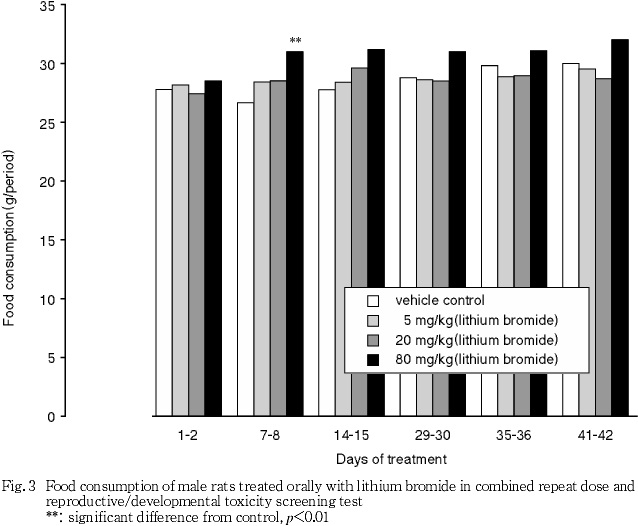
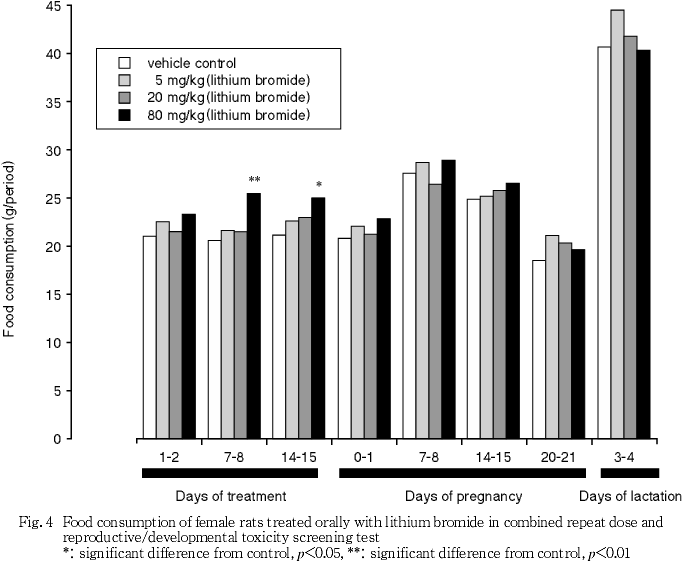
80 mg/kg投与群では雌雄ともに投与初期に摂餌量が増加して体重増加が促進された.急性経口投与毒性試 験2)では,雌において急性期の毒性が回復した後に体重増加が亢進する傾向が認められている.また,ヒトあるいはラットにリチウム塩を投与すると体重が増加する3)ことから,摂餌量および体重増加の亢進は臭化リチウム投与による影響であると考えられる.雄では5 mg/kgおよび20 mg/kg投与群においても投与14〜21日における体重増加が亢進した.体重増加量に用量依存性が認められなかったこと,ならびにこの時期は交配期間中に当たり,特に雄動物では体重の変動が著しいことから,20 mg/kg以下の投与群に認められた体重増加は偶発的変化であると推測された.雌においても5 mg/kg投与群において,妊娠14〜20日の妊娠後期に当たる時期の体重増加に亢進が認められた.妊娠後期の体重は子宮内で発育する胎児の数および体重の影響を大きく受ける.5 mg/kg投与群における着床数および産児数は,有意差は認められないものの対照群に比べて若干多かったことから,5 mg/kg投与群における妊娠後期の体重増加の亢進は,被験物質投与には関連しない変化であると考えられる.
雄において投与38日に実施した24時間尿検査では,20 mg/kg以上の投与群において比重が低下し,80 mg/kg投与群では尿量が増加した.リチウムは,尿細管に影響を及ぼして尿の濃縮能を低下させる薬物のひとつに上げられていること4)から,これらの変化は臭化リチウム投与による影響と考えられる.これらの投与群では,カリウム排泄量が増加または増加傾向を示した.カリウムイオンは遠位尿細管においてナトリウムイオンが再吸収される際に尿中に分泌される.リチウムイオンは生体内でナトリウムイオンと挙動を等しくし,尿細管では競合して作用することが知られている5).尿細管腔のナトリウムイオン濃度が高くなると尿中へのカリウム分泌が亢進することから,臭化リチウム投与により原尿中のリチウムイオン濃度が上昇した動物においてナトリウムイオン濃度が上昇したのと同様の変化が生じたものと推測される.
雄において多尿が認められた20 mg/kg以上の投与群では尿中ナトリウム濃度はむしろ低値の傾向を示したが,尿比重が対照群と同様であった5 mg/kg投与群ではナトリウム濃度が増加した.ナトリウム1日排泄量は対照群と被験物質投与群との間で有意差を認めなかったことから,5 mg/kg投与群に認められた尿中ナトリウム濃度の増加は偶発的変化であると考えられる.
雄において投与43日に実施した血液生化学検査では,20 mg/kg以上の投与群において血漿中クレアチニン濃度が上昇し,ナトリウム濃度が低下した.同時に測定したヘマトクリット値から血液の濃縮はなかったものと考えられる.しかし,変化の程度は僅かであり,投与38日に測定したクレアチニンおよびナトリウムの尿中への1日排泄量に投与の影響は認められていないことから,被験物質投与による影響は否定できないが,軽微な影響と考えられる.また,80 mg/kg投与群において血漿中塩素濃度が低下した.同様の変化は雌においても認められ,被験物質投与による影響であると考えられる.塩素イオンは腎尿細管においてナトリムイオンとともに排泄・再吸収を受けるが,前述のように雄における血漿中ナトリウム濃度の低下は軽微であり,雌ではそうした変化は認められなかったことから,血漿中塩素濃度の低下はリチウムの排泄に付随した変化であると推測される.これらの他に,雄の血液生化学検査では80 mg/kg投与群においてトリグリセリド濃度の増加が認められた.ブドウ糖濃度および総コレステロ−ル濃度には対照群との間で差は認められなかったが,トリグリセリド濃度は用量に依存して増加したことから被験物質投与の影響であると考えられる.
雌では,哺育5日に実施した血液生化学検査において,20 mg/kg以上の投与群のアルブミン濃度が軽度に低下した.投与31日に実施した尿検査では蛋白尿などは認められなかったことから,軽微な変化であると考えられる.また,80 mg/kg投与群では尿素窒素濃度およびクレアチニン濃度も僅かに低下した.血液検査において測定したヘマトクリット値は対照群と同様であったことから,これらの変化は,これらの物質の生成低下,あるいは排泄の増加によるものと考えられるが,その変化は軽微である.これらの他に,全ての被験物質投与群においてA/G比が低下したが,用量に依存した変化ではないことから,被験物質投与の影響である可能性は乏しい.
雌雄動物の病理組織学検査において,いくつかの組織に所見が認められたが被験物質投与に起因すると考えられる変化は認められなかった.
雄では,80 mg/kg投与群において肝臓重量が増加した.相対重量は対照群と有意差を認めなかったこと,病理組織学検査のほかに血液生化学検査においても肝臓機能の異常を示唆する変化は認められなかったことから,被験物質投与により惹起された体重増加に起因した変化であると考えられる.80 mg/kg投与群の雄に認められた脳相対重量の低下も,体重増加によりもたらされた相対的変化であると考えられる.一方,20 mg/kg以上の投与群において腎臓の相対重量が低下した.対照群との間に有意差は認められないが実測値も低下の傾向が認められたことから,これらの投与群における腎臓の相対重量低下は被験物質投与に起因した変化であると考えられる.また,80 mg/kg投与群において下垂体重量の実測値および相対重量がともに対照群と比較して有意な低値を示した.実測値および相対重量のいずれも変化したことから被験物質投与による影響が疑われた.以上の所見に加え,雄では,80 mg/kg投与群において白血球百分比に占める単球の割合が増加した.用量に依存して増加していることから被験物質投与による影響であると考えられる.
受胎率,黄体数,着床数,着床率,産児数および分娩率は対照群と被験物質投与群との間で差は認められず,被験物質投与は,排卵,受胎,着床および出生までの胚・胎児の生存性に影響を及ぼさないものと考えられる.
80 mg/kg投与群の1例に分娩状態の不良が認められ,これにより全出生児が死亡し,母動物の全身状態が悪化した.対照群においても分娩不良,およびそれによると考えられる全出生児の死亡が認められたが,全身状態の異常は認められなかった.80 mg/kg投与群の例では前述のように腎機能の低下が認められており,分娩状態の不良はそれに起因した変化であると考えられる.出産率および妊娠期間にも対照群と被験物質投与群の間で差は認められないことから,被験物質投与は分娩状態に影響を及ぼさないものと考えられる.哺育状態についても投与の影響は認められなかった.
出生児の生存性,体重増加にみる発育,性比に被験物質投与の影響は認められなかった.
出生児の形態観察では,20 mg/kg投与群において生存産児および死亡児の形態異常が各1例の腹に観察された.これらのうち死亡児には全身浮腫を伴う口蓋裂が観察されたが,口蓋裂は本系統のラットでは自然発生すること6),80 mg/kg投与群の産児には形態異常は認められなかったところから,これらの変化は自然発生によるものと考えられる.したがって,被験物質投与は出生児の形態に異常を及ぼさないものと考えられる.
| 1) | "The Merck Index, an encyclopedia of chemicals, drugs, and biologicals," 11th ed., eds. by S. Budavari, M.J. O'Neil, Merck & Co., Inc., Rahway 1989, p.870. |
| 2) | 代田眞理子,化学物質毒性試験報告,10,323(2003). |
| 3) | T. Baptista L. Teneud, Q. Contreras, T. Alastre, J.L. Burguera, E. de Baptista, S. Weiss, L. Hernandez, Pharmacopsychiat. 28, 35(1995). |
| 4) | E. Piperno, "Toxicology of the Kidney," ed. by J.B. Hook, Raven Press, New York, 1981 pp.31-55. |
| 5) | R.A. Goyer, "Casarett and Doull's Toxicology, The Basic Science of Poisons," 5th ed. by C.D. Klaasseen, McGraw-Hill, New York, 1996, pp.691-736. |
| 6) | K. Tago, M. Kuwagara, R. Ohta, M. Sato, H. Takashima, K. Wada, C. Watanabe, M Shirota, "Biological Reference Data on CD(SD)IGS Rats-2001," eds. by Y. Maeda, H. Inoue, CD(SD)IGS Study Group, Yokohama, 2001, pp.111-114. |
| 連絡先 | |||
| 試験責任者: | 代田眞理子 | ||
| 試験担当者: | 田子和美 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | ||||
| Authors: | Mariko Shirota (Study director) Kazumi Tago | |||
| Hatano Research Institute, Food and Drug Safety Center | ||||
| 729-5 Ochiai, Hadano-shi, Kanagawa 257-8523, Japan | ||||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | |||