N-(カルボキシメチル)-N,N-ジメチル-1-ドデカナミニウムはカルボキシベタイン型の両性界面活性剤で,繊維仕上げ剤,化粧品,シャンプー,医薬品,金属イオン封鎖剤等の幅広い分野で使用されている1).毒性情報として,OECD TG423で実施した経口投与による急性毒性試験ではCategory 4(>300-2000)に分類された2).しかし,反復投与および生殖発生毒性についての知見はない.
N-(カルボキシメチル)-N,N-ジメチル-1-ドデカナミニウムを10,60および300 mg/kg/dayの用量でSD系ラット(1群雌雄各12匹,雌はサテライト動物として対照群および300 mg/kg群に各5匹を追加)に交配前14日から交配を経て雄は42日間,雌は妊娠,分娩を経て哺育4日,雌サテライト動物は雄と同様に42日間までそれぞれ経口投与し,反復投与毒性および生殖発生毒性について検討した.
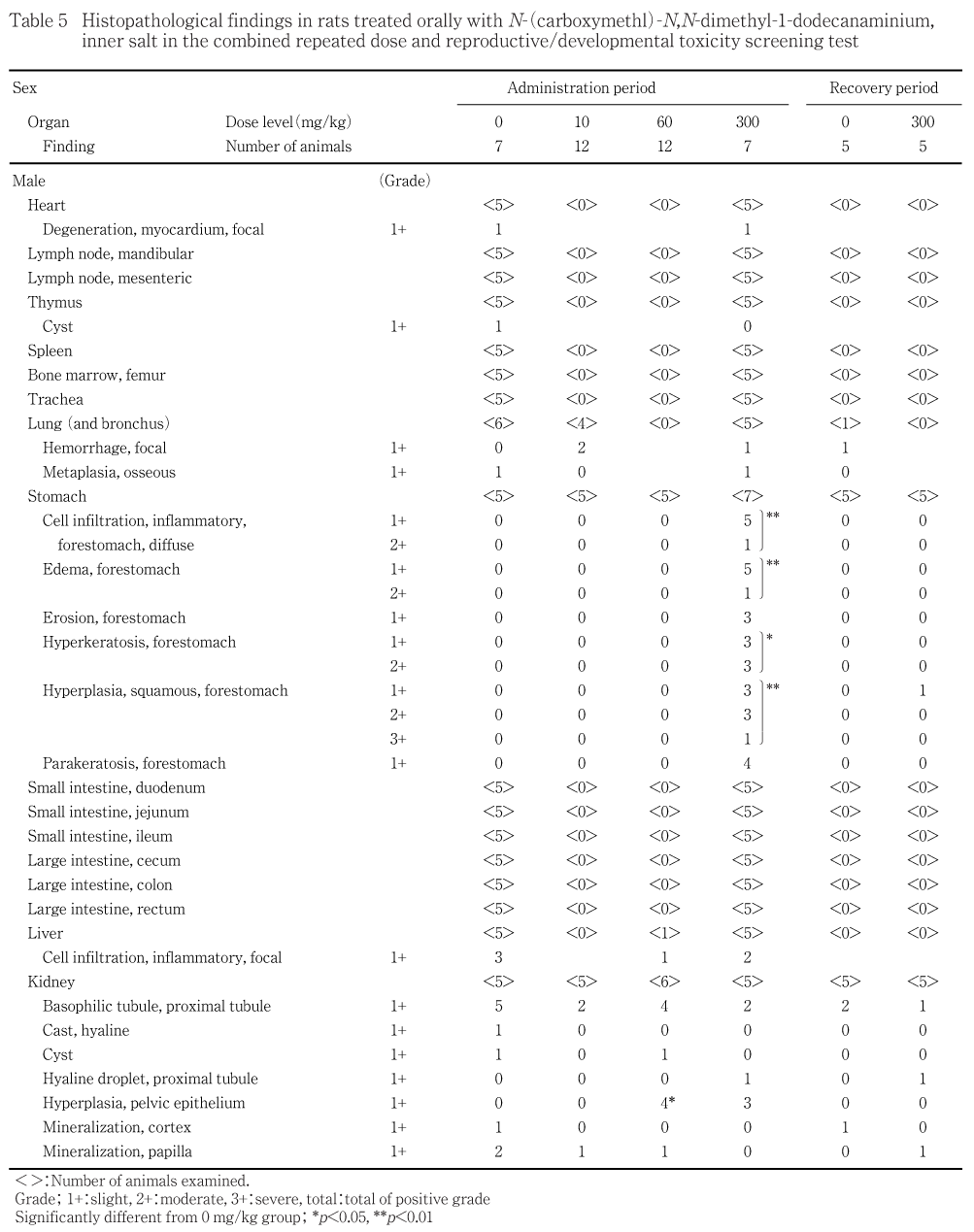
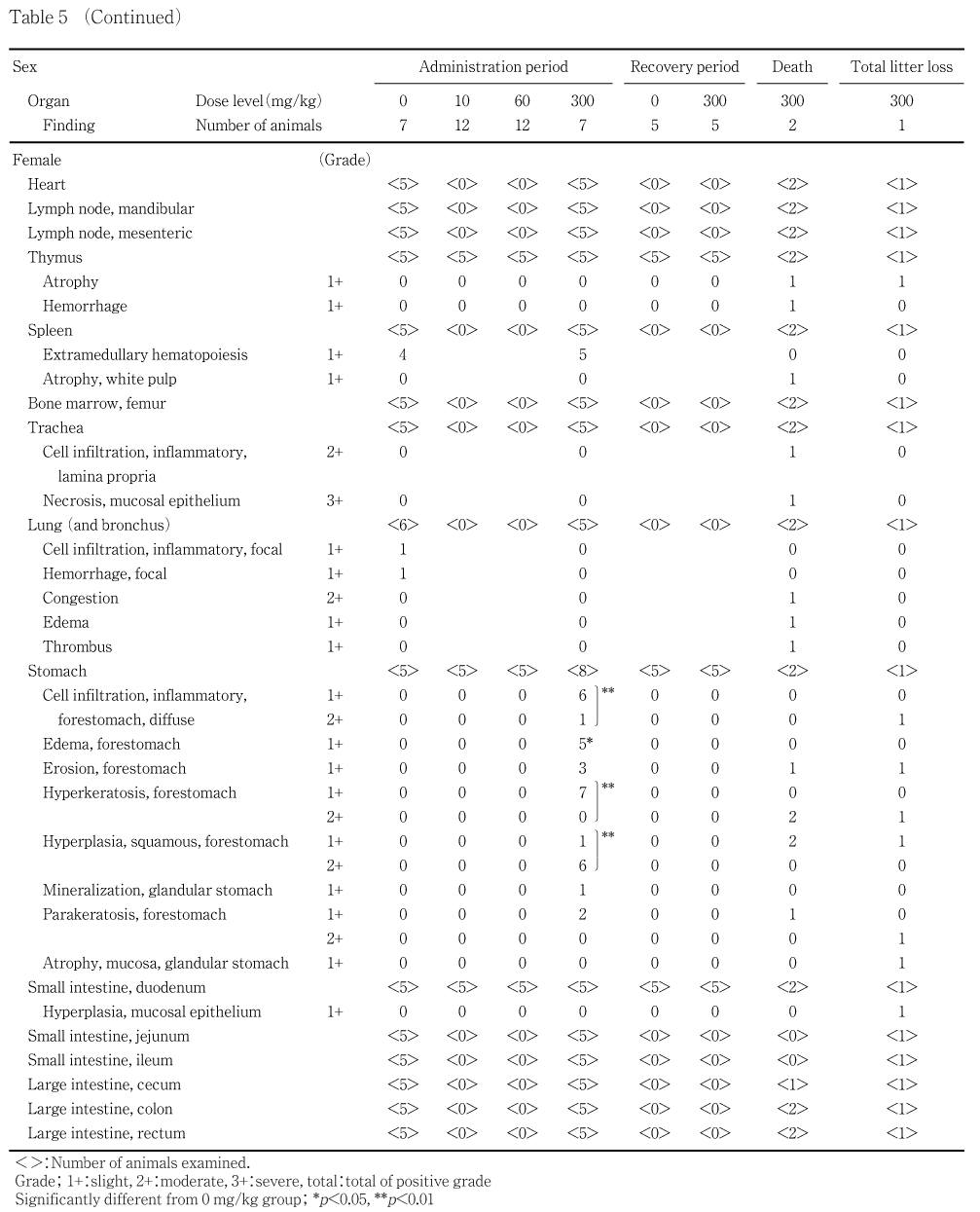
死亡が妊娠20日および23日に各1例,流涎が雌雄全例でいずれも300 mg/kg群で認められた.病理学検査の結果,被験物質に起因する変化として,剖検では前胃粘膜の肥厚,黄色化および隆起巣,組織学検査では扁平上皮過形成,角化亢進,錯角化,び漫性炎症性細胞浸潤,びらんおよび粘膜下織の水腫が300 mg/kg群の雌雄で認められた.また,腎臓の尿細管上皮の壊死および腎盂上皮の過形成,膀胱の粘膜上皮過形成が60および300 mg/kg群の雌雄で認められた.血液生化学検査では,尿素窒素の増加が300 mg/kg群の雌雄で認められた.
投与期間で認められた変化は2週間の回復期間により消失するか,変化がみられても病変程度が明らかに軽減していることから,回復傾向を示しているものと判断された.
全出産児死亡が哺育0日に1例,妊娠期間の延長,出産児数の減少,ならびに出生率の低下が300 mg/kg群で認められた.その他,親動物では性周期,交尾率,受胎率,分娩率,黄体数,着床数および着床率,新生児では性比,新生児の4日生存率,外表,一般状態,体重および剖検のいずれにもに被験物質に起因する変化は認められなかった.
以上の結果から,N-(カルボキシメチル)-N,N-ジメチル-1-ドデカナミニウムの本試験条件下における反復投与毒性に関する無毒性量は雌雄とも10 mg/kg/day,生殖発生毒性に関する無毒性量は雄親動物で300 mg/kg/day,雌親動物ならびに児動物では60 mg/kg/dayと考えられる.
N-(カルボキシメチル)-N,N-ジメチル-1-ドデカナミニウム(花王,東京),ロット番号3047,純度27.1 %は,石油エーテル可溶分0.1 %,乾燥減量65.8 %,強熱残分7.0 %を有する透明液体である.被験物質は室温,暗所,密栓容器にて保存し,試験期間中安定であることを確認した.投与液の調製には,被験物質の有効成分の純度が27.1 %であることから,所定量の3.7倍を秤量し,媒体(日本薬局方注射用水,大塚製薬工場)に溶解させた.投与液中の被験物質の安定性を投与開始前に調製後8日間安定であることを確認した.投与液は投与に供するまで冷蔵・遮光・密栓保存条件下で保存し,調製後7日以内に使用した.また,初回および最終調製時に投与液中の被験物質濃度が設定濃度±10 %以内にあることを確認した.
日本チャールス・リバー(厚木生産所)から入手した雌雄のSD系ラット(Crj:CD(SD)IGS,SPF)を5日間検疫・馴化した.その後も馴化を継続し雌雄の一般状態,さらに雌は性周期を7日間観察し,異常のない動物を試験に供した.投与開始前日に体重層別化無作為抽出法により,1群あたり雌雄各12匹に振り分けた.さらに,雌サテライト動物(回復動物)として対照群および300 mg/kg群に各5匹の雌を追加した.投与開始時の週齢は雌雄とも9週齢,体重範囲は雄318〜381 g,雌が197〜250 gであった.検疫・馴化期間を含む全飼育期間を通じて,温度22 ± 3℃,相対湿度55 ± 20 %,換気約6〜20回/時,照明12時間/日(7:00-19:00)に自動調節した飼育室を使用した.動物飼育には,妊娠・哺育期間を除く期間はステンレス製つり下げ式金網製ケージを,妊娠・哺育期間は実験動物用床敷(ベータチップ,日本チャールス・リバー)を敷いたポリカーボネート製ケージを使用した.交配期間は雌雄各1匹,哺育期間は1腹,検疫・馴化期間を含むその他の期間は1匹ずつ収容した.動物にはオートクレーブ滅菌した実験動物用固型飼料(CRF-1,オリエンタル酵母工業)と,5 μmのフィルター濾過後,紫外線照射した水道水を自由に摂取させた.
投与用量は用量設定試験の結果を参考に決定した.すなわち被験物質を0,30,100,300および1000 mg/kgの用量で,1群雌雄各3匹のSD系ラットに14日間反復経口投与した.その結果1000 mg/kg群の雌雄全例で死亡するか,あるいは瀕死期解剖された.300 mg/kg群では流涎が雌雄の全例,赤血球数の低値が雌,前胃の水腫あるいは肥厚が雌雄に認められた.30および100 mg/kg群では被験物質に起因する変化は認められなかった.これらの結果および本試験の投与期間を考慮し,本試験の高用量は明らかな毒性発現が予想される300 mg/kgとし,以下公比約5で中用量は60 mg/kg,低用量は10 mg/kgの3用量を設定した.また,媒体(日本薬局方注射用水)のみを投与する対照群を設けた.
投与経路は経口とした.投与期間について,雄は交配前14日間および交配期間を経て剖検前日までの計42日間,雌は交配前14日間,交配期間,妊娠期間および分娩を経て哺育4日までとした.分娩しなかった雌は剖検前日までとした.なお,雌サテライト動物は交配は行わず雄と同様に42日間投与した.また,対照群と300 mg/kg群の雄各5匹および同群の雌サテライト動物各5匹は,投与期間終了後14日間の回復期間を設けた.
投与の際はテフロン製胃ゾンデを用いて1日1回,午前中に強制経口投与した.投与液量は4 mL/kgとし,至近日に測定した体重に基づいて算出した.
全例について,生死,外観,行動等を投与前および投与後に毎日観察した.回復動物は1日1回午前中に観察した.
雌雄全例について,詳細な症状観察(ホームケージ内,ハンドリング時,オープンフィールドでの観察)を,投与開始前日に1回,投与期間中は1回/週,いずれも午後に行った.雌雄とも各群5匹を選抜し,機能検査(刺激に対する反応性,握力)および自発運動の測定を,第6週の午後に1回行った.握力はデジタルフォースゲージ(DPS-5),自発運動量にはSUPERMEX(室町機械)を用いて測定した.投与期間中の検査で被験物質の影響が疑われる変化が認められなかったため,回復期間の検査は行わなかった.
雄では第1,4,8,15,22,29,36,42および43日,さらに雄回復動物では第50および56日に測定した.雌サテライト動物は雄と同様の頻度で測定した.雌では第1,4,8および15日,交尾した雌は妊娠0,7,14および20日,分娩した雌は哺育0および4日に測定した.摂餌量は,交配期間を除き体重測定日に測定し,各測定日間の1匹あたりの1日平均摂餌量を算出した.
雄では第42日,雄回復動物および雌サテライト動物では第56日,雌では哺育4日に,全生存動物を午後4時頃より絶食させた.測定対象動物(採血動物)は,雄は5例,雄回復動物および雌サテライト動物は全例,雌は分娩日の順に5例とした.これらの動物は,チオペンタールナトリウムの腹腔内投与による麻酔下で,後大静脈より採血した.採取した血液を用いて以下に示す項目を測定した.
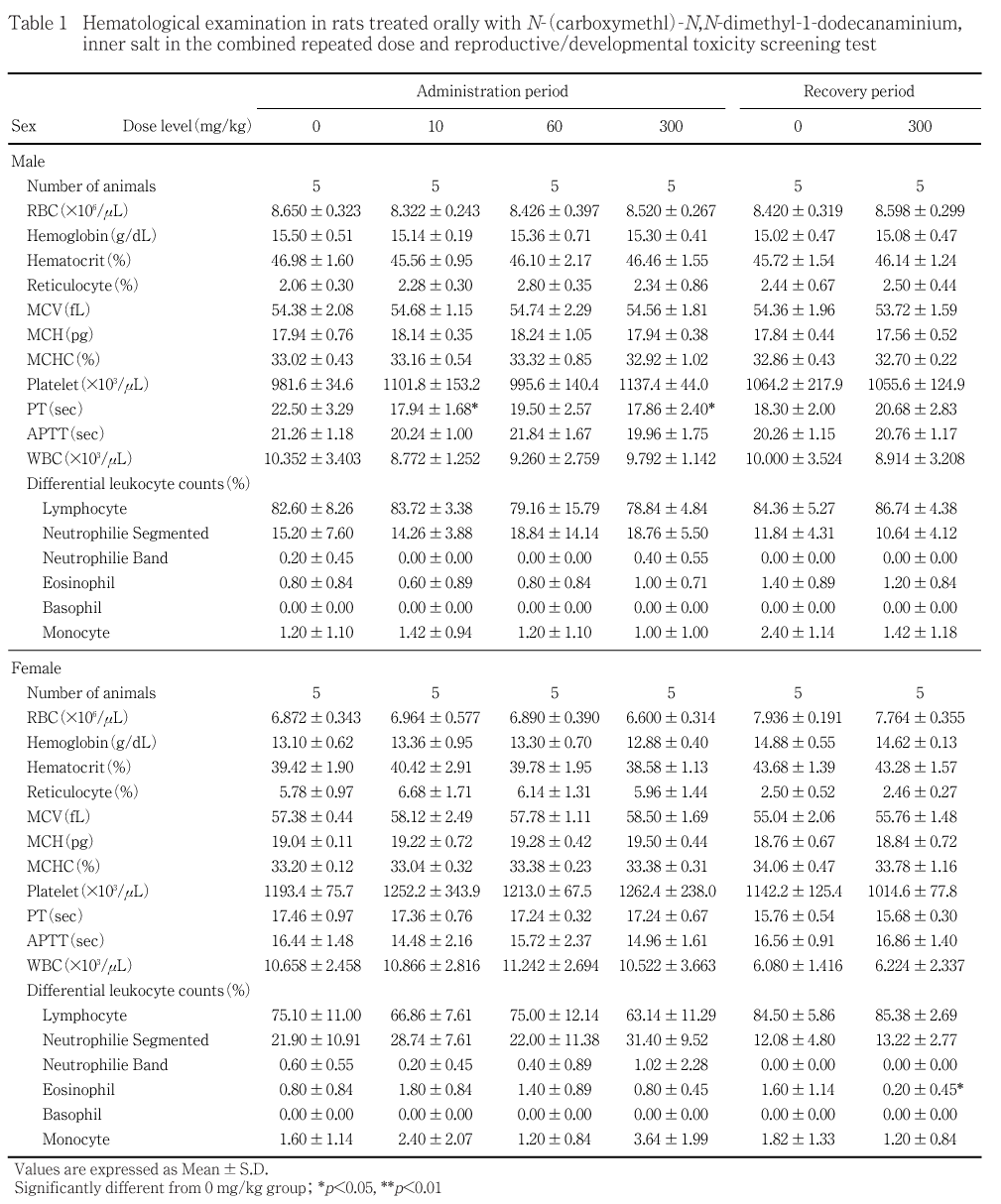
EDTA-2Kにより抗凝固処理し,赤血球数(球状化処理二次元レーザーFCM法),ヘモグロビン濃度(シアンメトヘモグロビン法),ヘマトクリット値(球状化処理二次元レーザーFCM法),網赤血球数(RNA染色によるレーザーFCM法),血小板数(球状化処理二次元レーザーFCM法),白血球数(酸性界面活性剤によるレーザーFCM法)を多項目自動血球分析装置(ADVIA120,バイエル メディカル),白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROX HEG-50,HEG-50 VFオムロン)を用いて測定した.また,検査結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.血液の一部を3.2 w/v%クエン酸三ナトリウム水溶液で抗凝固処理し,遠心分離して得られた血漿を用いてプロトロンビン時間(PT)および活性化部分トロンボプラスチン時間(APTT)(光散乱検出方式)を血液凝固自動分析装置(CA-510,シスメックス)を用いて測定した.
計画解剖日に採取した血液の一部を室温・遮光下で約30分間静置後遠心分離し,得られた血清を用いて以下の項目を測定した.
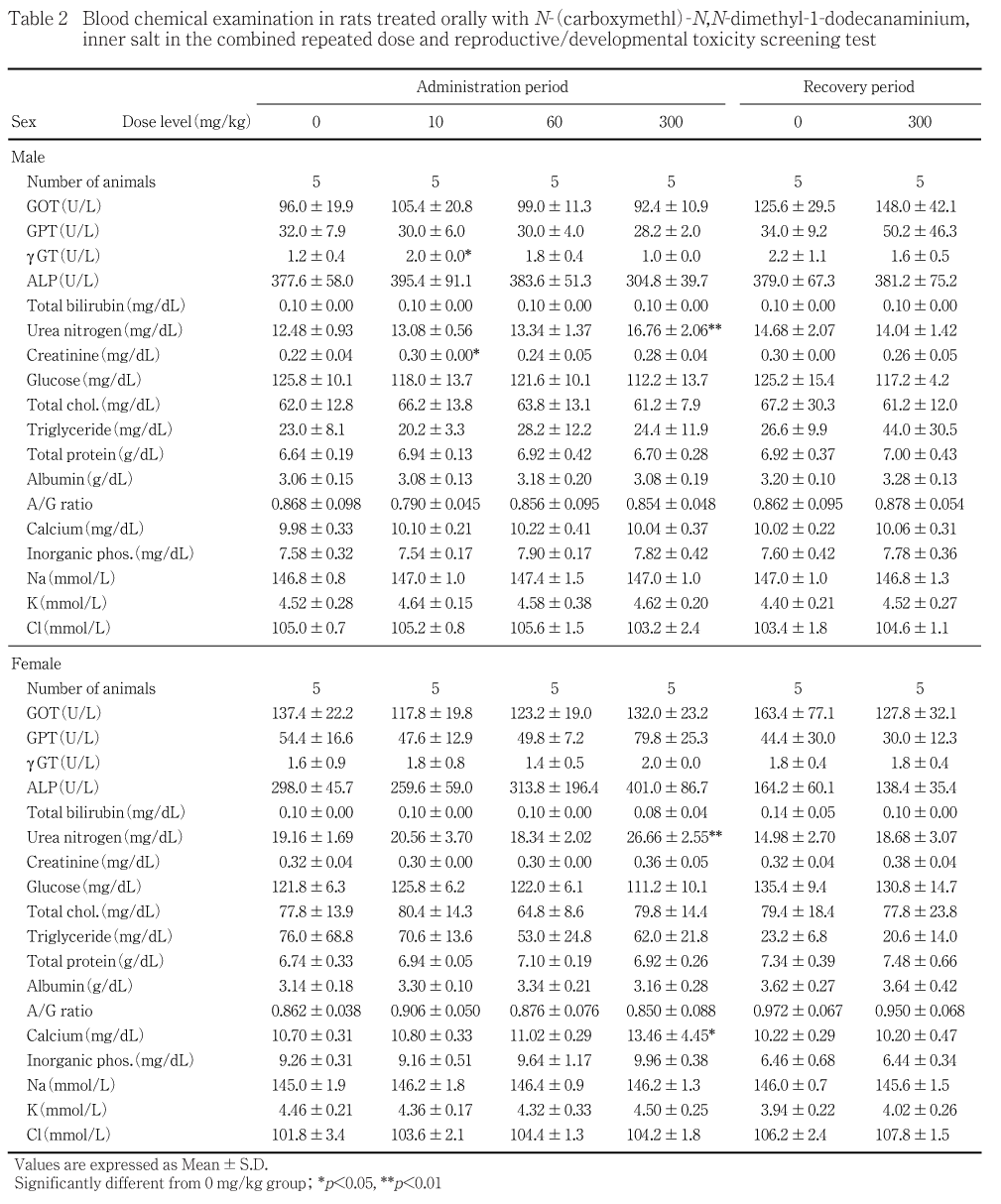
GOTおよびGPT(UV-rate法(JSCC改良法)),g-GT (g-グルタミン-p-ニトロアニリド基質法(SSCC改良法)),ALP(p-ニトロフェニルリン酸基質法(JSCC改良法)),総ビリルビン(酵素法(BOD法)),尿素窒素(酵素-UV法(Urease-LEDH法)),クレアチニン(酵素法(Creatininase-POD法)),グルコース(酵素-UV法(HK-G6PDH法)),総コレステロール(酵素法(CO- HDAOS法)),トリグリセライド(酵素法(GPO-HDAOS法,グリセリン消去法)),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(酵素法(PNP-XOD-POD法)),ナトリウム,カリウムおよびクロール(イオン選択電極法)を自動分析装置(TBA- 200FR,東芝)を用いて測定した.
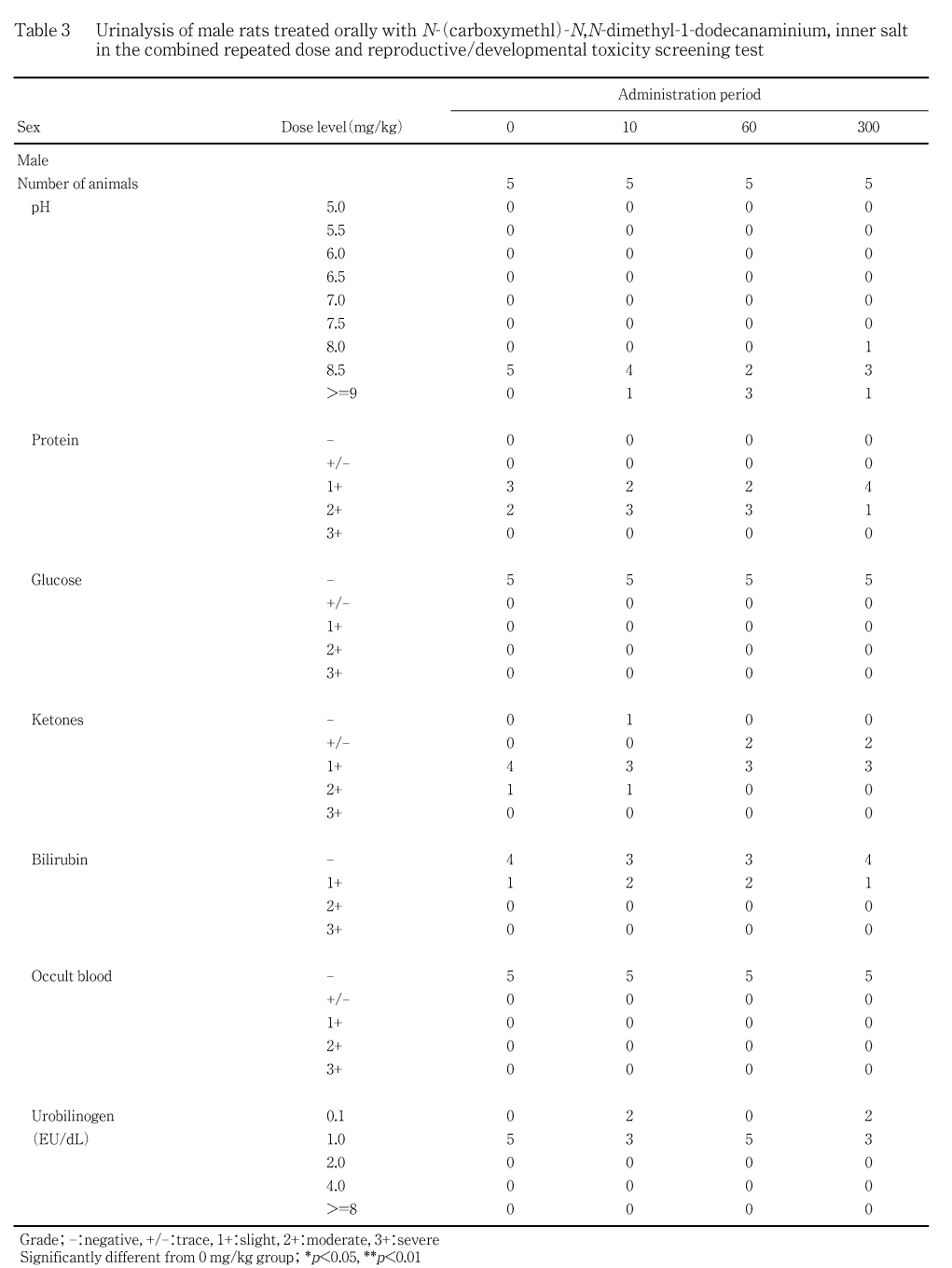
雄について,第38日の投与前に各用量群5匹の新鮮尿を採取し,pH,蛋白,グルコース,ケトン体,ビリルビン,潜血およびウロビリノーゲン(試験紙法,マルティスティックス:バイエルメディカル)を自動尿分析器(クリニテック100,バイエル メディカル)により測定した.被験物質の影響が疑われる変化が認められなかったため,尿沈渣,蓄積尿を用いた検査,回復動物の尿検査は行わなかった.
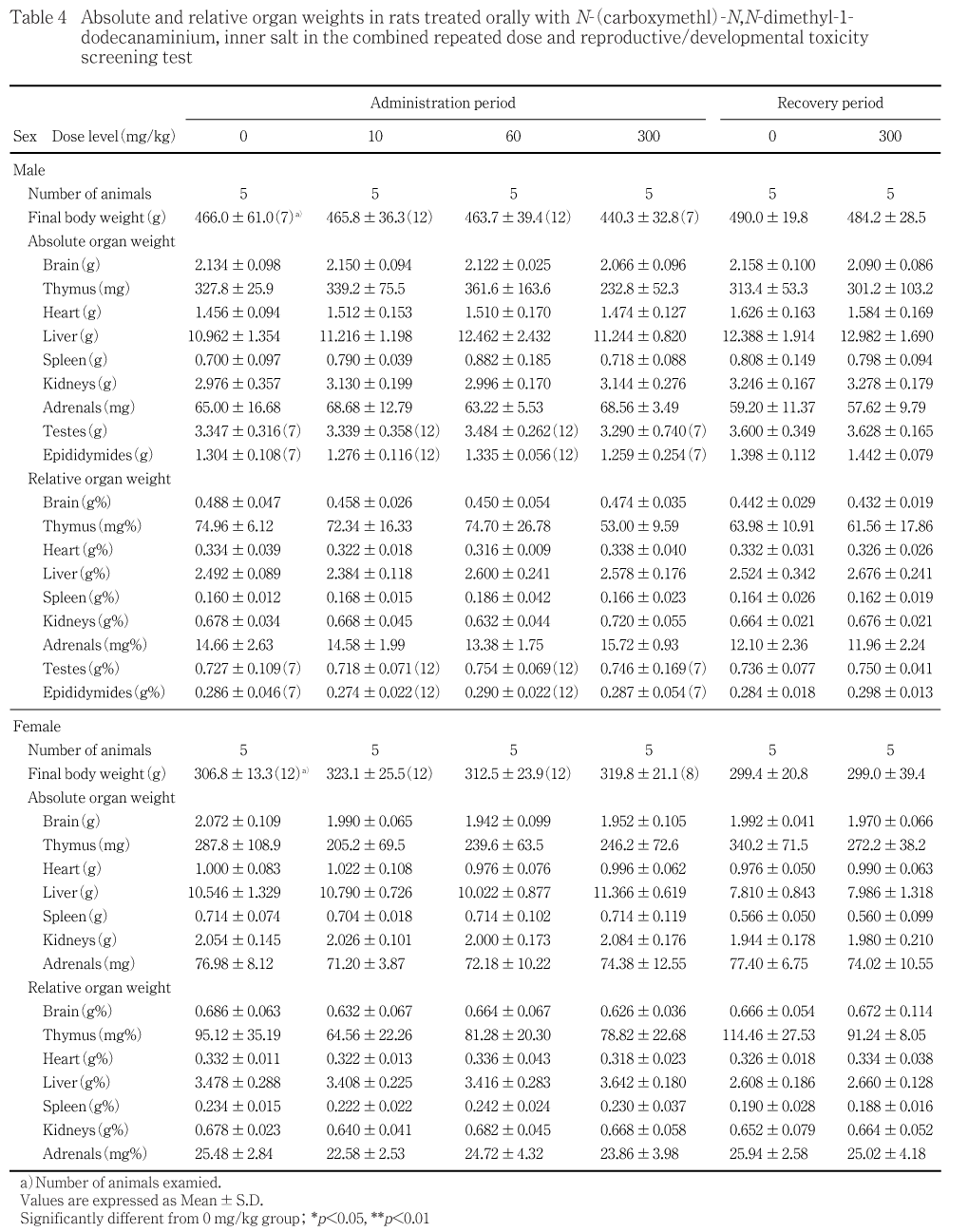
雌雄全例について,解剖日にチオペンタールナトリウムの腹腔内投与による麻酔下で,腹大動脈の切断・放血により安楽死させて解剖した.計画解剖動物のうち,血液学検査の対象動物と同じ雌雄5匹(回復・サテライト動物は全例)の脳,心臓,肝臓,腎臓,副腎,胸腺,脾臓,精巣および精巣上体の重量を測定した.ただし,精巣および精巣上体は雄全例について測定した.また,解剖日の体重を基に相対重量(対体重比)を算出した.さらに雌雄全例については上記の器官に加えて,下垂体,リンパ節(下顎・腸間膜),気管,肺,胃,腸管(十二指腸,空腸,回腸,盲腸,結腸,直腸),甲状腺・上皮小体,膀胱,精のう,前立腺腹葉,卵巣,子宮,膣,骨髄(大腿骨),坐骨神経,脊髄および肉眼的異常部位を採取し,10 v/v%中性リン酸緩衝ホルマリン液で固定して保存した.ただし,精巣および精巣上体はブアン液で固定後,保存した.病理組織学検査は,対照群と300 mg/kg群の投与後解剖動物のうち,雌雄各5例(血液学検査および器官重量測定対象動物と同様)の上記器官,死亡動物および全出産児が死亡した母動物の上記器官,対照群を含む全動物の肉眼的異常部位および非妊娠雌1例の卵巣について,常法に従ってヘマトキシリン・エオジン染色標本を作製し,鏡検した.この結果,被験物質に起因すると思われる変化が雌雄の胃,腎臓,膀胱および雌の胸腺と十二指腸に認められた.このため,10および60 mg/kg群の上述の基準で選択した各5例と回復後解剖動物の雌雄全例の当該器官・組織の検査を行った.
投与開始日から交配開始日まで雌の膣垢を毎日午前中に採取,性周期を検査し,平均性周期日数および異常性周期動物の発現率を算出した.交配前の投与期間終了後,各群内で雄1雌1の交配対を設け,第15日(交配開始日)の16:00頃から4日間昼夜同居させた.交尾確認は毎日午前中に行い,膣栓形成あるいは膣垢標本中に精子が認められた場合を交尾成立とし,その日を妊娠0日とした.交配した対は雌雄を分離し,以後の検査に供した.これらの結果から,交尾所要日数(交配開始後,交尾成立までに要した日数),交尾成立までに逸した発情期の回数,交尾率〔(交尾動物数/同居動物数)×100〕,受胎率〔(受胎動物数/交尾動物数)×100〕を算出した.
交尾が確認された雌は全例を自然分娩させ,分娩状態を観察した.午前9時の時点で分娩が完了している動物を当該日分娩とし,その日を哺育0日とした.交尾確認後25日を経ても分娩しない場合は,非分娩雌とした.分娩した動物は新生児を生後4日(哺育4日)まで哺育させ,授乳,営巣,食殺の有無等の哺育状態を毎日観察した.母動物は剖検時に卵巣および子宮を摘出し,黄体数および着床数を検査した.これらの結果から,妊娠期間(妊娠0日から分娩完了日までの期間),出産率〔(生児出産雌数/受胎雌数)×100〕,着床率〔(着床数/黄体数)×100〕,分娩率〔(総出産児数/着床数)×100〕を算出した.
哺育0日に出産児数(出産生児数,死産児数),性別および外表異常の有無を検査した.その後は,一般状態,死亡の有無を哺育4日まで毎日観察した.哺育0および4日の生存児数から出生率〔(出産生児数/総出産児数)× 100〕,新生児の4日の生存率〔(哺育4日生児数/出産生児数)×100〕を算出した.
生後0および4日に全生存児を個体ごとに測定した.
生後4日に全生存児の口腔を含む外表を検査した後,親動物と同様に安楽死させ,剖検した.死亡動物については10 v/v%中性リン酸緩衝ホルマリン液に浸漬,固定した後,実体顕微鏡下で剖検した.なお,分娩途中で死亡した母動物から出産された新生児のうち,生存していた新生児も同様に安楽死させた後,剖検した.
計量データについて,パラメトリックデータはBartlett法による等分散性の検定を行い,分散が等しい場合は一元配置分散分析を行った.分散が等しくない場合およびノンパラメトリックデータはKruskal-Wallisの検定を行った.群間に有意差が認められた場合はDunnett法またはDunnett型の多重比較を行った.計数データのうち尿検査はKruskal-Wallisの検定を行い,有意差が認められた場合はDunnett型の多重比較を,病理組織所見はWilcoxonの順位和検定で対照群との2群間比較を行った.その他の計数データはFisherの直接確率法により検定した.各検定の有意水準は5 %とした.新生児に関するデータは各母動物ごとに算出した平均値を標本単位とした.
死亡が300 mg/kgの雌で2例,全出産児死亡が同群の1例で認められた.死亡動物の1例は妊娠20日に,他の1例は妊娠22日から分娩を開始し,妊娠23日の分娩途中に死亡した.全出産児死亡の1例は,分娩完了までに2日間(妊娠22日〜24日,難産)を要し,分娩完了時には出産児が全例死亡していたため瀕死期解剖とした.
投与後の症状として,300 mg/kg群では流涎が第7日から観察され,剖検までの間に雌雄全例で認められた.鼻周囲あるいは下腹部の汚れが同群の雌雄各2例でみられ,雌2例の内1例は難産を示した動物,他1例は分娩途中で死亡した動物であった.軟便が300 mg/kg群の雄1例に認められた.
詳細な症状観察,機能検査および自発運動量測定のいずれも被験物質の影響と考えられる変化は認められなかった.
被験物質の影響と考えられる変化は雌雄とも認められなかった.

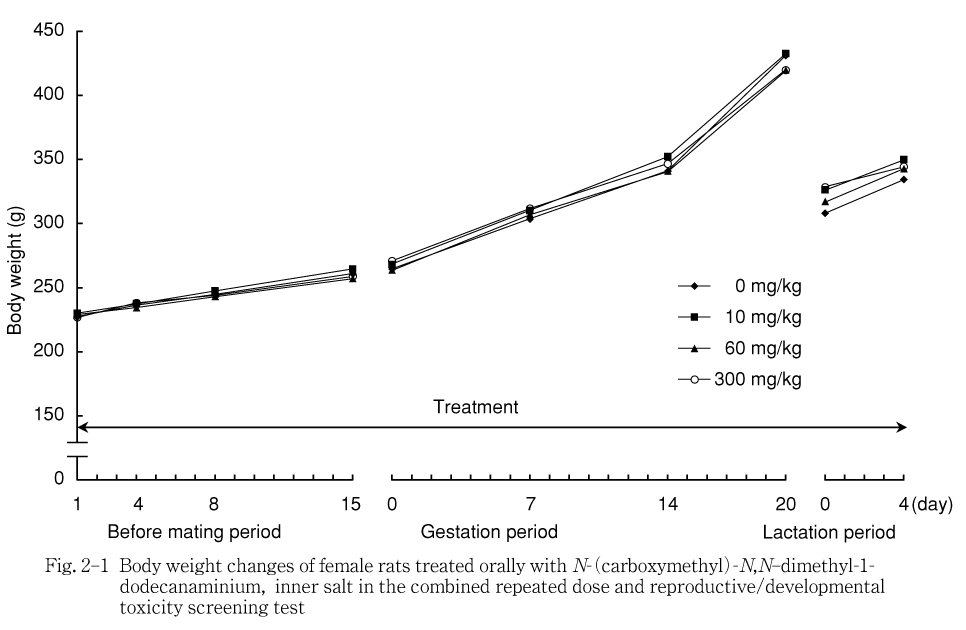
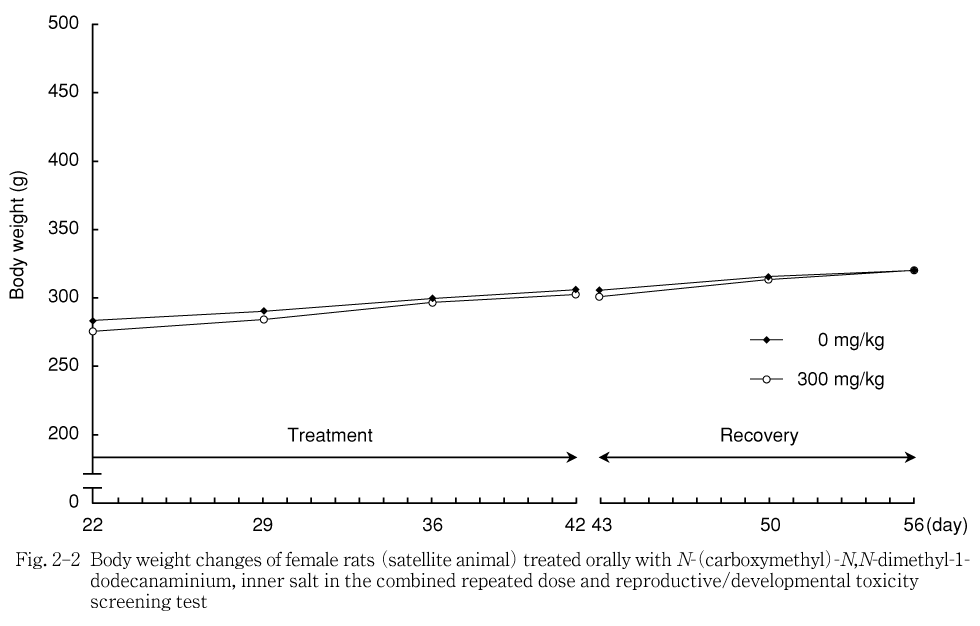
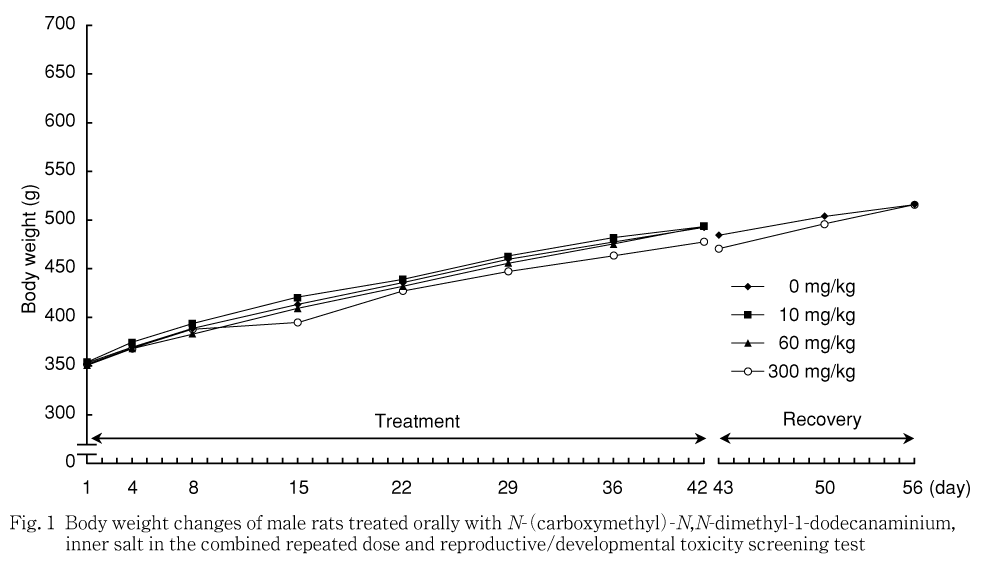
被験物質の影響と考えられる変化は雌雄とも認められなかった.
なお,投与期間では摂餌量の有意な低値が10および300 mg/kg群の雄の第38日に認められたが,60 mg/kg群で変化がないこと,さらに実験期間を通してみると摂餌量の低値は一過性の変化であることから,被験物質に関連するものではないと考えられる.回復期間では摂餌量の有意な高値が300 mg/kg群の雄の第50日にみられたが,投与期間中の摂餌量と同程度と判断され,偶発的な変化と考えられる.雌では投与および回復期間のいずれにも変化は認められず,対照群と同様に推移した.
被験物質の影響と考えられる変化は雌雄とも認められなかった.
10 および300 mg/kg群の雄のプロトロンビン時間が対照群の22.50 secに対し,それぞれ17.94 secおよび17.86 secと有意な低値を示した.しかし,当研究所の背景データ(平均18.51 sec<Min-Max, 17.07-20.50 sec>, 2000-2003年)から,10および300 mg/kg群の値は背景データ内の変動であり,対照群の値が高値を示したものと思われ,被験物質と関連のない偶発的な変化と考えられる.また,300 mg/kg群の雌の回復終了後検査では好酸球比率の有意な低値が認められたが,投与終了後検査では変化がなかったことから,偶発的な変化と考えられる.
被験物質の影響と考えられる変化が,300 mg/kg群の雌雄で尿素窒素の高値,同群の雌でカルシウムの高値が認められた.
投与終了後検査では10 mg/kg群の雄でgGTおよびクレアチニンの有意な高値が認められたが,60および300 mg/kg群では変化がなく用量との関連がないことから,被験物質に起因する変化ではないと考えられる.
被験物質の影響と考えられる変化は認められなかった.
被験物質の影響と考えられる変化は認められなかった.
被験物質の影響と考えられる変化が300 mg/kg群の雌雄の胃に認められた.
前胃粘膜の肥厚が投与後解剖動物の300 mg/kg群で雄7例雌6例に認められた.このうち,雄4例では同部位粘膜の黄色化を伴っていた.前胃粘膜の隆起巣が投与後解剖動物の300 mg/kg群の雌1例で認められた.回復後解剖動物では,これらの変化は認められなかった.
死亡動物の剖検では,投与後解剖動物と同様に前胃粘膜の肥厚が2例に認められた.この他,1例では下垂体の腫大が認められた.全出産児が死亡した動物の剖検では,前胃粘膜の肥厚および胸腺の萎縮が認められた.
生殖器系への変化として,片側性の精巣上体尾部の黄色斑が対照群および60 mg/kg群の雄各1例,片側性の精巣および精巣上体の小型が対照群の雄1例,両側性の精巣および精巣上体の小型が300 mg/kg群の雄1例に認められた.本所見は用量に関係なくみられ,雌との交尾も全例で成立した.ただし,両側性の精巣および精巣上体の小型を示した300 mg/kg群の雄1例の相手雌は受胎しなかった.
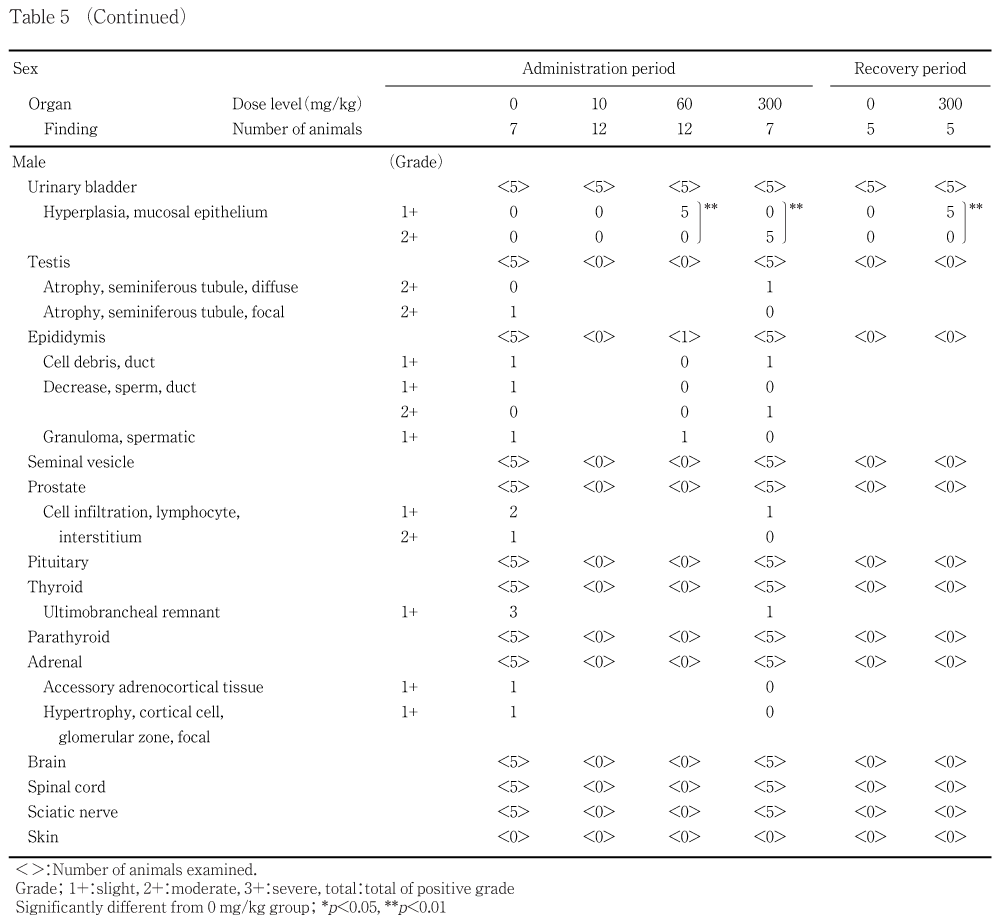
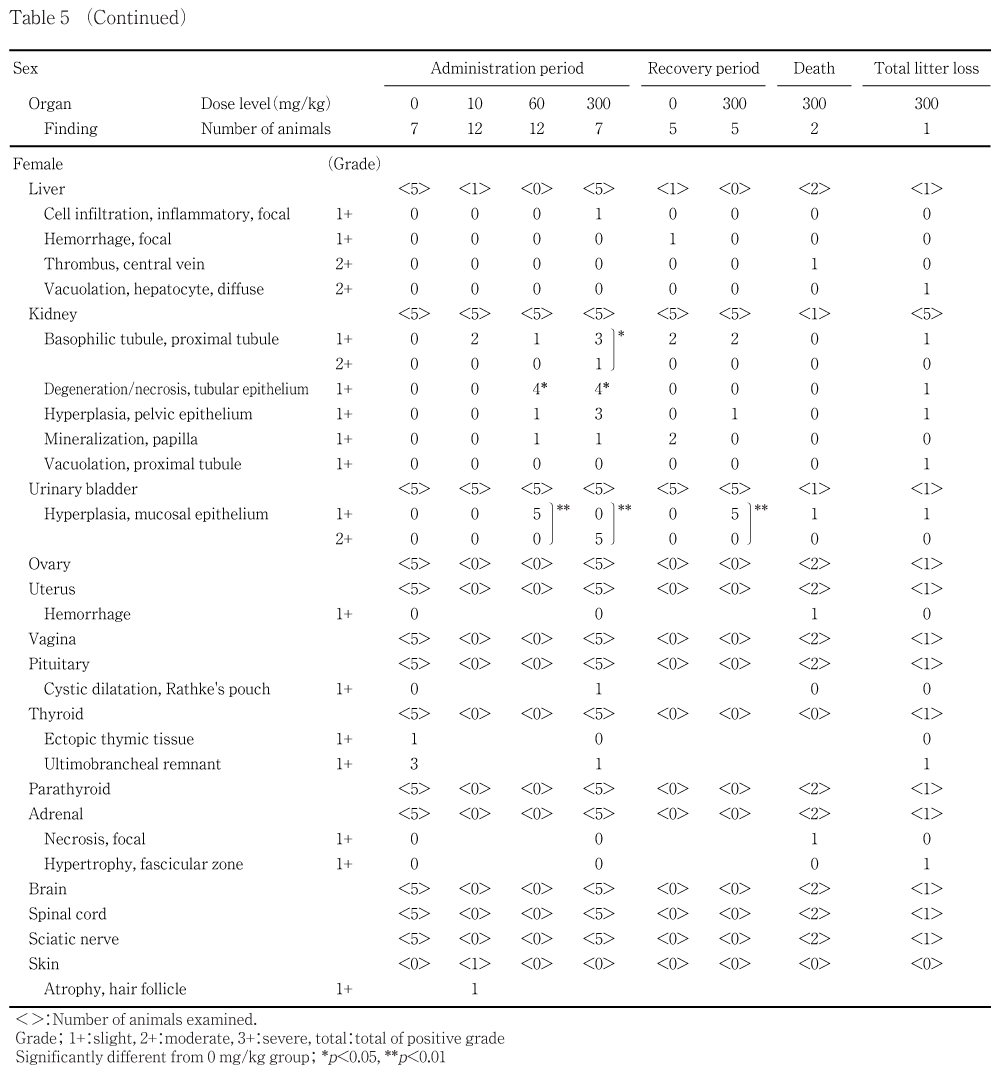
被験物質の影響と考えられる変化が300 mg/kg群の雌雄の胃,60および300 mg/kg群の雌雄の腎臓ならびに膀胱に認められた.
前胃:扁平上皮過形成が投与後解剖動物の300 mg/kg群の雄3例雌1例で軽度,雄3例雌6例で中等度,雄1例で重度に認められた.300 mg/kg群ではこれに伴い,角化亢進が雄3例雌7例で軽度,雄3例で中等度,錯角化が雄4例雌2例で軽度,び漫性炎症性細胞浸潤が雄5例雌6例で軽度,雌雄各1例で中等度,粘膜下織の水腫が雌雄各5例で軽度,雄1例で中等度に認められた.また,びらんが300 mg/kg群の雌雄各3例で軽度に認められた.回復後解剖動物ではこれらの変化のうち,300 mg/kg群の雄1例に扁平上皮過形成が軽度に認められたのみであった.
腎臓:細胞質の強好酸性化,核濃縮および尿細管腔内への脱落を特徴とする尿細管上皮の変性/壊死が,投与後解剖動物の60および300 mg/kg群の雌各4例で軽度に認められた.この変化は,回復後解剖動物では認められなかった.腎盂上皮の過形成が60 mg/kg群の雄4例雌1例,300 mg/kg群の雌雄各3例で軽度に認められた.この変化は回復後解剖動物では300 mg/kg群の雌1例に軽度に認められたのみであった.
膀胱:粘膜上皮の過形成が60 mg/kg群の雌雄全例で軽度,300 mg/kg群の雌雄全例で中等度に認められた.この変化は,回復後解剖動物でも300 mg/kg群の雌雄全例で軽度に認められた.剖検時に認められた片側性の精巣上体尾部の黄色斑は精子肉芽腫,片側性の精巣の小型は限局性精細管萎縮,それに伴う精巣上体の小型は腔内精子減少,両側性の精巣の小型はび漫性精細管萎縮,それに伴う精巣上体の小型は腔内精子減少であった.
死亡動物では,被験物質に起因する変化として,前胃の扁平上皮過形成,角化亢進およびびらん,錯角化が雌2例ともにみられ,加えて1例では膀胱の粘膜上皮の過形成,胸腺の萎縮も認められた.なお,死後の自己融解が強く2例の腎臓,1例の膀胱は評価できなかった.その他,個々に認められた所見として1例では,気管に重度の粘膜上皮の壊死と中等度の固有層の炎症性細胞浸潤,肺に中等度のうっ血と軽度の水腫が認められた.他の1例では,肺の静脈および肝臓の中心静脈に血栓が認められ,死因として播種性血管内凝固症候群(DIC)が疑われた.この他,胸腺および子宮における出血,脾臓の白脾髄の萎縮,副腎の限局性壊死が認められた.なお,剖検でみられた下垂体の腫大は,特記すべき組織学的変化は認められなかった.
全出産児が死亡した動物では,被験物質に起因する変化として,前胃の扁平上皮過形成,角化亢進,錯角化,びらんおよび炎症性細胞浸潤,腎臓の尿細管上皮の変性/壊死および腎盂上皮の過形成,膀胱の粘膜上皮の過形成および胸腺の萎縮が認められた.この他,腺胃粘膜の萎縮,肝臓の肝細胞および腎臓の近位尿細管に脂肪滴と思われる空胞化,副腎の束状帯の過形成が認められた.なお,十二指腸粘膜上皮の過形成が認められ,被験物質の影響を疑ったが,投与後解剖動物および回復後解剖動物でこの変化は認められなかった.
雌の胸腺で被験物質の影響を疑い,10および60 mg/kg群ならびに回復後解剖動物の胸腺も合わせて精査したが,対照群との差は認められなかった.300 mg/kg群の雌で認められた胸腺の萎縮は,死亡および全出産児動物に限られた衰弱性の変化と考えられる.
この他にもいくつかの変化が認められたが,ラットでは非特異的に発現する変化であり,その発現状況に明らかな群差がみられないことから,被験物質とは関連のない変化と判断した.
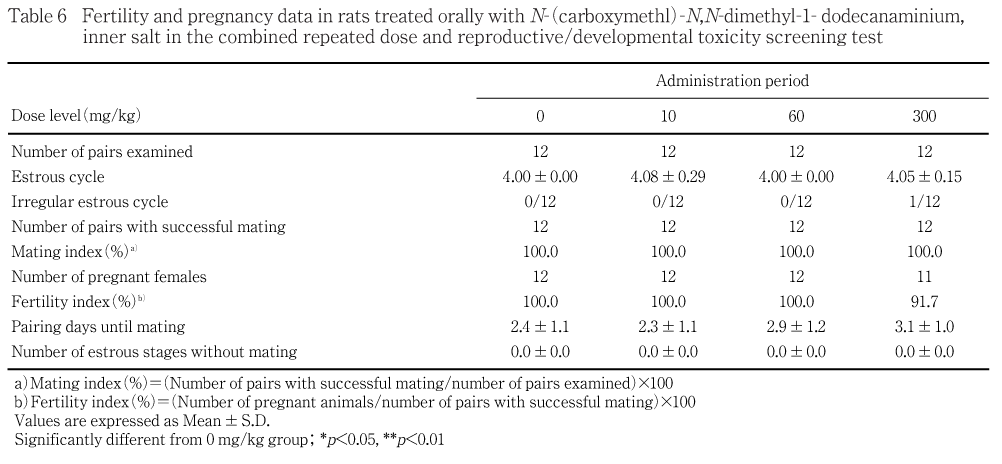
性周期検査では,4日周期を示した動物が対照群,10,60および300 mg/kg群でそれぞれ各群12例中,12,11,12および10例であり,被験物質投与による性周期の延長あるいは短縮は認められなかった.なお,300 mg/kg群の1例で発情休止期の継続がみられたが,雄との同居後に性周期が回帰し交尾した.その他に,異常性周期を示す動物は認められなかった.
各群の全例が交尾し,交尾率,交尾所要日数,交尾成立までに逸した発情期の回数ともに被験物質投与群と対照群との間に有意差は認められなかった.非妊娠の動物は300 mg/kg群の1例にみられただけで,受胎率にも被験物質投与群と対照群との間に有意差は認められなかった.なお,非妊娠雌の相手雄は両側性の精巣および精巣上体の小型がみられ,非妊娠は雄が原因と考えられたが,本所見は稀にみられる変化で,被験物質による影響ではないと考えられる.
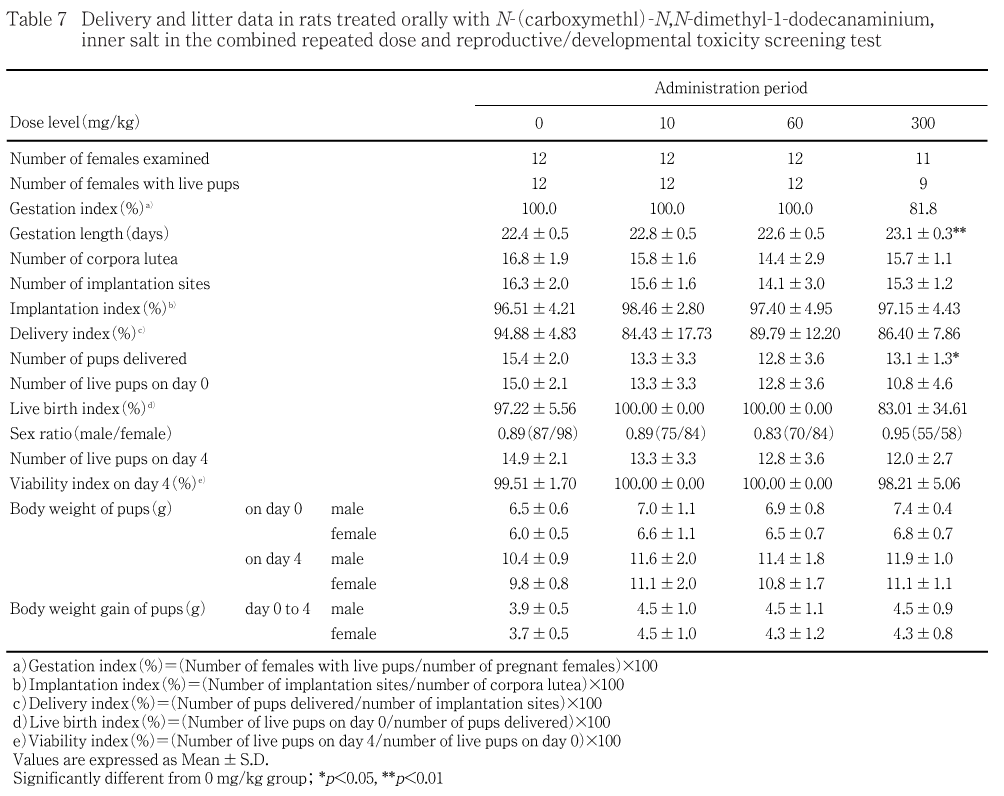
妊娠期間の延長および出産児数の低値が300 mg/kg群で認められた.その他,黄体数,着床数,着床率,出生率および分娩率のいずれにも被験物質投与群と対照群との間に有意な差は認められなかった.
分娩状態の観察で300 mg/kg群の2例に以下の変化が認められた.1例では,妊娠22日の分娩途中の観察で出産児5例が娩出されていたが,翌日には7例の死亡児が確認され,母動物も死亡していた.この母動物の子宮内には5例の胎児が遺残していた.また,娩出された出産児の内3例は母動物の死亡発見時には生存していた.他の1例は,分娩完了までに2日間(妊娠22日〜24日)を要し難産を示した母動物であった.本母動物では妊娠23日に16例の出産児が観察されたが,触診の結果,子宮内に遺残している胎児が確認されたため観察を続けた.妊娠24日の観察時にはすべての胎児が娩出されたが,全出産児は死亡していた.この母動物は授乳,胎盤摂取,児動物を回集するなどの哺育行動が認められなかった.その他の母動物に分娩および哺育行動の異常は認められなかった.
300 mg/kg群で出産児数の低値を示し,それに伴い出生率も低値傾向を示した.なお,性比に変化は認められなかった.
一般状態および外表異常の観察では,被験物質に起因する変化は認められなかった.
雌雄の体重および体重増加量とも被験物質投与群に変化は認められなかった.
哺育4日の生存児の剖検および死亡児の剖検では,被験物質に起因する異常所見は認められなかった.
死亡が300 mg/kgの妊娠20日に雌1例,妊娠23日の分娩途中に雌1例で認められた.投与後の症状として,流涎が300 mg/kg群の雌雄全例に認められた.被験物質はウサギの眼粘膜に対し強い刺激性を有することか知られている3)こと,被験物質投与による神経症状が認められていないことから,流涎は被験物質の刺激性に起因する変化と考えられる.
病理学検査の結果,被験物質に起因する変化が胃,腎臓および膀胱に認められた.剖検において前胃粘膜の肥厚,黄色化および隆起巣が300 mg/kg群の雌雄でみられ,組織学的には扁平上皮過形成,角化亢進,錯角化,び漫性炎症性細胞浸潤,びらんおよび粘膜下織の水腫が同群の雌雄で認められた.その他,腎臓の尿細管上皮の壊死および腎盂上皮の過形成,膀胱の粘膜上皮過形成が60および300 mg/kg群の雌雄で認められた.
前胃の扁平上皮過形成は,種々の刺激性化学物質の経口投与によって誘発され,角化亢進や炎症性細胞浸潤,水腫を伴うこともあり,投与を中止することにより回復することが報告されている4).胃の変化は,上述のように流涎が300 mg/kg群の全例で認められていることから,被験物質の刺激性に起因する変化と考えられる.腎臓の尿細管上皮の壊死は多くの薬物によって誘発され,その機序は様々である4).壊死は近位尿細管に見られることが多く5),本試験での発現部位はそれに一致していた.膀胱の粘膜上皮過形成は,種々の原因による移行上皮の損傷部における再生像として認められる6).被験物質は消毒剤に用いられ殺菌力が強力であることが知られている1)こと,両性界面活性剤のうち市販殺菌消毒剤の代謝についての実験では,高用量投与における排泄は主として腎臓より行われる7)ことから,腎臓および膀胱の変化は被験物質により誘発されたものと考えられる.
血液生化学検査では,尿素窒素の増加が300 mg/kg群の雌雄で認められた.血清尿素は腎機能の指標として用いられており8),前述のように腎臓への影響が組織学的にみられていることから,それに伴う増加と考えられる.
これら投与期間で認められた変化は,2週間の回復期間により消失するか,変化がみられても病変程度が明らかに軽減し,回復傾向を示しているものと考えられる.
分娩途中で死亡した300 mg/kg群の1例では,交配前に一過性の変化として鼻周囲および下腹部の汚れ,性周期検査で発情休止期の継続,剖検では前胃粘膜の肥厚,組織学的には,被験物質に起因する前述の変化の他,肺の静脈および肝臓の中心静脈に血栓が認められた.周産期に死亡した動物を組織検査すると,静脈に血栓がみられ,播種性血管内凝固症候群(DIC)を呈することがしばしば認められる.本動物も同様の変化を示していることから,死因として播種性血管内凝固症候群(DIC)の可能性が示唆された.他の死亡動物では,被験物質に起因する前述の変化の他,病理組織学検査では気管に重度の粘膜上皮の壊死と中等度の固有層の炎症性細胞浸潤,肺に中等度のうっ血と軽度の水腫が認められた.また,本死亡動物は死亡前日に流涎が観察されていたことから,流涎の発症と気管・肺の組織学的変化から誤嚥した可能性が考えられ,死亡したものと推察された.
雄の生殖器系への変化として,精巣および精巣上体の小型および精細管萎縮などが認められたが,本系統の動物でしばしば観察される自然発生性の変化と考えられ,さらに用量に関係なくみられていることから,被験物質に起因するものではないと判断した.その他,体重,摂餌量,血液学検査,尿検査(雄)および器官重量では,被験物質に起因する影響は認められなかった.また,詳細な症状観察,機能検査および自発運動量測定でも被験物質の影響はなく,神経症状を示唆する変化は認められなかった.
全出産児死亡が300 mg/kg群の雌1例の哺育0日に認められた.本動物は分娩完了までに2日間(妊娠22日〜24日)を要し難産を示し,分娩完了の観察時には全出産児が死亡していた.分娩途中の観察においても,授乳,胎盤摂取あるいは児動物を回集するなどの哺育行動が認められなかった.また,妊娠期間の延長および出産児数の減少が300 mg/kg群で認められた.300 mg/kg群の雌では妊娠末期の死亡,分娩途中の死亡,全出産児死亡がみられ,いずれも周産期に集中して認められていることから,妊娠期間の延長や出産児数の減少を招いたものと考えられる.この他,性周期,交尾率,受胎率,分娩率,黄体数,着床数,着床率および出産率では被験物質に起因する変化は認められなかった.
新生児の検査において,出産児数が300 mg/kg群で減少し,それに伴い出生率も低値傾向を示した.生後4日の生存率,性比,外表,一般状態,体重および剖検では被験物質に起因する変化は認められなかった.したがって,出産児数の減少がみられたが,次世代の発育へ影響を及ぼすものではないと考えられる.
以上のように,N-(カルボキシメチル)-N,N-ジメチル-1-ドデカナミニウムを反復経口投与した結果,一般毒性学的な主な変化として300 mg/kg群で周産期における雌の死亡,雌雄全例に流涎がみられ,前胃粘膜の肥厚と組織学的には扁平上皮過形成が認められた.60および300 mg/kg群の雌雄では腎臓の尿細管上皮の壊死および膀胱の粘膜上皮過形成が認められ,加えて血清尿素窒素の高値が300 mg/kg群の雌雄で認められた.これら投与期間で認められた変化は2週間の回復期間により消失するか,変化がみられても病変程度が軽減し,回復傾向を示しているものと判断された.生殖発生毒性に及ぼす影響として,300 mg/kg群で全出産児死亡,妊娠期間の延長,出産児数の減少が認められた.したがって,本試験条件下における反復投与毒性に関する無毒性量は雌雄とも10 mg/kg/day,生殖発生毒性に関する無毒性量は雄親動物で300 mg/kg/day,雌親動物ならびに児動物では60 mg/kg/dayと考えられる.
| 1) | 「13901の化学商品」化学工業日報社,東京 (2001) pp.1262-1264. |
| 2) | 星野信人ら:N-(カルボキシメチル)-N,N-ジメチル-1-ドデカナミニウムのラットを用いる単回経口投与毒性試験.化学物質毒性試験報告,13: 85-86 (2006). |
| 3) | アンヒトール24B.製品安全性データシート,花王 (2003). |
| 4) | Gopinath C, Prentice DE, Lewis DJ:The alimentary system and pancreas. Stomach. In "Atlas of experimental toxicological pathology", Gopinath C, Prentice DE, Lewis DJ (ed), MTP Press, Lancaster (1987) pp.64-65. |
| 5) | 渡辺満利,西川秋佳:腎臓.非腫瘍性病変.尿細管上皮細胞の壊死.In「毒性病理組織学」前川昭彦(責任編集),日本毒性病理学会,名古屋 (2000) p.254. |
| 6) | 福島昭治:膀胱/尿管/尿道.増殖性および腫瘍性病変.膀胱.過形成.In「毒性病理組織学」前川昭彦(責任編集),日本毒性病理学会,名古屋 (2000) p.272. |
| 7) | 界面活性剤の安全性および生分解性に関するデータシート集(第4集),日本界面活性剤工業界,東京 (1988) pp.168-170. |
| 8) | 河合忠,屋形稔,伊藤喜久:「異常値の出るメカニズム」医学書院,東京 (2001) p.119. |
| 連絡先 | |||
| 試験責任者: | 星野信人 | ||
| 試験担当者: | 佐藤ゆかり,藤代真弓,小山 隆 爰島洋子,豊田直人 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-0255 茨城県神栖市砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | |||
| Authors: | Nobuhito Hoshino (Study director) Yukari Sato, Mayumi Fujishiro, Takashi Koyama, Hiroko Kokoshima, Naoto Toyota |
||
| Kashima Laboratory Mitsubishi Chemical Safety Institute Ltd., | |||
| 14 Sunayama, Kamisu-shi, Ibaraki, 314-0255, Japan | |||
| Tel +81-479-46-2871 | Fax+81-479-46-2874 | ||