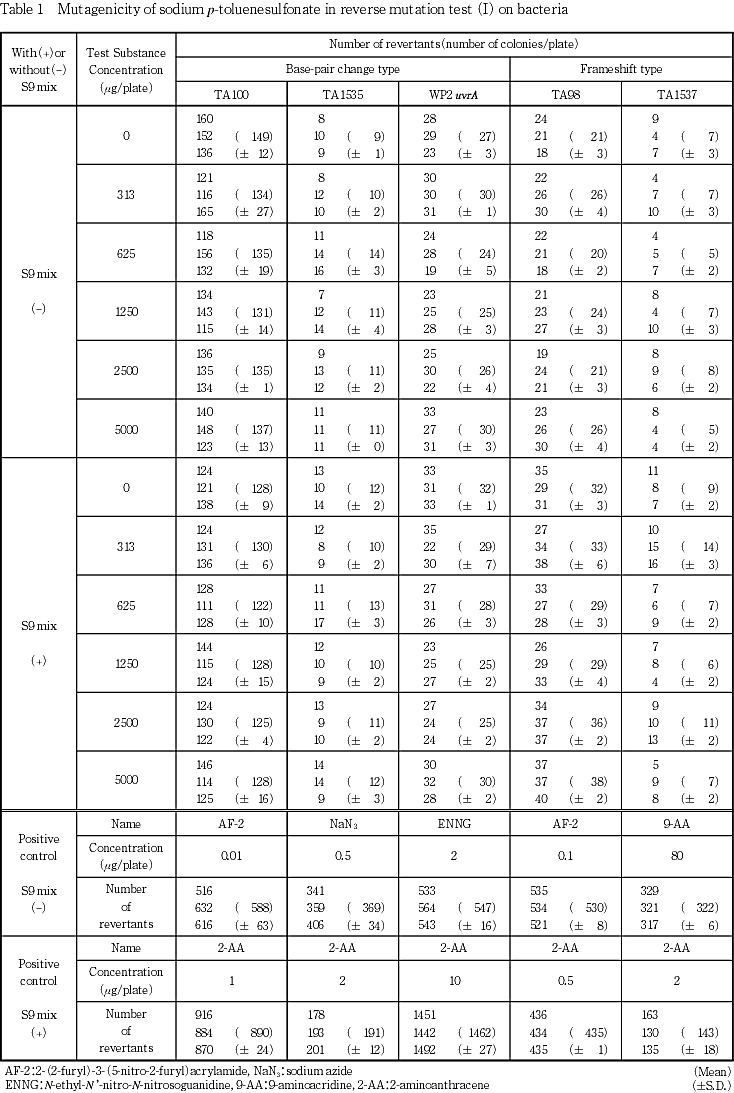
ρ-トルエンスルホン酸ナトリウムについてSalmonella typhimurium TA100,TA1535,TA98,TA1537およびEscherichia coli WP2 uvrAを用いる復帰変異試験を実施した.
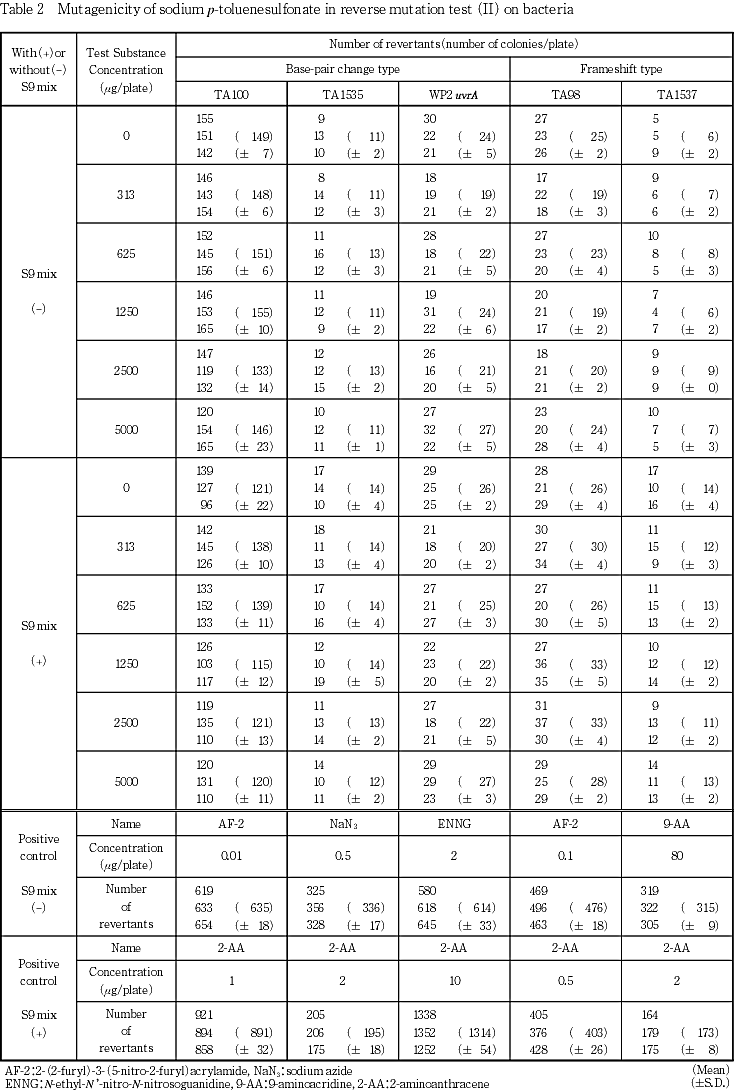
予備試験の結果をもとに,本試験ではS9 mix非共存下および共存下の各菌株について5000〜313 μg/plate(公比2)の5用量を設定した.
2回の本試験の結果,S9 mixの有無によらず,いずれの菌株においても陰性(溶媒)対照値の2倍以上を示す復帰変異コロニー数の増加は認められなかった.
以上の結果から,ρ-トルエンスルホン酸ナトリウムは本試験系において変異原性を有さない(陰性)と判定した.
980900,明友産業(株)(大阪)提供)は,純度92.7 %(不純物として,硫酸ナトリウム5.5 %を含有)の白色粉末である.被験物質は使用時まで室温に保存した.
被験物質原体は,熱,光に安定である.
| AF-2 | : | 2-(2-フリル)-3-(5-ニトロ-2-フリル)アクリルアミド(和光純薬工業(株)) |
| NaN3 | : | アジ化ナトリウム(和光純薬工業(株)) |
| ENNG | : | N-エチル-N'-ニトロ-N-ニトロソグアニジン(Sigma Chemical Co.) |
| 9-AA | : | 9-アミノアクリジン(Sigma Chemical Co.) |
| 2-AA | : | 2-アミノアントラセン(和光純薬工業(株)) |
| NaN3はDWに,その他はDMSOに溶解したものを使用した. | ||
| 硫酸マグネシウム・七水塩 | 0.2 g |
| クエン酸・一水塩 | 2 g |
| リン酸水素二カリウム | 10 g |
| リン酸一アンモニウム | 1.92 g |
| 水酸化ナトリウム | 0.66 g |
| グルコース | 20 g |
| 寒天(OXOID Agar No. 1) | 15 g |
| S9* | 0.1 mL |
| 塩化マグネシウム六水塩 | 8 μmol |
| 塩化カリウム | 33 μmol |
| D-グルコース6-リン酸 | 5 μmol |
| β-NADPH | 4 μmol |
| β-NADH | 4 μmol |
| ナトリウム-リン酸緩衝液(pH 7.4) | 100 μmol |
| 滅菌精製水 | 残 量 |
滅菌した試験管に被験物質溶液を0.1 mL,0.1 Mナトリウム-リン酸緩衝液(pH 7.4)を0.5 mLおよび菌懸濁液を0.1 mL加え,37 ℃で20分間振盪培養した.S9 mixを共存させる場合には,0.1 Mナトリウム-リン酸緩衝液の代わりにS9 mix(10 %あるいは30 %)を0.5 mL添加した.プレインキュベーション後,トップアガー2 mLを上記の混合液に加え混和し,最少グルコース寒天平板培地上に重層した.重層したトップアガーが凝固した後,37 ℃で48時間培養した.
実体顕微鏡を用いて菌叢の生育状態を観察し,被験物質による抗菌性の有無を調べた後,目視により被験物質の沈殿の有無を確認した.プレート上の復帰変異コロニー数を自動コロニーカウンターで計測した.予備試験は各用量につき1枚のプレートを使用した.本試験は各用量につき3枚のプレートを使用し,再現性を確認するため2回実施した.また,被験物質溶液の代わりに陰性対照物質(溶媒)および各菌株毎の陽性対照物質を用いて,被験物質群と同様の操作を行う対照群を設けた.
なお,S9 mix非共存下および共存下において陽性対照が各菌株に誘発した復帰変異コロニー数は,各菌株の陰性対照の復帰変異コロニー数と比較して,明らかに2倍を超えて増加し,陽性の結果を示した.
以上の結果から,ρ-トルエンスルホン酸ナトリウムは本試験系において変異原性を有さない(陰性)と判定した.
なお,類似化合物であるo-トルエンスルホンアミド3)および2-アミノ-5-メチルベンゼンスルホン酸3)は,いずれも細菌を用いる復帰変異試験で陰性の結果が報告されている.また,同じく類似化合物であるρ-トルエンスルホニルヒドラジド3)は陽性の結果が報告されている.

| 1) | D. M. Maron and B. N. Ames, Mutation Research, 113, 173(1983). |
| 2) | M. H. L. Green and W. J. Muriel, Mutation Research, 38, 3(1976). |
| 3) | 労働省安全衛生部化学物質調査課監修,“労働安全衛生法 有害性調査制度に基づく既存化学物質変異原性試験データ集,”日本化学物質安全・情報センター,東京,1996, p.85, p.113, p.342. |
| 連絡先 | |||
| 試験責任者: | 榎本佳明 | ||
| 試験担当者: | 榎本佳明,清水優子,大久保智子 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-0255 茨城県鹿島郡波崎町砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | ||||
| Authors: | Yoshiaki Enomoto(Study director) Yoshiaki Enomoto, Yuko Shimizu, Tomoko Okubo | |||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | ||||
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255 Japan | ||||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |||