フマル酸ジエチルのラットを用いる反復経口投与毒性・生殖発生毒性併合試験
Combined Repeat Dose and Reproductive/Developmental Toxicity
Screening Test of Diethyl Fumarate by Oral Administration in Rats
要約
フマル酸ジエチル(CAS No. 623-91-6)の11,30および100mg/kg/dayを雄ラットの交配14日前より46日間,雌ラットの交配前14日間,交配および妊娠期間,哺育3日までの期間に経口反復投与し,雌雄動物への反復投与による影響,雌雄動物の生殖および次世代の発生に及ぼす影響についてスクリーニング試験を実施して,以下の知見を得た.
反復投与毒性では,前胃において,粘膜層の肥厚が11mg/kg以上の群の雌雄で,過角化が11mg/kg以上の群の雄および30mg/kg以上の群の雌で認められ,出現例数,所見の程度ともに用量依存的に増大する傾向がみられた.また,粘膜下織における水腫,潰瘍および限局性の粘膜固有層における水腫が30mg/kg群の雄あるいは雌に,粘膜層表層における水胞形成が30mg/kg以上の群の雄に認められた.また,腎臓および肝臓において,重量あるいは体重重量比の増加が100mg/kg群の雌雄で認められた.胸腺においては,萎縮が30および100mg/kg群の雌で認められた.その他に,一般状態観察,体重推移,摂餌量,尿検査,血液学的検査および血液化学的検査では,被験物質投与による影響は認められなかった.以上より,フマル酸ジエチル反復投与による無影響量(NOEL)は雌雄ともに11mg/kg/day(投与可能最小量)未満であることが示唆された.
生殖発生毒性では,生殖能検査,生殖器の重量および病理組織学的検査,分娩および母性行動観察,新生児の生存性,一般状態観察,体重推移および剖検で,被験物質投与による影響は認められなかったことから,フマル酸ジエチルの雌雄動物の生殖および次世代の発生に対する無影響量は100mg/kg/dayであることが示唆された.
方法
1.動物および飼育条件
生後8週齢のCrj:CD(SD)系SPFラットを日本チャールス・リバーより受け入れ,18日間馴化飼育した後,順調な発育を示し,かつ雌では性周期に異常の認められない動物を試験に用いた.
動物は,温度23±3℃,湿度55±10%,換気回数10〜15回/時間,照明時間午前8時〜午後8時に設定された飼育室において,ブラケット式金属製金網床ケージに収容して飼育した.雌については妊娠17日より,実験動物用床敷(ホワイトフレーク,日本チャ−ルス・リバー)を敷いたステンレス製受皿を使用した.飼料は固型飼料(CRF-1,オリエンタル酵母工業)を,飲料水は水道水をそれぞれ自由摂取させた.飼料および床敷の混入物質,飲料水の水質について検査を実施し,異常のみられないことを確認した.
2.被験物質
フマル酸ジエチル(Lot No.:0158,純度:約98%,製造者:黒金化成)は樹脂改質共重合に使用され,特有の刺激臭を有する無色透明の液体(比重 1.053)である.被験物質は密栓し,遮光,室温の条件下で保管し,投与には原液をそのまま使用した.
3.試験群の設定
本試験の用量設定試験(14日間反復経口投与試験)の結果,1000mg/kg群で死亡例あるいは衰弱屠殺例が雌雄全例に,100および300mg/kg群で前胃粘膜上皮の肥厚および過角化が雌雄全例に,腎臓の重量あるいは体重重量比の増加が雌雄に認められたことから,本試験では投与期間の延長を考慮して高用量を100mg/kg/day,低用量を11mg/kg/day(投与可能最小量),中間用量を等比中項である30mg/kg/day(公比約3)とし,さらに日本薬局方精製水を投与する対照群を設け,計4群とした.1群の動物数は雌雄各12匹とし,投与開始前日に各群の体重が均一になるように体重別層化無作為抽出法により群分けした.
4.投与方法
投与経路は経口とし,投与は胃ゾンデを用いて胃内に強制的に行った.投与容量は,体重1kg当たり0.010,0.028および0.095mlとして投与日に最も近い日に測定した体重に基づいて算出した.なお,対照物質の投与量は0.095ml/kgとした.投与期間は,雄については交配前14日間および交配期間を含む46日間,雌については交配前14日間および交尾成立までの交配期間,さらに交尾成立例は妊娠期間および哺育3日までの期間とした.投与は10週齢から開始し,平均体重(体重範囲)は雄で413.1g((388〜447g),雌で239.5g(220〜261g)であった.
5.観察,測定および検査項目
(1)一般状態観察,体重および摂餌量測定
一般状態は,試験期間中1日1回以上の頻度で観察した.体重は,投与1日(投与前),投与2,5,7,10および14日,その後は雄は7日毎に(投与終了日を含む)および剖検日,雌は妊娠0,1,3,5,7,10,14,17および20日,哺育0,1および4日に測定し,体重増加量および増加率を算出した.摂餌量は,雄は交配期間および剖検日を除いて,雌は妊娠0日および哺育0日を除いて体重測定と同じ日に測定した.
(2)尿検査
投与43〜44日に雄の各群5例について代謝ケージに収容して非絶食下で採尿を行った.約3時間の蓄尿について,pH,蛋白,糖,ケトン体,ウロビリノーゲン,ビリルビンおよび潜血反応(以上,試験紙マルティスティックス;マイルス・三共),沈渣(鏡検)を検査し,21時間蓄尿について,比重(アタゴ製屈折計ユリコン),ナトリウム,カリウム(以上,炎光法:コーニング480型炎光光度計),クロール(電気滴定法:平沼CL-6M型クロライドカウンター),尿量を測定した.
(3)剖検および器官重量測定
交尾成立例については雄は投与46日の翌日,雌は哺育4日に,交尾不成立例は交配期間終了の翌日に,妊娠25日まで分娩の認められない例(分娩遅延例・不妊例)は妊娠26日に,エーテル麻酔下で採血後放血致死させた後,剖検した.器官重量は肝臓,腎臓,胸腺,副腎,精巣,精巣上体および卵巣について測定し,器官体重重量比を算出した.
(4)血液学的検査
剖検時に雄の全例について約16時間絶食した後,エーテル麻酔下で大腿静脈より採血し,無処理血液を用いて凝固時間(流体粘度変化による空気圧測定法:グライナー社製マイクロコアグロメーター)を,EDTA・2Kで処理した血液を用いて赤血球数,平均赤血球容積,血小板数,白血球数(以上,電気抵抗法),血色素量(シアンメトヘモグロビン法),ヘマトクリット値(RBC,MCVより算出),平均赤血球ヘモグロビン量(RBC,Hbより算出),平均赤血球ヘモグロビン濃度(Ht,Hbより算出),(以上,コールターカウンターT660型),網赤血球率(Brecher法),白血球型別百分率(鏡検)を測定した.さらに,腹部大動脈より採血し,クエン酸ナトリウムで処理した後,3000rpmで10分間遠心分離して得られた血漿を用いてプロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,AMELUNG KC-10A バクスターKK)を測定した.
(5)血液化学的検査
剖検時に雄の全例について,血液学的検査のための採血後,腹部大動脈より採血し3000rpmで10分間遠心分離して得られた血清を用いてGOT,GPT(以上,IFCC法),γ-GTP(包接L-γ-グルタミル-p-ニトロアニリド基質法),アルカリフォスファターゼ(ベッセイ・ローリー法),コリンエステラーゼ(ヨウ化ブチリルチオコリン基質法),血糖(ヘキソキナーゼ法),総コレステロール,リン脂質(以上,酵素法),トリグリセリド(遊離グリセロール法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(ヤッフェ法),カルシウム(OCPC法),無機リン(フィスケ・サバロー法),総蛋白(ビウレット法),アルブミン(BCG法),A/G比(TP,Alpより算出),(以上,日立7150形自動分析装置),カリウム,ナトリウム(以上,炎光法:コーニング480型炎光光度計),クロール(電気滴定法:平沼CL-6M型クロライドカウンター),蛋白分画(電気泳動法)を測定した.
(6)病理組織学的検査
全例の肝臓,腎臓,脾臓,心臓,肺,脳,下垂体,胸腺,副腎,甲状腺,胃(前胃・腺胃),十二指腸,空腸,回腸,盲腸,結腸,直腸,精巣,精巣上体,前立腺,卵巣および異常所見部位について,10%中性緩衝ホルマリン液あるいはブアン液(精巣,精巣上体のみ)で固定し,パラフィン包埋後薄切し,ヘマトキシリン・エオジン染色あるいは雌の異常所見例の1例の子宮について,アルシアン青染色標本を作製し検査した.
(7)生殖能検査
雌について,投与前10日から交尾成立までの連日,ギムザ染色による腟垢塗抹標本を作製し,性周期の異常の有無を検査した.
投与14日の雌雄について,同試験群内で夕方より1対1で最長14日間同居させた.交尾の成立は雌の腟垢中に精子が確認された場合とし,妊娠の成立は雌の子宮に着床痕が確認された場合とした.また,交尾率および受胎率を算出した.
(8)分娩および母性行動観察
交尾した雌全例について,分娩状態,母性行動,総出産児数,生存児数および死亡児数,出産児の性別および外表を観察した.また,着床率,出産率,分娩率,出生率,哺育4日時哺育率,性比および妊娠期間を算出した.なお,哺育日数は分娩終了を確認した日を哺育0日として起算した.
(9)新生児の生存性,一般状態観察および体重測定
新生児は1日1回,生死を確認し,一般状態および外表を観察した.また,新生児生存率を算出した.体重は哺育0,1および4日に測定し,体重増加量および増加率を算出した.
死亡例は発見後直ちに,その他の例は,哺育4日に二酸化炭素吸入法により安楽致死させた後,剖検した.
6.統計処理
交尾率,受胎率,出産率および哺育率はFisherの正確確率検定法により対照群と被験物質投与群との比較を行った.その他の項目はBartlettの検定法によって分散を検定した.その結果,等分散(P>0.05)を示した項目は一元配置分散分析法によって解析し,有意な場合(P<0.10)には,Dunnettの検定法(各試料の大きさが違う場合は有効反復数を用いた)により対照群と被験物質投与群との比較を行った.不等分散(P<0.05)を示した項目はKruskal-Wallis法により解析し,有意な場合((P<0.10)には,Mann-WhitneyのU-検定法により対照群と被験物質投与群との比較を行った.なお,分娩および母性行動観察結果,新生児の生存性および体重については1腹を単位として検定を行い,対照群との検定は危険率5%以下を統計学的に有意とした.
結果
1.反復投与毒性
(1)一般状態
30mg/kg群の雌1例(分娩遅延例)で妊娠19日に腟からの出血および手足・耳介の蒼白,妊娠19および20日に眼球の褪色が認められた.
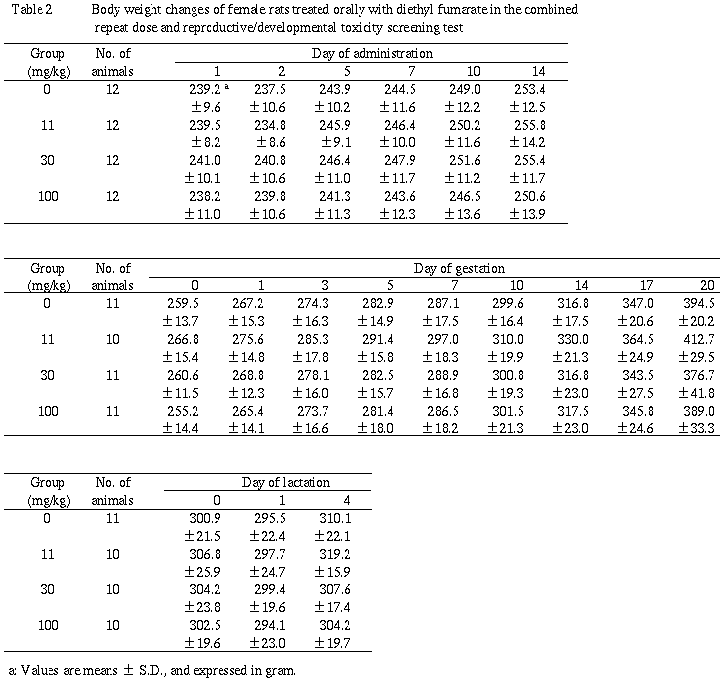
(2)体重(Table 1, 2)および摂餌量
雌雄ともに被験物質投与と関連した変化は認められなかった.
(3)雄の尿検査,血液学的検査および血液化学的検査
被験物質投与と関連した変化は認められなかった.

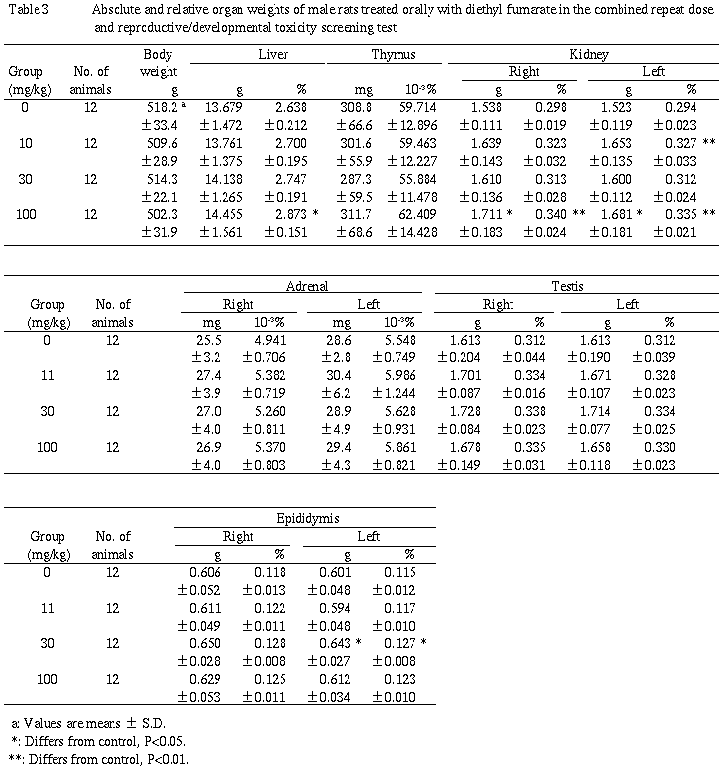
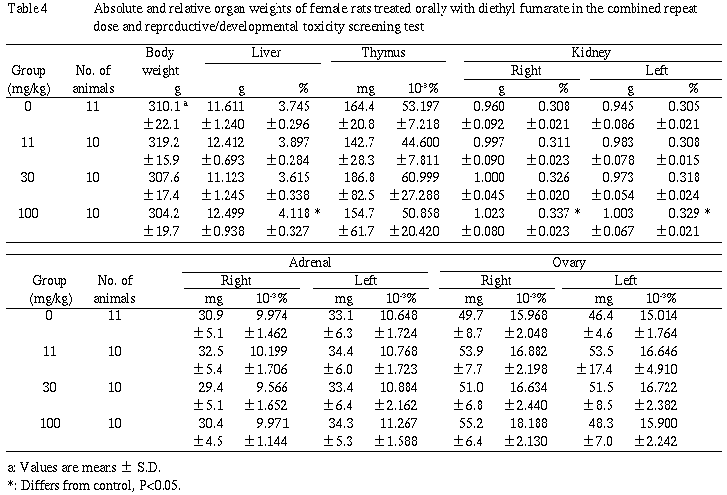
(4)器官重量(Table 3,4)
100mg/kg群の雄で肝臓の体重重量比,腎臓の重量および体重重量比の増加が,同群の雌で肝臓および腎臓の体重重量比の増加が認められた.
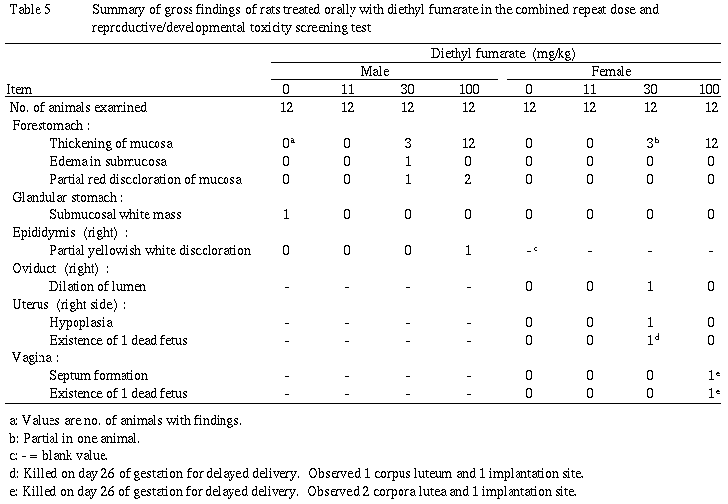
(5)剖検(Table 5)
前胃において,粘膜の肥厚が30mg/kg以上の群の雌雄に認められ,さらに雄の30あるいは100mg/kg群では粘膜下水腫,粘膜の一部暗赤色化も認められた.
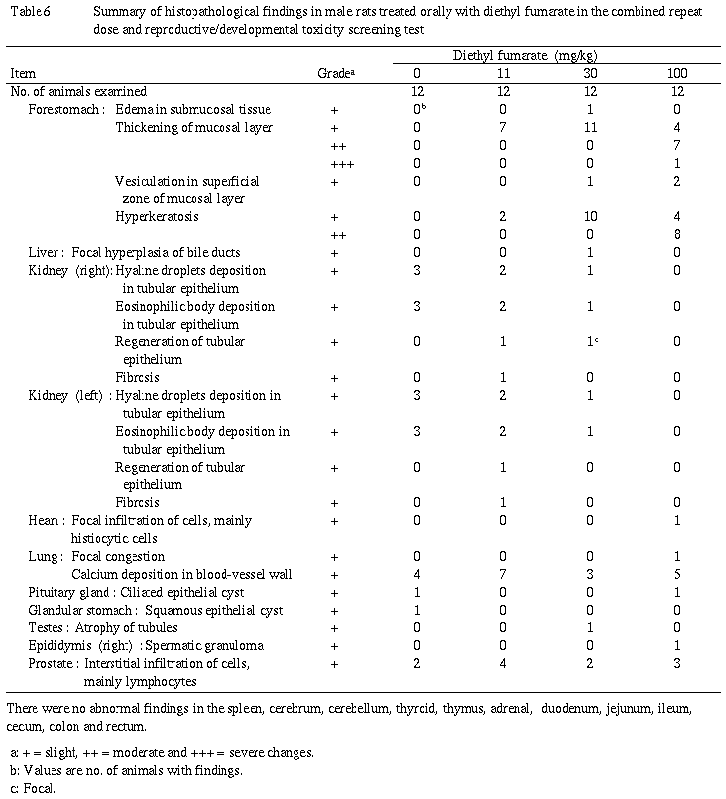
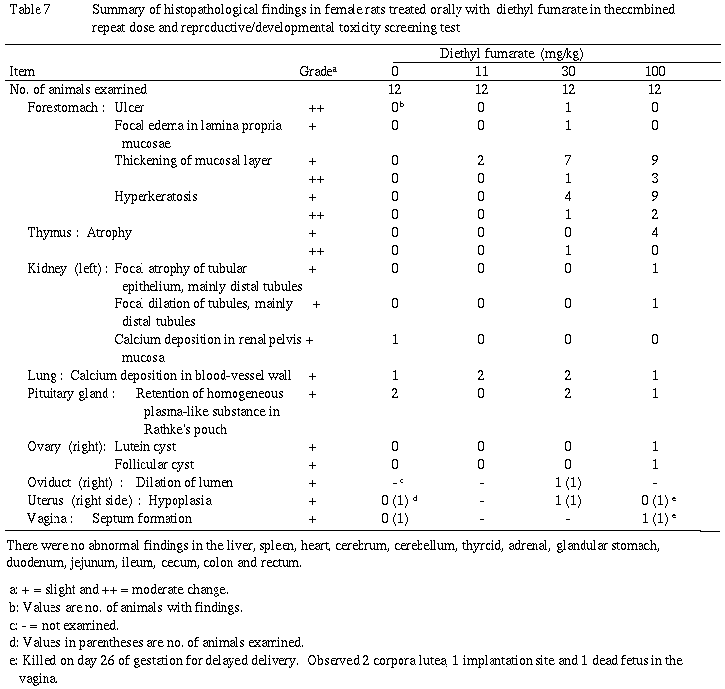
(6)病理組織学的検査(Table 6,7)
前胃において,粘膜層の肥厚が11mg/kg以上の群の雌雄で,過角化が11mg/kg以上の群の雄および30mg/kg以上の群の雌で認められ,出現例数,所見の程度ともに用量依存的に増大する傾向がみられた.これらの所見と伴って,粘膜下織における水腫が30mg/kg群の雄で,粘膜層表層における水胞形成が30mg/kg以上の群の雄で,潰瘍,限局性の粘膜固有層における水腫が30mg/kg群の雌で認められた.胸腺において,萎縮が30mg/kg以上の群の雌で認められたが、用量依存性はなく被験物質投与の関連はないと考えられた.不妊例ではその原因を示唆する所見は認められなかった.
2.生殖発生毒性
(1)生殖能検査(Table 8)
性周期について被験物質投与と関連した異常は認められなかった.交尾は全例成立し,受胎不成立は,対照群の1例,11mg/kg群の2例,30および100mg/kg群の各1例にみられたが,発現例数に用量依存性はみられなかった.
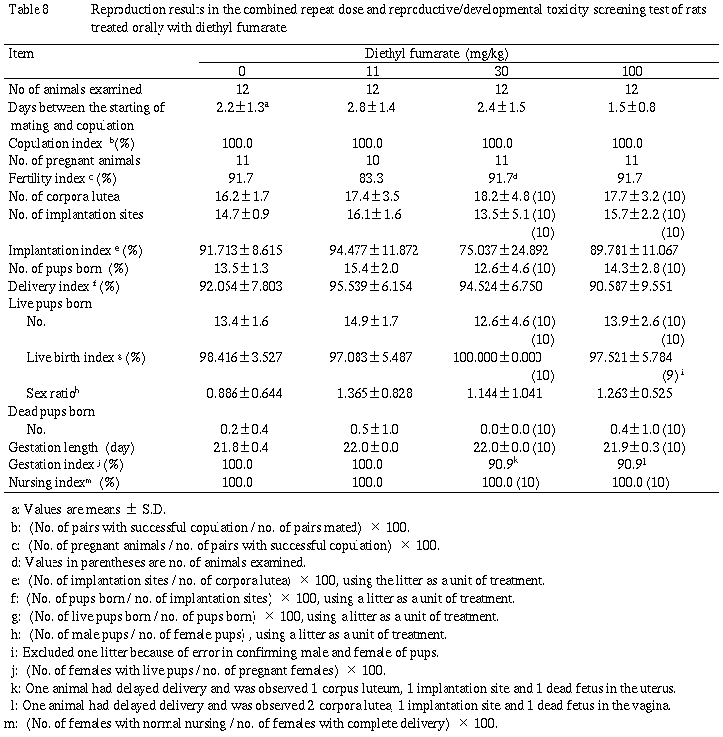
(2)分娩および母性行動観察(Table 8)
分娩および母性行動の観察項目について被験物質投与と関連した変化は認められなかった.なお,分娩異常として,30および100mg/kg群の各1例に分娩遅延(妊娠26日まで未分娩)が認められた.このうち30mg/kg群の例では子宮内に死亡胎児が1例,妊娠黄体および着床痕が各1箇認められた.100mg/kg群の例では腟内に死亡胎児が1例,妊娠黄体が2箇,着床痕が1箇認められ,また,腟の隔壁形成が認められた.
(3)新生児の生存性,一般状態,体重および剖検
雌雄ともに被験物質と関連した変化は認められなかった.
考察
被験物質の直接刺激によると考えられる所見として,前胃において粘膜層の肥厚が11mg/kg以上の群の雌雄で,過角化が11mg/kg以上の群の雄および30mg/kg以上の群の雌で認められ,出現例数,所見の程度ともに用量依存的に増大する傾向がみられた.また,粘膜下織における水腫,潰瘍および限局性の粘膜固有層における水腫が30mg/kg群の雄あるいは雌に,粘膜層表層における水胞形成が30mg/kg以上の群の雄に認められた.腎臓および肝臓において,重量あるいは体重重量比の増加が100mg/kg群の雌雄で認められた.しかしながら,形態的には異常は認められず,雄の尿および血液検査においても関連する変化は認められなかった.その他に一般状態,体重推移,摂餌量,尿検査,血液学的検査および血液化学的検査では被験物質投与による影響は認められなかった.
以上より,11mg/kg群の雌雄でも前胃に被験物質の刺激による変化が認められたことから,本スクリーニング試験におけるフマル酸ジエチル反復投与による無影響量(NOEL)は雌雄ともに11mg/kg/day(投与可能最小量)未満であることが示唆された.
生殖能検査では,雌の性周期,雌雄の交尾,受胎,生殖器の重量および病理組織学的検査において被験物質投与による影響は認められなかった.分娩遅延が30および100mg/kg群で各1例に認められた.30mg/kg群の例では妊娠末期に腟からの出血や手足・耳介の蒼白および眼球の褪色が認められており,剖検では子宮内に死亡胎児が1例認められ,両者の関連が示唆された.100mg/kg群の例では腟内に死亡胎児が1例認められ,腟では隔壁形成もみられており,先天的な要因による産道障害で腟内に胎児が停留したものと考えられた.この2例は,妊娠黄体および着床痕が1あるいは2箇と少数であり,同様の例は試験施設背景データでも認められていることから,被験物質投与との関連はないものと考えられた.以上のことから,妊娠,分娩および母性行動に関して,被験物質投与による影響はないものと考えられた.新生児の観察では,生存性,一般状態,体重推移および剖検において被験物質投与による影響は認められなかった.
以上より,生殖・発生について被験物質投与による影響は認められないことから,本スクリーニング試験におけるフマル酸ジエチルの雌雄動物の生殖および次世代の発生に対する無影響量は100mg/kg/dayであることが示唆された.
| 連絡先 |
| 試験責任者: | 釜田 悟 |
| 試験担当者: | 八幡昭子,常見邦順,小林裕幸,
長谷淳一,岡澤平一 |
| (株)化合物安全性研究所 |
| 〒004 北海道札幌市豊平区真栄363番24号 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Satoru Kamada (Study director),
Akiko Yahata,Kuninori Tsunemi,Hiroyuki Kobayashi,
Jyu-nichi Nagaya,Heiichi Okazawa |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
|
363-24 Shin-ei, Toyohira-ku,Sapporo,Hokkaido, 004, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |








