3-アミノフェノールのラットを用いる単回経口投与毒性試験
Single Dose Oral Toxicity Test of 3-Aminophenol in Rats
要約
3-アミノフェノールは染料あるいは医薬品PASの原料として使用されている.1 %カルメロースナトリウム水溶液に懸濁した3-アミノフェノールの0,500,700,1000および1400 mg/kgを,1群あたり雌雄各5匹のCrj:CD(SD)IGSラットに単回経口投与してその急性毒性を検討し,以下の成績を得た.死亡は雌雄とも投与後3日までに700 mg/kg以上の投与群で認められた.一般状態では,投与日に500 mg/kg以上の投与群で,振戦,流涎,褐色尿,腹臥,横臥が投与後数分から4時間の間に発現した.その他に,手足・耳介の蒼白,自発運動の減少等も観察された.体重では,雌雄の700 mg/kg投与群で投与後1日に低値が認められ,雄ではその後も増加抑制傾向が継続したが,雌では著明でなかった.剖検では,雌雄の死亡例に腺胃粘膜の菲薄化,腺胃粘膜の暗赤色斑等の障害性変化が認められ,うっ血による脾臓の腫大も認められた.生存例では,雄の700 mg/kg投与群で精巣,精巣上体および精嚢の小型が,雌の700および1000 mg/kg投与群で脾臓の暗赤色化,腎臓の暗褐色化,尾の先端部の暗紫色化が認められた.また,雌雄の700 mg/kg投与群で肝臓および脾臓の相対重量の高値がみられ,病理組織学検査では,雌で肝臓のクッパー細胞,腎臓の近位尿細管上皮および脾臓への褐色色素の沈着が認められた.死亡例では,雌雄とも脾臓のうっ血が認められ,雄で肝臓の限局性壊死,肝臓のクッパー細胞および腎臓の近位尿細管上皮への軽度な褐色色素の沈着が認められた.LD50値は,雄で693 mg/kg,雌で856 mg/kgであった.
方法
1. 被験物質および投与液の調製
3-アミノフェノール(純度:99.70 %,Lot No. 720208,三井化学(株),東京)は,淡灰色の結晶である.入手後の被験物質は遮光気密容器に入れ,4〜10 ℃の冷暗所で保存し,残余被験物質を製造業者が分析し,投与期間中の被験物質の安定性を確認した.媒体はカルメロースナトリウム(丸石製薬(株)を精製水(ヤクハン製薬(株)に溶解して調製した1 %水溶液(1 % CMC-Na)を用い,これに被験物質を所定の濃度となるように懸濁させた.調製液は,冷暗所,遮光下で8日間安定であることから,調製後直ちに遮光気密容器に入れて冷蔵庫で保存し,室温に戻して使用した.また,これらの調製液について濃度を確認し,設定値の± 10 %以内にあることを確認した.
2. 試験動物および飼育条件
日本チャールス・リバー(株)より受け入れた4週齢のSprague-Dawley系ラット(Crj:CD(SD)IGS)の雌雄を8日間の検疫・馴化を行った後,雌雄各25匹を選択して5週齢で試験に供した.投与日の体重は雄が132〜146 g,雌が103〜116 gであった.動物は,温度20〜23 ℃,湿度51〜59 %,換気回数10〜15回/時間および照明時間12時間(8時から20時まで点灯)に制御されたバリアシステムの飼育室で,ブラケット式金属製金網床ケージに群分け前は1ケージあたり4あるいは5匹を収容し,群分け後は個別飼育した.飼料は,g線照射固型飼料(CRF-1,オリエンタル酵母工業(株)を金属製給餌器を用いて,飲料水は札幌市水道水を自動給水装置を用いてそれぞれ自由に摂取させた.
3. 投与量および投与方法
投与量設定試験では雌雄のラットに500,700,1000,1400および2000 mg/kgの5用量を1群3匹に単回投与し,雌雄とも700,1000,1400および2000 mg/kg投与群でそれぞれ1/3,2/3,3/3および3/3例が死亡した.このことから,本試験の投与量は雌雄とも最低用量を500 mg/kgとし,公比約1.4で500,700,1000および1400 mg/kgを設定し,これに1 % CMC-Naを投与する対照群を含めた雌雄各5群を設定した.1群の動物数は雌雄とも5匹とし,投与前日の体重に基づいて層化無作為抽出法により群分けを行った.
動物は,投与前に約17時間絶食させ,投与日の体重に基づいて5 mL/kgの容量でラット用胃ゾンデを用いて強制的に胃内に単回投与した.なお,給餌の再開は投与後4時間に行った.
4. 検査項目
1) 一般状態観察
投与後6時間までは頻繁に,その後は投与後14日の剖検日まで1日1回観察した.
2) 体重測定
投与日の投与前,投与後1,3,5,7,10および14日に測定した.得られた体重から,体重増加量[(投与後14日体重)-(投与日体重)]および体重増加率[(体重増加量)/(投与日体重)×100]を算出した.
3) 剖検
死亡例は発見後速やかに,生存例は投与後14日に体外表を観察した後,エーテル麻酔下で放血致死させ,全身の器官・組織を肉眼的に観察した.
4) 器官重量測定
剖検時に生存例の全例について,肝臓,腎臓および脾臓の重量を測定し,絶対重量を剖検当日の体重で除し,100を乗じて相対重量を算出した.
5) 病理組織学検査
死亡例を含めた雌雄全例について,肝臓,腎臓および脾臓のパラフィン包埋切片にヘマトキシリン・エオジン染色あるいは特殊染色(ベルリン青染色,Masson trichrome染色,PAS染色,PTAH染色,シュモール反応)を施して鏡検した.
5. 統計解析
雌雄の動物数および死亡動物数を用いて,probit法によりLD50値を算出した.
体重,体重増加量,体重増加率,器官重量の絶対重量および相対重量について,Bartlettの検定法によって等分散性を解析し,等分散の場合は一元配置分散分析法で解析し,有意差がみられた場合はDunnettの検定法により解析した.不等分散の場合はKruskal-Wallis法で解析し,有意差がみられた場合はMann-WhitneyのU-検定法を用いて解析した.これら対照群と被験物質投与群との間の検定においては,いずれも有意水準を5 %とした.
結果
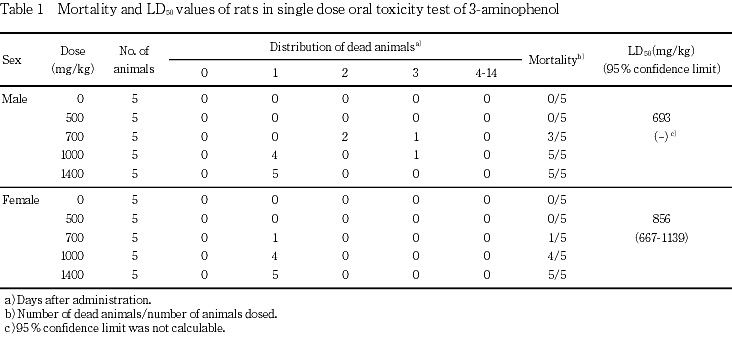
1. 死亡状況およびLD50値(Table 1)
死亡は,700,1000および1400 mg/kg投与群において,雄で各々3,5および5例に,雌で各々1,4および5例に,投与後3日までに認められた.
LD50値は雄で693 mg/kg,雌で856 mg/kgであった.
2. 一般状態
投与日には,500 mg/kg投与群で雌雄に振戦,雌に流涎,褐色尿,腹臥が,700 mg/kg以上の投与群で雌雄とも流涎,褐色尿,腹臥,横臥がみられ,手足・耳介の蒼白も遅れてみられた.これらの症状は投与後数分から4時間までに発現し,投与後1日から投与後3日まで雌雄の700 mg/kg以上の投与群で手足・耳介の蒼白がみられた.他に,自発運動の減少,尾の先端部の暗赤色および外傷,腹臥,呼吸促迫も散見され,死亡例も認められた.投与後14日まで生存した例においても,手足・耳介の蒼白,尾の先端部の暗紫色および欠落が散見された.
3. 体重
投与後1日に雌雄の700 mg/kg投与群で低値がみられ,投与量依存的な増加抑制傾向が認められた.雄では投与後14日まで増加抑制傾向が継続したが,雌では投与後3日以降は対照群を上回る順調な体重増加を示した.
4. 剖検
死亡例には雄で腺胃粘膜の菲薄化がみられ,雌雄ともに腺胃粘膜の暗赤色斑あるいは暗褐色斑,脾臓の腫大がみられ,尾の先端部の暗赤色化・外傷および胸水,副腎の暗赤色化が散見された.生存例では,雄の700 mg/kg投与群の1例に精巣,精巣上体および精嚢の小型がみられた.雌の700および1000 mg/kg投与群で脾臓の暗赤色化,腎臓の暗褐色化,尾の先端部の暗紫色化および欠落が散見された.
5. 器官重量
雄の700 mg/kg投与群で肝臓および脾臓の相対重量に高値傾向がみられた.雌の700 mg/kg投与群では脾臓の絶対重量が高値を示し,相対重量にも高値傾向がみられた.700および1000 mg/kg投与群では肝臓の相対重量に高値傾向がみられた.1000 mg/kg投与群の1例には脾臓の相対重量の高値傾向がみられた.
6. 病理組織学検査
死亡例では,雌雄の700,1000および雄の1400 mg/kg投与群で脾臓に軽度なうっ血がみられ,雄の700および1000 mg/kg投与群で肝臓に軽度ないし中等度な限局性あるいは広範な壊死がみられた.肝臓のクッパー細胞および腎臓の近位尿細管上皮に,いずれも軽度なヘモジデリン様の褐色色素の沈着もみられた.雌雄の700 mg/kg投与群で,腎臓の近位尿細管上皮にPAS染色陽性を示す軽度な好酸性細胞質内封入体がみられた.
生存例では,雌の700および1000 mg/kg投与群で肝臓のクッパー細胞および腎臓の近位尿細管上皮に,いずれも軽度なヘモジデリン様の褐色色素の沈着がみられた.雌の500,700および1000 mg/kg投与群で脾臓にも軽度なヘモジデリン様の褐色色素の沈着がみられた.一方,雄に変化はみられなかった.
考察
雌雄いずれも振戦,流涎,褐色尿,横臥あるいは腹臥,手足・耳介の蒼白等が500 mg/kg以上の投与群で多くの例に認められ,投与後3日までに死亡した.また,1例ではあるが雌の1000 mg/kg投与群で尾の先端部の暗紫色および欠落がみられた.これらの症状の内,振戦および流涎についてはLloydら1)により報告されている.褐色尿および手足・耳介の蒼白については,後述の溶血との関連が考えられた.
体重では,投与後数日間に雌雄いずれにも増加抑制傾向がみられ,雄では投与後14日まで継続した.雌では700 mg/kg投与群で,投与後14日間の体重増加率に対照群と比べて有意な高値が認められた.この有意差は対照群の体重が投与後3日以降に低値で推移したことによると考えられた.
剖検では,死亡例に雌雄とも腺胃粘膜の菲薄化および暗赤色斑あるいは暗褐色斑がみられ,3-アミノフェノールの粘膜障害性が示唆された.Lloydら1)はウサギを用いた刺激性試験において,有傷皮膚および無傷皮膚いずれにも軽度な浮腫を報告し,3-アミノフェノールを軽度な刺激性物質としていることから腺胃粘膜の変化との関連が考えられた.
脾臓の腫大が雄の死亡例に多数みられ,雌雄とも生存例に脾臓の相対重量の高値もみられた.また,投与日に褐色尿が多くの例にみられたこと,病理組織学検査で腎臓および脾臓に褐色色素が沈着し,へモジデリン様の赤血球由来の色素であると考えられたこと,Reら2)の報告において溶血の可能性が示唆されていることから,本試験においても3-アミノフェノール投与により溶血が惹起されたと考えられた.また,脾臓の腫大も,赤血球系の障害に起因する脾臓の老廃赤血球処理機能の亢進による変化と考えられ,病理組織学的にはうっ血が認められた.一般状態でみられた手足・耳介の蒼白および尾の先端部の暗紫色も溶血による貧血状態を反映した変化,あるいは循環障害による可能性が考えられた.雄の生存例の1例にみられた生殖器官の小型については,生殖器官の変化に関する報告はないことから,尾と同様に循環障害による二次的変化としての成長阻害である可能性が考えられた.
なお,単回投与後7日まで観察して剖検した投与量設定試験では,肝臓および腎臓の暗褐色化が観察されたが,本試験では投与後14日まで観察して剖検した結果,同様の変化は認められなかった.本試験において肝臓および腎臓に認められたへモジデリン様の褐色色素は,赤血球由来の色素であると考えられることから,各器官の色調の変化はこれらの褐色色素に由来し,観察期間の延長により排泄が進行することで軽減したものと考えられた.
以上のことから,3-アミノフェノールのラットにおける単回経口投与では,急性の中毒症状として振戦,流涎,褐色尿,横臥あるいは腹臥,手足・耳介の蒼白等を呈した後,投与後1日から投与後3日までの間に死亡した.死亡例の剖検所見として腺胃粘膜に障害性変化がみられ,死亡例,生存例いずれにもうっ血による脾臓の腫大あるいは器官重量の高値,褐色色素の沈着等がみられた.なお,本試験条件下でのLD50値は雄で693 mg/kg,雌で856 mg/kgであった.
文献
| 1) | G. K. Lloyd, M. P. Liggett, S. R. Kynoch and R. E. Davies, Food Cosmet. Toxicol., 15, 607(1977). |
| 2) | T. A. Re, R. F. Loehr, S. C. Rodriguez, D. E. Rodwell and C. M. Burnett, Fundam. Appl. Toxicol., 4, 98(1984).
|
| 連絡先 |
| 試験責任者: | 須永昌男 |
| 試験担当者: | 堀川裕尚,咲間正志,山本美代子,古川正敏 |
| (株)化合物安全性研究所 |
| 〒004-0839 札幌市清田区真栄363番24 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Masao Sunaga(Study director)
Hironao Horikawa, Masashi Sakuma, Miyoko Yamamoto, Masatoshi Furukawa |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo, Hokkaido, 004-0839, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |

