3-メトキシ-3-メチル-1-ブタノールのラットを用いる
28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test
of 3-Methoxy-3-methyl-1-butanol in Rats
要約
3-メトキシ-3-メチル-1-ブタノールはイソブチレンとメタノールを原料として製造され,塗料,インキ,シンナー,染料,洗剤,剥離剤,農薬原料,可塑剤原料等に広く用いられている化学物質である.しかしながら,本物質の毒性について,これを調べた報告はみられず,ほとんど知られていないのが現状である.
今回,3-メトキシ-3-メチル-1-ブタノールについて,SD系[Crj:CD(SD)IGS]ラットを用い,0,15,60,250および1000 mg/kg用量で28日間反復経口投与毒性試験を実施した.動物数は1群雌雄各5匹とし,投与期間終了後屠殺群の5群,並びに14日間回復群として対照群および1000 mg/kg群の2群を設定した.
その結果,血液生化学検査において,1000 mg/kg群で雌雄に塩素の有意な減少,雄にA/G比および無機リンの有意な増加が認められた.器官重量においては,250 mg/kg群で雄および1000 mg/kg群で雌雄に腎臓相対重量,さらに1000 mg/kg群で雌雄に肝臓相対重量のいずれも有意な増加が認められた.動物の一般状態,体重,摂餌量,尿検査,血液学検査,剖検および病理組織学検査においては,被験物質の投与に起因する変化は認められなかった.
回復群においては,投与期間終了時屠殺動物で認められた変化のうち,雄の肝臓重量は有意差が残るものの回復傾向を示し,その他の変化はいずれも回復した.
以上の結果から,3-メトキシ-3-メチル-1-ブタノールのラットへの28日間反復経口投与により認められた主な毒性は,肝臓および腎臓に対する影響であった.無影響量は雄で60 mg/kg/day,雌で250 mg/kg/dayと判断された.
方法
1. 被験物質
3-メトキシ-3-メチル-1-ブタノールは,水に可溶な無色透明の液体である.試験には(株)クラレ(大阪)製造のもの(ロット番号22517,純度99.19 %,不純物として2-メトキシ-4-メトキシメチル-2-ブチルブタン0.2 %,4-t-ブトキシ-4-メチル-2-ブタノール0.1 %を含む)を入手し,冷暗所(4 ℃),密栓下で保管し,使用した.被験物質の投与液は,局方精製水[共栄製薬(株)]を溶媒として,所定の投与用量となる濃度の水溶液に調製し,使用時まで冷暗所(4 ℃)で密栓保管し,調製後7日間以内に使用した.なお,保管条件下および投与形態での被験物質は安定であることを確認した.
2. 供試動物および飼育条件
動物はSD系[Crj:CD(SD)IGS]ラットを,日本チャールス・リバー(株)(神奈川)より搬入,雄は7日,雌は8日間検疫を兼ねて試験環境に馴化させた後,5週齢で試験に供した.1群の動物数は雌雄各5匹とし,対照群および最高用量群については別に雌雄各5匹の14日間回復群を設けた.投与開始時の体重は雄で133〜155 g,雌で119〜142 gであった.ラットは,温度22〜23 ℃,湿度58〜65 %に制御した飼育室で,金網ケージに個体別に収容し,固型飼料[ラボMRストック,日本農産工業(株)]および水を自由に摂取させて飼育した.
3. 投与量および投与方法
投与量設定試験として,1群雌雄各4匹のラットに被験物質を0,50,100,200,500および1000 mg/kg用量で14日間反復経口投与した結果,200 mg/kg群の雄並びに500および1000 mg/kg群の雌雄に,肝臓相対重量の増加が認められた.また,500および1000 mg/kg群の雄に尿pHの低下,さらに1000 mg/kg群の雄に血清ナトリウムおよび塩素の低値が認められた.したがって,本試験における投与量は,1000 mg/kg群を最高用量とし,以下250,60および15 mg/kgの4用量を設定した.投与方法は,投与液量を体重1 kg当たり5 mLとし,テフロン製胃ゾンデを装着した注射筒を用いて1日1回(午前中),28日間にわたって経口投与した.対照群には,局方精製水を同様に投与した.
4. 観察および検査
1) 一般状態観察
28日間の投与期間およびそれに続く14日間の回復期間を通じて,動物の生死,外観,行動等を毎日観察した.
2) 体重および摂餌量測定
体重は,週2回,3あるいは4日ごと,および屠殺日に測定した.摂餌量は,毎週1回,1日(24時間)の飼料消費量を測定した.
3) 尿検査
雄は投与26日および投与期間終了後13日,雌は投与25日および投与期間終了後12日に,腰部を刺激して新鮮尿を採取し,外観の観察並びにpH,潜血,タンパク,糖,ケトン体,ビリルビンおよびウロビリノーゲン(以上,試験紙法:マルティスティックス®,バイエル・三共(株))の定性的検査を行った.
4) 血液学検査
採血は,投与期間および回復期間終了翌日にエーテル麻酔下で開腹して腹大動脈より行なった.動物は採血前日の午後5時から除餌し,水のみを給与した.採取した血液は3分割し,その一部は,EDTA-2Kで凝固防止処理し,多項目自動血球計数装置[東亜医用電子(株),E- 4000]により,赤血球数(電気抵抗検出方式),血色素量(ラウリル硫酸ナトリウム-ヘモグロビン法),ヘマトクリット値(パルス検出方式),平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC,以上計算値),白血球数および血小板数(以上,電気抵抗検出方式)を,また塗抹標本を作製して網状赤血球数(Brilliant cresyl blueで染色して鏡検)および白血球百分率(May-Giemsaで染色して鏡検)を測定した.また一部は,3.8 %クエン酸ナトリウム液で凝固阻止処理して血漿を分離し,血液凝固自動測定装置(アメルング社,KC-10A)により,プロトロンビン時間(PT,Quick一段法)および活性化部分トロンボプラスチン時間(APTT,エラジン酸活性化法)を測定した.
5) 血液生化学検査
採取した血液の一部から血清を分離し,生化学自動分析装置[日本電子(株),JCA-BM8]により,総タンパク(Biuret法),アルブミン(BCG法),A/G比(計算値),グルコース,トリグリセライド,総コレステロール(以上,酵素法),総ビリルビン(ジアゾ法),尿素窒素(Urease-UV法),クレアチニン(Jaff 法),GOT,GPT,ALP(以上,JSCC法),γ-GTP(SSCC法),LDH(SFBC法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-132]により,ナトリウム,カリウムおよび塩素を測定した.
法),GOT,GPT,ALP(以上,JSCC法),γ-GTP(SSCC法),LDH(SFBC法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-132]により,ナトリウム,カリウムおよび塩素を測定した.
6) 病理学検査
投与期間あるいは回復期間終了翌日の採血に続いて放血屠殺して剖検した.また,脳,心臓,胸腺,肝臓,腎臓,脾臓,副腎,精巣,精巣上体,卵巣および子宮を秤量(絶対重量)し,また,対体重比(相対重量)を算出した.病理組織学検査は,採取した器官を10 %中性リン酸緩衝ホルマリン液(精巣および精巣上体のみブアン液で固定)固定後,対照群および1000 mg/kg群については,脳,甲状腺(上皮小体を含む),胸腺,心臓,肺,肝臓,腎臓,脾臓,副腎,胃,膀胱,脊髄,坐骨神経,骨髄,小腸,大腸,リンパ節,さらに雄では精巣,精巣上体,前立腺,雌では卵巣,子宮を検査した.他の投与群並びに回復群については,1000 mg/kg群で被験物質の投与に起因する変化が認められなかったので,検査は実施しなかった.検査は,常法によりパラフィン切片を作製し,ヘマトキシリン・エオジン染色を施して鏡検した.
5. 統計処理
パラメトリックデータはBartlettの分散検定を行い,分散が一様な場合は一元配置の分散分析を行った.分散が一様でない場合およびノンパラメトリックデータは,Kruskal-Wallisの順位検定を行った.それらの結果,有意差を認めた場合,Dunnett法またはScheff 群間で標本数が異なる場合)の方法により対照群に対する各群の比較検定を行った.カテゴリカルデータには,Fisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.
群間で標本数が異なる場合)の方法により対照群に対する各群の比較検定を行った.カテゴリカルデータには,Fisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.
結果
1. 一般状態および死亡
投与および回復期間を通じて,雌雄のいずれにも一般状態の変化および死亡は認められなかった.
2. 体重(Fig. 1)
投与および回復期間を通じて,体重に有意な変化は認められなかった.
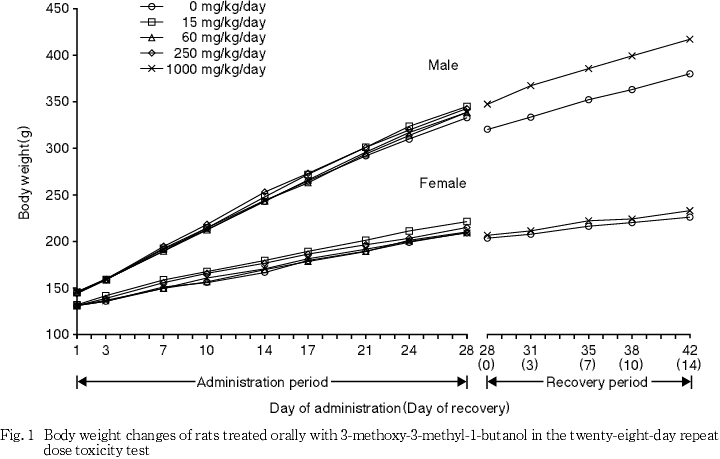
3. 摂餌量
投与および回復期間を通じて,摂餌量に有意な変化は認められなかった.
4. 尿検査
投与期間中および回復期間中の検査を通じて,各検査項目に有意な変化は認められなかった.
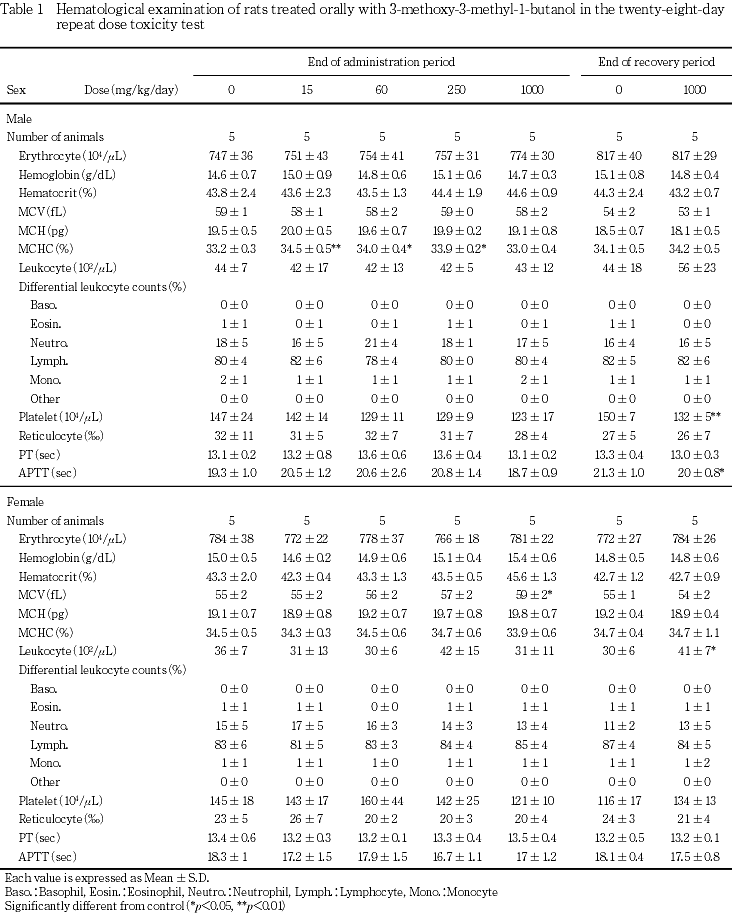
5. 血液学検査(Table 1)
投与期間終了時の検査において,1000 mg/kg群で雌に平均赤血球容積の有意な増加が認められた.これは対照群と比べてヘマトクリット値が高値傾向にあったためであるが,ヘマトクリット値の変化に有意差は認められなかった.また,15,60および250 mg/kg群の雄の平均血色素濃度は対照群と比べて高値を示し,有意差が認められたが,変化に用量相関性は認められなかった.
回復期間終了時の検査においては,投与期間終了時の検査で認められた平均赤血球容積の変化は認められな
かった.
なお,回復群で雄に活性化部分トロンボプラスチン時間および血小板数の有意な低値,雌に白血球数の有意な高値が認められたが,これらはいずれも投与期間終了時の検査では認められなかった変化で,しかも背景データにおける正常範囲内の変動であったことから,被験物質の投与とは無関係な偶発的所見と判断された.
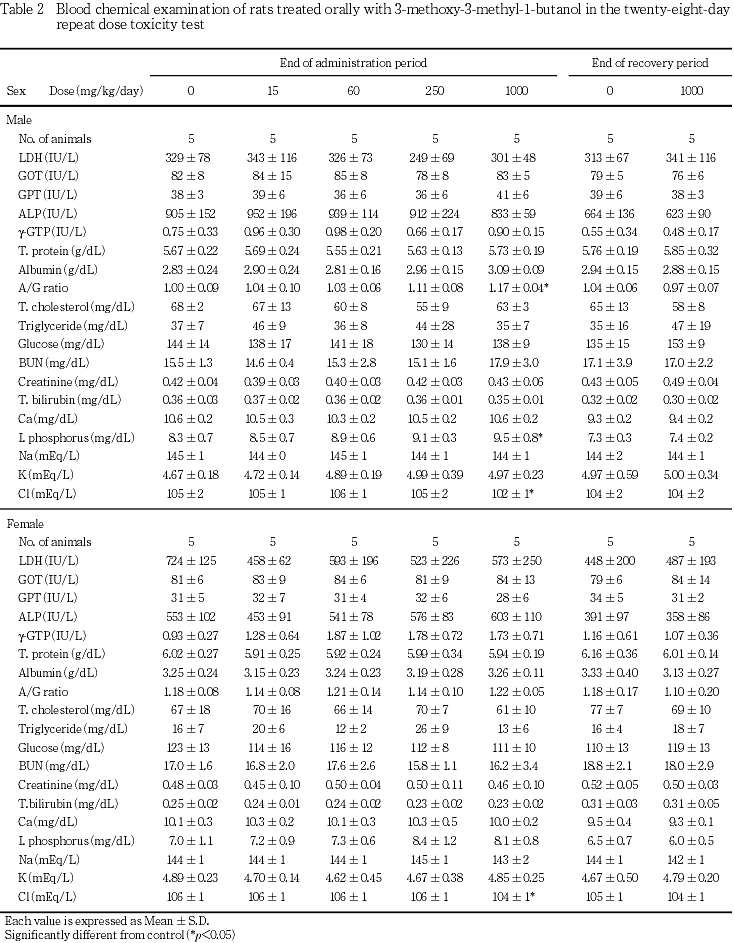
6. 血液生化学検査(Table 2)
投与期間終了時の検査において,1000 mg/kg群で雌雄に塩素の有意な減少並びに雄に主にアルブミンの増加傾向によるA/G比の有意な増加および無機リンの有意な増加が認められた.
回復期間終了時の検査においては,各検査項目に有意な変化は認められなかった.
7. 剖検
被験物質の投与に起因する変化は認められなかった.
投与とは無関係な所見として,投与期間終了時屠殺動物において,胸腺の赤色斑が対照群の雄の1匹に,また,子宮の子宮腔水腫が雌の対照群および1000 mg/kg群の各1匹に認められた.
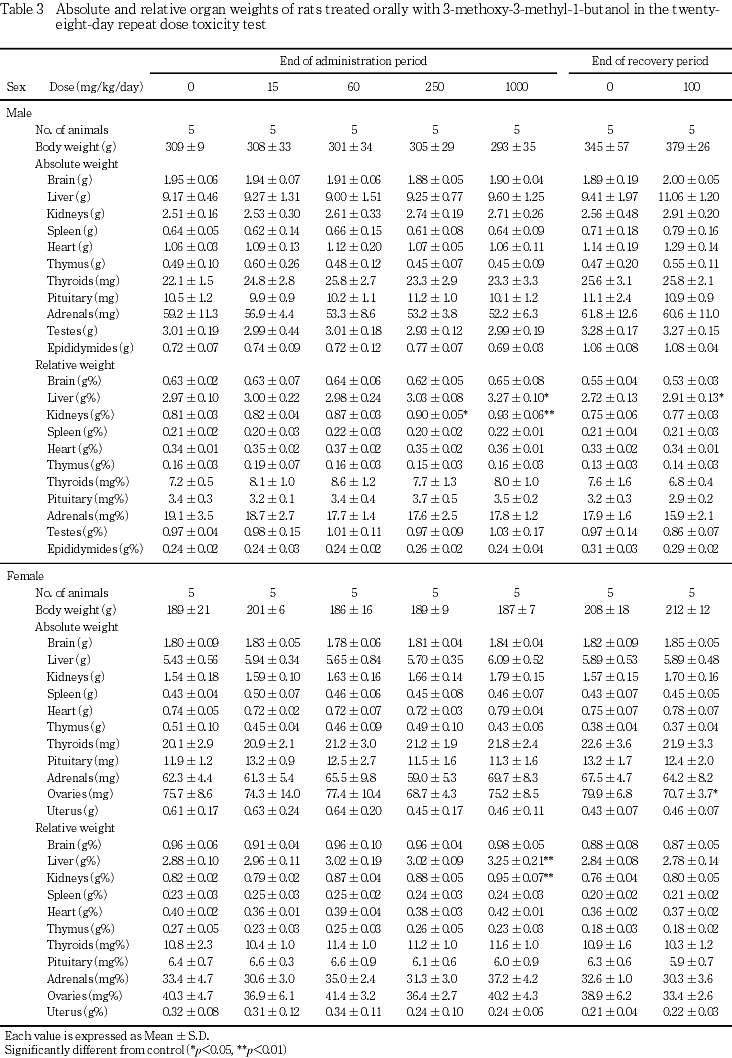
8. 器官重量(Table 3)
投与期間終了時屠殺動物において,250 mg/kg群の雄および1000 mg/kg群の雌雄に腎臓の相対重量の有意な増加,また,1000 mg/kg群の雌雄に肝臓の相対重量の有意な増加が認められた.
回復期間終了時屠殺動物において,雄の肝臓の相対重量に有意差が残るものの,変化の程度は投与期間終了時屠殺動物と比べて軽減する傾向にあり,雌の肝臓および雌雄の腎臓の相対重量には有意な変化は認められなかった.
なお,回復群の雌で卵巣の絶対重量に有意な低値が認められたが,投与期間終了時屠殺動物には認められない変化であり,被験物質の投与とは無関係な偶発的所見と判断された.
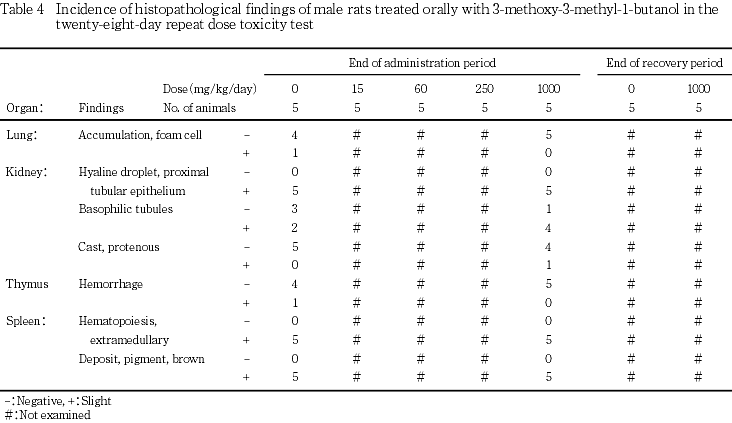
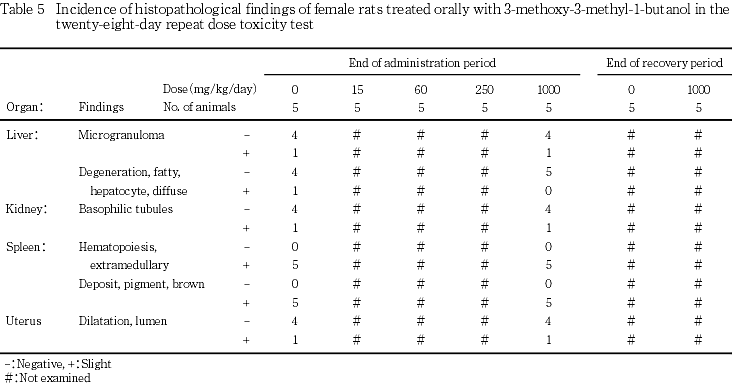
9. 病理組織学検査(Tables 4, 5)
投与期間終了時屠殺動物において,被験物質の投与に起因する変化は認められなかった.
なお,被験物質の投与とは無関係と考えられる変化として,対照群および1000 mg/kg群の雌雄あるいはそのいずれかに,肺の泡沫細胞集簇,肝臓の微小肉芽腫および肝細胞脂肪変性,腎臓の好塩基性尿細管および片側性蛋白円柱,胸腺の出血,子宮の子宮腔拡張が認められたが,散発的な変化であった.また,脾臓の髄外造血および褐色色素沈着が雌雄の全例に,腎臓の近位尿細管上皮の硝子滴が雄の全例に認められたが,対照群と比べて変化の程度に差は認められなかった.
考察
3-メトキシ-3-メチル-1-ブタノールのラットへの28日間反復投与において,主に肝臓および腎臓に対する影響が認められた.
肝臓に対する影響について,肝臓相対重量の増加が1000 mg/kg群の雌雄に認められた.1000 mg/kg群の雄に認められた主にアルブミンの増加傾向によるA/G比の増加も,肝臓に対する影響と関連する変化と考えられる.しかしながら,肝臓には被験物質の投与に起因する病理組織学的変化は認められず,血液生化学検査においてもGOT,GPTの増加等,肝機能障害を示唆する変化は認められなかった.
腎臓に対する影響について,腎臓相対重量の増加が250 mg/kg群の雄並びに1000 mg/kg群の雌雄に認められた.血液生化学検査で1000 mg/kg群の雌雄に認められた塩素の減少および雄に認められた無機リンの増加は,腎機能に対する影響を示唆する変化と考えられる.しかしながら,病理組織学検査では,腎臓に被験物質の投与に起因する変化は認められなかった.
3-メトキシ-3-メチル-1-ブタノールを8,40,200および1000 mg/kg/dayでラットに投与して実施した簡易生殖毒性試験において,親動物に肝臓重量の増加が1000 mg/kg群の雌,腎臓重量の増加が200 mg/kg群の雄および1000 mg/kg群の雌雄に認められている1).本試験においても肝臓および腎臓に対する影響がほぼ同じ用量で発現し,簡易生殖毒性試験での親動物に対する影響と類似した結果であった.
なお,血液学検査で認められた1000 mg/kg群の雌の平均赤血球容積の増加については,各個体における値(56〜60 fL)が背景データにおける正常範囲(51〜61 fL)内のもので,他に関連する変化も認められなかったことから,被験物質の投与とは無関係な偶発的所見と判断される.
これらの投与期間終了時屠殺動物において認められた変化は,回復群では雄の肝臓相対重量の増加に有意差が残るものの回復傾向が認められ,その他の変化はいずれも回復した.したがって,3-メトキシ-3-メチル-1-ブタノールの毒性影響は,可逆的変化であると判断された.
以上の結果から,3-メトキシ-3-メチル-1-ブタノールのラットへの28日間反復経口投与において認められた主な毒性は,肝臓および腎臓に対する影響であった.無影響量は,雄で60 mg/kg/day,雌で250 mg/kg/dayと判断された.
文献
| 1) | 野田篤,山口真樹子,伊藤雅也,昆尚美,伊藤義彦,化学物質毒性試験報告,10, 586(2003). |
| 連絡先 |
| 試験責任者: | 伊藤義彦 |
| 試験担当者: | 野田 篤,伊藤雅也,赤木 博,山口真樹子 |
| (財)畜産生物科学安全研究所 |
| 〒229-1132 神奈川県相模原市橋本台3-7-11 |
| Tel 042-762-2775 | Fax 042-762-7979 | |
| Correspondence |
| Authors: | Yoshihiko Ito(Study director)
Atsushi Noda, Masaya Ito, Hiroshi Akagi, Makiko Yamaguchi |
| Research Institute for Animal Science in Biochemistry and Toxicology 3-7-11 |
| Hashimotodai, Sagamihara-shi, kanagawa, 229-1132 Japan |
| Tel +81-42-762-2775 | Fax +81-42-762-7979 | |

 法),GOT,GPT,ALP(以上,JSCC法),γ-GTP(SSCC法),LDH(SFBC法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-132]により,ナトリウム,カリウムおよび塩素を測定した.
法),GOT,GPT,ALP(以上,JSCC法),γ-GTP(SSCC法),LDH(SFBC法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置[東亜電波工業(株),NAKL-132]により,ナトリウム,カリウムおよび塩素を測定した.
 群間で標本数が異なる場合)の方法により対照群に対する各群の比較検定を行った.カテゴリカルデータには,Fisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.
群間で標本数が異なる場合)の方法により対照群に対する各群の比較検定を行った.カテゴリカルデータには,Fisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.





