イソチオシアン酸メチル(別名 メチルイソチオシアネート)は,化学物質管理促進法(PRTR法)で第一種指定化学物質に指定される劇物(化審法:2-1687)であるが,一部の野菜の辛味成分として含まれ,土壌燻蒸剤,ジチオカルバメート等のカルバメイト系殺虫剤の分解物質として環境中にも存在する物質である1〜3).イソチオシアン酸メチルの,雌雄動物に対する反復投与による影響とその回復性,親動物の生殖・発生および新生児の発育に及ぼす影響を検討するために,0(溶媒対照,コーン油),0.5,2および8 mg/kgのイソチオシアン酸メチルを雌雄のSprague-Dawley系ラット(各12匹/群)に反復経口投与した.投与2週間目に2週間を限度として交配させ,雄は交配期間終了2週間目に剖検した.雌は交配後,自然分娩させて母動物は哺育5日に,出生児は哺育4日に剖検した.また,0および8 mg/kg投与群の各雄5匹および雌の回復群(0および8 mg/kg)は42日間投与した後,14日間休薬させて剖検した.その結果を以下に要約した.
死亡および切迫屠殺動物はいずれの群でもみられなかった.イソチオシアン酸メチル投与に起因した変化として,投与期間中,2 mg/kg投与群の雄1例および8 mg/kg投与群の雌雄で,投与後に一時的な流涎が観察され,8 mg/kg投与群の雄では体重増加抑制および摂餌量の減少も認められた.
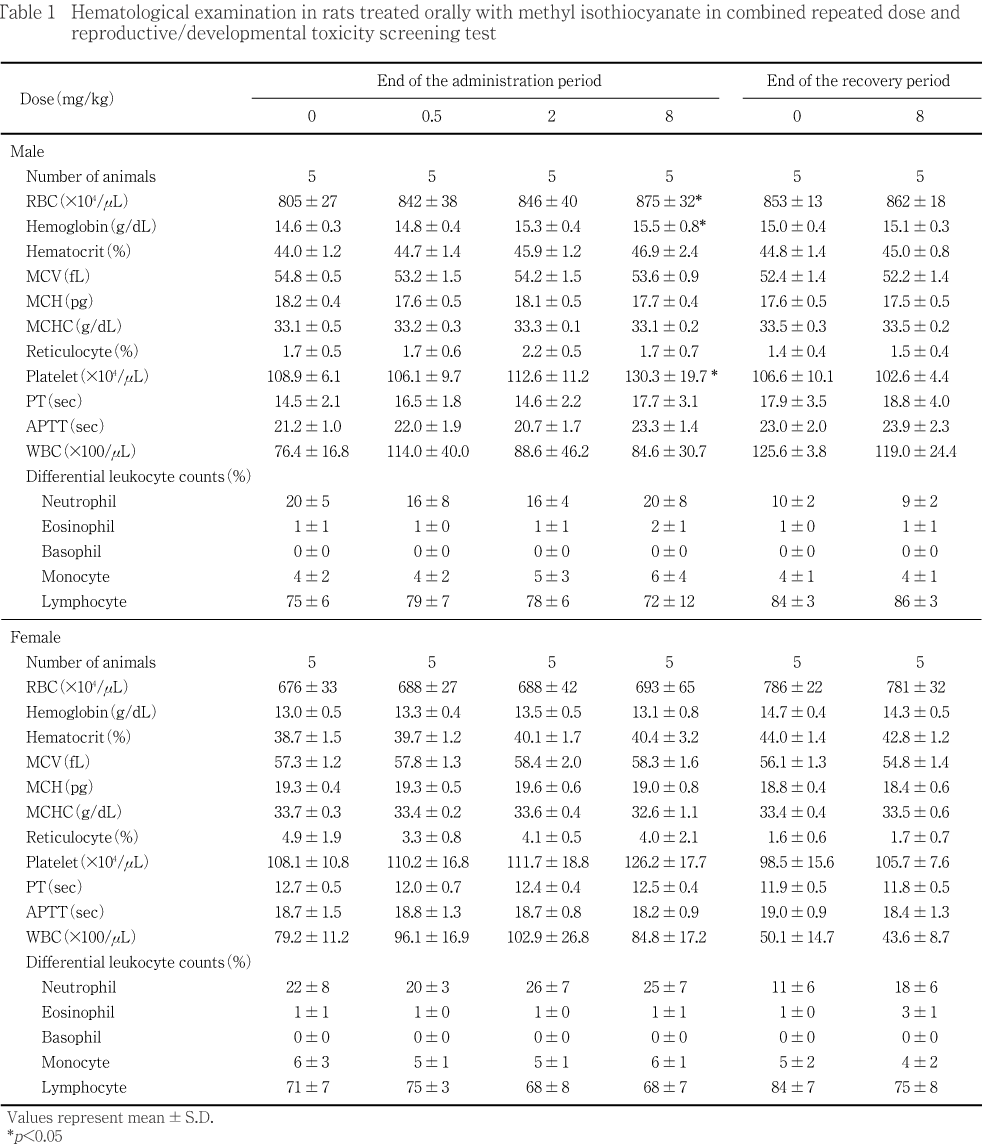
投与期間終了時の血液学検査では,8 mg/kg投与群の雄で赤血球数および血色素量の増加が認められ,病理学検査では,2および8 mg/kg投与群の雌雄で,肉眼的に前胃粘膜の肥厚あるいは水腫を呈し,組織学的には前胃粘膜に扁平上皮細胞の乳頭状過形成が認められた.
14日間の休薬により,8 mg/kg投与群の体重は対照群に比較して有意に増加し,赤血球数および血色素量は対照群と比較して差は認められなかった.一方,前胃粘膜の器質的変化は投与期間終了時に比較して軽減する傾向はみられたものの,完全に回復するには至らなかった.
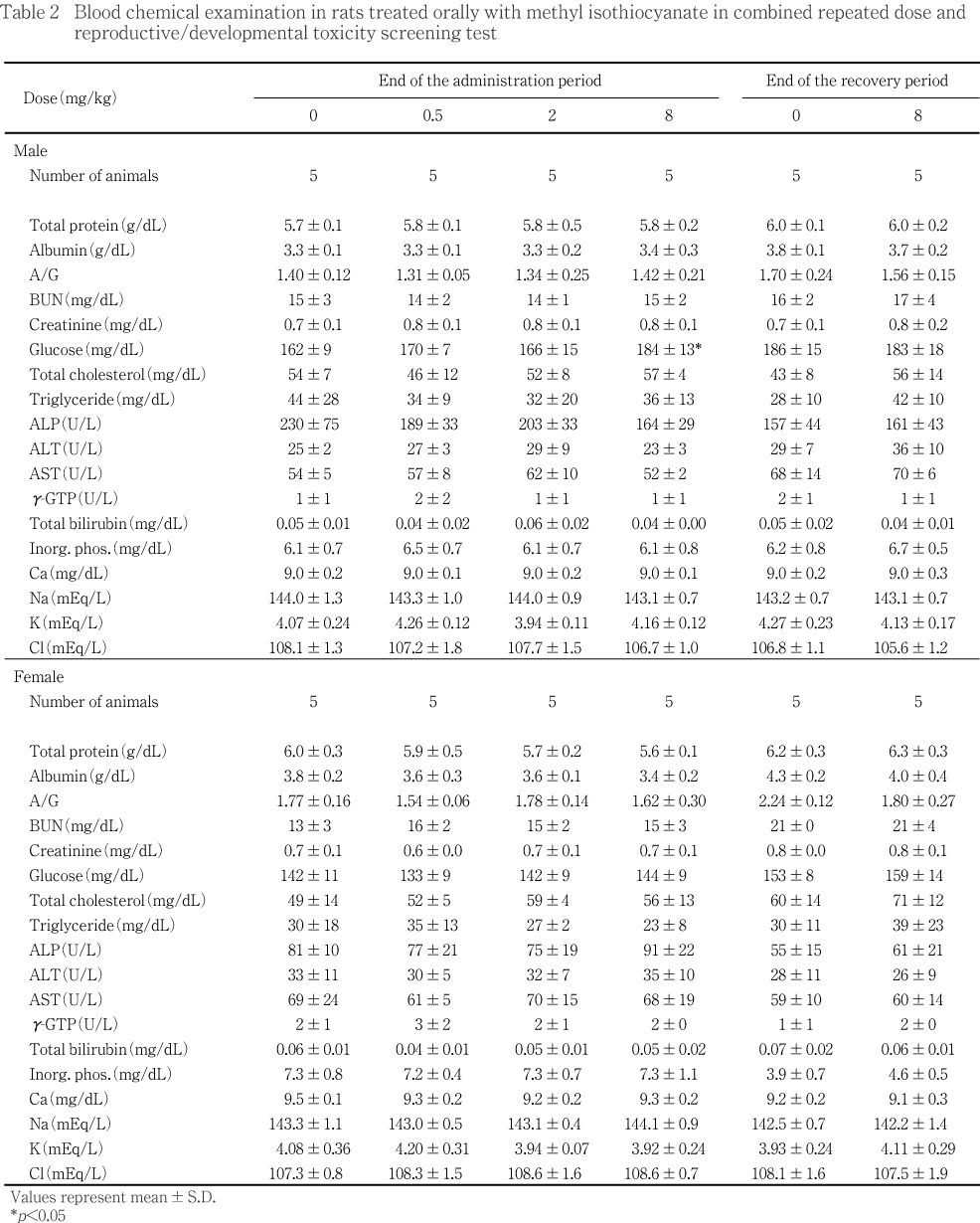
その他,血液生化学検査および器官重量結果には,イソチオシアン酸メチル投与による影響と断定できる変化は認められなかった.また,詳細な症状観察および機能検査でも異常は認められず,神経毒性を示唆する所見はみられなかった.
8 mg/kg投与群で,分娩/哺育状態の不良とそれによると考えられる全出生児の死亡がみられ,哺育4日の哺育児数および新生児生存率に低い傾向が認められた.生殖発生毒性に関しては,性周期,交尾率,受胎率,出産率,妊娠期間,黄体数,着床数,着床率,分娩率に被験物質投与の影響は認められなかった.哺育児の観察については,生児出産率,出生率および性比に被験物質投与の影響は認められなかった.また,出生児の体重に変化はみられず,投与に起因したと考えられる形態異常も認められなかった.
以上の結果より,本試験条件下でのイソチオシアン酸メチルの無作用量は以下の通りと推定された.
反復投与毒性に関しては,8 mg/kg投与群の雄で体重増加抑制および摂餌量の減少がみられ,2 mg/kg以上の投与群でイソチオシアン酸メチルの刺激性に起因した流涎および前胃粘膜における器質的変化が認められたことから,雌雄ともに0.5 mg/kg/dayと判断された.また,前胃粘膜の病理所見は14日間の休薬で投与期間終了時の変化と比較して軽減する傾向はみられたものの,消失するには至らなかった.
生殖発生毒性に関しては,8 mg/kg投与群の母動物で分娩/哺育状態の不良がみられたことから,雌では2 mg/kg/dayと判断された.雄および出生児については,8 mg/kg投与群でもイソチオシアン酸メチル投与に起因した影響が認められなかったことから,8 mg/kg/day以上と判断された.
被験物質として用いたイソチオシアン酸メチルは,水に不溶,エタノールおよびクロロホルムに混和する黄褐色澄明の液体で,強い刺激臭を有し凝固点は34.4℃,沸点は119℃である.本試験には和光純薬工業(大阪)から購入したイソチオシアン酸メチル'ロット番号: TWR4288,含量99.8 %(GC)"を用いた.被験物質は受領後,使用時まで密閉して冷蔵下で保管し,試験期間中の被験物質の安定性を残余被験物質を用いた品質試験成績により確認した.
試験には日本チャールス・リバー厚木飼育センター生産のSprague-Dawley(SD)系[Crj:CD(SD)IGS,SPF] の雌雄ラットを使用した.動物は8週齢で購入し,入荷日を含めて15日間予備飼育した.検疫・馴化期間中,毎日一般状態を観察し,入荷日および検疫終了日に体重を測定した.また,雌全例の性周期を入荷翌日から13日間観察したほか,検疫期間中に雌雄全例の詳細な症状観察を実施した.試験には一般状態ならびに詳細な一般状態の観察,体重ならびに性周期に異常の認められない動物を,検疫終了時の測定体重をもとに体重別層化無作為抽出法により,雄は1群12匹よりなる4群に,雌は1群12匹よりなる4群ならびに1群5匹よりなる2群(回復群)に群分けし使用した.
全飼育期間を通じ動物は金属製金網床ケージに1匹ずつ収容し,許容温度21.0〜25.0℃,許容湿度40.0〜75.0 %,換気回数約15回/時間,照明12時間(7時〜19時点灯)に制御された飼育室で,固形飼料(CE-2,日本クレア)および水道水(秦野市水道局給水)を自由に摂取させて飼育した.ただし,妊娠18日(腟栓あるいは精子発見日=妊娠0日)以降の母動物は,ラット用プラスチック製繁殖ケージに収容し,哺育4日(哺育0日=分娩日)まで紙パルプ製チップ(ペパークリーン,日本エスエルシー)を床敷として供給して飼育した.
被験物質を約37℃の温水中で融解させた後,秤量して媒体を加え,0.16 w/v%溶液を調製した.これを媒体で段階希釈して0.04および0.01 w/v%溶液を調製した.被験物質が水に不溶で油に溶解するため,媒体はコーン油(ロット番号V2E7069,製造元:ナカライテスク)を選択した.調製した投与検体は冷蔵下に保管した.
投与に先立ち本被験物質の0.01 および40 w/v%溶液について冷蔵条件下における調製後8日間の安定性を確認し,また,初回投与時検体中の被験物質含量をガスクロマトグラフ(GC)法により測定し規定範囲内にあることを確認した.なお,投与検体は溶液のため均一性試験は実施しなかった.
本試験の投与量は予備試験の結果をもとに設定した.イソチオシアン酸メチルの10,25あるいは50 mg/kgを妊娠14日から分娩までの雌に反復投与した結果,50 mg/kg投与群では3例中2例が死亡し残る1例も切迫屠殺に至った.死亡例の剖検結果では胃漿膜面と腹腔内諸器官との癒着,前胃粘膜の剥離と菲薄化,腹水の貯留が認められ,胸腺は著しく小型化していた.これらの所見から,50 mg/kg投与群に認められた毒性の原因は胃に対する本被験物質による刺激に基づくものと判断した.同様の所見は,程度は軽いものの25 mg/kg投与群の3例全例,10 mg/kg投与群の3例中1例でも認められた.以上の結果から,本試験での投与期間を考慮すると本被験物質の10 mg/kgの投与は最大耐量を若干上回るものと考えられた.従って,本試験における高用量群の投与量を8 mg/kgに設定し,以下,公比4で除して中用量を2 mg/kg,低用量を0.5 mg/kgとした.
雄では交配前2週間から最長2週間の交配期間を経て剖検前日に至るまでの連続42日間,雌は交配前2週間,交尾までの交配期間,妊娠期間および哺育4日まで,回復群の雌は連続42日間,それぞれ毎日1回,ラット用胃管を用いて強制的に経口投与した.投与容量は 5 mL/kgとし,雌雄とも最近時に測定した体重に基づいて各動物の投与液量を算出した.
回復試験動物として雄は対照群および高用量群のうち各5例,雌は回復群の全例を最終投与翌日(回復1日)から14日間休薬した.
全例について飼育期間中および回復期間中は毎日1回,投与期間中は投与前後の毎日2回観察した.
雄の全例について検疫期間中(全入荷動物対象)1回,投与7,14,21,28,35および42日,回復試験動物ではさらに回復7および14日にスコアリング法による詳細な症状観察を行った.雌の全例については,検疫期間中(全入荷動物対象)1回,投与7,14,21,28,35および42日に詳細な症状観察を実施した.なお,観察日が分娩中であった例は哺育0日に観察した.その他の分娩例は哺育0日から4日の間に1回観察し,さらに回復群は回復7および14日に観察した.詳細な症状観察は,まずケージ越しでの観察(姿勢・体位,自発運動,発声,振戦,痙攣)を行った後,ケージから取り出す際に外表を観察し(取り出し易さ,扱い易さ,心拍動,体温,被毛,皮膚色,可視粘膜,流涙,眼球突出,瞳孔径,流涎),作業台上での行動の正常性を観察(姿勢・体位,探索行動,身づくろい,発声,挙尾反応,歩行,常同行動,奇異行動,振戦,痙攣,立毛,眼裂)した.
雄では投与42日の詳細な症状観察に引き続き,各群の5例および雄の回復試験動物について,また,回復14日の詳細な症状観察の後,雄の回復試験動物全例について機能検査を実施した.雌では哺育4日に機能検査を実施したが,実施日における投与日数が近い各群5匹について行った.雌の回復試験動物では投与42日および回復14日のそれぞれ詳細な症状観察に引き続き全例の機能検査を実施した.機能検査はプライエル反応,瞳孔反射,視覚定位,驚愕反応,後肢引込み反射,眼瞼(瞬目)反射,正向反射の有無を観察した.
雄および雌の回復試験動物は全例について投与1(投与開始日),7,14,21,28,35および42日ならびに解剖日(最終投与翌日)に体重を測定し,雌雄の回復試験動物はさらに回復1,7および14日ならびに解剖日(回復15日)にも体重を測定した.母動物は,投与1,7および14日,交尾確認後は妊娠0(交尾確認日),7,14および20日,分娩後は哺育0(分娩日)および4日ならびに解剖日に体重を測定した.
雄および雌の回復試験動物は全例について投与1,7,14,29,35および41日に餌の重量を測定し翌日までの差をもって摂餌量とした.雌雄の回復試験動物はさらに回復6〜7および13〜14日に摂餌量を測定した.母動物は投与1〜2,7〜8および14〜15日,交尾確認後は妊娠0〜1,7〜8,14〜15および20〜21日,分娩後は哺育3〜4日に摂餌量を測定した.
回復試験動物を除く雌全例について,群分け前日までの性周期観察に引き続いて投与開始以降,腟スメア標本を毎日採取し各動物の同居後交尾が確認されるまで性周期を観察した.
性周期は発情期,発情前期および発情休止期に分類した.これらの分類に基づき性周期の型を4日あるいは5日間隔で発情を回帰するものをそれぞれの周期に,それ以外を不正周期に分類し,投与開始後,4あるいは5日間隔の性周期がそれ以外の性周期に変化した動物の頻度を群毎に算出した.
投与15日から回復試験動物の雌を除く雌雄全例を,同群内の雌雄の組み合わせで連日1:1で同居させ交配を行った.交配は交尾を確認するまで2週間を限度として実施し,交尾の確認は腟スメアの中の精子の存在あるいは腟栓を確認することにより行った.交尾が確認された雌は,交尾確認日を妊娠0日と起算して雄から分離し個別に飼育した.
交配結果から,雌雄同居開始日から交尾確認日までの日数およびその間に回帰した発情期の回数,各群の交尾率'(交尾動物数/交配動物数)×100,%"および受胎率'(妊娠動物数/交尾動物数)×100,%"を算出した.
各群とも交尾した雌は全例を自然分娩させて哺育させた.
分娩の確認は妊娠21日から分娩が確認されるまで毎日行い,午前11時までに分娩が完了した例についてその日を哺育0日とした.分娩状態を直接観察できた例は異常の有無を断続的に観察し,直接観察できなかった例は分娩前後の一般状態および産児の状態から異常の有無を判断した.
分娩した全例の妊娠期間(妊娠0日から分娩日までの日数)を求め,各群の出産率'(生児出産雌数/妊娠動物数)×100,%"を算出した.また,哺育1日から毎日,哺育状態を観察し,哺育5日の剖検時に観察した着床数および妊娠黄体数から着床率'(着床数/妊娠黄体数) ×100,%"を算出した.
哺育0日に生存児数および死亡児数を雌雄別に数えて性別および外表奇形の有無を観察し,分娩率'(産児数/着床痕数)×100,%",生児出産率'(出産生児数/着床痕数)×100,%"および出生率'(出産生児数/産児数) ×100,%"を算出した.哺育1〜4日まで毎日,一般状態を観察し,生児数と死亡児数を雌雄別に数え新生児生存率'(哺育4日の生児数/哺育0日の生児数)×100,%"を算出した.生存児については哺育0および4日に個別の体重を測定し,各腹ごとに雌雄別の平均値を算出するとともに,哺育0および4日における性比'哺育0あるいは4日の雄生児数/哺育0あるいは4日の雌生児数"を算出した.
雄の投与終了時剖検例は投与42日の翌日に,雌雄の回復試験動物は回復15日に,母動物は哺育4日の翌日にそれぞれ解剖した.全例いずれも解剖前18〜24時間絶食させた後,ペントバルビタールナトリウム麻酔下で放血致死あるいは採血後に放血致死させて解剖するとともに,血液学検査,血液生化学検査および病理学検査を実施した.なお,採血は腹部後大静脈から行い,雄の投与終了時剖検では各群の5例を,雌の投与終了時剖検では投与期間が近接した各群5例を選んで,雌雄の回復試験動物は全例を対象とした.
出生児のうち,死亡児は発見後すみやかに剖検し,0.1Mリン酸緩衝10 v/v%ホルマリン溶液に固定して保存した.生存児は全例を哺育4日にエーテル吸入により致死させ剖検した.
プロトロンビン時間および活性部分トロンボプラスチン時間は抗凝固剤として10分の1容のクエン酸ナトリウムを用いて採取した血液から血漿を分離し,全自動血液凝固測定装置(CA-1000,東亜医用電子)を用いて光散乱法によって測定した.また,抗凝固剤としてEDTA-2 Kを用いて採取した血液により,血液自動分析装置(CELL-DYN3500SL,ダイナボット)を用いて白血球数をフローサイトメトリー・レーザ光散乱法あるいは電気抵抗法で,白血球分類はフローサイトメトリー・レーザ光散乱法で,血小板数は電気抵抗法でそれぞれ測定した.同時に赤血球数ならびに平均赤血球容積を電気抵抗法で,血色素量を吸光度により測定し,ヘマトクリット値,平均赤血球血色素濃度および平均赤血球血色素量を計算した.また,EDTA-2 K加血液についてBrecher法で網状赤血球比率の測定を行った.
抗凝固剤としてヘパリンを用いて採取した血液から血漿を分離し,遠心方式生化学自動分析装置(COBAS MIRA plus,ロッシュダイアグノスティックス)を用いて,総蛋白濃度はビュウレット法で,アルブミン濃度はBCG法で,総コレステロール濃度はコレステロールオキシダーゼ・HDAOS法で,グルコース濃度はヘキソキナーゼ・G-6-PDH法で,尿素窒素濃度はウレアーゼGlDH法で,クレアチニン濃度はJaff事@で,アルカリフォスファターゼ(ALP)活性はGSCC法で,AST(GOT)活性,ALT(GPT)活性およびg-グルタミルトランスペプチダーゼ(g-GTP)活性はIFCC法で,トリグリセライド濃度はGPO・HDAOS法で,無機リン濃度はモリブデン酸直接法で,総ビリルビン濃度はアゾビリルビン法で,カルシウム濃度はOCPC法で測定し,A/G比は算出した.また,ヘパリン加血液からの血漿について全自動電解質分析装置(EA05, A&T)を用い,イオン電極法によってナトリウム,カリウムおよび塩素の各濃度を測定した.
全例を剖検し,器官・組織の肉眼的観察を行った.雌雄ともに血液学検査および血液生化学検査を実施した動物の脳,心臓,胸腺,肝臓,腎臓,脾臓,副腎,精巣および精巣上体の重量(実重量)を測定し,相対重量を算出した.また,全例の脳,下垂体,脊髄,心臓,気管,肺(気管支を含む),肝臓,腎臓,胸腺,脾臓,副腎,甲状腺および上皮小体,胃,十二指腸,空腸,回腸,盲腸,結腸,直腸,精巣,精巣上体,前立腺腹葉,凝固腺を含む精嚢,卵巣,子宮,腟,膀胱,下顎リンパ節,腸間膜リンパ節,坐骨神経,大腿骨髄,病変部を採取し,保存した.肺は0.1Mリン酸緩衝10 v/v%ホルマリン溶液で注入固定してから採取した.子宮は着床数を数えて,分娩例の卵巣は実体顕微鏡下で妊娠黄体数を数えた.採取した器官・組織のうち,精巣ならびに精巣上体はブアン液(長期保存は0.1Mリン酸緩衝10 v/v%ホルマリン溶液を使用)に固定し,その他は0.1Mリン酸緩衝10 v/v%ホルマリン溶液に固定した.
卵巣,精巣および精巣上体は全例について,肉眼的観察で変化がみられた病変部は該当動物のみについて,これ以外の器官・組織は雄の投与終了時剖検および母動物では対照群と高用量群のうち血液学検査および血液生化学検査を実施した各5例について,それぞれ病理組織学検査を実施した.また,肉眼的観察の結果,被験物質投与によると推定される異常が認められた胃については,投与終了剖検時での雌雄の低用量および中用量群の血液学検査および血液生化学検査を実施した各5例について,回復試験動物は雌雄の全例について病理組織学検査を実施した.これらの器官・組織はパラフィン包埋して薄切しヘマトキシリン・エオジン染色標本を作製して,光学顕微鏡を用いて検査した.
機能検査結果,性周期の変化した動物の頻度,交尾率,受胎率ならびに出生児の形態異常の出現頻度についてはFisherの直接確率検定を行った.
病理組織学検査所見では,グレード分けしたデータはMann-WhitneyのU検定により,陽性グレードの合計値はFisherの直接確率の片側検定により対照群と被験物質投与群との間で有意差検定を行った.その他のデータのうち解析の対象が3群以上の場合は多重比較検定を行った.すなわち,個体ごとに得られた値あるいはlitterごとの平均値を1標本とし,パラメトリックなデータは先ず,Bartlettの方法により等分散性の検定を行い,分散が一様である場合は一元配置分散分析を行った.いずれかの群で分散が0となった場合,分散が等しくない場合およびノンパラメトリックデータはKruskal-Wallisの順位検定を行った.群間に有意性が認められた場合は,Dunnett法またはDunnett型の検定法により群間の比較を行った.回復試験等,解析の対象が2群の場合にはまずF検定を行い,有意差が認められなければStudent's-t検定を,有意差が認められた場合は,Aspin-Welchの検定を行った.有意水準はいずれも5 %とした.
死亡および瀕死動物はいずれの群でも認められなかった.
投与期間中,8 mg/kg投与群の雌雄で投与直後の一時的な流涎が投与6日以降から投与期間を通して観察された.この流涎は,雄では12例中11例で,雌では17例中8例で認められ雄では雌に比較して発現頻度が高い傾向がみられた.また,2 mg/kg投与群の雄1例でも投与直後の一時的な流涎が1回のみ認められた.
8 mg/kg投与群の雌1例では分娩日(哺育0日)から腟からの出血によると思われる腟周囲の褐色の汚れが認められ,哺育2日には眼瞼周囲の汚れも観察された.同例の被毛の汚れは哺育3日には消失した.
その他,2 mg/kg投与群の雄1例では上顎切歯の欠損が投与3〜4週に観察されたが,これは被験物質投与の影響ではなく物理的衝撃によるものとみられた.この例では体重増加が一過性に抑制されたが切歯の萌出とともに回復した.
回復期間中には,いずれの群にも流涎等の一般状態の変化は認められなかった.
投与期間中および回復期間中ともに,いずれの群においても特記すべき変化は認められず,神経毒性を示唆する所見は観察されなかった.
投与期間終了時および回復期間終了時ともに,いずれの群においても異常は認められなかった.
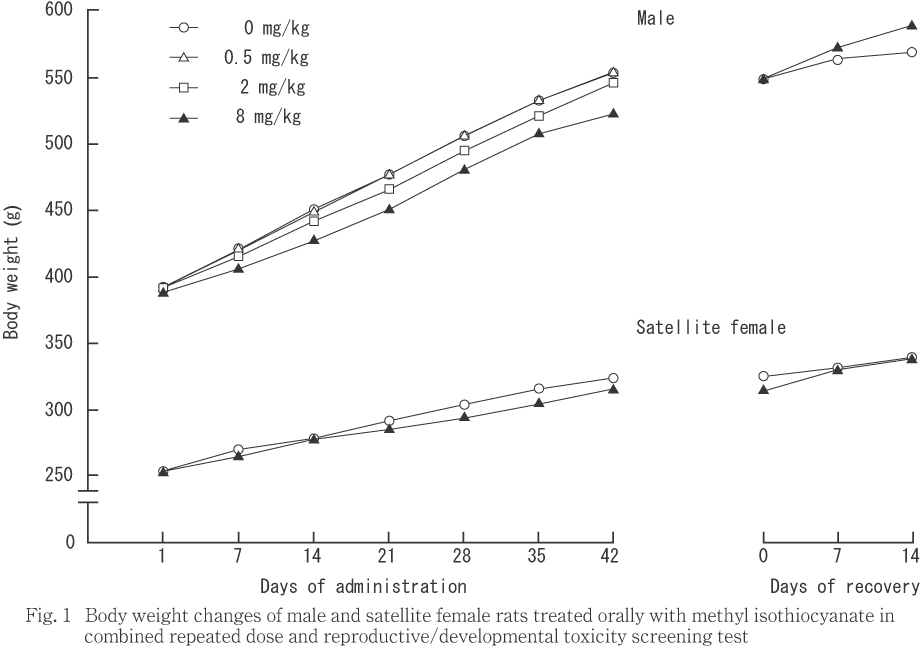
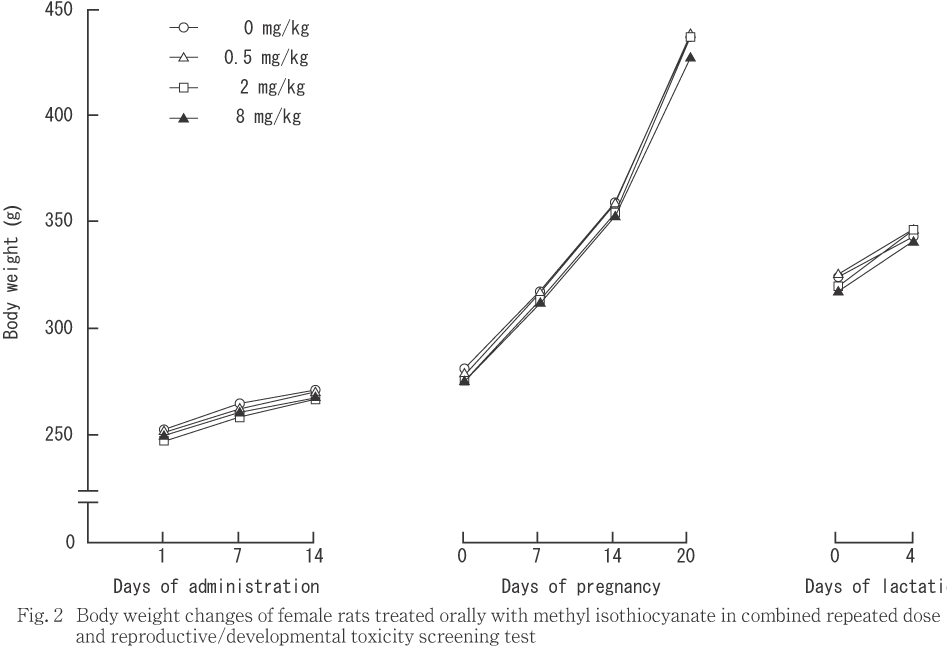
投与期間中,回復期間中を通じて被験物質投与群の体重と対照群の体重の間に有意差は認められなかったが,8 mg/kg投与群の雄では投与開始時からの体重増加量ならびに各測定点間の体重増加量が投与期間を通じて有意な低値を示し,回復期間中には投与終了時からの体重増加量ならびに各測定点間の体重増加量が有意な高値を呈した.

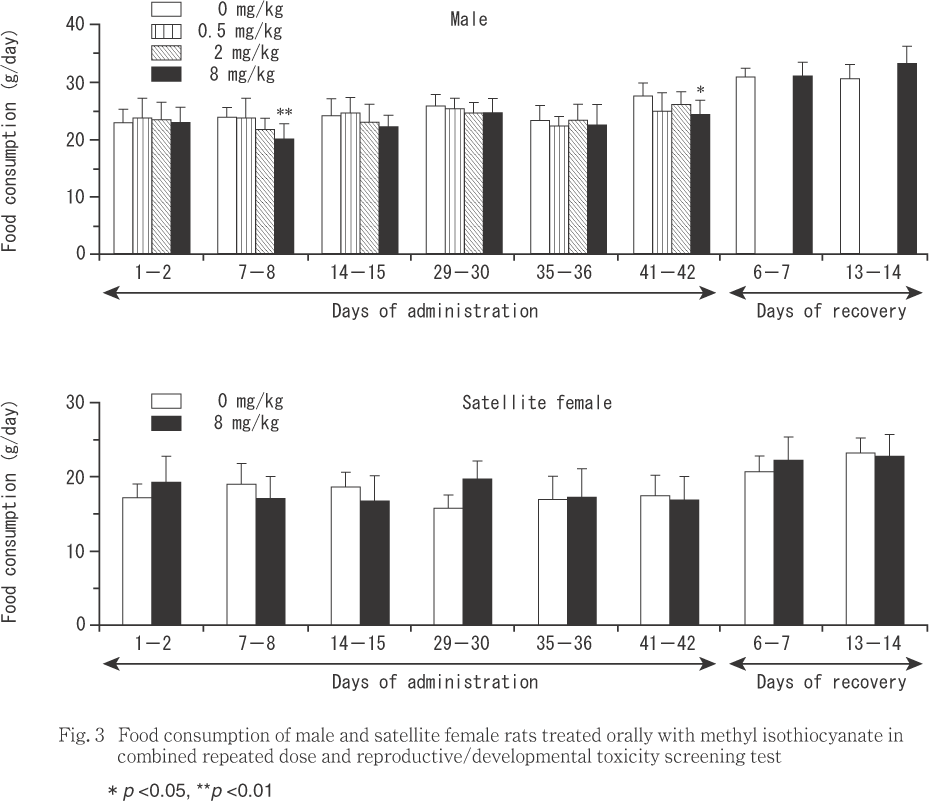
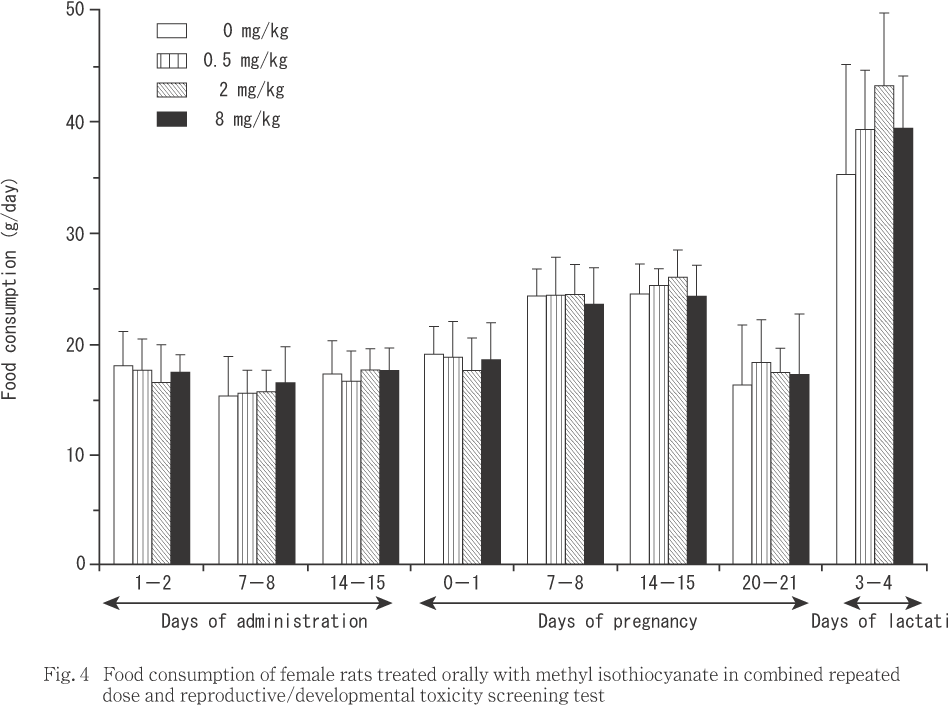
投与期間中,8 mg/kg投与群の雄では摂餌量が投与7〜8日および41〜42日に対照群に比較して有意な低値を示した.一方,雌の摂餌量はいずれの投与群においても対照群との間に有意差は認められなかった.
回復期間中には,雌雄ともいずれの投与群においても摂餌量に対照群との間で有意差は認められなかった.
投与期間終了時の検査では,8 mg/kg投与群の雄で赤血球数,血色素量および血小板数が対照群に比較して有意に増加した.一方,雌ではいずれの投与群においても対照群との間に有意差は認められなかった.
回復期間終了時の検査では,雌雄いずれの投与群においても対照群との間に有意差は認められなかった.
投与期間終了時の検査では,8 mg/kg投与群の雄でグルコース濃度が対照群に比較して有意に増加した.一方,雌ではいずれの投与群においても対照群との間に有意差は認められなかった.
回復期間終了時の検査では,雌雄いずれの投与群においても対照群との間に有意差は認められなかった.
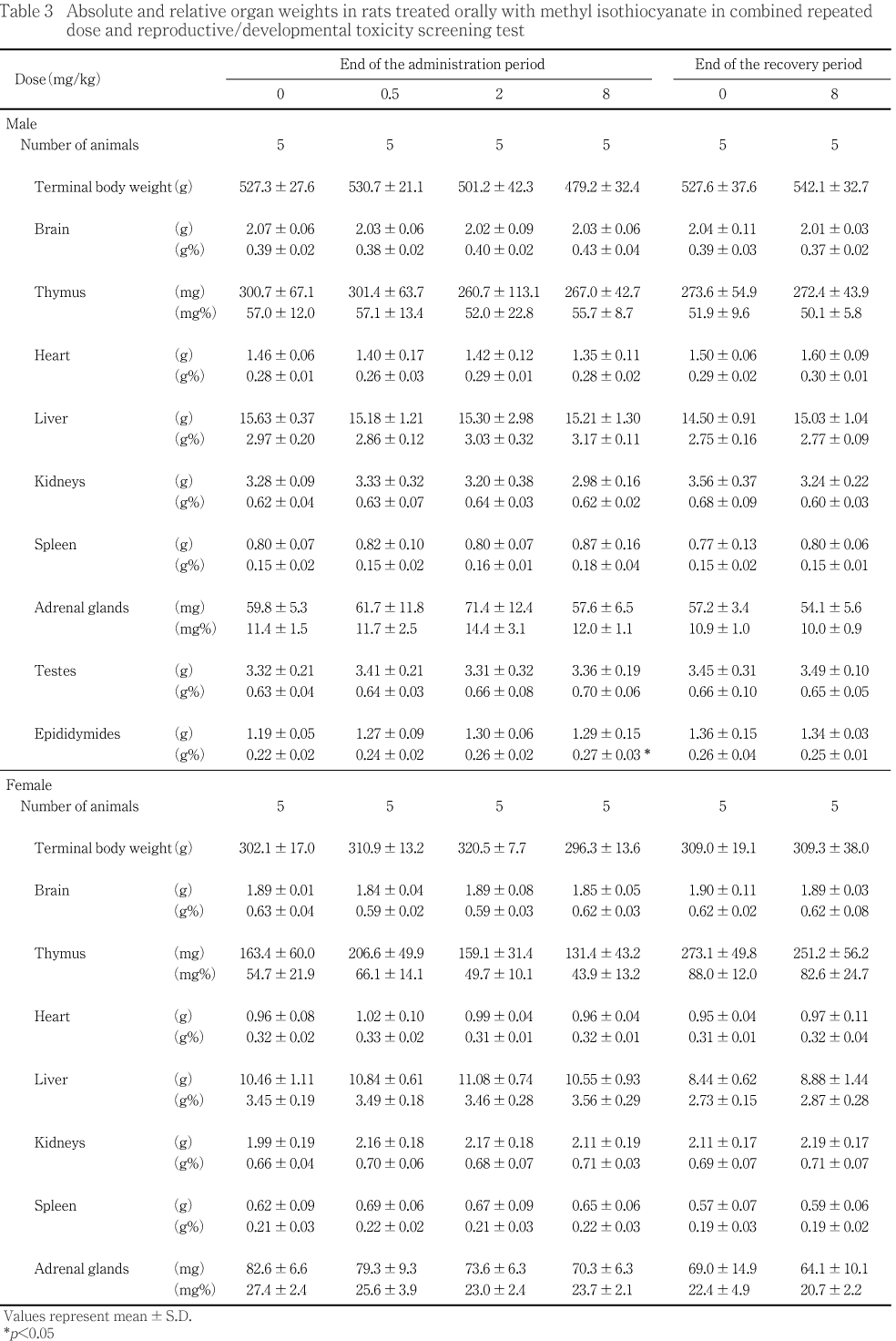
投与期間終了時の検査では,8 mg/kg投与群の雄で精巣上体の相対重量が対照群に比較して有意に増加した.一方,雌ではいずれの投与群においても対照群との間に有意差は認められなかった.回復期間終了時の検査では,雌雄いずれの投与群においても対照群との間に有意差は認められなかった.
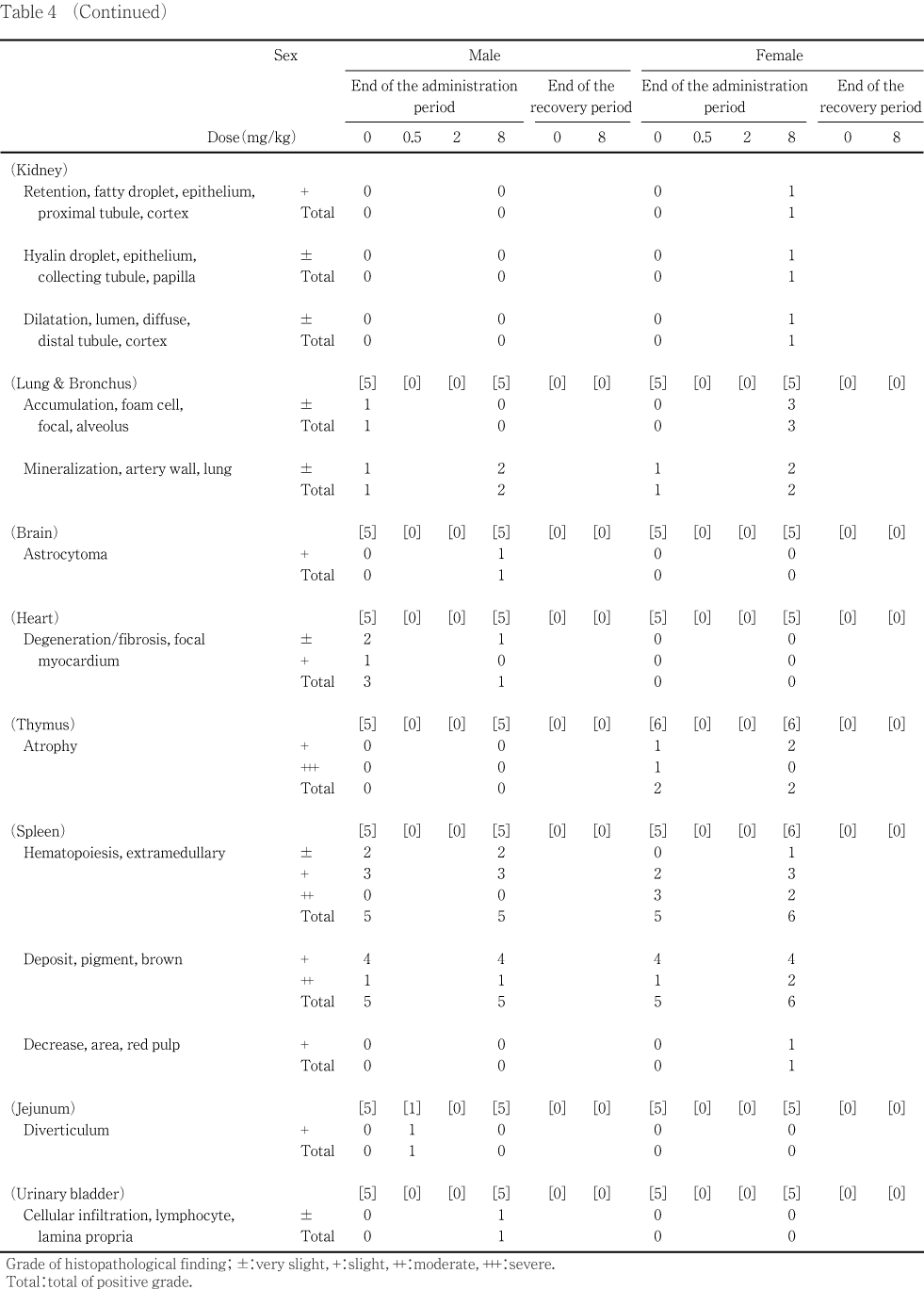
投与期間終了時の雄では,前胃粘膜の肥厚が2 mg/kg投与群の7例および8 mg/kg投与群の全例に認められ,そのうち8 mg/kg投与群の前胃粘膜には5例で水腫が,他の1例で白濁および黄色域が観察された.また,2 mg/kg投与群の1例には腺胃粘膜に白色結節が認められた.この他,肝臓の腫大が0.5 mg/kg投与群の1例および2 mg/kg投与群の5例にみられたが,8 mg/kg投与群には同様の所見は認められず用量依存性のある変化ではなかった.その他,右側腎臓の皮質に陥凹部が対照群および8 mg/kg投与群の各1例でみられたほか,空腸の憩室が0.5 mg/kg投与群の1例で,右側精巣上体尾部の結節および下顎リンパ節の腫大が8 mg/kg投与群の各1例で観察された.
投与期間終了時の雌では,前胃粘膜の肥厚が2 mg/kg投与群の4例および8 mg/kg投与群の6例で認められ,そのうち8 mg/kg投与群の前胃粘膜には4例で水腫が,他の1例では鋸の歯様の領域が観察された.また,腺胃粘膜の黒色点が対照群,0.5および2 mg/kg投与群の各1例にみられた.胸腺の小型化が対照群および8 mg/kg投与群の各1例にみられ,そのうち8 mg/kg投与群の例では脾臓も小型化を呈し,腎臓表面の粗造化も観察された.
回復試験期間終了時の雌雄では前胃粘膜の肥厚が8 mg/kg投与群の雄2例および雌1例で観察された.
投与期間終了時の雌雄で精巣および卵巣には異常所見は認められなかった.精巣上体では肉眼的観察で右側尾部に結節が認められた8 mg/kg投与群の1例で,右側尾部における精子肉芽腫が観察されたが,発現頻度および程度には対照群との間で差は認められなかった.
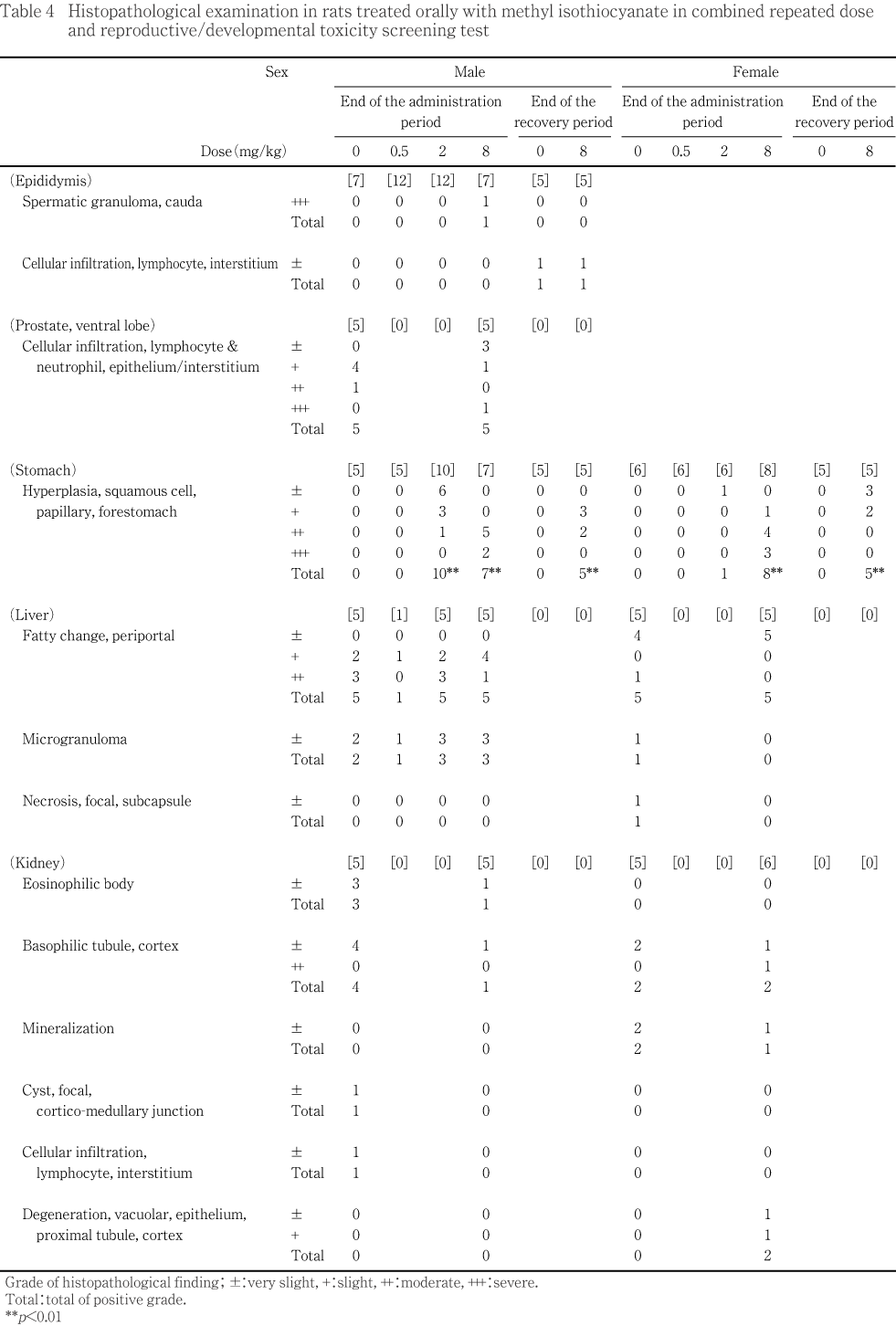
胃では,剖検時に異常所見が認められた例も含み,雄では対照群および0.5 mg/kg投与群の5例,2 mg/kg投与群の10例および8 mg/kg投与群の7例,雌では対照群,0.5および2 mg/kg投与群の各6例,8 mg/kg投与群の8例について病理組織学検査を実施した.その結果,雄では2および8 mg/kg投与群の観察した全例,雌でも2 mg/kg投与群の1例および8 mg/kg投与群の全例の前胃粘膜に扁平上皮細胞の乳頭状過形成がみられ,雄の2 mg/kg以上の投与群,雌の8 mg/kg投与群での同変化の発現頻度および程度は対照群に比較して有意に高かった.また,雌雄とも8 mg/kg投与群での前胃粘膜の変化の程度は,2 mg/kg投与群に比較して強い傾向がみられた.0.5 mg/kg投与群では雌雄とも前胃粘膜に異常所見は認められなかった.剖検所見において雄2 mg/kg投与群の1例の腺胃粘膜に白色結節が,雌の対照群,0.5および2 mg/kg投与群の各1例に腺胃粘膜の黒色点が認められたが,病理組織学検査の結果,肉眼所見を示唆する異常はみられなかった.
肝臓では,門脈周囲性の脂肪化が雌雄の対照群および8 mg/kg投与群の観察した全例でみられたが,両群間に程度の差は認められなかった.また,小肉芽腫が雌雄の対照群および雄の8 mg/kg投与群で観察されたが,両群間の発現頻度および程度に差は認められなかった.その他,肉眼的観察で肝臓の腫大が認められた雄の0.5および2 mg/kg投与群でも,門脈周囲性の脂肪化や小肉芽腫が観察された.雌の対照群で被膜下に限局した壊死巣が1例で観察された.
腎臓では好酸性小体が雄の対照群の3例および8 mg/kg投与群の1例で,皮質の塩基性尿細管が雄では対照群の4例および8 mg/kg投与群の1例で,雌では対照群の2例および8 mg/kg投与群の1例で,鉱質沈着が雌の対照群の2例および雌の8 mg/kg投与群の1例で,皮質近位尿細管の空胞変性が雌の8 mg/kg投与群の2例でそれぞれみられたが,いずれの例もごく軽度な変化であり対照群との間に発現頻度および程度の差は認められなかった.また,肉眼的観察で皮質に陥凹部がみられた雄の対照群の1例では皮髄境界部における限局性の嚢胞ならびに間質のリンパ球の浸潤が,腎臓表面の粗造化が認められた雌の8 mg/kg投与群の1例の皮質では中等度の塩基性尿細管のほか,ごく軽度あるいは軽度の近位尿細管上皮への脂肪滴の貯留および遠位尿細管の乳頭状拡張が認められ,乳頭部では集合管上皮の硝子滴が観察された.
その他,雌雄の対照群および8 mg/kg投与群の全例で脾臓の髄外造血および褐色色素の沈着がみられたが,両群間に程度の差は認められなかった.肉眼的観察で脾臓の小型化が認められた8 mg/kg投与群の雌の1例では,さらに赤脾髄領域の減少が観察された.雌の胸腺では萎縮が対照群の1例および8 mg/kg投与群の2例でみられたが,両群間に発現頻度および程度に差は認められなかった.また,肉眼的観察で胸腺の小型化が認められた雌の対照群および8 mg/kg投与群の各1例のうち対照例には強度の萎縮が観察された.前立腺腹葉では対象群および8 mg/kg投与群に上皮あるいは間質に好中球およびリンパ球の浸潤がみられたが両群間に程度の差は認められなかった.また,肺では肺胞に限局性の泡沫細胞の集簇および動脈壁に鉱質沈着が雌雄の対照群あるいは8 mg/kg投与群で観察され,雄では対照群あるいは8 mg/kg投与群で心臓における限局性の心筋の変性あるいは線維化が,膀胱では粘膜固有層にリンパ球の浸潤が散見されたほか,8 mg/kg投与群の1例では脳に星状膠細胞腫が観察されたが,いずれの変化も対照群との間で発現頻度および程度に差は認められなかった.雄の0.5 mg/kgの1例では空腸に憩室が観察された.肉眼的観察で下顎リンパ節の腫大がみられた雄の8 mg/kg投与群の1例の下顎リンパ節には,異常所見は認められなかった.
一方,回復試験期間終了時の雌雄では胃で8 mg/kg投与群の雌雄全例の前胃粘膜に扁平上皮細胞の乳頭状過形成がみられ,雌雄ともにこの変化の発現頻度および程度は対照群に比較して有意に高かった.同群の投与期間終了時屠殺例と比較すると,変化の程度は軽減している傾向がみられた.この他,精巣では異常所見は認められず,精巣上体では間質のリンパ球浸潤が対照群および8 mg/kg投与群の各1例でみられたが,両群間の発現頻度および程度に差は認められなかった.卵巣に異常所見は認められなかった.
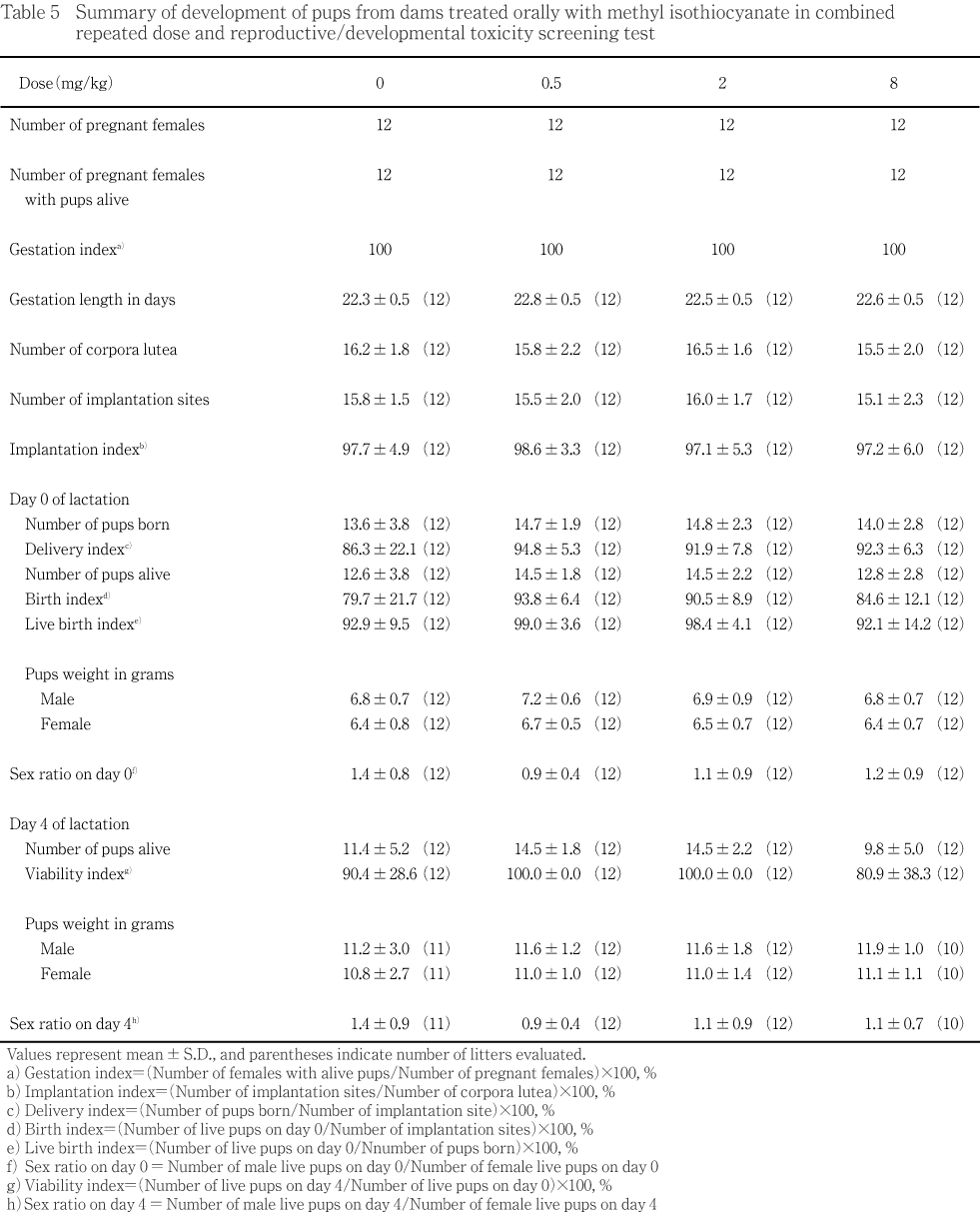
交配前の投与期間中,発情回帰しない動物が対照群で1例認められた以外,いずれの投与群においても投与による性周期への影響は認められなかった.
いずれの群においても全例の交尾が成立し受胎した.また,全例いずれも交尾は初回の発情期に行われた.
妊娠動物の全例が生児を出産し,妊娠期間には対照群と投与群との間に有意差は認められなかった.一方,直接観察できなかったものの分娩/哺育状態が不良であったと判断された動物が8 mg/kg投与群の2例で観察された.このうち1例では分娩後に産児を集めず分娩/哺育状態は不良であったが,分娩翌日以降は哺育状態の異常は認められなかった.他の1例では分娩後に産児を集めず産児に哺乳した形跡が認められなかった.この動物では分娩日に腟からの出血によると思われる腟周囲の褐色の汚れが認められ哺育2日にも継続してみられた.さらに,分娩翌日(哺育1日)にも産児の哺育が認められず哺育2日までに全出生児が死亡した.
黄体数および着床数ともに,対照群と投与群との間に有意差は認められなかった.
前述した通り,分娩/哺育状態が不良であった8 mg/kg投与群の1例では,哺育0および1日の産児に哺乳による腹部の白色化が認められず哺育2日までに全出生児が死亡した.また,8 mg/kg投与群では哺育4日の生児数および新生児生存率が対照群に比べて低い傾向がみられた.0.5および2 mg/kg投与群では雌出生児数が哺育0および4日ともに対照群に比較して有意に増加したが,性比には有意な変化は認められなかったことから被験物質投与による影響ではないと判断した.その他,分娩状態に異常が認められず出生児の一般状態にも異常が認められなかったものの,対照群の1例では哺育4日までに,8 mg/kg投与群の1例では哺育2日までに全出生児が死亡した.
哺育児体重には対照群と投与群との間で差は認められなかった.
また,生存産児および哺育4日の剖検児の形態観察では,8 mg/kg投与群の1例の雌生存産児1例で無尾が観察されたが,同腹の他の生存産児には形態異常は認められないことから,自然発生奇形と考えられた.死亡児では,いずれの動物にも形態異常は観察されなかった.
8 mg/kg投与群の雄においては体重増加抑制および摂餌量の減少が認められた.Fischer 344系ラットにイソチオシアン酸メチルを吸入曝露した結果,3.1 ppm投与群の雄では血中酸素分圧の低下,血色素量および肺重量の増加が,同群の雌雄では体重および摂餌量の減少,呼吸器における組織学的変化が報告されている4).本試験の投与経路は経口であり呼吸器系への影響や循環不全を示唆する所見はみられていないが,体重増加抑制および摂餌量の減少はイソチオシアン酸メチルの影響であると判断される.一方,本試験においては赤血球数および血色素量の増加がみられたが,骨髄像には変化がみられず肝臓等における髄外造血の亢進も認められない事から造血機能が亢進しているとは考え難い.これらの変化が体液量の減少等を示唆する可能性も考えられるが本試験のみからは機序を明らかにする事はできなかった.14日間の回復性試験の結果,休薬により8 mg/kg投与群の体重は対照群に比較して有意に増加し,赤血球数および血色素量は対照群と比較して差は認められなかったことから,これらの変化は可逆的であることが確認された.
また,8 mg/kg投与群の雌雄では投与直後の流涎が観察され,前胃粘膜は肉眼的に肥厚および水腫を呈し組織学的には扁平上皮細胞の乳頭状過形成が認められた.投与直後の流涎は2 mg/kg投与群の雄1例で,前胃粘膜の病理学的変化は2 mg/kg投与群の雌雄でも認められた.8 mg/kg投与群の前胃粘膜の病理学的変化の発現頻度および程度は,2 mg/kg投与群に比較して強い傾向がみられた.これらの変化は刺激性のある物質を経口投与した結果によるものと考えられ,イソチオシアン酸メチルが刺激性を有しているという報告4〜8)と一致する.本被験物質の単回経口投与毒性試験9)においても,流涎と前胃粘膜の肥厚および水腫が観察されている.回復性試験の結果,休薬中に流涎は認められず,前胃粘膜の器質的変化は投与期間終了時に比較して軽減する傾向がみられたものの完全に回復するには至らなかった.
投与期間終了時に8 mg/kg投与群の雄で認められた血小板数ならびに血漿中グルコース濃度の増加は,イソチオシアン酸メチル投与による継続的影響に対する代償性の変化である可能性を否定できない.その他,8 mg/kg投与群の雄では精巣上体重量の増加がみられたが器質的な変化は認められず偶発的変化の可能性が高いと考えられる.詳細な症状観察および機能検査においては神経毒性を示唆する所見は認められなかった.
8 mg/kg投与群で分娩/哺育状態の不良とそれによると考えられる全出生児の死亡がみられたほか,哺育4日の新生児生存率が低い傾向が認められた.これはイソチオシアン酸メチルの投与で分娩時の母動物の状態が悪化した結果,母児とも一般状態に特記すべき変化はみられなかったものの出生児が死亡したためと考えられた.性周期,排卵,交尾,受胎,着床,妊娠期間,分娩率,生児出産率および出生率に被験物質投与の影響は認められなかった.また,出生児の体重および性比に変化は認められず,投与に起因したと考えられる形態異常も認められなかった.
以上の結果より,本試験条件下でのイソチオシアン酸メチルの無作用量は,反復投与毒性に関しては,8 mg/kg投与群の雄で体重増加抑制および摂餌量の減少がみられ,2 mg/kg以上の投与群でイソチオシアン酸メチルの刺激性に起因した流涎および前胃粘膜の器質的変化が認められたことから,雌雄ともに0.5 mg/kg/dayと判断された.前胃粘膜の病理所見は14日間の休薬で投与期間終了時の変化と比較して軽減する傾向はみられたものの消失するには至らなかった.生殖発生毒性に関しては,8 mg/kg投与群の母動物で分娩/哺育状態の不良がみられたことから雌では2 mg/kg/dayと判断された.雄および出生児については,8 mg/kg投与群でもイソチオシアン酸メチル投与に起因した影響が認められなかったことから8 mg/kg/day以上と判断された.
| 1) | Kassie F et al.:Genotoxic effects of methyl isothiocyanate. Mutat Res, 490:1-9(2001). |
| 2) | Matthiessen JN, Shackleton MA:Advantageous attributes of larval whitefringed weevil, Naupactus leucoloma (Coleoptera:Curculionidae) for bioassaying soil fumigants and responses to pure and plant-derived isothiocyanates. Bull Entomol Res, 90:349-355(2000). |
| 3) | Pruett SB, Myers LP:Toxicology of metam sodium. J Toxicol Environ Health B Crit Rev, 4:207-222 (2001). |
| 4) | Dodd DE, Fowler EH:Methyl isocyanate subchronic vapor inhalation studies with Fischer 344 rats. Fundam Appl Toxicol, 7:502-522(1986). |
| 5) | Alexeeff GV et al.:Dose-response assessment of airborne methyl isothiocyanate (MITC) following a metam sodium spill. Risk Anal, 14:191-198(1994). |
| 6) | Cone JE et al.:Persistent respiratory health effects after a metam sodium pesticide spill. Chest, 106: 500-508(1994). |
| 7) | Rostron C:Metyl isothiocyanate in wine. Fd Chem Toxic, 30:821-828(1992). |
| 8) | Sharma BK et al.:Fetal poisoning with methyl isothiocyanate. Br Med J, 283:18-19(1981). |
| 9) | 高島宏昌ら:イソチオシアン酸メチルのラットを用いる単回経口投与毒性試験.化学物質毒性試験報告,12:343-344(2005). |
| 連絡先 | |||
| 試験責任者: | 高島宏昌 | ||
| 試験担当者: | 立花滋博,関 剛幸,丸茂秀樹, 堀内伸二,稲田浩子,三枝克彦, 安生孝子,古谷真美 | ||
| 7食品薬品安全センター秦野研究所 | |||
| 〒257-8523 神奈川県秦野市落合729-5 | |||
| Tel 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | |||
| Authors: | Hiromasa Takashima(Study director) Sigehiro Tachibana, Takayuki Seki, Hideki Marumo, Shinji Horiuchi, Hiroko Inada, Katsuhiko Saegusa, Takako Anjo, Mami Furuya | ||
| Hatano Research Institute, Food and Drug Safety Center | |||
| 729-5 Ochiai, Hadano, Kanagawa, 257-8523, Japan | |||
| Tel +81-463-82-4751 | Fax +81-463-82-9627 | ||