4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ���
��åȤ��Ѥ����и���Ϳ�ˤ��28���֤�ȿ����Ϳ�����
28-Day Repeated Dose Oral Toxicity Study of Monosodium 4-amino-5-hydroxy-2,7-naphthalenedisulfonate in Rats
����
4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ������������餫�ˤ��뤿�ᡢSD�ϡ�Crj:CD(SD)�ͥ�åȤˡ���ʪ����0��������Ϳ���оȡ���ͺ��12ɤ�ˡ�30�ʳ�6ɤ�ˡ�100�ʳ�6ɤ�ˡ�300�ʳ�6ɤ�ˤ����1,000 mg/kg/���ʳ�12ɤ�����̤�28���֤ˤ錄�äƶ����и���Ϳ�������ޤ����оȤ����1,000 mg/kg���λ�ͺ��6ɤ�ˤĤ��Ƥϡ���Ϳ��λ��14���֤β������֤��ߤ����Ѳ��βĵ����ˤĤ��Ƥ⸡Ƥ������30��100�����300 mg/kg���Ǥϡ����̾��֤δѻ����νŤ�����ݱ��̤�¬�ꡢǢ�����¤Ӥ˷�ճ�Ū�����������Ū�����������Ū�������ˤ����ơ�4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ����Ϳ�αƶ��ȹͤ������Ѳ���ǧ����ʤ��ä���1,000 mg/kg���ˤ����Ƥ⡢ñ�ʤ�����ʪ�����äˤ����IJ�η��٤ʳ�ĥ�㤬��ͺ��ǧ���줿������Ϳ���ֽ�λ���˻�ưʪ����Ӳ������ֽ�λ���˻�ưʪ�Ȥ⡢�����������ƶ��ȹͤ������Ѳ���ǧ����ʤ��ä����������äơ�4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ��Υ�å�28����ȿ���и���Ϳ�ˤ�����̵�ƶ��̤ϡ�1000 mg/kg/���ȿ��ꤵ�줿��
���
���λ�ϡ������ʤδ�¸����ʪ���������������Ȥΰ�ĤȤ��Ƽ»ܤ�����ΤǤ��ꡢ4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ����åȤ�28����ȿ���и���Ϳ������������Τε�ǽ����ӷ��֤��Ѳ���ѻ�������ʪ����ȿ����Ϳ������Ƥ�����Τǡ����η�̤���𤹤롣
��ˡ
1.�︳ʪ��
4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ��ϡ�ʬ����341.30��̵��ˤο�ˤ���Ϥ��ˤ���ø�쿧��ʴ���ǡ���ˤ�����������ȳ�����ҡ�����ˤ������줿��Ρʥ��å��ֹ�AZ01�ˤ��Ѥ���������줿4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ��ν��٤�87.4 %��̵��ʪ�Ȥ��ơˤǡ������Ϸ뾽��������ʤɤο�ʬ�Ǥ��ä����Ȥ��顢���Ѥ������äƤϽ��ٴ�����������Ϳ��λ�塢�︳ʪ����ʬ�Ϥ�����Ϳ���������Ǥ��ä����Ȥ��ǧ������
2.����ưʪ����ӻ�����
ưʪ�ϡ����ܥ��㡼�륹����С��ʳ��ˤ��Ƴ������SD�ϡ�Crj : CD(SD)�ͥ�åȤ�ͺ��42ɤ�Ѥ������Ʒ���ưʪ���ϡ���ͺ���줾���оȤ����1,000 mg/kg����12ɤ��30��100�����300 mg/kg����6ɤ�Ȥ������Τ����оȤ����1,000 mg/kg���λ�ͺ��6ɤ����Ϳ���ֽ�λ��14���֤β������Ԥ�����β����������Ƥ����Ʒ��ؤ�ưʪ�γ���դ��ϡ���Ϳ���������νŤ˴�Ť��ز�̵������ˡ���Ѥ��ƹԤä�����Ϳ���ϻ���ʿ���νš��ν��ϰϡˤϡ�ͺ179��170��188��g����143��131��156��g�Ǥ��ä���ưʪ�λ���ϡ��벽����Ϳ����Ӳ������֤Ȥ⡢����22��3�����55��10%���������10��ʾ塿���ʥ�����ե�å��奨���������ˡ�����12���֡ʸ���6�����������6�������ˤ����ꤷ���Хꥢ�������ƥ�ưʪ���ǡ����ƥ�쥹�����֥������˳�3ɤ���Ļ�ͺ�̤˼��Ƥ��ƹԤä��������������������ȡʳ��ˡ��Ƿ��������MR���ȥå��ͤȿ��1��m�����ȥ�å��ե��륿���ɲ��糰���ȼͤ������ݿ�ƻ��ˤϡ����줾���´浪��Ӽ�ư������֤ˤ�꼫ͳ�ݼ褵������
3.��Ϳ�̤������Ϳ��ˡ
��Ϳ�̤ϡ�14����ȿ����Ϳ�ˤ����Ϳ�������η�̤˴�Ť��ơ������̤������ˡ�����ɥ饤��ˤ��������̤�1,000 mg/kg/���Ȥ����ʲ�300��100�����30 mg/kg/�����̤ȡ����ޤΤ���Ϳ���оȤ����ꤷ�����︳ʪ���ϡ�����륻����������¸��������ȡʳ��ˡ�100cP�ͤ�1 w/v %���ϱա̿�϶��������ʳ��ˡ�����������ͤ����ޤȤ����ν�1kg���������Ϳ���̤�5ml�ǡ����ٴ����̤��������Ϳ���̤ˤʤ�褦��ǻ�١�30 mg/kg����0.686�ʽ��ٴ���ǻ��0.6��w/v % ; 100 mg/kg����2.29��Ʊ2��w/v % ; 300 mg/kg����6.86��Ʊ6) w/v % ; 1,000 mg/kg����22.9��Ʊ20��w/v %�ͤ��ϱ����ϡ��椪��ӹ�ǻ�٤ǤϷ����դȤ���Ĵ����������Ϳ�ϡ��ߥ���Ǥ����夷�����������Ѥ��ơ�1��1��28���֤ˤ錄�äƶ���Ū�˷и���Ϳ�������Ƹ��Τ���Ϳ���̤Ͻ�1���¬���νŤ˴�Ť��ƻ��Ф�������Ϳ������︳ʪ���϶Ѱ��ʬ�������ޤ��������Ǿ��ʤ��Ȥ�7���֤ϰ���Ǥ��뤳�Ȥ���ǧ����Ƥ���Τǡ�Ĵ��������Ϳ�դλ��Ѵ��֤�7������Ȥ�������ľ���ޤdz�ǻ�٤��Ȥ˾�ʬ�����������ʡ�4��˲����ݴɤ���������ˡ��ºݤ��Ѥ�����Ϳ�դˤĤ���ǻ��ʬ�Ϥ��������ǻ�٤�Ĵ������Ƥ��뤳�Ȥ��ǧ������
4.�ѻ�����Ӹ�������
1)���̾��ִѻ�
��Ϳ����Ӳ������������������प��ӳ��ѡ���ư����ѻ�������
2)�νŤ�����ݱ���¬��
�νŤϡ����Τ��Ȥ���Ϳ����������Ϳ����ľ���ˤ���Ӥ��θ���轵1��¬�ꤷ�����ݱ��̤ϡ����������Ȥ��轵1��24���֤ξ����̤�¬�ꤷ��1ɤ�������ʿ���ݱ��̤Ф�����
3)Ǣ����
��Ϳ����25����ͺ������27���ʻ�ˡ��¤Ӥ���Ϳ��λ��14����ͺ������13���ʻ�ˤ˹����������ɷ㤷�ƶ�����Ǣ������pH�����졢����ѥ����������ȥ��Ρ��ӥ��ӥ�ӥ����ӥ�Ρ�����̰ʾ塢�ޥ��륹�������ʳ��ˡ��ޥ�ƥ����ƥ��å���(R)�͡��¤Ӥ˳��Ѥ�������
4)��ճ�Ū����
�����դκμ�ϡ���Ϳ���֤���Ӳ������ֽ�λ�����ˤ������˻�˶�����˹Ԥä���ưʪ�Ϻη������θ��5�������¤�����Τߤ��Ϳ�������η�ϡ������ƥ���첼�dz�ʢ����ʢ��ư̮���Ԥä����μ褷����դ�3ʬ�䤷�����ΰ�����EDTA-2K�ǶŸ��˻߽�������¿���ܼ�ư�������֡��찡�����Żҡʳ��ˡ�E-4000�ͤˤ�ꡢ�ַ������ŵ����������ˡ��쿧���̡ʥ������إ⥰���ӥ�ˡ�ˡ��إޥȥ���å��͡ʥѥ륹���������ˡ�ʿ���ַ�����ѡ�ʿ���ַ��쿧���̡�ʿ���ַ��쿧��ǻ�١ʰʾ塢���͡ˡ����������ӷ쾮�Ŀ��ʰʾ塢�ŵ����������ˤޤ�����ɸ�ܤ�������ơ��־��ַ�����Brilliant cresyl blue�����ˤ��������ɴʬΨ��May-Giemsa�����ˤ�¬�ꤷ��������˰����η�դ�3.8%��������ʥȥꥦ��������Ʒ�����������նŸǼ�ư¬�����֡ʥ����ҡ�KC-10A�ˤˤ�ꡢ�ץ��ȥ���ӥ���֡�Quick����ˡ�ˤ���ӳ�������ʬ�ȥ���ܥץ饹������֡ʥ��饸���������ˡ�ˤ�¬�ꤷ����
5)���������Ū����
�μ褷����դΰ������������ʬΥ���������ؼ�ưʬ�����֡������Żҡʳ��ˡ�JCA-VX-1000������ʥ饤�����ͤˤ�ꡢ������ѥ���Biuretˡ�ˡ�����֥ߥ��BCGˡ�ˡ�A/G��ʷ��͡ˡ��������ȥꥰ�ꥻ�饤�ɡ������쥹�ƥ�����ʰʾ塢����ˡ�ˡ����ӥ��ӥ��Jendrassikˡ�ˡ�Ǣ�����ǡ�Urease-UVˡ�ˡ����쥢���˥��Jaffeˡ�ˡ�GOT��GPT����-GTP�ʰʾ塢SSCCˡ�ˡ����륫��ե����ե���������GSCCˡ�ˡ����륷�����OCPCˡ�ˤ����̵�����ʹ���ˡ�ˤޤ��Ų����ưʬ�����֡��찡���ȹ��ȡʳ��ˡ�NAKL-1�ͤˤ�ꡢ�ʥȥꥦ�ࡢ���ꥦ�प��ӱ��Ǥ�¬�ꤷ����
6)������Ū����
(1)˶��
�η��������˻�����˶����Ԥä���
(2)¡�����¬��
Ǿ����¡����¡�����ա�����������������̡����н��̡ˤ����˻������νŤ��Ȥ����ν�������н��̡ˤФ�������¡�����ա����㤪�������ϡ��������礷�����̤�����
(3)�����ȿ���Ū����
�оȷ������1,000 mg/kg���ο�¡����¡���¡����¡�����դ������IJ�ˤĤ��ơ�10%���������˾ץۥ�ޥ��դǸ���塢��ˡ�ˤ��ѥ�ե������Ҥ���������إޥȥ�������������H-E��������ܤ��ƶ���������
5.������
����줿ʿ���ͤ��뤤�����٤ˤĤ��ơ��оȷ��Ȥδ֤�ͭ�պ��ʴ���Ψ5%�ʲ��ˤ���ˡ�Ǹ��ꤷ�������ʤ����3���ʾ�ξ�硢����Ū�긫�ˤĤ��Ƥ�Bartlett��ʬ�������Ԥ���ʬ�������ͤʾ��ϰ층���֤�ʬ��ʬ�Ϥ�Ԥä���ʬ�������ͤǤʤ���硢����ɴʬΨ�����Ǣ�긫��Kruskal-Wallis�ν�̸����Ԥä��������η��ͭ�պ���ǧ���硢Dunnettˡ�ˤ���оȷ����Ф���Ʒ�����Ӹ����Ԥä����ޤ���˶������������ȿ���Ū�긫�ˤĤ��ƤϦ�^2������Ѥ�����������2���ξ�硢����Ū�긫�ˤĤ��Ƥ�F�����Ԥ������η��ʬ�������ͤʾ���Student�� t ������ͤǤʤ�����Aspin-Welch�� t �����Ԥä����ޤ�������ɴʬΨ�����Ǣ�긫�ˤĤ��Ƥ�Mann-Whitney��U�����˶������������ȿ���Ū�긫�ˤĤ��Ƥϡ�Fisher��ľ�ܳ�Ψˡ���Ѥ������ݱ��̤ˤĤ��Ƥϡ����������Ȥ��̤�¬�ꤹ��ΤdzƷ��ˤ�����¬���ͤο������ʤ���ͭ�պ�����ϼ»ܤ��ʤ��ä���
���
1.���̾��֤���ӻ�˴
�оȷ��¤Ӥ�30��100��300�����1,000 mg/kg���λ�ͺ�Ȥ⡢�ѻ����֤��̤��ư��̾��֤��Ѳ����˴��ǧ����ʤ��ä���
2.�νš�Figure 1��
��Ϳ����Ӳ������֤��̤��ơ��︳ʪ����Ϳ�Ʒ����νŤϡ��оȷ�����٤����׳�Ū��ͭ�դʺ���ǧ����ʤ��ä�����β������ֽ�λ���˻�ưʪ�ˤ����ơ�1,000 mg/kg�����νŤ���Ϳ��λ�������оȷ����䲼��äƤ�����������������ξ�����νŤϤۤ�ʿ�Ԥ��ƿ�ܤ�����ư��ǧ����ʤ��ä���
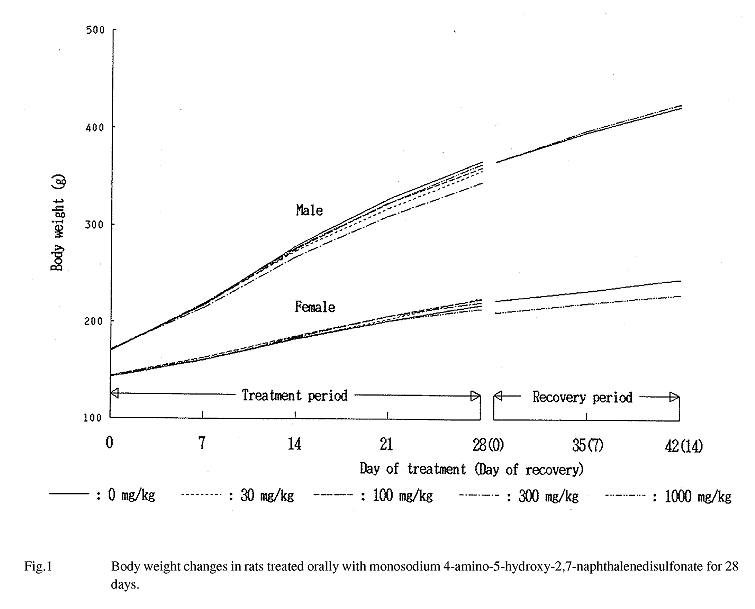
3.�ݱ���
��Ϳ����Ӳ������֤��̤��ơ��︳ʪ����Ϳ�Ʒ����ݱ��̤��оȷ�����٤ƺ���ǧ����ʤ��ä���
4.Ǣ�긫
��Ϳ���֤���Ӳ������ֽ�λ���Τ�����θ����ˤ����Ƥ⡢�Ƹ������ܤ�4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ����Ϳ�αƶ����ͤ������Ѳ���ǧ����ʤ��ä�����Ϳ���ֽ�λ����1,000 mg/kg����ͺ��pH�ϡ��������˷���������ǧ���줿�������׳�Ū��ͭ�դ��Ѳ��ǤϤʤ��ä�����Ϳ���ֽ�λ���θ����ˤ����ơ��ӥ��ӥ�ӥ����ӥ�Ρ������ѻ�����100 mg/kg�ʾ�����̷����︳Ǣ���Ф���������迧ȿ���ʥӥ��ӥ�ø�쿧�������ӥ�Ρ����������ˤȤϰۤʤ뿧Ĵ�ʥӥ��ӥ�:�ֻ翧�������ӥ�Ρ�����:�������ˤ�ȯ������Ƚ�꤬����Ǥ��ä�������ȯ���ϡ�4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ����ϱա�100 ppm�ˤ��Ф��Ƥ�ȯ�����뤳�Ȥ���ǧ���줿��
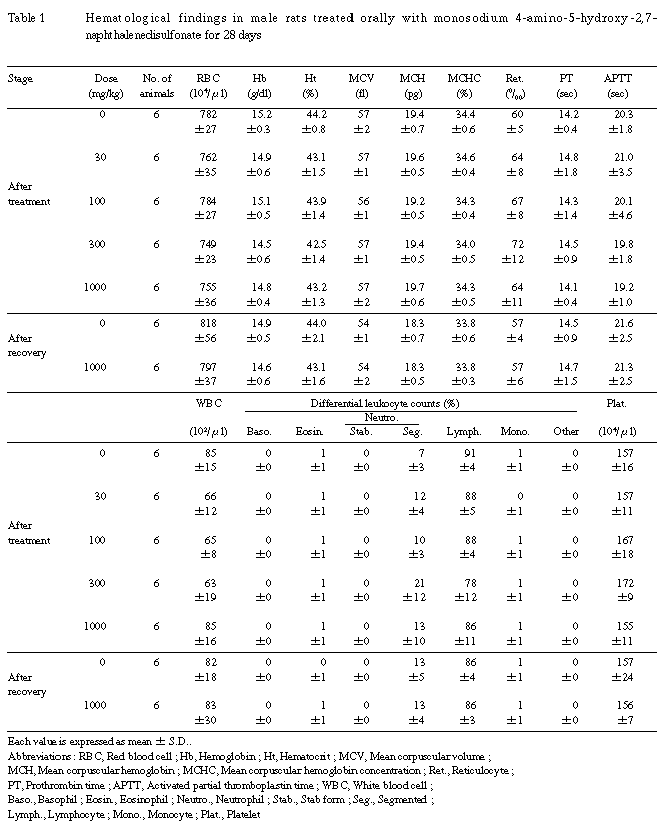
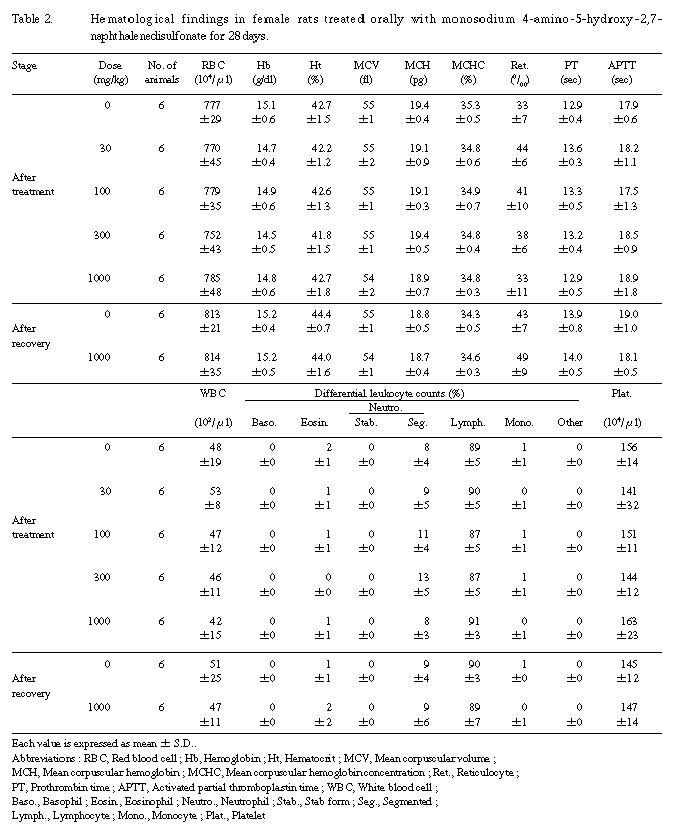
5.��ճ�Ū�긫��Table1, 2��
��Ϳ���֤���Ӳ������ֽ�λ���˻�ưʪ���̤��ơ��︳ʪ����Ϳ�Ʒ��λ�ͺ�Ȥ⡢�Ƹ������ܤ��оȷ�����٤����׳�Ū��ͭ�դ��Ѳ���ǧ����ʤ��ä���
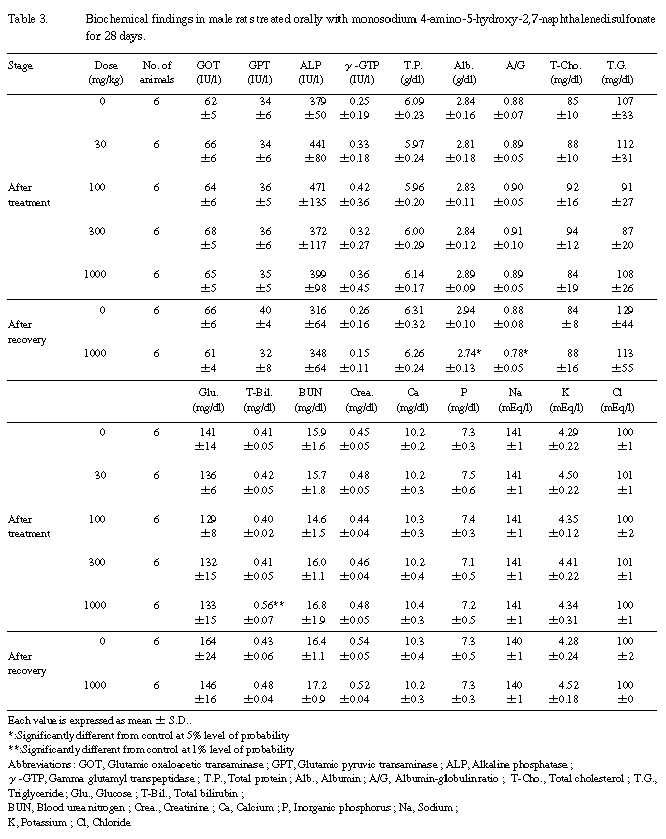
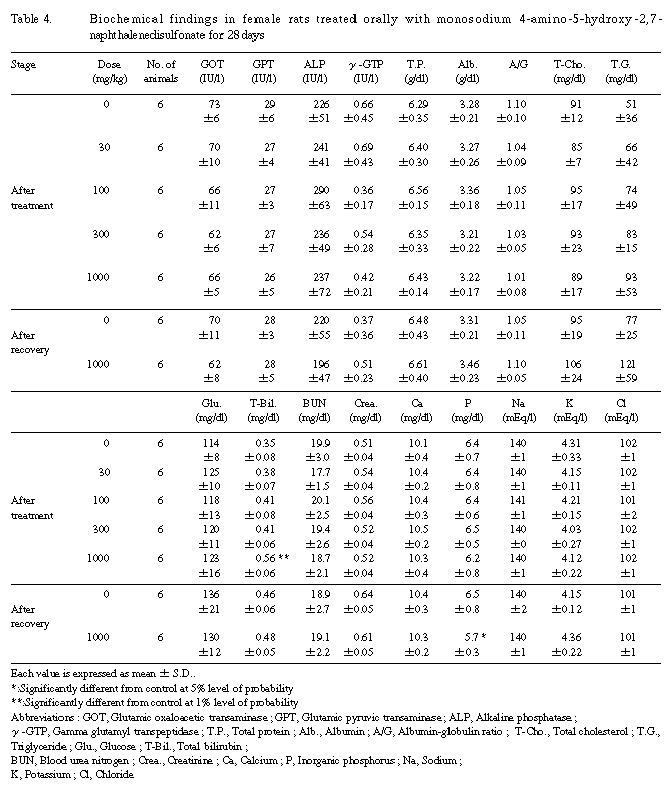
6.���������Ū�긫��Table 3,4��
��Ϳ���ֽ�λ���˻�ưʪ�ˤ����ơ���ͺ�Ȥ�1,000 mg/kg�������ӥ��ӥ��̤Τߤ��оȷ�����ٹ��ͤ������׳�Ūͭ�պ���ǧ���줿���ӥ��ӥ��ѻ������︳ʪ�����ϱա�0.1��1000ppm�ˤ�������̡��︳ʪ����ǻ�٤˰�¸���ƻ�����ȿ�����뤳�Ȥ���ǧ���줿���������ֽ�λ���˻�ưʪ�Ǥϡ���Ϳ���ֽ�λ���˻�ưʪ��ǧ���줿�ӥ��ӥ���Ѳ���ǧ����ʤ��ä���������������Ȥ��̤ˡ�1,000 mg/kg���ˤ����ơ����������٤ʥ���֥ߥ��̤θ�������Ӥ����ȼ��A/G����㲼��ͺ�ˡ�̵������̤θ��������ǧ���줿��
7.������Ū�긫
1)˶���긫
��Ϳ���ֽ�λ���˻�ưʪ�ˤ����ơ�30��100�����300 mg/kg���Ǥϡ��︳ʪ����Ϳ�αƶ�������������۾��ǧ����ʤ��ä���1,000 mg/kg���Ǥϡ���IJ�η��٤ʳ�ĥ����6ɤ��ͺ��2ɤ�Ȼ��4ɤ��ǧ���줿���������ֽ�λ���˻�ưʪ�ˤ����Ƥϡ��۾��ǧ����ʤ��ä���
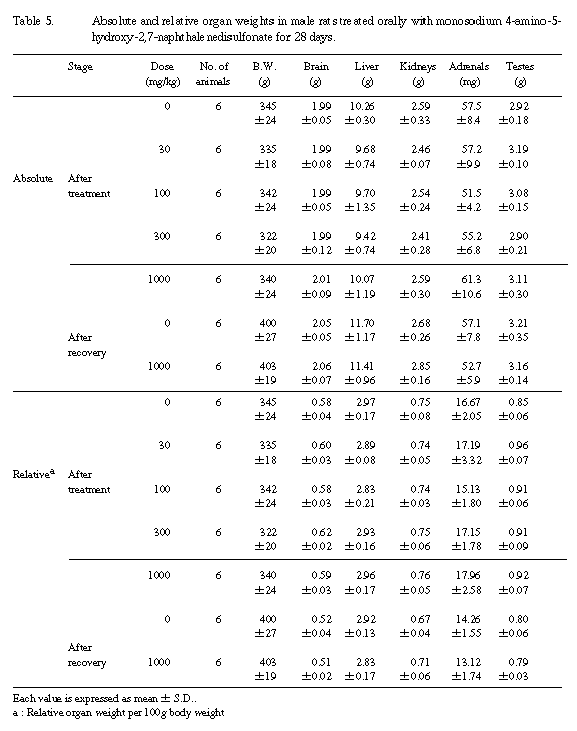
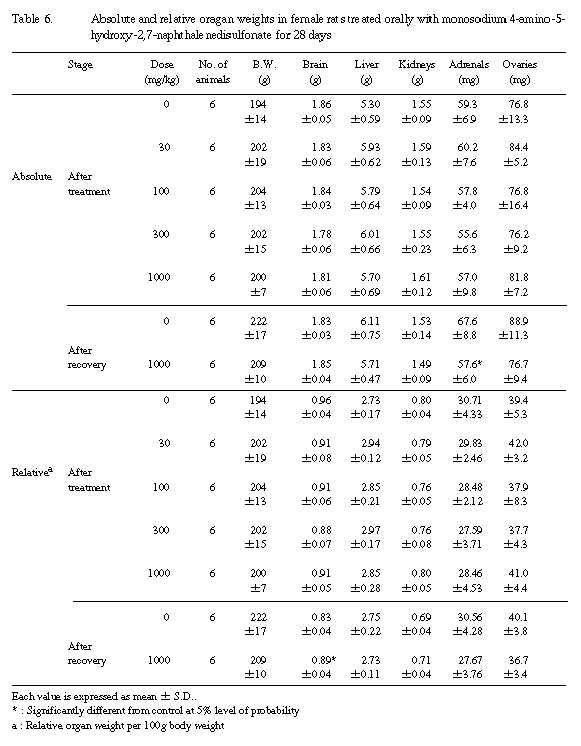
2)¡����̡�Table 5,6��
��Ϳ���ֽ�λ���˻�ưʪ�ˤ����ơ��︳ʪ����Ϳ�Ʒ���¬�ꤷ����¡��ν��̤ϡ����Ф�������н��̤Τ�����ˤ����Ƥ⡢�оȷ�����٤����׳�Ū��ͭ�դ��Ѳ���ǧ����ʤ��ä����������ֽ�λ���˻�ưʪ�ˤ����Ƥϡ���ˤ�����1,000 mg/kg�����νŤ��оȷ����䲼��ä����ᡢ���դ����н��̤Τߤθ�����Ǿ�����н��̤Τߤ����ä����������Ф�������н��̤˶��̤��ư�����Ѳ�������¡���ǧ����ʤ��ä���
3)�����ȿ���Ū�긫��Table 7��
�оȷ������1,000 mg/kg���λ�ͺ�ˤĤ��ơ���¡����¡���¡����¡��������դ��������ޤ���˶������IJ�γ�ĥ��ǧ���줿�Τ���IJ�ˤĤ��Ƥ⸡�����������η�̡��ѻ�������¡��ˡ��︳ʪ����Ϳ�αƶ����ͤ������Ѳ���ǧ����ʤ��ä�������Ū�˳�ĥ���Ƥ�����IJ�ϡ�Ǵ�����ؤο�Ÿ�Ϥߤ�줿����Ū�۾��ǧ����ʤ��ä���
�ͻ�
4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ��Υ�åȤ��Ѥ����и���Ϳ�ˤ��28���֤�ȿ����Ϳ�������0���оȡˡ�30��100��300�����1,000 mg/kg����5���ǹԤä����ޤ����оȷ������1,000 mg/kg���ˤĤ��Ƥϡ���Ϳ���ֽ�λ��14���֤β������֤��ߤ����Ѳ��βĵ����ˤĤ��Ƥ⸡Ƥ������
��Ϳ���ֽ�λ���˻�ưʪ�ˤ����ơ�30��100�����300 mg/kg���Ǥϡ���ͺ�Ȥ��︳ʪ����Ϳ�������ƶ��ȹͤ������Ѳ���ǧ����ʤ��ä���1,000 mg/kg���ˤ����Ƥ⡢�����ȿ���Ū�Ѳ���ȼ��ʤ�ñ�����IJ�γ�ĥ�㤬��ͺ��ǧ���줿�Τߤǡ�����¾�ä��Ѳ���ǧ����ʤ��ä���

���餫�������ȿ���Ū�Ѳ���ȼ��ʤ���IJ�γ�ĥ�ϡ�������ʪ�����ʬ�Ҳ���ʪ�Υ�åȤ䥦�����ʤɤ���IJ���礭��ưʪ��ؤ���Ϳ���ˤ��Ф���ǧ���졢IJ��ٶ��Ѥ����ˤ���Ѳ��ȹͤ����Ƥ��롣
�︳ʪ����Ϳ�ˤ����IJ��ĥ��ȯ�������ˤĤ��Ƥ������Ǥ��뤬��������ˤ��Ƥ�ñ�ʤ���IJ����ʪ�����äˤ����٤��Ѳ��Ǥ��ꡢ��Ρ���ΰ��̾��֤��Ѳ�����Ĺ���Ф���ƶ���ǧ����Ƥ��ʤ����Ȥ��顢��ʪ��Ū�ˤ�������Ū�ˤ��ä�����Ȥʤ�褦���Ѳ��ǤϤʤ���Ƚ�Ǥ���롣
�ʤ���Ǣ��ӥ��ӥ�ӥ����ӥ�Ρ����������Ū�����ˤ����ơ�100 mg/kg�ʾ�����̷��λ�ͺ��Ǣ���Ф�Ƚ����ˤʤ���Ĵ���迧ȿ�������졢Ƚ�꤬����Ǥ��ä����ޤ������������Ū�����ˤ����ơ���Ϣ�����Ѳ���ȼ��ʤ��ӥ��ӥ��̤Τߤι��ͤ�1,000 mg/kg���λ�ͺ��ǧ���줿��
�ӥ��ӥ�ˤĤ��Ƥϡ�Ǣ����ӷ����Ѹ��������Ȥ⥸�����������Ѥ��Ƥ��ꡢ4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ��ϥʥեȡ���ͶƳ�ΤǤ��뤳�Ȥ��顢���Υ������������ưפ�ȿ�����뤳�Ȥ������ͤ����롣�ޤ���Ehrlichȿ������Ѥ���Ǣ��Υ����ӥ�Ρ����������Ū�����ˤĤ��Ƥ⡢Ehrlich�����ϸŤ����饢�ߥδ������������ȯ�������Ȥ����Ѥ����Ƥ��ꡢ�ʥե��륢�ߥ�ͶƳ�ΤǤ����︳ʪ�����Ф��Ƥ�ȿ�����뤳�ȤϽ�ʬͽ�ۤ���롣�����Τ��Ȥϡ��︳ʪ�����ϱդ��Ф��ơ������λ�����ȿ���������Ȥˤ���ǧ���줿��
�������äơ�Ǣ��ˤ�����ӥ��ӥ�䥦���ӥ�Ρ����������ˤ��ȯ��������ӥ��ӥ�ι��ͤϡ�Ǣ�椢�뤤�Ϸ�����︳ʪ������Ӥ������ʪ�Ȼ����Ȥ�ȿ�������Τˤ���Τȹͤ���졢�︳ʪ���������ƶ��������Ѳ��ǤϤʤ���Ƚ�Ǥ��줿��
�������������ֽ�λ���˻�ưʪ�Ǥϡ���Ϳ���ֽ�λ���˻�ưʪ��ǧ���줿��IJ�γ�ĥ��ǧ���줺���������Ƥ�����
����Ȥ��̤ˡ��������ֽ�λ���˻�ưʪ��1,000 mg/kg���ˤ����ơ���������������֥ߥ��̤θ�������Ӥ����ȼ��A/G����㲼��ͺ�ˡ�̵������̤θ��������ǧ���줿�������������١����ġ��������ˤ�����Хå������ɥǡ�������ߤ�����Ū�ϰ������ư�Ǥ��ꡢ¾�˴�Ϣ�����Ѳ���ǧ����ʤ����Ȥ��顢�︳ʪ����Ϳ�ȴ�Ϣ�դ���ΤϺ���Ǥ��ä�������ˡ�1,000 mg/kg���λ�ˤ�����Ǿ�����н������ä����դ����н��̸����ˤĤ��Ƥ⡢���Ф�������н��̤˶��̤��ư�����Ѳ���������ΤǤϤʤ����νŤ��оȷ����䲼��ä����Ȥ�ȼ����Ū���Ѳ���Ƚ�Ǥ���롣
���Τ褦�ˡ�4�ݥ��ߥΡ�5�ݥҥɥ�������2, 7�ݥʥե������ۥ����Υʥȥꥦ��ϥ�åȤؤ�28����ȿ����Ϳ�ˤ����ơ�1,000 mg/kg���ˤ����Ƥ��ä�����Ȥʤ�褦�������ƶ���ǧ����ʤ��ä����������äơ�̵�ƶ��̡�NOEL�ˤ�1,000 mg/kg/day�ȿ��ꤵ�줿��
| Ϣ���衧 |
| ���Ǥ�� | ��ƣ��ɧ |
| �ʺ���ܻ���ʪ�ʳذ�������� |
| �� 229 ��������ϸ��Զ����� 3-7-11 |
| Tel 0427-62-2775 | Fax 0427-62-7979 | |
| Correspondence: |
| Ito, Yoshihiko |
| Research Institute for Animal Science in Biochemistry and Toxicology, Japan |
| 3-7-11 Hashimotodai, Sagamihara-shi, Kanagawa, 229, Japan |
| Tel 81-427-62-2775 | Fax 81-427-62-7979 | |








