3�ݥ�ȥ����٥ʥߥ�Υޥ������Ѥ��뾮�˻
Micronucleus Test of 3-Methoxybenzenamine on Mice
����
�︳ʪ��3�ݥ�ȥ����٥ʥߥ��������ˤ������˦������Ū�ƶ���ɾ�����뤿��ˡ�Crj: BDF1ͺ����ӻ�ޥ������Ѥ��붯���и���Ϳ�ˤ�뾮�˻��»ܤ�������̤ϰʲ��Τ褦������롣
1.����ͽ���
3�ݥ�ȥ����٥ʥߥ������ͽ�����Ԥä���̡�Crj: BDF1ͺ����ӻ�ޥ����ˤ�����������̤ϡ����줾��1000 mg/kg�����600 mg/kg�Ǥ��ä��������ǡ�����ͽ�������Ӿ����ܻ�ˤ�����3�ݥ�ȥ����٥ʥߥ�ι����̤�ͺ��1000 mg/kg�Ȥ������600 mg/kg�Ȥ�����
2.����ͽ���
3�ݥ�ȥ����٥ʥߥ��1000 mg/kg��ͺ�ˡ�600 mg/kg������Ϳ��������ͽ�����»ܤ����Ȥ�����ͺ�ޥ����˻�˴��ǧ���줿�������ǿ�����ͺ�ޥ����ˤ�800 mg/kg����Ϳ������Ϳ��24��48��72�����ܤ˹��������ɸ�ܤ����������ɸ�ܴѻ��η�̡����˽и����١ʾ��ˤ�ͭ����¿�����ַ��γ��ˤϡ�ͺ�Ǥ�72���ַ��ˤ����ƺǹ��ͤ���ͭ�պ�����η�̡�24���ַ�����١�72���ַ��ξ��˽и����٤�5%����ͭ�դ˹⤫�ä�����������ǤϾ��˽и����٤ηл�Ū�Ѳ������餫�ǤϤʤ��ä������ַ�����Ψ���ɸ�Ȥ��������˦�����������ϡ�ͺ��Ȥ��ǧ����ʤ��ä��������η�̤��顢�����ܻ�Ǥ�ɸ�ܺ�����������Ϳ����ɸ�ܺ����ޤǤλ��֡ˤ�ͺ����Ϳ��72���֡������Ϳ��24���֤˷��ꤷ����
3.�����ܻ
ͺ�ޥ����ˤ�3�ݥ�ȥ����٥ʥߥ��200��400�����800 mg/kg����Ϳ������Ϳ��72�����ܤ˹��������ɸ�ܤ����������������ޥ����ˤ�150��300�����600 mg/kg����Ϳ������Ϳ��24�����ܤ˹��������ɸ�ܤ����������ɸ�ܴѻ��η�̡�ͺ��800 mg/kg��Ϳ���ˤ����뾮�˽и����٤������оȷ�����Ӥ���ͭ�դ����ä���������ˤ����ƤϤ�����θ�����Ϳ���Ȥ�ͭ�դ����äϴѻ�����ʤ��ä����ַ������������ַ�����Ψ�ϡ�ͺ��Ȥ�ˤΤ��������Ϳ���ˤ����Ƥ⡢�������㲼���ʤ��ä���
4.����
�ʾ�η�̤��顢3�ݥ�ȥ����٥ʥߥ�ϡ��ܻ��ﲼ�ǡ�BDF1ͺ�ޥ����ˤ�����800 mg/kg����Ϳ�ˤ�ꡢ�����˦�ˡ����ˤ�Ͷȯ������ѤΤ��뤳�Ȥ������ޤ��������˦�������������Ѥϡ�ͺ��Ȥ�˼����ʤ��ä���
���
�������̴�¸����ʪ���ǡ����߽�ʬ�ʰ����������Τʤ�3�ݥ�ȥ����٥ʥߥ�ˤĤ��ơ�OECD���濴�Ȥ��ƹԤ��Ƥ����ݶ��Ϥˤ��������������Ȥΰ�ĤȤ��ơ�������ˤ������˦������Ū�ƶ���Ĵ�٤뤿��ˡ�ͺ����ӻ�ޥ������Ѥ��ƹ����˦�ˤ����뾮�˻��»ܤ������ޤ��������ܻ���Ѥ�����Ϳ�̤���ꤹ�뤿�������ͽ�����Ԥäƺ������̤��ᡢ�����ܻ�ˤ�����ɸ�ܺ�����������ꤹ�뤿��˾���ͽ�����Ԥ��������η�̤˴�Ť��ƾ����ܻ��Ԥä����ܻ�ϡֿ�������ʪ���˷�������ˡ�ˤĤ��ơסʾ���62ǯ3��31�������ݶ���237�桢��ȯ��306�桢62�����303��ˤ����OECD�����ʻˡ�����ɥ饤��474�˽������ʪ��GLP�ʾ���59ǯ3��31�������ݶ���39�桢��ȯ��229�桢59�����85�桢��������63ǯ11��18�����Ĵ븦��233�桢������38�桢63�����823��ˤ˴�Ť��Ƽ»ܤ�����
�¸�����
1.�¸�ưʪ�Ȼ�����
�¸��ˤϡ����ܥ��㡼�륹����С���CRJ�ˤ����������8�����Crj: BDF1��C57BL/6��DBA/2�ζ��ϴ�F1��ͺ����ӻ�ޥ�����1���ְʾ�ͽ�����餷���塢�۾��ǧ����ʤ��ä�ưʪ��9��10����ǻ�˶�������
ưʪ�ϡ����ߤȤ��ƥۥ磻�ȡ��ե졼����CRJ�ˤ����줿TPX��������������143��293��148 mm, CRJ�ˤ�1ɤ���ļ��Ƥ����Хꥢ�������ƥ�λ��鼼�����꼼����23��1����꼾�١�55��5%�������������15���֡����ť������롧����7�����������7�������ˤǡ��ޥ����˿��ѸǷ������ʣΣͣơ����ꥨ����칩�ȡˤȿ�ƻ���ͳ���ݼ褵���ƻ��餷����ưʪ�η�ʬ����̵�����Фˤ��Ԥä������μ��̤ϥޥ��������˥ե���ȥڥ�ǥޡ��������������ˤϷ����Ȥ˿��ΰۤʤ륫���ɤˡ��������ưʪ�ֹ�ܤ��Ƹ��μ��̤�����Ȥ�������Ϳ�����ν��ϰϤ�ͺ��24��29�硢���19��22��Ǥ��ä���
2.�︳ʪ��
| ��̾�Ρ� | 3�ݥ�ȥ����٥ʥߥ�
��3-Methoxybenzenamine�� |
| ��CAS No.�� | 536-90-3 |
| ����̾�� | m-Anisidine, 3-Aminoanisole,
3-Methoxyaniline |
| �ʥ��å��ֹ�� | FBX01������������� (��) ���� |
| ��ʬ�Ҽ��� | C7H9NO |
| ��ʬ���̡� | 123.17 |
| �������� | ø�������Ρ���ˤ�����ϡ�������ӥ��륳����˲���, ʨ��251�ͻ����1��1�� |
| ����š� | 1.10 |
| �ʽ��١� | 98%�ʾ� |
| ���ԡ� | (��) ���ܲ��ع��ȶ��� |
| ������ǯ������ | 1991ǯ7��12�� |
| ���ݴɾ��� | ������ |
����ͽ���
1.��ˡ
1)�¸���������
���˻���Ѥ����︳ʪ��3�ݥ�ȥ����٥ʥߥ����Ϳ�̤���ꤹ�뤿�ᡢͺ��Ȥ�˳�5ɤ���Ĥ���ʤ�8�����ߤ�����Ϳ�̤줾�졢0�������оȡ��ʶɡ˥���������¸��������ȡˡ͡�100��200��400��600��800��1000�����1500 mg/kg�Ȥ�����
2)���Τ�Ĵ������Ϳ��ˡ
���Τ���Ϳ���̤ϥޥ������ν�kg������10 ml�Ȥ������ǹ����̤���Ϳ���Τ�3�ݥ�ȥ����٥ʥߥ�ν����̤����Τ˺μ褷���ʶɡ˥�������˷�������Ĵ������������ʲ������̤ˤĤ��Ƥϡ��ǹ����̤�Ĵ���դ�����Ǵ��ᤷ�ƽ����ǻ�٤�Ĵ���������ޤ�����Ϳ���ΤϤ��٤��ѻ�Ĵ���Ȥ�������Ϳ�ϡ�ñ�����и���Ϳ�Ȥ�����
3)��˴Ψ�����̾��֤δѻ�������ν�¬��
��Ϳ������0���Ȥ���4���֤ˤ錄���������̾��֤�ѻ�������˴��̵ͭ��Ĵ�٤����ޤ����ޥ������νŤ���Ϳ����3���ܤδѻ���λ����¬�ꤷ����
2.���
1)��˴Ψ�����̾��֤�����νſ��
���ޤΤߤ���Ϳ�������Ǥϡ�ͺ��Ȥ�˰��̾��֤��Ѳ��ϸ���줺���νŤ�鷺�������ä�����������3�ݥ�ȥ����٥ʥߥ����Ϳ�������Ǥϡ�ͺ��600 mg/kg�����800 mg/kg�ʾ����Ϳ���Ǽ�ȯ��ư���㲼��ǧ���졢���̤����äȤȤ�ˡ����顢��ɽ���㲼�ʤɤ�����ħ�������줿����˴��ϡ�ͺ��1500 mg/kg��Ϳ����ǧ���졢��Ǥ�800 mg/kg�����1500 mg/kg��Ϳ����ǧ���줿����¸���Τˤ����Ƥϡ�ͺ��Ȥ��600 mg/kg�ʾ����Ϳ�������餫���νŤθ�����ǧ���줿���ʾ�η�̤��顢3�ݥ�ȥ����٥ʥߥ��ñ�����и���Ϳ�ˤ��BDF1ͺ����ӻ�ޥ����κ������̤ϡ����줾��1000�����600mg/kg �Ǥ���ȷ������줿��
2)���˻���Ѥ�����Ϳ��
����ͽ�������Ӿ����ܻ���Ѥ����︳ʪ���ι����̤�ͺ��1000 mg/kg�Ȥ������600 mg/kg�˷��ꤷ�����ޤ���������Ȥˤ��ơ�����2�Ǹ�����ͺ�Ǥ������̤�500 mg/kg������������̤�250 mg/kg�Ȥ�����Ǥ������̤�300 mg/kg������������̤�150 mg/kg�ˤ��줾����ꤷ����
����ͽ���
1.��ˡ
1)�¸���������
�ܻ�ˤ�����Ŭ�ڤ�ɸ�ܺ�����������ꤹ�뤿��ˡ�ͺ��Ȥ�˳�5ɤ���Ĥ���ʤ�3����24���ַ���48���ַ���72���ַ��ˤ��ߤ�������Ϳ�̤�ͺ����ӻ�ޥ����ˤ����ơ����줾������̤�1000 mg/kg�����600 mg/kg�Ȥ�������������1000 mg/kg����Ϳ����ͺ�ޥ����ˤ����ơ�15ɤ��2ɤ����Ϳ��1���ܤ˻�˴�������ᡢ���̤�800 mg/kg�Ȥ���ͺ�ޥ����γ�5ɤ����ʤ�3����24���ַ���48���ַ���72���ַ��ˤ����ߤ�����
2)���Τ�Ĵ������Ϳ��ˡ
���Τ�Ĵ������Ϳ��ˡ������ͽ����ξ���Ʊ�ͤ˹Ԥä�����Ϳ�ϡ�ñ�����и���Ϳ�Ȥ�����
3)ɸ�ܤκ���
���ˤδѻ��Τ����ɸ�ܤ�Schmid����ˡ1, 2�ˤ˽��äƺ������������ʤ������Ϳ�����λ��֤�����æ��ˡ�ˤ��ޥ������व���ƺ��������ܹ���Ŧ�Ф���������ξ��ü�����Ǥ��ơ������˦��0.6 ml�Υ����ۻ�������Hazleton�ˤ������Ф��������ɤ˽��ᡢ1000 rpm��5ʬ�ֱ�ʬΥ���ơ�����������������֤�ԥڥåƥ��塢��˦��ͷ�դΰ����饤�ɥ��饹��������ʳƸ��ΤˤĤ�2���ɸ�ܡˤ������롢�������������������礷������ɸ�ܤ�5ʬ�֥�Ρ���Ǹ��ꤷ�����ॶ������pH6.8�Υ����˾ױդ�5%�˴��ᤷ�����ॶ�ա�Merck�ˤ�25ʬ�֡ͤ�Ԥä��塢pH 6.8�Υ����˾ױա�0.004%����������ϱդ���Ӿ�α��ǽ缡������������������
�ޤ������ַ���reticulocytes�ˤδѻ��Τ���˥˥塼������֥롼�ˤ��Ķ����������Ԥä������ʤ�����嵭���DZ����ɤ˻Ĥä���˦��ͷ�դ�Ʊ�̤Υ˥塼������֥롼�աʥ˥塼������֥롼0.5 g�ȥ��奦�����ꥦ��1.6 g��100 ml�ξ�α����Ϥ�������Ρˤ�ä���3ʬ���������������ˡ����ˤ�ɸ�ܺ����ξ���Ʊ�ͤ˥��饤�ɥ��饹��������ʳƸ��ΤˤĤ�2���ɸ�ܡˤ��������������Ρ���Ǹ��ꤷ���嵭���ॶ�դ�25ʬ����������pH 6.8�Υ����˾ױդ���Ӿ�α��ǽ缡������������������
4)���ˤδѻ�
�����������줾��ι���ɸ�ܤ˰��ֹ����ͺ�줾��ˤĤ��ơ�2̾�δѻ��Ԥˤ��֥饤���ˡ�Ǵѻ�������1���Τ�����2000�Ĥ�¿�����ַ���polychromatic erythrocytes�ˤ�ѻ�����������ξ��ˤ�ͭ�����Το���Ͽ�������ޤ��ַ���1���Τ�����1000�Ĵѻ��������Τʤ������ַ�����Ψ��Ĵ�٤ơ������˦�����������λ�ɸ�Ȥ�����
5)ͭ�պ�����
ͺ�줾��ξ��˽и����٤ˤĤ��ơ�Kastenbaum and Bowman��1970��3�ˤ�ɽ�ˤ�ꡢ24���ַ���¾�η��Ȥδ֤�5%����ͭ�պ������Ԥä��������֤������ȼ��¿�����Ϲ�θ���ʤ��ä���
2.���
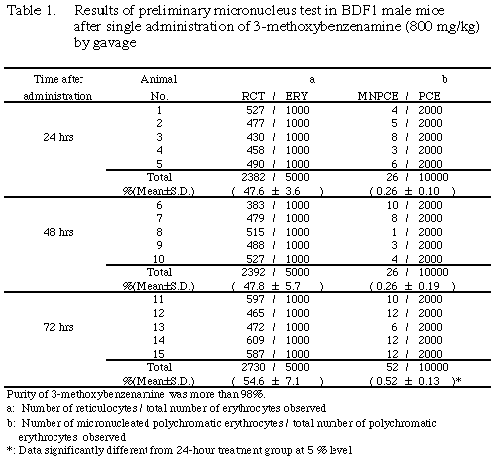
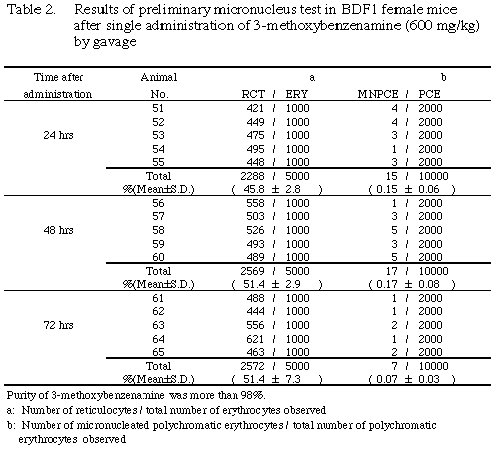
ͺ����ӻ�ξ���ͽ����η�̤��줾��Table 1�����2�˼��������˽и����٤ϡ�ͺ�Ǥ�72���ַ�����Ǥ�48���ַ��˺ǹ��ͤ�����ͭ�պ�����η�̡�ͺ�Ǥ�72���ַ��ξ��˽и����٤���24���ַ�����Ӥ���5%����ͭ�դ˹⤫�ä�������Ǥ�24���ַ���¾�λ��ַ��Ȥδ֤�ͭ�պ���ǧ����ʤ��ä������ַ�����Ψ���ɸ�Ȥ��������˦�����������ϡ����٤Ƥλ��ַ���ͺ��Ȥ��ǧ����ʤ��ä����ʾ�η�̤��顢�����ܻ�ˤ�����ɸ�ܺ��������ϡ�ͺ����Ϳ��72���֡����24���֤˷��ꤷ����
�����ܻ
1.��ˡ
1)�¸���������
����ͽ����η�̤˴�Ť���ͺ��Ȥ�˳�5ɤ���Ĥ���ʤ�5����ʲ��Τ褦���ߤ������ޤ��������̷��˻�˴������줿����ͽ�����ΤȤ��ơ�ͺ����ӻ��800 mg/kg�����600 mg/kg�줾���̤�2ɤ����Ϳ������
ͺ
| 1) | �����оȷ��ʥ�������� |
| 2) | 3�ݥ�ȥ����٥ʥߥ� 200 mg/kg��Ϳ�� |
| 3) | 3�ݥ�ȥ����٥ʥߥ� 400 mg/kg��Ϳ�� |
| 4) | 3�ݥ�ȥ����٥ʥߥ� 800 mg/kg��Ϳ�� |
| 5) | �����оȷ���cyclophosphamide, CPA��50 mg/kg��* |
��
| 1) | �����оȷ��ʥ�������� |
| 2) | 3�ݥ�ȥ����٥ʥߥ� 150 mg/kg��Ϳ�� |
| 3) | 3�ݥ�ȥ����٥ʥߥ� 300 mg/kg��Ϳ�� |
| 4) | 3�ݥ�ȥ����٥ʥߥ� 600 mg/kg��Ϳ�� |
| 5) | �����оȷ���cyclophosphamide, CPA��50 mg/kg��* |
* �����漼�ǡ������̤�CPA�ζ����и���Ϳ�ˤ�꾮�ˤ�ͭ�դ�Ͷȯ����뤳�Ȥ�ǧ����Ƥ��롣
2)���Τ�Ĵ������Ϳ��ˡ
��Ϳ���Τ�Ĵ���������Ϳ��ˡ������ͽ����ξ���Ʊ�ͤ˹Ԥä����ޤ��������о�ʪ����CPA, Sigma�ˤϡ��������������աʾ����������ȡˤ��ϲƽ����ǻ�٤�Ĵ����������Ϳ�ϡ�ñ�����и���Ϳ�Ȥ�����
�ʤ����������ˤ�����Ĵ�����Τμ����ˤ�������������»ܤ��������ʤ����3�ݥ�ȥ����٥ʥߥ��ʶɡ˥�������˷�������15 mg/ml�ϱա���Ϳ���̤�ޥ������ν�������10 ml�Ȥ�������150 mg/kg�������ˤ����80 mg/ml�ϱա�Ʊ800 mg/kg�������ˤ�Ĵ������ʬ�ϲ��ظ��漼�ǹ�®���Υ����ޥȥ���ե�����HPLC�ˤ��Ѥ��ơ�Ĵ��ľ�太���7����δ��̤�¬�ꤷ�������η�̡�ξĴ�����Τ�Ĵ��7�����ʿ�Ѵ������Ĵ�����Τ��줾��99.5�����109%�Ǥ��ä����������äơ������ܻ���Ѥ���ǻ���ϰϤ�����Ĵ�����Τϡ�������Ĵ����7���ְ���Ǥ��뤳�Ȥ���ǧ���줿��
�ޤ��������ܻ�ˤ����롢�����̷�����������̷�����Ϳ���ΤˤĤ��ơ�HPLC���Ѥ��ƶѰ���������ʬ�Ϥ�Ԥä������η�̡��︳ʪ����ʿ�Ѵ��̤�ź���̤�115��131%�ȹ⤤�ͤ��������η�̤˴ؤ��Ƥϡ�����ʬ���Ѥ�Ĵ�����Τ�μ褹��ݡ����ޤ��Ѥ�������������ԥڥåȤμ��Ϥ����夷���������ߤʤɤˤ�ä�ʬ�ϸ��Τ˺����������η�̡�ʬ���ͤ��⤤�ͤ�����ǽ�����ͤ���줿�������Ǻ��١�Ʊ�ͤ˸��Τ�Ĵ�������������ƺμ������ʬ�ϻ��»ܤ��������η�̡��︳ʪ����ʿ�Ѵ��̤�ź���̤�98.6��109%���ϰϤˤ��ꡢ����ץ�֤ΤФ�Ĥ���ʿ���ͤ�6%����Ǥ��ä����������ͤ���������ɸ��������δ��ʷ����ո��Τ�ʿ�Ѵ��̤�ź���̤�85%�ʾ塢����¬���ͤΤФ�Ĥ��ϡ�������ʿ���͡�10%����ˤ��������Ƥ�����
3)ɸ�ܤκ�����ˡ����Ӿ��ˤδѻ�
ɸ�ܤκ�������Ӿ��ˤδѻ��ϡ�����ͽ����ξ���Ʊ�ͤ˹Ԥä���������ɸ�ܤ��������Ͼ���ͽ����η�̤˴�Ť���ͺ����Ϳ��72���֤ˡ������Ϳ��24���֤˹Ԥä��������оȷ��ˤĤ��Ƥϡ���ײ��ε��ܤ˽��äơ�ͺ��Ȥ����Ϳ��24���֤˹Ԥä���
4)ͭ�պ�����
���˽и����٤ˤĤ��ơ�Kastenbaum and Bowman��ɽ�ˤ�ꡢͺ��ˤĤ����줾�������оȷ��ȡ�3�ݥ�ȥ����٥ʥߥ�γƸ�����Ϳ������������оȷ��Ȥδ֤�5%����ͭ�պ������Ԥä��������֤������ȼ��¿�����Ϲ�θ���ʤ��ä������ˡ����˽и������٤����̡��п��͡˰�¸���ˤĤ��ơ�Cochran-Armitage�η�������4, 5�ˤ�5%���ǹԤä���
�ޤ����ַ������������ַ�����Ψ�ˤĤ��ơ�ͺ��ˤĤ����줾�������оȷ��ȡ�3�ݥ�ȥ����٥ʥߥ�γ���Ϳ������������оȷ��Ȥδ֤�5%���ǣ������Ԥä��������֤������ȼ��¿�����Ϲ�θ���ʤ��ä���
2.��̤���ӹͻ�
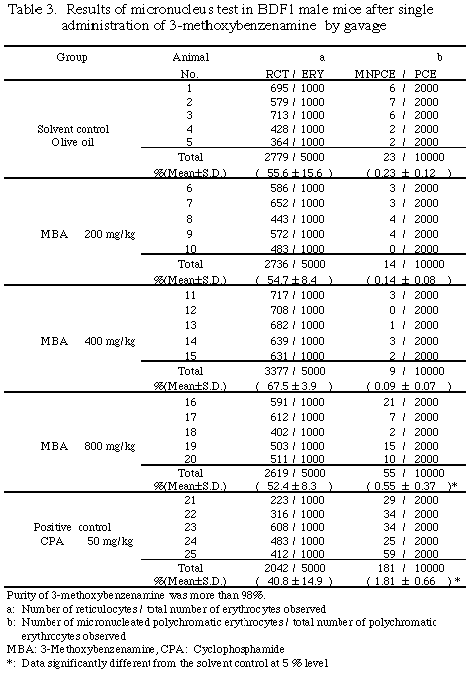
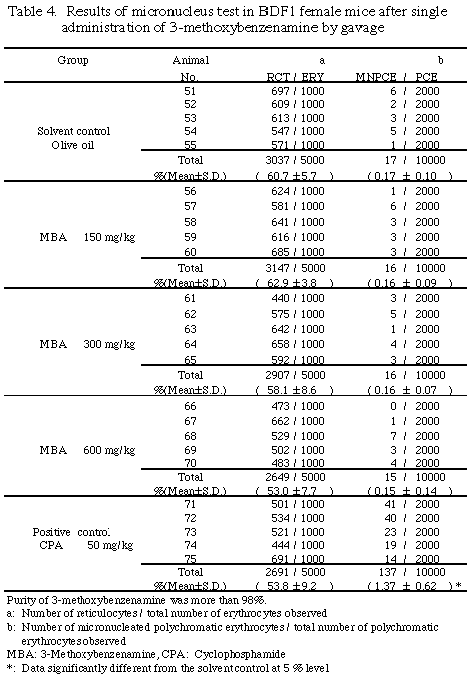
ͺ����ӻ�ξ����ܻ�η�̤��줾��Table 3�����4�˼��������˽и����٤ϡ�ͺ�ˤĤ��Ƥ�Kastenbaum and Bowman��ɽ���Ѥ���5%����ͭ�պ�����η�̡�3�ݥ�ȥ����٥ʥߥ��800 mg/kg��Ϳ�����ͤ��������оȷ����ͭ�դ˹⤫�ä�����Cochran-Armitage�η�������η�̤ϡ�3�ݥ�ȥ����٥ʥߥ�����̤˰�¸������ͭ�դ����÷������ʤ��ä���������������ͽ�����72���ַ��Ⱦ����ܻ��800 mg/kg��Ϳ�����ͤϡ��Ȥ��������꤬���5ǯ�֤�52��»ܤ�����BDF1ͺ�ޥ������Ѥ������˻�������оȷ����ͤ���ư�ϰϡ�0.04��0.23%�ˤ�Ϥ뤫�˱ۤ��Ƥ���������ˡ��������ͤˤĤ��Ƥϡ�Kastenbaum and Bowman��ɽ�ˤ�븡���1%���ǹԤä���̤Ǥ⡢�Ȥ��ͭ�պ���ǧ���줿���������äơ�3�ݥ�ȥ����٥ʥߥ�Ϥ������̤ǡ�ͺ�ޥ����ι����˦�ˤ����ơ����ˤ�Ͷȯ�����Τȹͤ����롣��ξ��˽и����٤ˤĤ��Ƥϡ�Kastenbaum and Bowman��ɽ���Ѥ������ꤪ���Cochran-Armitage�η��������Ԥä���̡�������ˤ����Ƥ�ͭ�պ���ǧ����ʤ��ä���������CPA��50 mg/kg��Ϳ���������оȷ��Ǥξ��˽и����٤�ͺ��Ȥ��5%����ͭ�դ����ä��ߤ�줿��
�ַ������������ַ�����Ψ�ϡ�ͺ��Ȥ�ˡ�3�ݥ�ȥ����٥ʥߥ�Τ��������Ϳ���ˤ����Ƥ������оȷ��Ȥδ֤�ͭ�պ���ǧ����ʤ��ä���
ʸ��
| 1) | W. Schmid, Mutation Res. 31 , 9-15 (1975) |
| 2) | W. Schmid, "Chemical Mutagen," Vol. 4 ed. by
A. Hollaender, Plenum Press, N.Y.-London, 1976,
pp. 31-53. |
| 3) | M.A. Kastenbaum and K.O.Bowman, Mutation Res. 9, 527-549 (1970). |
| 4) | W.G. Cochran, Biometrics, 10, 417-451 (1954). |
| 5) | P.Armitage, Biometrics, 11, 375-386 (1955). |
| Ϣ���衧 |
| ���Ǥ�� | ߧëŰ |
| �ʺ�˿������ʰ������������� |
| ��257 ������������� 729-5 |
| Tel 0463-82-4751 | Fax 0463-82-9627 | |
| Correspondence: |
| Shibuya, Tohru |
| Hatano Research Institute, Food and Drug Safety Center |
| 729-5 Ochiai, Hadano-shi, Kanagawa, 257, Japan |
| Tel 81-463-82-4751 | Fax 81-463-82-9627 | |




