2,3-ジブロモこはく酸のラットを用いた28日間反復経口投与毒性試験
Twenty-eight-day Repeat Dose Oral Toxicity Test of 2,3-Diburomosuccinic acid in Rats
要約
2,3-ジブロモこはく酸の20,140および1000 mg/kgをSD系ラットの雌雄に28日間反復投与し,その毒性について検討した.対照群および1000 mg/kg群については14日間の回復期間を設けた.
体重,摂餌量,血液学的検査,血液生化学的検査,尿検査および病理学的検査において,雌雄とも被験物質投与に起因する変化は認められなかった.1000 mg/kg群で雌雄ともに軽度の流挺が認められたが,その頻度も役与期間中1〜2回のみであり,毒性学的意義はないと考えられた.
以上の結果より,本試験条件下における2,3-ジブロモはく酸の無影響量は,雌雄ともに1000 mg/kgと考えられる.
方法
1.被験物質
2,3-ジブロモこはく酸(東京化成工業(株),ロット番号:DW01,純度:99.8%)は,分子量275.88,水,メタノール,エタノール,アセトンに可溶の白色粉末である.本ロットについては試験期間中安定であることが確認された.
2.試験動物およぴ飼育条件
日本チャールス・リバー(株)より入手したSD系ラット(Crj:CD,SPF)の雌雄を9日間検疫・馴化し,試験に使用した.投与開始前に動物を体重別層化無作為抽出法により群分けした.1群の動物数は雌雄各6匹とし,対照および高用量群についてはこの他に雌雄各6匹の回復群を設けた.投与開始時の週齢は雌雄とも5週齢,体重範囲は雄が171〜199 g,雌が136〜169 gであった.
検疫・馴化期間を含めた全飼育期間中,温度20〜25℃,湿度40〜70%R.H.,換気約12回/時,照明12時目(7:00〜l9:00)に自動調節された飼育室を使用した.動物は.実験動物用床敷(ベータチップ:日本チャールス・リバー(株))を敷いたポリカーボネート製ケージに1ケージ当り2匹で収容し飼育した.
動物には,実験動物用固型飼科(MF:オリエンタル酵母工業(株))および5 mmのフィルター濾過後紫外線照射した水道水を,それぞれ自由摂取させた.
3.投与量およぴ投与方法
被験物質を100,300および1000 mg/kgの各用量でSD系ラットに7日間反復経口役与した結果,いずれの用量においても明瞭な毒性兆候は認められなかった.従って,本試験では高用量を1000 mg/kgとし,以下公比約7で中用量を140 mg/kg,低用量を20 mg/kgとした.さらに,溶媒のみを投与する対照群を設定した.
投与期間は,剖検前日までの28日間とし,対照および1000 mg/kg群については14目間の回復期間を設けた.被験物質を0.5%カルボキシメチルセルロース・ナトリウム水溶液に懸濁させ,毎日1回,午前中に胃ゾンデを用いて強制経口投与した.役与液量は10 ml/kgとし,至近測定日の体重を基に算出した.
4.観察およぴ検査方法
1) 一般状態,体重およぴ授餌量
全例について一般状態を毎日観祭した.体重は投与開始日およびその後毎週1回測定した.また,摂餌量については,投与開始日およびその後毎週1回,ケージ単位で風袋込み重量を測定し,各期間毎の1匹当りの1目の平均摂餌量を算出した.
2) 血液学的検査
各計画殺時の全動物について,チオペンタールナトリウムの腹腔内役与による麻酔下で後大静脈より採血し,赤血球数(シースフローDCインピーダンス検出法)白血球数(RF/DCインピーダンス検出法),血小板数(シースフローDCインピーダンス検出法),ヘモグロビン濃度(SLSヘモグロビン法),ヘマトクリット値(赤血球パルス波高値検出法)を多項目自動血球分析装置(NE-4500:東亞医用電子(株)),白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROXHEG-70A:(株)立石電機),網状赤血球数(アルゴンレーザーを用いたフローサイトメトリー法)を自動網赤血球測定装置(R-2000:束亞医用電子(株)),プロトロンビン時間(PT;Quick一段法),活性化部分トロンボプラスチン時間(APTT;活性化セファロプラスチン法)を血液凝固自動測定装置(KC-10A:アメルング社)により測定した.また,検査の結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.凝固阻止剤として,プロトロンビン時間および活性化部分トロンボプラスチン時間測定には3.13%クエン酸ナトリウム水溶液を,それ以外の項目の測定にはEDTA-2Kを用いた.
3) 血液生化学的検査
採取した血液を室温で約30分間放置した後,3000 r.p.m.,10分間遠心分離し,得られた血清を用いて総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),グルコース(GK-G6PDH法),トリグリセライド(LPL-GK-G3PO-POD法),総コレステロール(CES-CO-POD法),尿素窒素(Urease-GLDH法),クレアチニン(Jaff 法),カルシウム(O-CPC法),無機リン(UV法),GPT(SSCC改良法),γ-GTP(SSCC改良法),ALP(GSCC改良法),ナトリウム,カリウム(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
法),カルシウム(O-CPC法),無機リン(UV法),GPT(SSCC改良法),γ-GTP(SSCC改良法),ALP(GSCC改良法),ナトリウム,カリウム(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
なお,クロライドについては2,3-ジブロモこはく酸に含まれるBrが選択電極法によるClイオンの測定値に影響を与えることが考えられたため,影響を受ける可能性の少ない電量滴定法(クロライドメーター,Model 925:コーニングメディカル(株))により測定した.
4) 尿検査
投与終了時の解剖の2日前に全生存動物の新鮮尿を採取し,pH,潜血,蛋白,糖,ケトン体,ビリルビン,ウロビリノーゲン(試験紙法,N-マルチスティックスSG:マイルス・三共(株)を尿分析器(クリニテック10:マイルス・三共(株))により測定した.
5) 病理学的検査
各計画殺時,全動物について採血後に腹大動脈を切断して放血致死させ剖検し,脳,肝臓,腎臓,副腎,精巣および卵巣の重量を測定した.また,これらの器官に加え,下垂体,眼球(付属腺を含む),肺,胃,甲状腺(上皮小体を含む),心臓,脾臓,膀胱,骨髄(大腿骨)を採取し,10%中性リン酸緩衝ホルマリン液(眼球およびハーダー腺はDavidson液)にて固定後保存した.
投与終了時解剖動物の対照および1000 mg/kg群の雌雄の心臓,肝臓,腎臓,副腎および脾臓を対象に,常法に従いヘマトキシリン・エオジン染色標本を作製し鏡検した.
6.統計学的解析
計量データについては,Bartlett法による等分散の検定を行い,分散が一様の場合は一元配置分散分析を行った後,Dunnett法またはScheff 法により平均値の比較を行った.分散が一様でない場全にはKruskal-Wallisの検定を行い,Dunnett型またはScheff
法により平均値の比較を行った.分散が一様でない場全にはKruskal-Wallisの検定を行い,Dunnett型またはScheff 型の順位和検定を行った.尿の定性検査で得られたデータについては,Armitageのx^2検定を用いた.有意水準は5%以下とした.
型の順位和検定を行った.尿の定性検査で得られたデータについては,Armitageのx^2検定を用いた.有意水準は5%以下とした.
結果
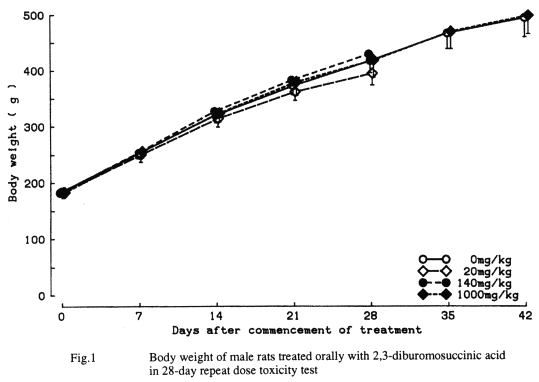
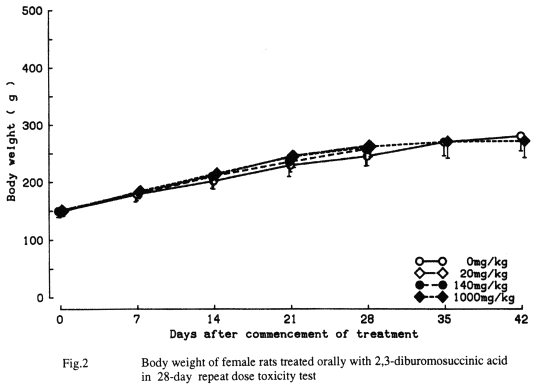
1.一般状態,体重および摂餌量(Fig. 1,2)
1000 mg/kg群で雌雄とも軽度の流挺が認められたが.投与期間後半に1〜2回観察されたのみであった.体重は雌雄ともに対照群と同様な推移を示したが.摂餌量において,1000 mg/kg群の雌で投与開始後14日および21日に増加,回復期間終了時に減少が認められた.
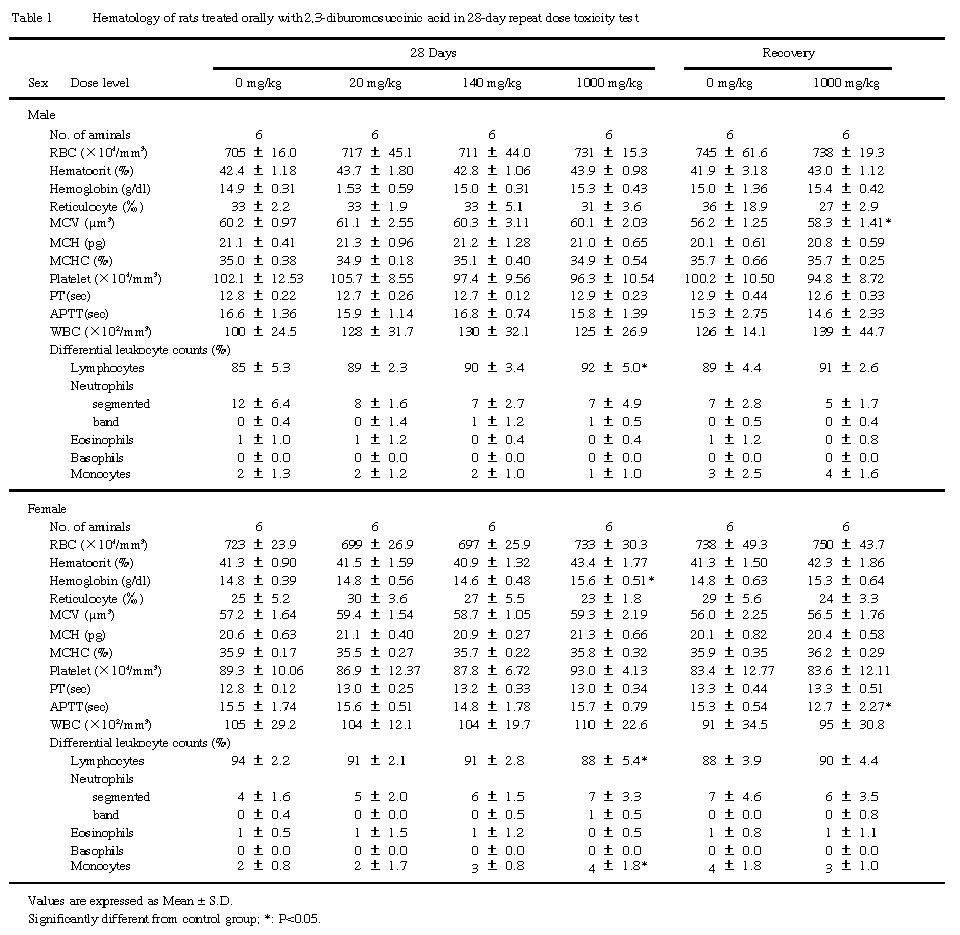
2.血液学的雌(Table 1)
投与終了時の検査において,1000 mg/kg群の雄でリンパ球の増加,雌でヘモグロピン濃度の増加,リンパ球の減少および単球の増加が認められたが,いずれも軽微な変化であるため,生理的変動範囲内の変化と判断した.また,回復終了時の検査において,1000 mg/kg群の雄で平均赤血球容積の増加,雌でAPTTの短縮が認められたが,いずれも軽微な変化であり,投与終了時の検査では変化は認められていないことから,被験物質投与とは関連のない変化と判断した.
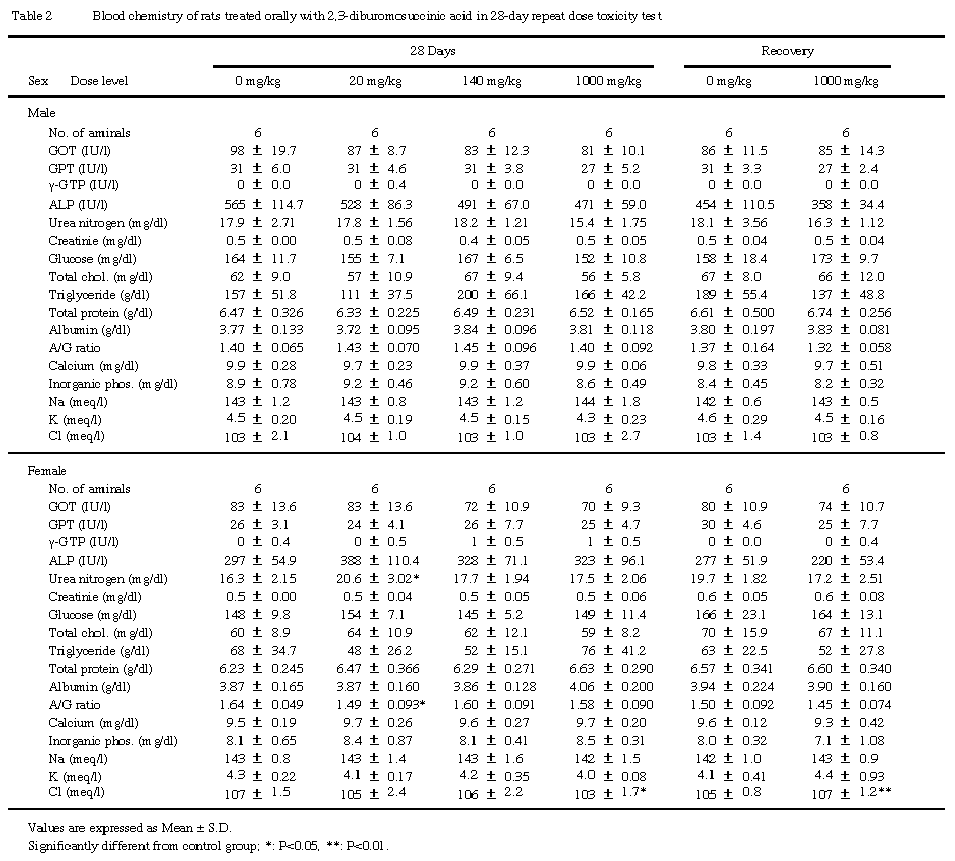
3.血液生化学的検査(Table 2)
投与終了時の検査では,20 mg/kg群の雌で尿素窒素の増加,A/G比の減少,1000 mg/kg群の雌でクロライドの減少,また,回復終了時の検杏では,1000 mg/kg群の雌でクロライドの増加が認められたが,これらはいずれも用量依存性がないか,あるいは軽微な変化であるため,生理的変動範囲内の偶発的変化と判断した.
4.尿検査
20 mg/kg群の雄で蛋自およびケトン体の減少,糖の増加が認められたが,用量依存性のない軽微な変化であるため,被験物質投与とは関連のない変化と判断した.
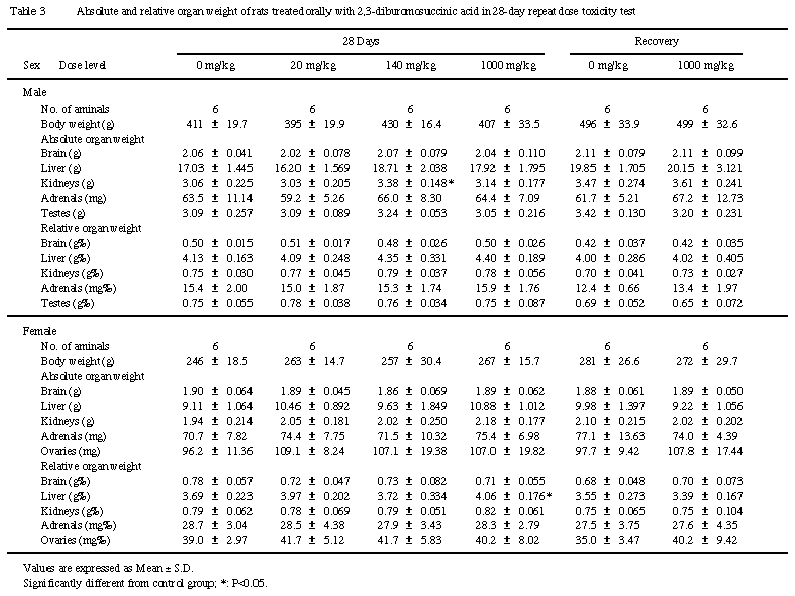
5.器官重量(Table 3)
投与終了時の検査において,1000 mg/kg群の雌で肝臓の対体重比の増加が認められたが,実重量では差は認められなかった.
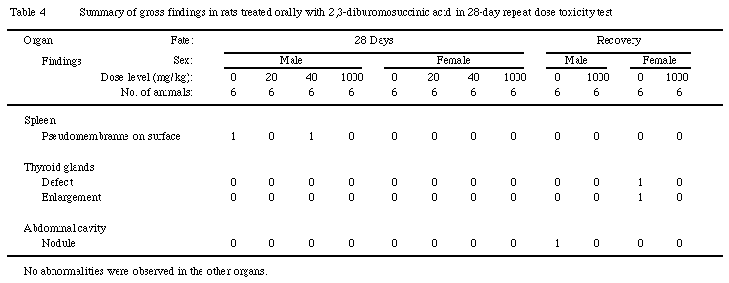
6.病理解剖検査(Table 4)
被験物質投与に起因する変化は認められなかった.偶発性変化として脾臓表層の偽膜形成,甲状腺の片側性の欠損と肥大および腹腔内結節が認められた.
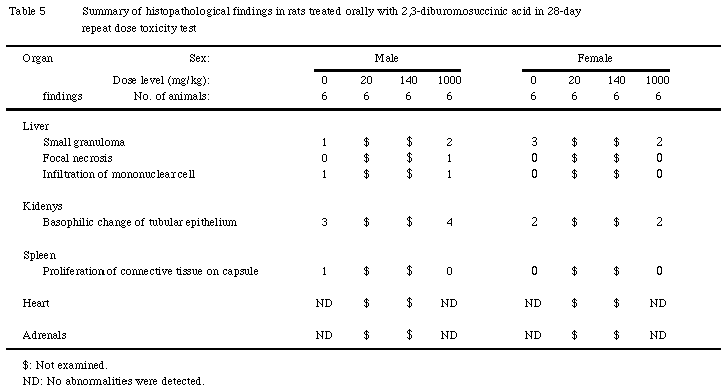
7.病理組織学的検査(Table 5)
被験物質投与に起因する変化は認められなかった.偶発性変化として,肝臓の巣状壊死,小肉芽腫,単核細胞の浸潤,腎臓の尿細管上皮の好塩基性変化および脾臓の被膜表層部における結合組織の増生が認められた.
考察
2,3-ジブロモこはく酸の20,140および1000 mg/kgをSD系ラットの雌雄に28日間反復経口投与し,その毒性について検討した.
1000 mg/kg群において,雌雄ともに軽度の流涎が観察されたが,投与期間後半に1〜2回散見された程皮の極低頻度のもので,経時的な一定の傾向もなかったことから,同群の投与液がpH 1〜2の強酸性であることに起因した毒性学的意義に乏しい変化と考えられる.また,雌の摂餌量に軽微な変化が認められたが,他の検査ではこれに関連する変化は認められなかったことから,毒性学的意義はないと考えられる.さらに,雌の肝臓の対体重比の増加についても,実重量では有意な差がなく,病理学組織学的検杏においても肝臓に異常は認められなかったことから,偶発的な変化と考えられる.
その他,体重,血液学的検査,血液生化学的検査,尿検査および病理学的検査のいずれにおいても,被験物質投与に起因する変化は認められなかった.
以上の結果から,本試験条件下における2,3-ジブロモこはく酸の無影響量は雌雄ともに1000 mg/kgと考えられる.
| 連絡先 |
| 試験責任者: | 松浦郁夫 |
| 試験担当者: | 大保真由美,土谷稔,武知雅人,豊田直人 |
| (株)三菱化学安全科学研究所 鹿島研究所 |
| 〒314-02 茨城県鹿島郡波崎町砂山14 |
| Tel 0479-46-2871 | Fax 0479-46-2874 | |
| Correspondence |
| Authors: | Ikuo Matsuura(Study director)
Mayumi Ohbo,
Minoru Tsuchitani
Masato Takechi,
Naoto Toyota |
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory |
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-02, Japan |
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |

 法),カルシウム(O-CPC法),無機リン(UV法),GPT(SSCC改良法),γ-GTP(SSCC改良法),ALP(GSCC改良法),ナトリウム,カリウム(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
法),カルシウム(O-CPC法),無機リン(UV法),GPT(SSCC改良法),γ-GTP(SSCC改良法),ALP(GSCC改良法),ナトリウム,カリウム(イオン選択電極法)を自動分析装置(日立736-10形:(株)日立製作所)により測定した.
 法により平均値の比較を行った.分散が一様でない場全にはKruskal-Wallisの検定を行い,Dunnett型またはScheff
法により平均値の比較を行った.分散が一様でない場全にはKruskal-Wallisの検定を行い,Dunnett型またはScheff 型の順位和検定を行った.尿の定性検査で得られたデータについては,Armitageのx^2検定を用いた.有意水準は5%以下とした.
型の順位和検定を行った.尿の定性検査で得られたデータについては,Armitageのx^2検定を用いた.有意水準は5%以下とした.






