 法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT 活性(SSCC法),GPT (SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OPCP法),無機リン濃度(モリブデン酸直接法),コリンエステラーゼ活性(DTNB法),γ-GTP活性(γ- グルタミル-p- ニトロアニリド基質法), ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(電量滴定法),A/G 比(計算)について分析した.
法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT 活性(SSCC法),GPT (SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OPCP法),無機リン濃度(モリブデン酸直接法),コリンエステラーゼ活性(DTNB法),γ-GTP活性(γ- グルタミル-p- ニトロアニリド基質法), ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(電量滴定法),A/G 比(計算)について分析した.雌雄とも,全例について試験期間中毎日観察した.
B. 体重
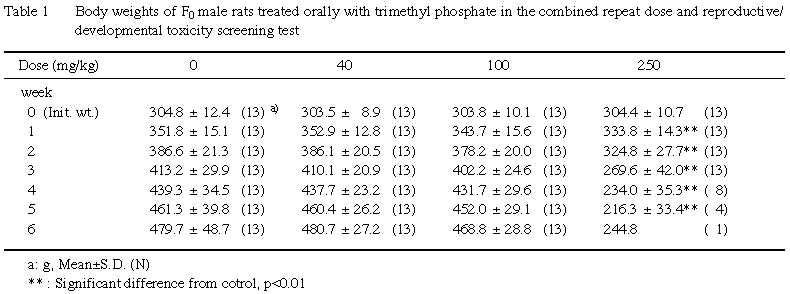
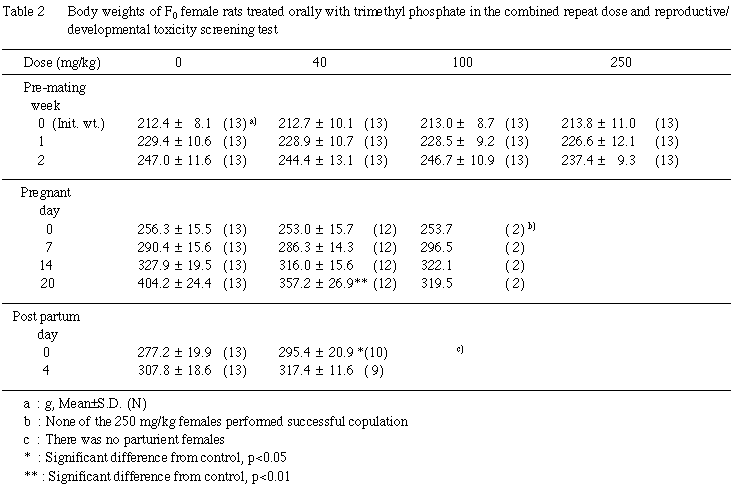
雌雄とも,全例について体重を試験期間中週1回〔雄:投与0,7,14,21,28,35,42日,雌:投与0,7,14,21日〕および解剖日に測定した.また,交尾成立雌では妊娠0,7,14,20日,分娩した雌では分娩後0および4日(哺育0および4日)の体重を測定した.
C. 摂餌量
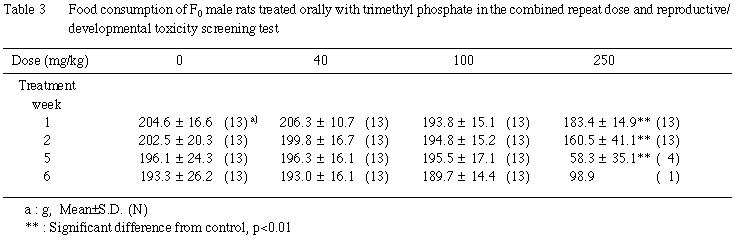
雌雄とも,全例について体重測定日と同日に餌重量を測定し,測定日から次の測定日までの間の摂餌量を算定した.交配期間中の摂餌量は測定しなかった.交尾成立雌では妊娠 0〜7,7〜14,14〜20 日,分娩した雌では哺育 0-4日の摂餌量を測定した.
D. 交配
交配は,投与14日(15回投与日)の夕方から最長2週間,同一群内の雌雄を1対1で同居させて行った.交尾成立の確認は,毎朝,腟内の腟栓および腟垢中の精子の存在を調べることにより行い,交尾が確認された雌は,その日を妊娠0日と起算して雄から分離し,個別に飼育した.交配結果から,各群について交尾率[(交尾動物数/同居動物数)×100 ],受胎率[(妊娠動物数/交尾動物数)× 100]および同居開始日から交尾確認日までの日数を求めた.
E.分娩状態
各群とも交尾成立雌は,全例を自然分娩させた.分娩状態の直接観察は,可能なものについて行った.ただし,直接観察できなかった個体についても分娩後の徴候から分娩困難や分娩遅延などの分娩障害の有無を判断し,個別に記録した.
F. 分娩日の算定
分娩の確認は,午前9時〜11時に限定し,この時間帯に分娩が完了していることを確認した個体について,その日を哺育0日,その前日を分娩日と規定した.午前11時を過ぎて分娩した個体については,翌日を哺育0日とした.分娩を確認した全例について妊娠期間(妊娠0日〜分娩日の日数)を算定し,出産率[(生児出産雌数/妊娠雌数)× 100]を各群について求めた.
G. 病理学的検査
a) 雄動物
イ. 剖検,器官重量および病理組織学的検査
最終投与日の翌日(投与42日相当日)にペントバルビタール深麻酔下で放血・致死させて剖検した.その際,全例について胸腺,肝臓,腎臓,精巣および精巣上体の重量を測定した.また,これらの器官と脳,心臓,脾臓,副腎,膀胱および頸髄,腰髄,坐骨神経,骨格筋(以上の4組織は,神経症状が発現したため追加)ならびに剖検において異常を認めた器官は10%ホルマリンに固定して保存し,パラフィン包埋,薄切,ヘマトキシリン・エオジン染色を施した後に全例について病理組織学的検査を行った.なお,精巣および精巣上体は,いったんブアン液に固定した後に10%ホルマリンに固定して保存した.
ロ. 血液学的検査
全例について,剖検に先立ち,ペントバルビタール麻酔下で腹部後大静脈より EDTA を抗凝固剤として採血し,赤血球数(RBC),白血球数(WBC),血色素濃度(Hb),平均赤血球容積(MCV),ヘマトクリット値(Ht),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC),血小板数を多項目血液自動測定機(Coulter Counter Model S-PLUS IV) により測定した.また,白血球分類は,血液塗沫標本(Wright-Giemsa 染色)を光学顕微鏡により観察して行った.
ハ. 血液生化学的検査
全例について,血液学的検査のための採血に引き続き,ヘパリンを抗凝固剤として用いて採血し,それぞれ血漿を分離して遠心方式生化学自動分析装置(COBAS- FARA)およびNa-K-Cl アナライザーIT-3型を用い,総蛋白濃度(ビウレット法),アルブミン濃度(BCG 法),総コレステロール濃度(COD・DAOS法),ブドウ糖濃度(グルコキナーゼ・G6PDH 法),尿素窒素濃度(ウレアーゼ・Gl.DH 法),クレアチニン濃度(Jaff 法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT 活性(SSCC法),GPT (SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OPCP法),無機リン濃度(モリブデン酸直接法),コリンエステラーゼ活性(DTNB法),γ-GTP活性(γ- グルタミル-p- ニトロアニリド基質法), ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(電量滴定法),A/G 比(計算)について分析した.
法),アルカリフォスファターゼ活性(p-ニトロフェニルリン酸基質法),GOT 活性(SSCC法),GPT (SSCC法),総ビリルビン濃度(ビリルビン「ロシュ」キットS シリーズ),カルシウム濃度(OPCP法),無機リン濃度(モリブデン酸直接法),コリンエステラーゼ活性(DTNB法),γ-GTP活性(γ- グルタミル-p- ニトロアニリド基質法), ナトリウム濃度(イオン電極法),カリウム濃度(イオン電極法),塩素濃度(電量滴定法),A/G 比(計算)について分析した.
b) 雌動物
イ. 剖検,器官重量および病理組織学的検査
分娩した雌は哺育4日に,交尾したが分娩しない雌は妊娠25日相当日に,また,交尾のみられなかった雌(未交尾雌)は交配期間終了日にそれぞれエーテル深麻酔下で放血・致死させ,剖検した.妊・不妊および未交尾のいずれの例においても卵巣および子宮を摘出し,子宮については Salewski 法5)を応用して着床痕を染色して着床数を確認した.卵巣はブアン液に固定して保存し,実体顕微鏡下で黄体数を数えた.不妊例および未交尾例の卵巣については,病理組織学的検査を行った.また,胸腺,肝臓および腎臓の重量を全例について測定した.これらの器官と脳,心臓,脾臓,副腎,膀胱,子宮および頸髄,腰髄,坐骨神経,骨格筋(以上の4組織は,神経症状が発現したため追加)ならびに剖検において異常を認めた器官は10%ホルマリンに固定して保存し,パラフィン包埋,薄切,ヘマトキシリン・エオジン染色を施した後に全例について病理組織学的検査を行った.
2)出生児
A. 産児数の算定
哺育0日に産児数(生存児+死亡児)を調べ,児の分娩率[(産児数/着床痕数)×100 ]および出生率[(出産生児数/着床痕数)× 100]を求めた.産児の性別を調べ,外表異常の有無を観察した.
B. 死亡児数の算定
死亡児数を毎日調べ,哺育0日の生存率[(生児数/産児数)× 100]および哺育4日の生存率[(哺育4日の生児数/哺育1日の生児数)× 100]を求めた.死亡児は剖検し,胸腔および腹腔内の器官を除去した後,エタノールに固定して保存した.
C. 体重測定
哺育0日および4日に一腹単位で雌雄別に体重(litter 重量)を測定し,[litter 重量/測定児数]を各腹について求めた.
D. 剖検
哺育4日に全例をエーテル深麻酔下で致死させ,剖検した.胸腔および腹腔内の器官は,一括して摘出し,各腹ごとに10%ホルマリンに固定して保存した.カーカスは,各腹ごとにエタノールに固定して保存した.
 法により対照群と各被験物質投与群との間で平均値の差の検定を行った.分散が一様でなかった場合は,Kruskal-Wallisの順位検定を行い,群間に有意性が認められた場合に対照群と各被験物質投与群との差について Dunnett型あるいは Scheff
法により対照群と各被験物質投与群との間で平均値の差の検定を行った.分散が一様でなかった場合は,Kruskal-Wallisの順位検定を行い,群間に有意性が認められた場合に対照群と各被験物質投与群との差について Dunnett型あるいは Scheff 型の検定を行った.有意水準は,5%および1%とした.なお,病理組織学的検査所見中,対照群と被験物質投与群の双方に認められ,被験物質投与群において頻度,程度が増強している所見については,Wilcoxonの順位和検定法による有意差検定を追加した.
型の検定を行った.有意水準は,5%および1%とした.なお,病理組織学的検査所見中,対照群と被験物質投与群の双方に認められ,被験物質投与群において頻度,程度が増強している所見については,Wilcoxonの順位和検定法による有意差検定を追加した.

a) 血液学的検査所見 (Table 5)
赤血球数,血色素量,ヘマトクリット値の有意な減少ならびに血小板数,分葉核好中球比率の有意な増加が,100 mg/kg 投与群において認められた.40 mg/kg投与群の所見には被験物質の投与に起因したと推定される変化はみられなかった.250 mg/kg 投与群の生存例1例では,赤血球数,血色素量,ヘマトクリット値が明らかな低値を示し,分葉核好中球比率,単球比率の増加およびリンパ球比率の低下がみられたが,血小板数に変化は認められなかった.
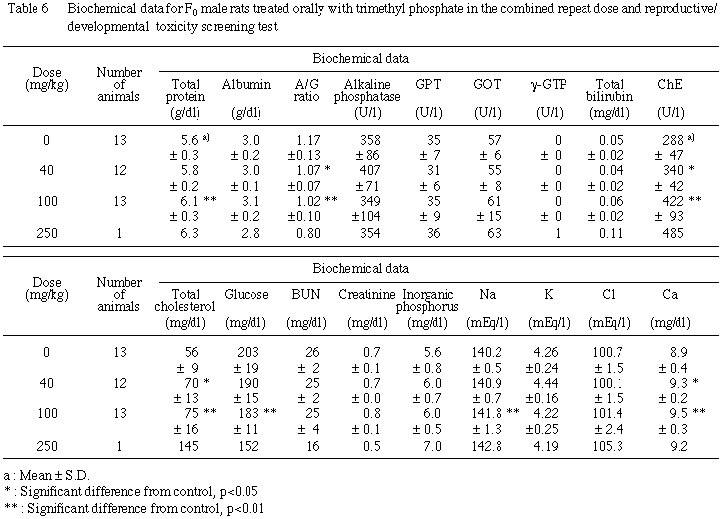
b) 血液生化学的検査所見 (Table 6)
用量依存的な変化としてA/G比の有意な低下,コリンエステラーゼ活性,総コレステロール濃度,カルシウム濃度の有意な上昇が, 40 および100 mg/kg 投与群に,ブドウ糖濃度の有意な低下,総タンパク濃度,ナトリウム濃度の有意な上昇が,100 mg/kg 投与群に認められた.これらの傾向は,250 mg/kg 投与群の生存例1例においても明らかであった.
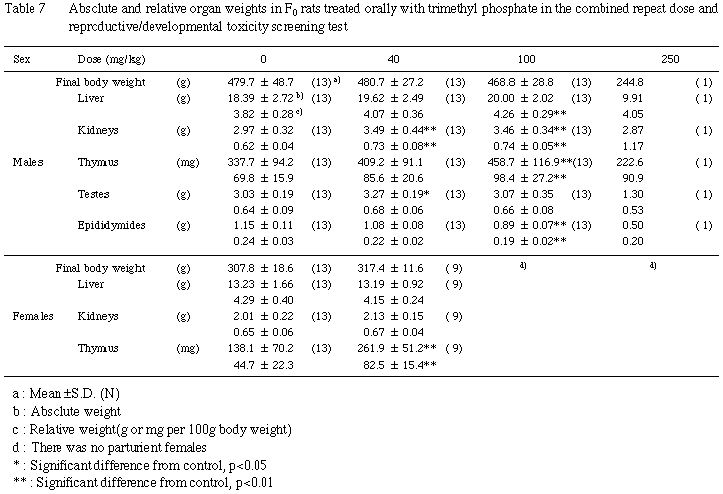
c) 器官重量 (Table 7)
用量依存的な変化として腎臓重量とその比体重値の有意な増加が 40 および100 mg/kg 投与群に,胸腺重量とその比体重値,肝臓の比体重値の有意な増加ならびに精巣上体重量とその比体重値の有意な低下が 100 mg/kg投与群に認められた.250 mg/kg 投与群の生存例1例では,低体重であることと関連して測定器官の重量は全て対照群の平均値を下回った.比体重値では胸腺,肝臓,腎臓の比体重値が高値を示したが,精巣および精巣上体の比体重値は対照群と比較して低値であった.
d) 剖検所見
100 mg/kg 投与群では,肺の暗色点,脾臓の暗色化,腎臓の淡色化,精巣,精巣上体の萎縮などが,低率に認められた.250 mg/kg 投与群では,死亡例,生存例ともに削痩,体脂肪の減少が顕著であり,胸腺の萎縮,肺の暗色領域,肝臓の暗色化・萎縮,腺胃の暗色領域,腸管内容の鬱滞,腸間膜リンパ節の萎縮,脾臓の萎縮・暗色化・濾胞の不明瞭化,副腎の腫大,腎臓の腫大,大量の膀胱内尿貯留,精巣・副生殖器の萎縮,骨髄の暗色化が高率に観察された.40 mg/kg投与群には,特記すべき異常所見は認められなかった.
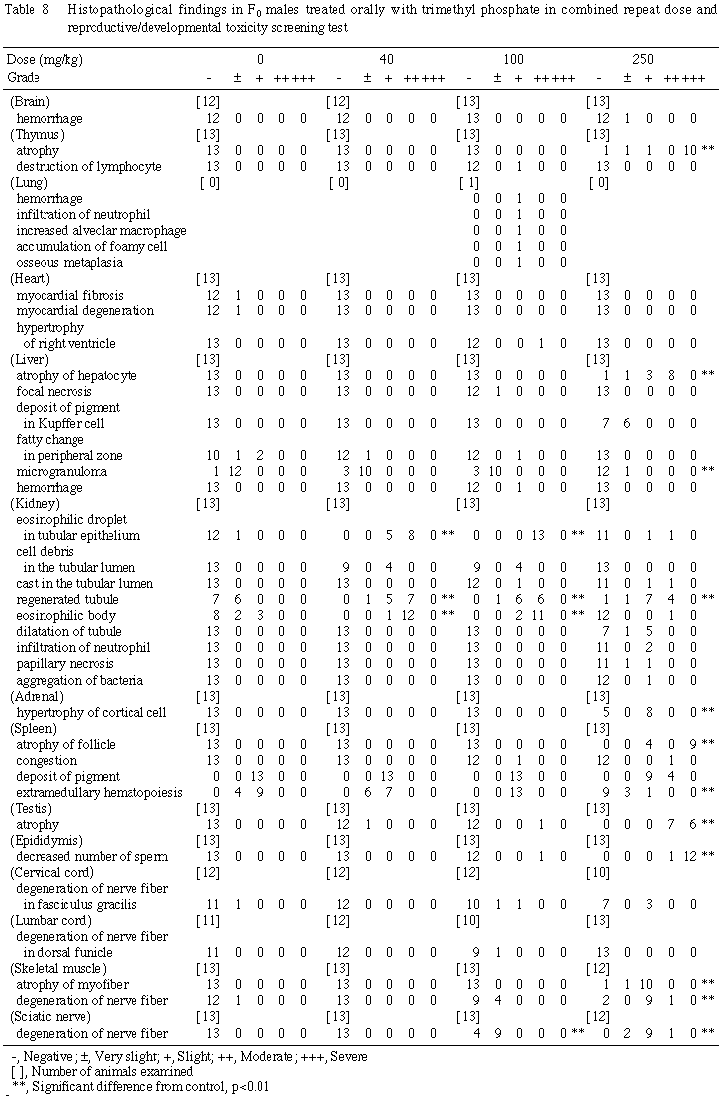
e) 病理組織学的検査所見 (Table 8)
40 mg/kg投与群:肝臓について小葉周辺性の脂肪化に軽減傾向がみられた.腎臓では,全例で近位尿細管上皮細胞内に好酸性で球状の滴状物がみられたほか,eosinophilic bodyおよび再生尿細管の頻度・程度が増強し,4例で再生尿細管腔内に細胞変性物がみられた.他の器官・組織については,ごく軽度の精巣萎縮が1例に認められたほかに特記すべき変化はみられなかった.100 mg/kg 投与群:肝臓で小葉周辺性の脂肪化に軽減傾向がみられ,ごく軽度の巣状壊死と出血が各1例に認められた.腎臓では,全例で近位尿細管上皮細胞内に好酸性で球状の滴状物が高度にみられ,eosinophilic bodyおよび再生尿細管の頻度・程度が増強したほか,1例で尿円柱の形成,4例で再生尿細管腔内に細胞変性物がみられた.脾臓については全例で髄外造血の軽度の亢進がみられた.精巣では,1例に中等度の萎縮がみられ,この例の精巣上体では腔内の精子が乏しかった.このほか2例の頸髄薄束,1例の腰髄背索,4例の骨格筋を走行する神経,9例の坐骨神経に神経線維の変性が認められた.250 mg/kg 投与群:死亡例全例で胸腺の萎縮がみられ,うち10例の変化は高度であった.生存例に胸腺の萎縮はみられなかった.肝臓では,死亡例全例で肝細胞に萎縮があり,生存例を含む6例の Kupffer細胞に色素沈着が認められた.一方,小肉芽腫はいずれの例にもみられず,小葉周辺性の脂肪化にも軽減傾向がみられた.腎臓では,死亡例2例でのみ近位尿細管上皮細胞内に好酸性・球状滴状物がみられ,eosinophilic bodyの出現も対照群より軽度であったが,再生尿細管の頻度・程度は増強し,腎乳頭の壊死が死亡例2例に認められた.副腎については,皮質束状帯細胞の肥大が死亡例8例にみられた.脾臓では,色素沈着の程度がやや強く,髄外造血は軽度であったが,濾胞の萎縮が全例に認められた.精巣については,全例で高度の萎縮がみられ,顕著な例では精細管内に精子形成細胞がなく,腔内はセルトリ細胞でほぼ占有されていた.精巣上体の腔内に精子はほとんどみられなかった.このほか生存例を含む3例の頸髄薄束,10例の骨格筋を走行する神経,全例の坐骨神経に神経線維の変性がみられ,11例に骨格筋線維のびまん性の萎縮が認められた.

B. 雌〔解剖日:哺育4日,全児死亡日,妊娠25日相当日(全胚吸収および不妊例)〕
a)器官重量 (Table 7)
胸腺重量とその比体重値は,40 mg/kg投与群において有意な高値を示し,100 mg/kg 投与群では高値となる傾向がみられた.250 mg/kg 投与群の胸腺重量には対照群と比較して著しい差は認められなかった.肝臓重量は,100 mg/kg 以上の投与群で低下傾向を示し,腎臓重量は 100 mg/kg投与群で増加傾向,250 mg/kg 投与群で低下傾向を示した.
b)剖検所見
100 mg/kg 投与群では,肝臓の暗色化が比較的高率に,250 mg/kg 投与群では,肺の暗色領域,肝臓の暗色化,腸管内容の鬱滞,脾臓の暗色化,副腎の腫大,卵巣の萎縮,骨髄の暗色化などが高率に観察された.40 mg/kg投与群には,特記すべき異常所見は認められなかった.
c)病理組織学的検査所見 (Table 9)
40 mg/kg投与群:胸腺の軽度の萎縮が2例にみられたのみであった(対照群では全例の胸腺が萎縮していた).他の器官・組織に特記すべき変化は認められなかった.
100 mg/kg 投与群:胸腺の萎縮は,いずれの例にもみられなかった.肝臓では,1例に巣状壊死が認められた.腎臓については,再生尿細管の頻度が増加し,1例で再生尿細管腔内に細胞変性物の貯留がみられたが,そのほかには石灰沈着あるいは腎盂の拡張が各1例にみられたのみであった.脾臓では,色素沈着の増強,髄外造血の減少がみられた.他の器官・組織に特記すべき変化は認められなかった.
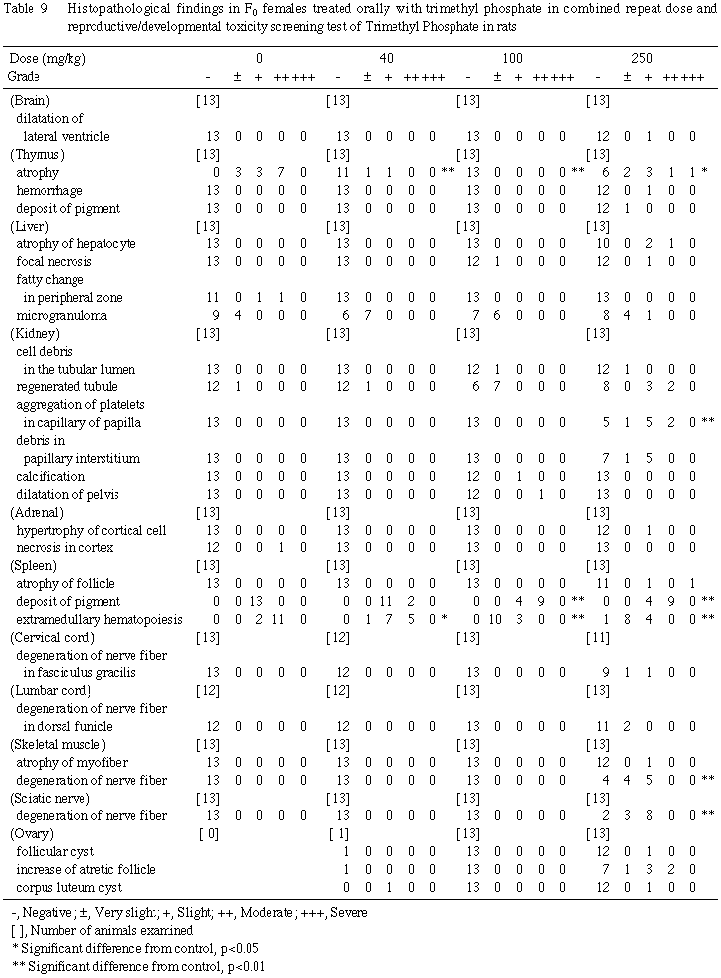
250 mg/kg 投与群:胸腺の萎縮が約半数にみられた.肝臓では,3例の肝細胞に萎縮があり,巣状壊死が1例に認められた.腎臓では,再生尿細管の頻度・程度が増強し,1例の再生尿細管腔内に細胞変性物の貯留を認めた.また,8例で腎乳頭の毛細血管腔内に血小板の凝集があり,6例で腎乳頭間質に細胞変性物と推定される好酸性の小塊が認められた.副腎については,皮質束状帯細胞の肥大が1例にみられた.脾臓では,色素沈着の増強,髄外造血の減少があり,濾胞の萎縮が2例に認められた.卵巣については,観察した9例中1例に卵胞性嚢胞,6例に閉鎖卵胞の増加,1例に黄体嚢胞がみられた.このほか神経線維の変性が,2例の頸髄薄束および腰髄背索,9例の骨格筋神経,11例の坐骨神経にみられ,1例では骨格筋線維にびまん性の萎縮が認められた.
250 mg/kg 投与群では,交尾率が著しく低下し,13組中2組でしか交尾が成立しなかった.また,交尾した2例の雌のいずれにも胚の着床はみられなかった.100 mg/kg 以下の投与群および対照群では,全例で交尾が成立し,同居開始から交尾成立までに要した日数にも対照群と各被験物質投与群との間で有意差は認められなかった.しかし,胚の着床は100 mg/kg 投与群では2例にしかみられず,同投与群では受胎率が著しく低下した. 40 mg/kg 投与群の受胎率には,対照群と比較して有意差は認められなかった.
2) 分娩および哺育状態
対照群では13例全例,40 mg/kg投与群では12例中10例の妊娠雌が児を分娩したが,いずれの雌においても分娩状態に異常があった証拠は得られなかった.哺育状態についても生児1例を分娩した40 mg/kg投与群の雌1例で分娩当日に児が死亡したほかには,異常を示唆する所見は認められなかった.なお,40 mg/kg投与群の2例,100 mg/kg 投与群の2例の妊娠雌は,いずれも早期全胚吸収例であり,これらの雌では必然的に分娩はみられなかった.
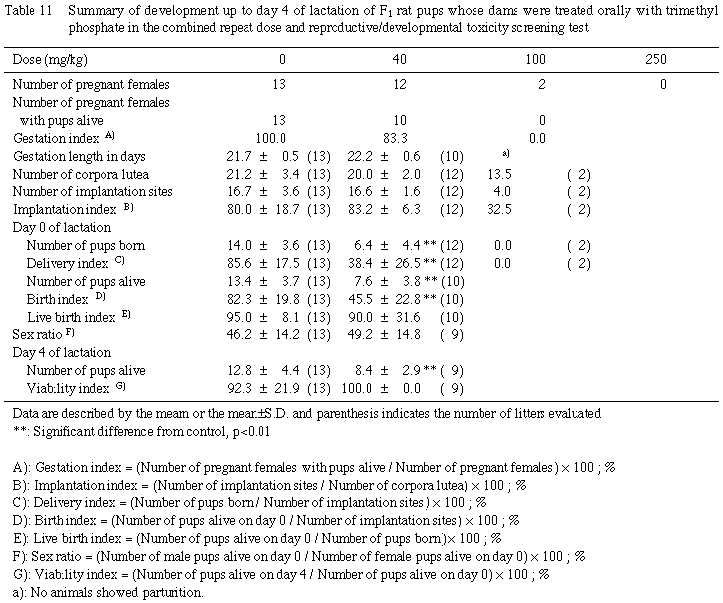
3) 妊娠黄体数,着床数および着床率 (Table 11)
対照群と40 mg/kg投与群の妊娠黄体数,着床数および着床率に有意差は認められなかった.100 mg/kg 投与群の早期全胚吸収例2例では,妊娠黄体数,着床数が対照群の平均値と比較して明らかに少なく,着床率も顕著に低下した.
4) 出産率および妊娠期間 (Table 11)
対照群と40 mg/kg投与群の出産率および妊娠期間に有意差は認められなかった.
40 mg/kg投与群では,産児数および出産生児数が有意に減少し,児の分娩率[(産児数/着床痕数)× 100]および出生率[(出産生児数/着床痕数)×100]も有意に低下した.しかし,新生児に死亡はみられず,哺育0日および4日の生存率はともに 100%であった.
2) 体重 (Table 12)
40 mg/kg 投与群の児の体重は,哺育0日および4日のいずれにおいても対照群と比較して有意な高値を示した.
3) 形態
哺育0日の外表観察,死亡児および哺育4日における全新生児の剖検において被験物質の投与に起因したと推定される外表および内臓の異常は認められなかった.

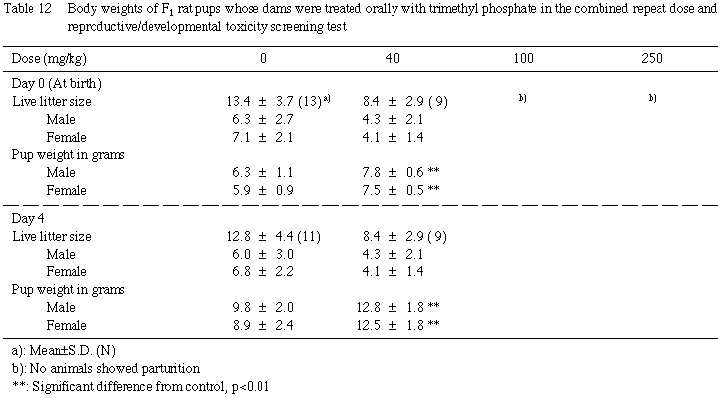
本試験条件下では,リン酸トリメチルの反復投与毒性および生殖発生毒性に関する無毒性量は,雌雄ともにいずれも 40 mg/kg/day を下回る量と推定される.
| 1) | T.H. Connor, Mutat. Res., 65, 121-131 (1979). |
| 2) | W.B. Deichmann, S. Witherup, J. Pharm. Exp. Ther., 88, 338-342 (1946). |
| 3) | Bioassay of trimethylphosphate for possible carcinogenicity, National Cancer Institute, Technical Report Series No. 81 (NIH) (1978). |
| 4) | A.R. Jones, H. Jackson, Br. J. Pharm., 37, 531-532 (1969). |
| 5) | H. Jackson, A.R. Jones, Nature (London), 220, 591-592 (1968). |
| 6) | R.D. Harbison, D. Dwivedi, M.A. Evans, Toxicol. Appl. Pharmacol., 35, 481-490 (1976). |
| 7) | H. Oishi, S. Oishi, K. Hiraga, Toxicol. Lett., 13, 29-34 (1982). |
| 連絡先 | |||
| 試験責任者: | 橋本 豊 | ||
| 試験担当者: | 田子和美,加藤博康 | ||
| (財)食品薬品安全センター秦野研究所 | |||
| 〒257 神奈川県秦野市落合729-5 | |||
| Tel. 0463-82-4751 | Fax 0463-82-9627 | ||
| Correspondence | |||
| Authors: | Yutaka Hashimoto (Study director) Kazumi Tago, Hiroyasu Kato | ||
| Hatano Research Institute, Food and Drug Safety Center | |||
| 729-5 Ochiai, Hadano, Kanagawa, 257, Japan | |||
| Tel. +81-463-82-4751 | Fax +81-463-82-9627 | ||