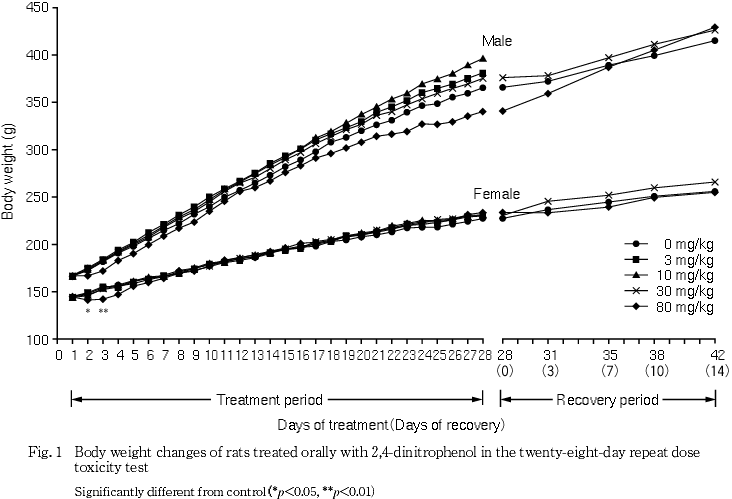
今回,2,4-ジニトロフェノールについて,SD系[Crj:CD(SD)IGS]ラットを用い,0(溶媒),3,10,30および80 mg/kg用量で28日間反復経口投与毒性試験を実施した.動物は1群雌雄各6匹とし,投与期間終了後屠殺群の5群,ならびに14日間回復群として対照,30および80 mg/kgの3群を設定した.
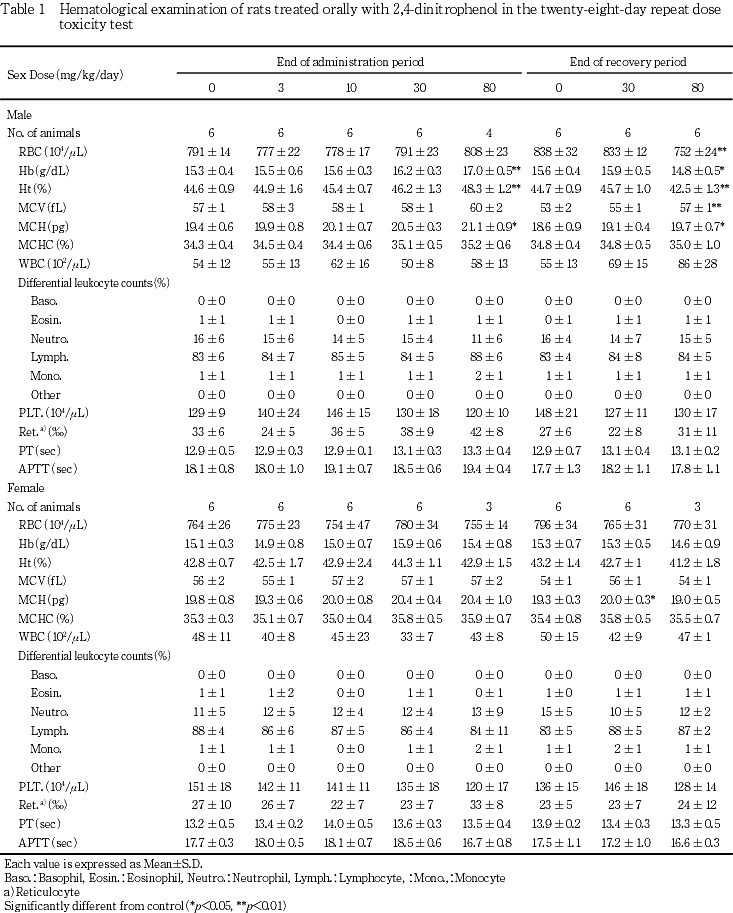
その結果,30および80 mg/kg群で雌雄に自発運動の低下および流涎,80 mg/kg群ではさらに雌雄に腹臥姿勢,浅速呼吸,眼瞼下垂,歩行時の這いずり姿勢,下腹部被毛の尿による汚れおよび死亡が認められた.死亡動物には,死亡直前に強直性痙攣および死亡直後に硬直が認められた.体重は,80 mg/kg群で雌に投与初期の増加抑制が一過性に認められ,雄には投与の後半に増加の抑制傾向が認められた.摂餌量は30および80 mg/kg群で雌雄に有意な増加が認められた.尿検査では,30および80 mg/kg群で雌雄に尿の褐色化傾向,さらに80 mg/kg群で雄に比重の有意な低下およびケトン体の有意な減少が認められた.血液学検査では,80 mg/kg群で雄にヘモグロビン量,ヘマトクリット値および平均赤血球血色素量の有意な増加,血液生化学検査では30および80 mg/kg群で雄に塩素の有意な減少が認められた.器官重量では,80 mg/kg群で雌雄に肝臓の相対重量の有意な増加,さらに雄に腎臓の相対重量の有意な増加が認められた.病理組織学検査では,80 mg/kg群で雌雄に腎臓皮髄境界部の鉱質沈着が,雄に脾臓の髄外造血巣の減少による赤脾髄の萎縮傾向が認められた.
回復群では,80 mg/kg群で雌雄に腎臓皮髄境界部の鉱質沈着が残存していたものの,その他の変化は回復ないし回復傾向を示した.なお,雄に,赤血球数,ヘモグロビン量およびヘマトクリット値の減少ならびに脾臓の髄外造血巣の増加が認められた.30 mg/kg群では,変化は認められなかった.
以上の結果から,2,4-ジニトロフェノールのラットへの28日間反復投与による主な毒性は,一般状態の変化であり,多血症および腎臓や肝臓に対する影響も認められた.無影響量は,雌雄とも10 mg/kg/dayと推定された.
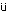 nwald-Giemsaで染色して鏡検)を測定した.また一部は,3.8 %クエン酸ナトリウム液で凝固阻止処理して血漿を分離し,血液凝固自動測定装置(アメルング社:KC-10A)により,プロトロンビン時間(PT, Quick一段法)および活性化部分トロンボプラスチン時間(APTT,エラジン酸活性化法)を測定した.
nwald-Giemsaで染色して鏡検)を測定した.また一部は,3.8 %クエン酸ナトリウム液で凝固阻止処理して血漿を分離し,血液凝固自動測定装置(アメルング社:KC-10A)により,プロトロンビン時間(PT, Quick一段法)および活性化部分トロンボプラスチン時間(APTT,エラジン酸活性化法)を測定した.
 法),GOT,GPT,γ-GTP,ALP(以上,JSCC法),LDH(SFBC法),コリンエステラーゼ(BTC-DTNB法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置〔東亜電波工業(株),NAKL-132〕により,ナトリウム,カリウムおよび塩素を測定した.
法),GOT,GPT,γ-GTP,ALP(以上,JSCC法),LDH(SFBC法),コリンエステラーゼ(BTC-DTNB法),カルシウム(OCPC法)および無機リン(酵素法)を,また電解質自動分析装置〔東亜電波工業(株),NAKL-132〕により,ナトリウム,カリウムおよび塩素を測定した.
 法(群間で標本数が異なる場合)により対照群に対する各群の比較検定を行った.分散が一様でない場合およびノンパラメトリックデータはKruskal-Wallisの順位検定を行い,その結果有意差を認めた場合,Dunnett型またはSheff
法(群間で標本数が異なる場合)により対照群に対する各群の比較検定を行った.分散が一様でない場合およびノンパラメトリックデータはKruskal-Wallisの順位検定を行い,その結果有意差を認めた場合,Dunnett型またはSheff 法(群間で標本数が異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータにはFisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.
法(群間で標本数が異なる場合)により対照群に対する各群の比較検定を行った.カテゴリカルデータにはFisherの直接確率法を用いた.有意水準は,いずれの場合も5 %とした.
回復期間中の観察では,80 mg/kg群で投与期間中の下腹部被毛の汚れが短期間残存していた例を除いて,雌雄のいずれも変化は認められなかった.
回復期間においては,投与期間中に増加抑制の傾向が認められた80 mg/kg群の雄の体重は回復傾向を示した.

回復期間において,投与期間中に認められた摂餌量の変化は,30および80 mg/kg群の雌雄とも回復した.
回復期間中の検査において,各検査項目に変化は認められなかった.
回復期間終了時の検査において,80 mg/kg群で雄に赤血球数,ヘモグロビン量,ヘマトクリット値の有意な減少,平均赤血球容積および平均赤血球血色素量の有意な増加が認められた.30 mg/kg群では雌に平均赤血球血色素量の有意な増加が認められたが,用量依存性の認められない変化であった.
回復期間終了時の検査において,投与期間終了時の検査で認められた変化は認められなかった.30 mg/kg群で雌のLDHは有意な高値,BUNおよび無機リンは有意な低値を示したが,いずれも用量依存性の認められない変化であった.

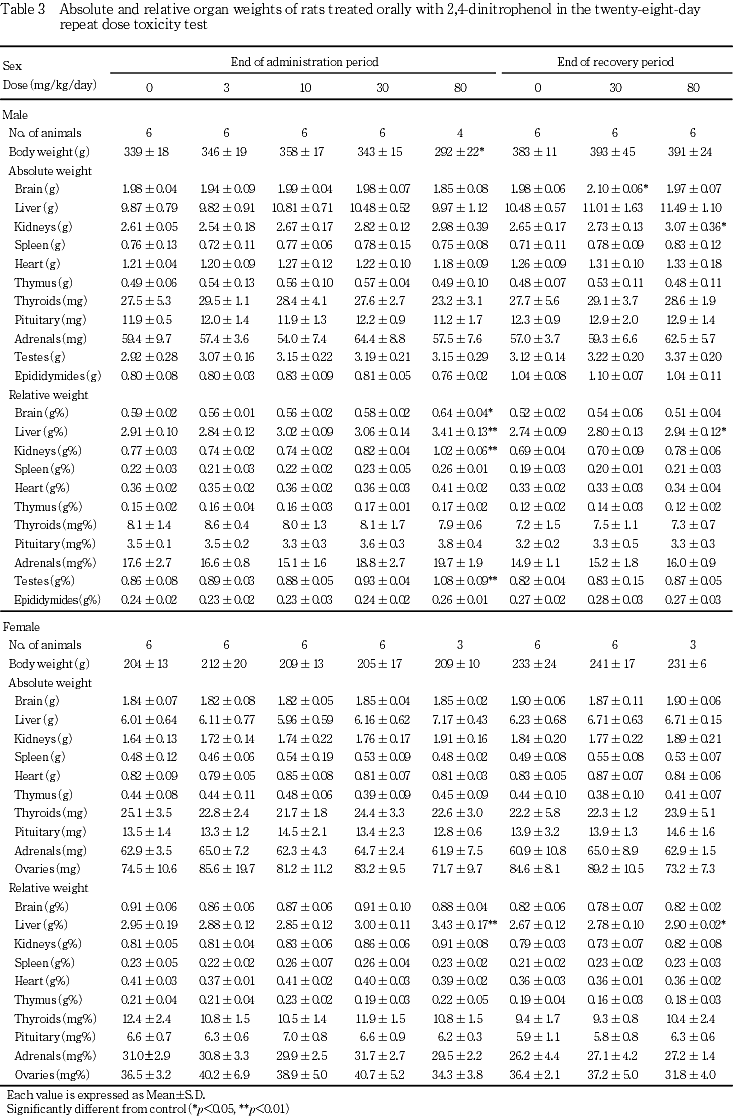
回復期間終了時屠殺動物では,80 mg/kg群で雌雄の肝臓の相対重量に有意差が残るものの,投与期間終了時屠殺動物に比べて変化は軽減する傾向が認められた.また,80 mg/kg群で雄に腎臓の絶対重量のみの有意な増加が認められた.なお,30 mg/kg群の雄の脳の絶対重量は対照群と比べて有意な高値を示したが,変化に用量依存性は認められなかった.
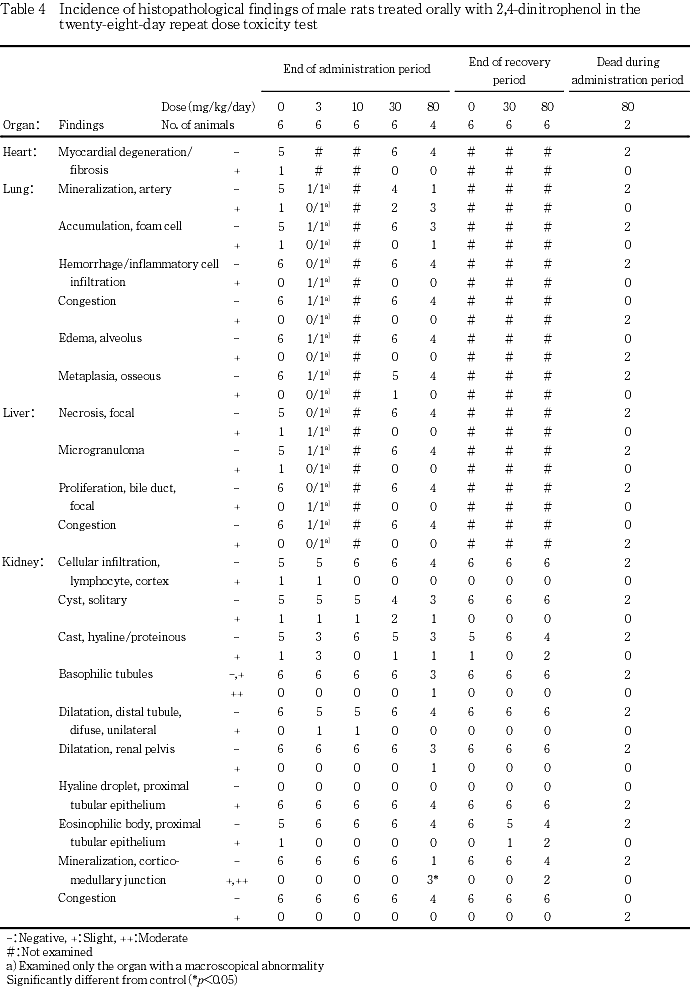
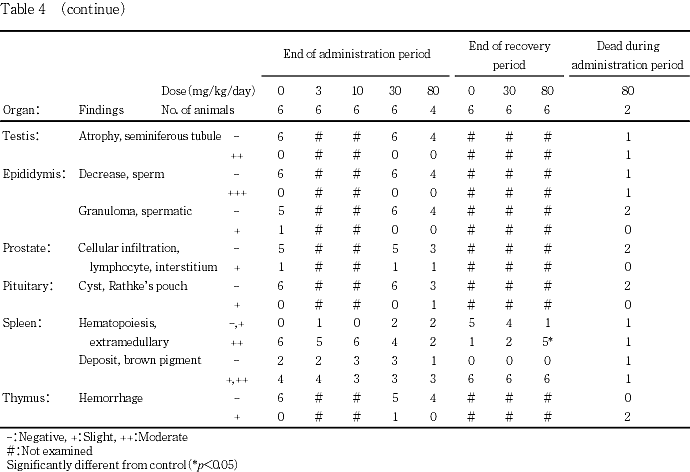
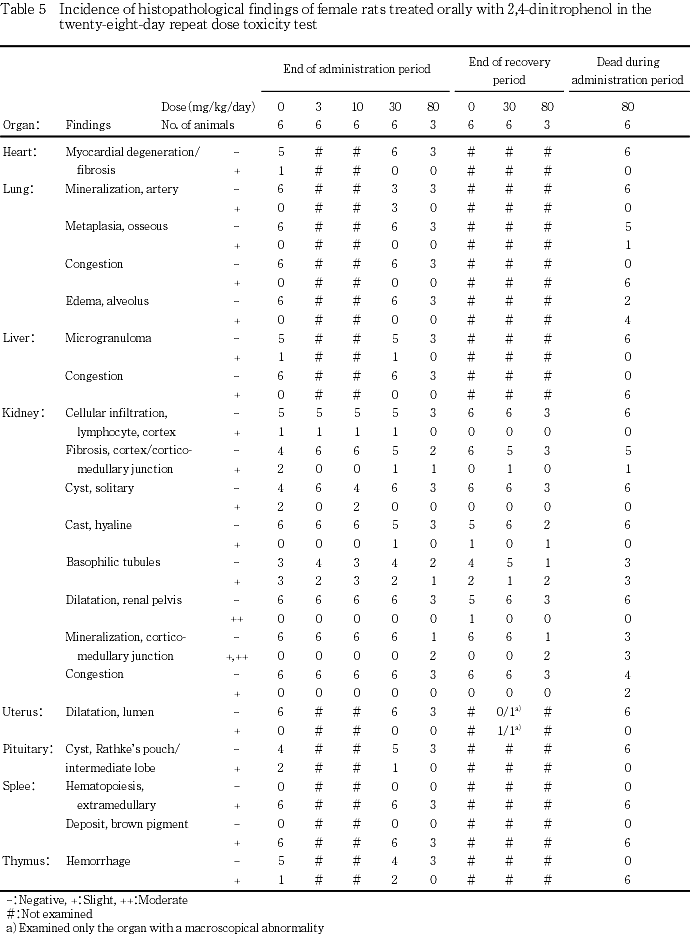
投与期間終了時屠殺動物において,腎臓に皮髄境界部の軽度ないし中等度の鉱質沈着が80 mg/kg群で雄の4匹中3匹および雌の3匹中2匹に認められ,雄の発現率には対照群と比べて有意差が認められた.脾臓においては,髄外造血巣は雄で対照群は6匹の全例が中等度に認められたのに対して,80 mg/kg群は2匹が軽度および他の2匹が中等度で,80 mg/kg群の雄では髄外造血巣の減少による赤脾髄の萎縮傾向が認められた.
投与期間中死亡動物において,腎臓に皮髄境界部の軽度ないし中等度の鉱質沈着が80 mg/kg群で雌の6匹中3匹に認められた.また,剖検で認められた赤色化した肺にはうっ血あるいはうっ血水腫,暗色調化した肝臓ではうっ血,軟化した精巣には精細管萎縮が認められた.
回復期間終了時屠殺動物において,腎臓に皮髄境界部の軽度な鉱質沈着が80 mg/kg群で雄の4匹中2匹および雌の3匹中2匹に認められた.また,脾臓に髄外造血巣の有意な増加が80 mg/kg群で雄に認められた.剖検で被験物質投与とは無関係に認められた雄の精巣上体の結節には精子肉芽腫,肺の赤色点には出血を伴った炎症性細胞浸潤巣,肝臓の横隔膜結節には胆管増生巣および巣状壊死,胸腺の赤色斑には出血が,雌の水腎症には腎盂拡張,子宮腔水腫には内腔拡張が認められた.
以上の変化以外にも,投与期間終了時屠殺動物,投与期間中死亡動物および回復期間終了時屠殺動物の検査した各器官に変化が認められたが,散発的なあるいは用量依存性の認められない所見であった.
一般状態の変化について,30 mg/kg群で雌雄に自発運動の低下および流涎,80 mg/kg群ではさらに雌雄に歩行時の這いずり姿勢,腹臥姿勢,浅速呼吸,眼瞼下垂,下腹部被毛の尿による汚れ,死亡動物で強直性痙攣および死亡直後の硬直が認められた.
ジニトロフェノ−ルは酸化的リン酸化の脱共役作用を有し,生体内の高エネルギーリン酸化合物の貯蔵量を減少させることが知られており,急性中毒では酸化代謝機構,次いで熱産生が刺激され,酸素消費量の増加,体温上昇,呼吸数および心拍数の増加を呈し,循環性あるいは呼吸性ショックにより死に至ると考えられている5).2,4-ジニトロフェノ−ルの急性中毒症状として,ラットでは腹臥姿勢,浅速呼吸,強直性痙攣,振戦,死亡直前直後の四肢硬直など,イヌではさらに心拍数の増加および体温の上昇が報告3)されている.
2,4-ジニトロフェノ−ルの反復投与による血中濃度の推移について,イヌでは毎日の投与後2〜3時間でピ−クに達した後24時間でほぼ消失し,投与の反復による血中濃度の蓄積的増加は認めらないと報告3)されている.今回のラットへの反復投与試験においても,毎日の投与後一過性の急性中毒症状が繰り返し認められ,反復投与による症状の増強は認められなかった.また,死亡の多くは投与1ないし2日に認められ,痙攣を伴った急性中毒死と推察されるものであった.
体重および摂餌量について,80 mg/kg群で雌は投与初期に体重増加の抑制,雄は投与の後半に同様の抑制傾向が認められた.一方,摂餌量は30 mg/kg以上の群で雌雄に増加傾向が認められた.この飼料効率の低下が伺われる変化については,上述の酸化的リン酸化の脱共役作用による酸化的代謝の亢進と関連しているものと推察される.
多血症について,80 mg/kg群で雄にヘモグロビン量,ヘマトクリット値および平均赤血球血色素量の増加が認められたが,この変化についてもジニトロフェノ−ル類の酸素消費量増加作用と関連した変化と考えられる.また,同群の雄に認められた脾臓における髄外造血の低下傾向は,多血症に対する生体の適応反応と判断される.
腎臓に対する影響について,病理組織学検査で80 mg/kg群の雌雄に皮髄境界部における鉱質沈着の発現率の増加が認められ,雄では腎臓相対重量の増加も認められた.腎臓皮髄境界部における鉱質沈着はラットに自然発生的にも認められる変化で,雌の発生率が高く,ホルモンの影響6, 7)や飼料成分の影響8)によるものと考えられている.本試験で認められた鉱質沈着の発現機序は不明であるが,投与初期の死亡動物にも認められ,投与開始後短期間で沈着するものと考えられる.また,尿検査で80 mg/kg群の雄に認められた比重の低下ならびに血液生化学検査で30および80 mg/kg群の雄に認められた塩素の減少も,腎臓に対する影響を示唆する変化と考えられる.
肝臓に対する影響について,80 mg/kg群で雌雄に肝臓の相対重量の増加が認められた.病理組織学検査では肝臓に被験物質の投与に起因する変化は認められなかったが,2,4-ジニトロフェノ−ルは肝臓に対し毒性を有するとの報告9)があり,相対重量の増加は被験物質の投与による影響と判断された.
なお,血液生化学検査で,10 mg/kg以上の群の雌に背景データ内あるいはこれを僅かに越える総ビリルビンの増加が認められたが,溶血性変化や胆汁のうっ滞等これと関連する変化は認められなかった.2,4-ジニトロフェノ−ルの代謝物の1つとして,2-アミノ-4-ニトロフェノールが知られている10).ビリルビンはジアゾ化法で測定しており,アミノ基を有する物質が存在すると試薬(スルファニル酸,亜硝酸ナトリウム)と反応してジアゾ化し,本来のビリルビンに加算されて測定されることがあり,したがって,本試験で認められた総ビリルビンの増加は,ビリルビンの測定に対して代謝物が影響した可能性が高く,毒性とは無関係な変化であると判断された.
また,尿検査で,30 mg/kg以上の群の雄および80 mg/kg群の雌で認められた尿の褐色化については,尿により汚れた被毛が被験物質の色調と類似した黄色を呈したことから,尿中排泄された被験物質あるいはその代謝物の色調と関連した変化と推察される.80 mg/kg群の雄に認められたケトン体の変化については,減少性の変化で毒性学的意義は小さいものと判断される.
さらに,器官重量で80 mg/kg群の雄に脳および精巣の相対重量のみの増加が認められたが,当該器官に病理組織学変化は認められなかったことから,体重増加抑制に伴う変化と判断された.
一方,回復群においては,投与期間中あるいは投与期間終了時の検査で認められた変化のうち,腎臓の病理組織学変化を除いて,いずれも回復あるいは回復傾向が認められた.
腎臓の鉱質沈着について,雌ラットの自然発生初期に卵巣割去すると発生が抑制されるが,発生後に卵巣割去しても1か月後の発生率は卵巣割去前とほとんど差は認められなかったとの報告11)があり,沈着した鉱質が消失するには長期間を要するものと推察される.
なお,血液学検査で,80 mg/kgの回復群の雄に,投与期間終了時に認められた多血症とは逆に貧血所見が認められ,病理組織学検査では脾臓に髄外造血巣の増加が認められた.この貧血所見については多血症の回復期におけるリバウンド現象と考えられ,脾臓の髄外造血巣の増加については貧血に対する生体の適応反応と解釈される.
以上の結果から,2,4-ジニトロフェノールのラットへの28日間反復経口投与により認められた主な毒性影響は,30 mg/kg以上の群の雌雄の一般状態の変化ならびに雄の血清中塩素濃度の減少,80 mg/kg群の雌雄の死亡,雄の多血症,尿比重の低下,腎臓および肝臓の相対重量増加,脾臓および腎臓の病理組織学変化ならびに雌の肝臓の相対重量増加であった.したがって,無影響量は,雌雄とも10 mg/kg/dayと推定された.
| 1) | 化学工業日報社編,“12394の化学商品,”化学工業日報社,東京,1994, p.587. |
| 2) | 竹内康信,“毒性試験講座18−産業化学物質,環境化学物質,”和田攻編, 地人書館,東京,1991, p.142. |
| 3) | J. A. Kaiser, Toxicol. Appl., Pharmacol., 6, 232(1964). |
| 4) | J. E. Gibson, Fd. Cosmet. Toxicol., 11, 31(1973). |
| 5) | R. R. Beard, J. T. Noe, “Patty's Industrial Hygine and Toxicology,” 3, Vol. 2A, eds. by G. D. Clayton and F. E. Clayton, Interscience Publishers, New York, 1981, pp.2426-2427. |
| 6) | C. P. Geary, F. B. Cousins, Nature, 211, 980(1966). |
| 7) | C. P. Geary, F. B. Cousins, Br. J. Exp. Path., 50, 507(1969). |
| 8) | J. C. Woodard, Lab. Invest., 20, 9(1969). |
| 9) | C. Cessi, G. Montaldo, Lo Sperimentale, 116, 27(1966). |
| 10) | M. L. Richardson, S. G. Gangolli, “The Dictionary of Substances and their Effects,” Vol. 4, The royal society of chemisty, Cambridge, 1994, pp.29-31. |
| 11) | 岩田聖,廣内康彦,井上博之,榎本真,Exp. Anim., 35(3), 299(1986). |
| 連絡先 | |||
| 試験責任者: | 山本 譲 | ||
| 試験担当者: | 伊藤義彦,伊藤雅也,加藤史子, 赤木 博,山口真樹子 | ||
| (財)畜産生物科学安全研究所 | |||
| 〒229-1132 神奈川県相模原市橋本台3-7-11 | |||
| Tel 042-762-2775 | Fax 042-762-7979 | ||
| Correspondence | ||||
| Authors: | Yuzuru Yamamoto(Study director) Yoshihiko Ito, Masaya Ito, Satoko Kato, Hiroshi Akagi, Makiko Yamaguchi | |||
| Research Institute for Animal Science in Biochemistry and Toxicology | ||||
| 3-7-11 Hashimotodai Sagamihara-shi, Kanagawa, 229-1132, Japan | ||||
| Tel +81-42-762-2775 | Fax +81-42-762-7979 | |||