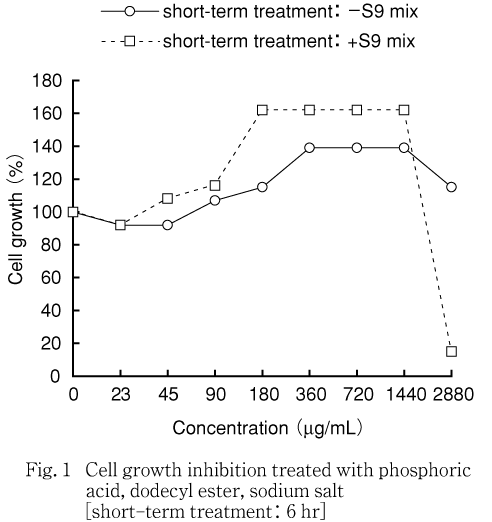
初めに,最高用量を毒性試験ガイドラインに定められた10 mMに相当する2880 μg/mLとして,細胞増殖抑制試験を実施した.被験物質は染色体異常試験に推奨されている全ての溶媒に対して不溶であったため,0.5 %カルボキシメチルセルロースナトリウム水溶液に懸濁して試験を実施した.その結果,短時間処理法では360 μg/mL以上の用量で,連続処理法では180 μg/mL以上の用量で,それぞれ被験物質と推測される物質が細胞密度測定用標本のプレート底面へ固着したため,単層培養細胞密度計(モノセレータ)を用いての細胞密度測定において信頼出来る50 %細胞増殖抑制濃度(概略値)が算出できなかった.しかし,細胞状態の観察においては,これらの用量では細胞毒性が認められたことから,最高用量を固着した物質によって染色体異常観察用標本の作製及び観察が妨げられる可能性があり,かつ細胞毒性が確認された最低濃度と定め,短時間処理法では360 μg/mLを,連続処理法では180 μg/mLを最高用量として,以下公比2で希釈した各4試験用量を設定し染色体異常誘発能を検討した.
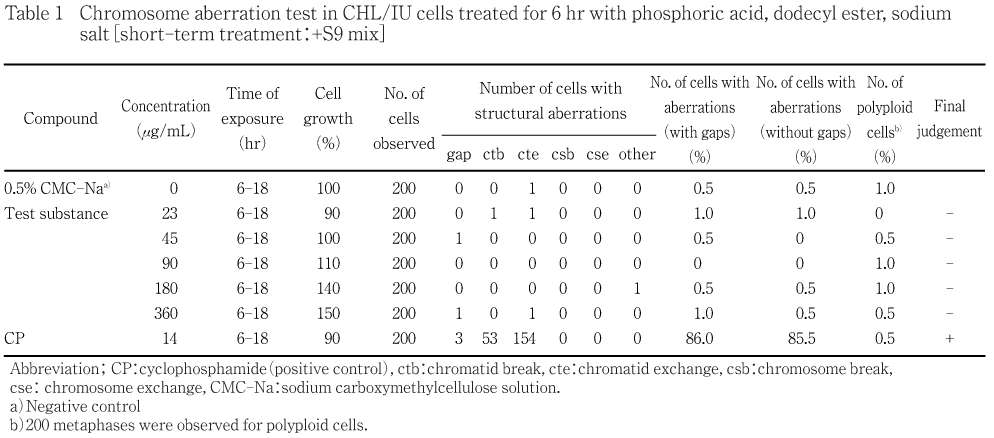
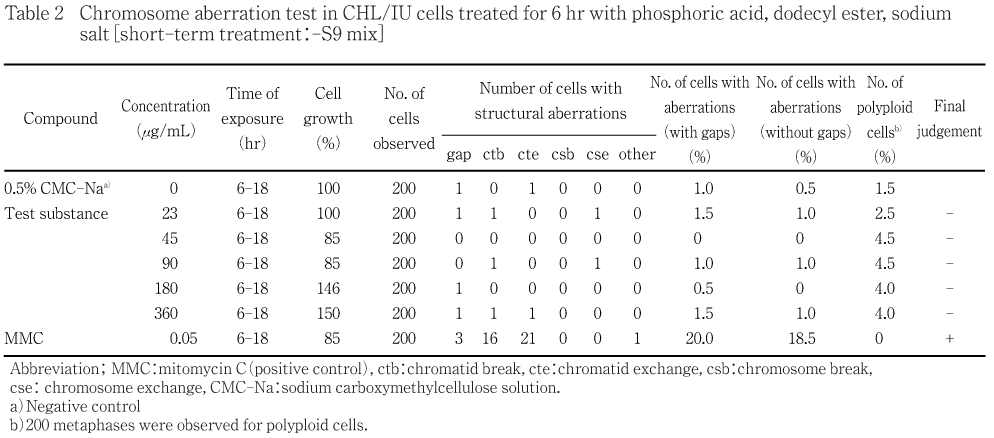
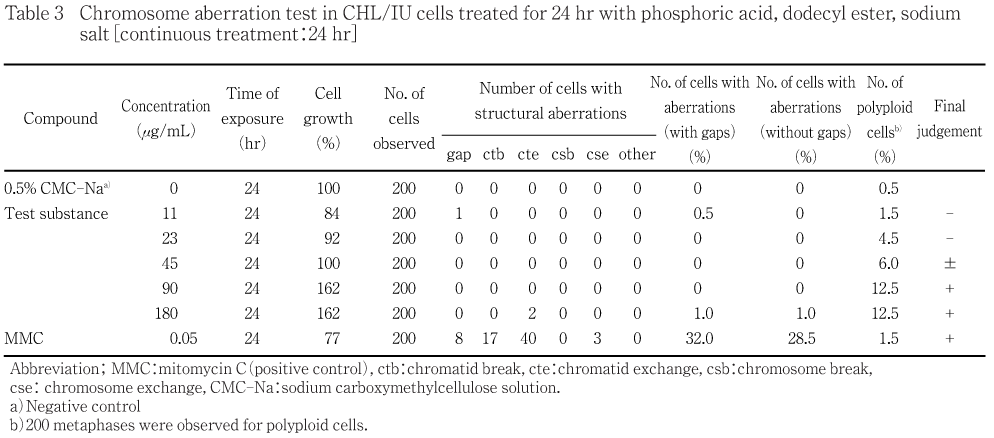
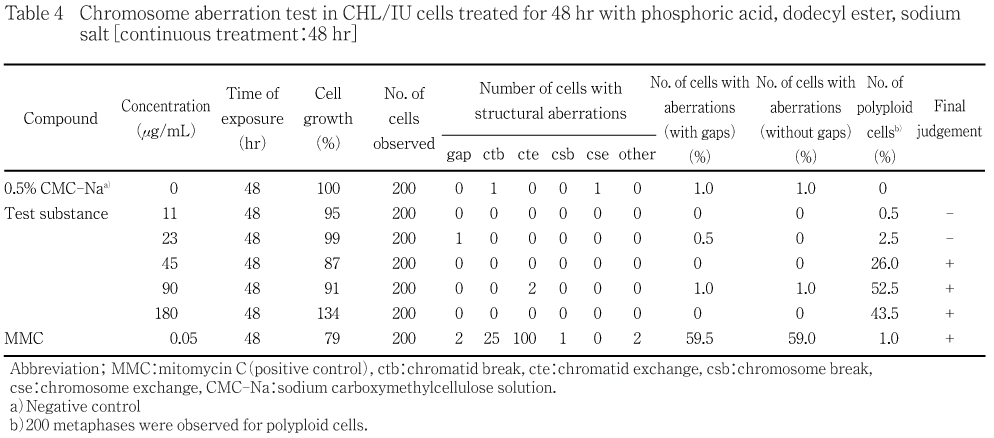
染色体異常試験の結果,短時間処理法の代謝活性化においては構造異常及び数的異常(倍数体)の出現率は増加しなかった.短時間処理法の非代謝活性化においては構造異常の出現率は増加しなかったが,数的異常(倍数体)の出現率にわずかな増加が認められた.これに対して,連続処理法では,24時間処理及び48時間処理ともに構造異常の出現率は増加しなかったが,数的異常(倍数体)の用量依存的な著しい出現率の増加が認められた.なお,観察細胞の20 %に倍数体が認められる用量であるPD20値は24時間処理では1.02 mg/mL,48時間処理では0.03 mg/mLであった.各処理法ともに陰性及び陽性対照における構造異常の出現率は各々陰性及び陽性の判定基準内にあり,さらに試験施設の背景値と同様であった.また,陰性対照群における数的異常(倍数体)の出現率は各々陰性の判定基準内にあり,さらに試験施設の背景値と同様であった.従って試験は適切に実施されたものと考えられる.
以上の結果から,リン酸ドデシルエステルナトリウム塩は,本試験条件下において染色体の構造異常の誘発能を有さないが,数的異常(倍数体)の誘発能を有する(陽性)と判定した.
ヒューマンサイエンス研究資源バンクから入手(2001年12月26日)したチャイニーズ・ハムスターの肺由来線維芽細胞株(CHL/IU細胞)を用いた.なお,試験には細胞増殖抑制試験で23継代目,染色体異常試験で5及び9継代目の細胞を使用した.
培養には,非働化(56℃,30分)した仔牛血清(Invitrogen)を10 vol%添加したEagle's MEM (Life Technologies)を用いた.調製後の培養液の保存は冷蔵とした.
細胞は,炭酸ガス培養装置を用い,CO2濃度5 %,温度37℃の高湿度条件下で培養した.継代培養は3〜4日ごとに行った.試験に際しては2×10^4個の細胞を,培養液5 mLを入れた直径6 cmのプラスチックプレートに播種し,3日目に被験物質を処理した.
フェノバルビタール及び5,6-ベンゾフラボンを7週齢のSprague Dawley系雄ラットに腹腔内投与した肝臓から調製されたS9並びに補酵素をオリエンタル酵母工業から購入し,S9 mixを調製した.S9 mixの組成は松岡らの方法 1)に従いS9の培地への添加量を5 vol%とした.
リン酸ドデシルエステルナトリウム塩(ロット番号: 3724,日光ケミカルズ,東京)は,わずかに特異なにおいがある白色粉末で,室温で密封し保存した.被験物質は試験期間中安定であった.
溶媒は,0.5 %カルボキシメチルセルロースナトリウム水溶液(日本薬局方,丸石製薬)を用いた.被験物質を溶媒で懸濁して原液(28.8 mg/mL)を調製し,ついで順次溶媒で希釈して各濃度の被験液を調製した.被験液は,培養液の10 vol%になるように添加した.
染色体異常試験における被験物質の処理濃度を設定するため,被験物質の細胞増殖に及ぼす影響を調べた.被験物質の細胞増殖抑制作用は,単層培養細胞密度計(モノセレータ,オリンパス光学工業)を用いて細胞密度を測定し,被験物質処理群の陰性(媒体)対照群に対する細胞密度の比をもって指標とした.
その結果,短時間処理法では360 μg/mL以上の用量で,連続処理法では180 μg/mL以上の用量で,それぞれ被験物質と推測される物質が細胞密度測定用標本のプレート底面へ固着したため,単層培養細胞密度計(モノセレータ)を用いての細胞密度測定において信頼出来る50 %細胞増殖抑制濃度(概略値)が算出できなかった.しかし,細胞状態の観察では,これらの用量で細胞毒性が認められたため,固着した物質によって染色体異常観察用標本の作製及び観察が妨げられる可能性があり,かつ細胞毒性が確認された最低濃度である短時間処理法では360 μg/mLを,連続処理法では180 μg/mLを最高用量とし,以下公比2で希釈した各4試験用量を設定し染色体異常誘発能を検討した(Fig. 1, 2).

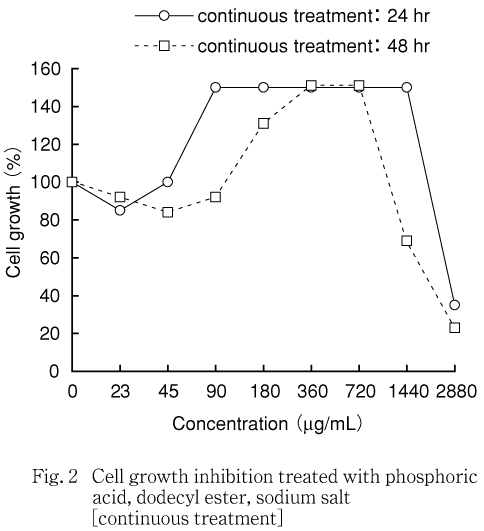
細胞増殖抑制試験で得られた50 %細胞増殖抑制濃度をもとに,染色体異常試験では短時間処理法においては360 μg/mLを,連続処理法においては180 μg/mLを最高濃度とし,以下公比2で希釈した計5濃度並びに陰性(媒体)対照群を設定した.なお,陽性対照として+S9 mix処理ではシクロフォスファミド(CP,和光純薬工業,14 μg/mL),-S9 mix処理ではマイトマイシンC(MMC,協和醗酵工業,0.05 μg/mL)を用いた.
濃度当たり4枚のプレートに処理し,2枚を染色体標本作製用,2枚を細胞増殖率測定用とした.
培養終了の2時間前に,最終濃度が0.2 μg/mLとなるようコルセミドを加えた.以下,染色体標本は空気乾燥法によって作製した.スライド標本は各プレートにつき2枚作製し,2 vol%ギムザ液で15分間染色した.
各用量当たり200個(プレート当たり100個)の分裂中期像についてギャップ(gap),染色分体型切断(ctb),染色分体型交換(cte),染色体型切断(csb),染色体型交換(cse)及びその他の異常など構造異常の種類並びに異常を持つ細胞の数を記録した.同時に倍数性細胞の数も記録した.
客観的な観察を行うため,スライド標本をコード化した状態で分析した.
染色体構造異常を有する細胞の出現率は,ギャップを含む場合と含まない場合について集計し,ギャップを含まない場合で判定した.
判定は石館らの基準 2)に従い,染色体異常を有する細胞の出現頻度が5 %未満を陰性(-),5 %以上10 %未満を疑陽性(±),10 %以上を陽性(+)とした.最終的には異常細胞の出現に用量依存性又は再現性が認められた場合を陽性と判定した.
短時間処理法の結果をTable 1及び2に,連続処理法の結果をTable 3及び4に示した.
短時間処理法の代謝活性化では構造異常及び数的異常(倍数体)ともに出現率の増加は認められなかった.非代謝活性化では構造異常の出現率の増加は認められなかったが,数的異常(倍数体)のわずかな増加が認められた.また,連続処理法では,24時間処理及び48時間処理ともに構造異常の出現率の増加は認められなかったが, 数的異常(倍数体)の出現率に用量依存性を伴う著しい増加が認められた.出現した倍数体には8倍体が多く認められ,さらに細粉化(pulverization)又はpremature chromosome condensationを伴う倍数体が出現した.倍数体の増加を生じた機序については不明であるが,細粉化(pulverization)やpremature chromosome condensationは細胞融合,細胞質分裂阻害,紡錘糸阻害,染色体橋,染色体断片などによって生じた多核細胞や小核を含む細胞が非同調的に細胞分裂に入った時に内的要因によって生じる事実が明らかにされている3)こと,核内倍加体の出現が全く認められなかったことから,本被験物質は細胞融合や細胞質分裂に及ぼす影響によって倍数体を生じたものと推察される.
リン酸ドデシルエステルナトリウム塩の類縁体であるSulfuric acid, monododecyl ester, sodium saltはAspergillus ndulantsにおいてmitotic aneuploidを誘発しないこと4),マウスリンフォーマアッセイでは非代謝活性化系において陰性であること5)が報告されている.
一方,陰性対照における染色体の構造異常を有する細胞の出現率は,いずれの処理法においても5 %未満であった.また,陽性対照物質のCPあるいはMMCを処理した細胞では,染色体構造異常の顕著な誘発が認められた.更に,2枚のシャーレ間における染色体異常細胞の出現率に著しい差はなく,培養条件などの試験環境の異常も認められなかった.これらのことから,試験は適切に実施されたものと考えられた.
以上の結果から,リン酸ドデシルエステルナトリウム塩は本試験条件下において染色体の構造異常の誘発能を有さないが,数的異常(倍数体)の誘発能を有する(陽性)と判定した.
| 1) | Matsuoka A et al.: Chromosomal aberration tests on 29 chemicals combined with S9 mix in vitro. Mutation Res, 66: 277-290(1979). |
| 2) | 石館基(監修):「染色体異常試験データ集」エル・アイ・シー,東京(1987) pp.19-24. |
| 3) | 日本環境変異原学会・哺乳動物試験分科会編:「化学物質による染色体異常アトラス」朝倉書店,東京(1988) pp.29-31. |
| 4) | Assinder SJ, Upshall A: Paramorphogenic and genotoxic activity of Triton X-100 and sodium dodecyl sulphate in Aspergillus nidulans. Mutation Res, 142: 179-181(1985). |
| 5) | McGregor DB et al.: Responses of the L5178Y tk+/tk- mouse lymphoma cell forward mutation assay: III. 72 coded chemicals. Environ Mol Mutagen, 12: 85-154(1988). |
| 連絡先 | |||
| 試験責任者: | 園 明 | ||
| 試験担当者: | 高部道仁,藤原 聖 | ||
| (株)ボゾリサーチセンター | |||
| 〒412-0039 静岡県御殿場市かまど1284 | |||
| Tel & Fax 0550-82-9922 | |||
| Correspondence | |||
| Authors: | Akira Sono(Study Director) Michihito Takabe, Sho Fujiwara, |
||
| Bozo Research Center Inc. | |||
| 1284 Kamado, Gotemba-shi, Shizuoka, 412-0039, Japan | |||
| Tel & Fax +81-550-82-9922 | |||