
死亡は,1600 mg/kg以上の群の雄および1280 mg/kg以上の群の雌で3日目から13日目にみられた.LD50値(95 %信頼限界)は,雄で1565 mg/kg(1406〜1742 mg/kg),雌で1496 mg/kg(1256〜1782 mg/kg)であった.一般状態の観察では,軟便が投与日(1日目)からすべての被験物質投与群の雌雄にみられ,3日目からは自発運動の低下および緩徐呼吸が1600 mg/kg以上の群の雄および1280 mg/kg以上の群の雌にみられた.更に,死亡例では肛門周囲の汚れ,尿による下腹部の汚れ,腹臥位,チアノーゼ,皮膚蒼白,眼球蒼白,体温低下または痩削がみられた.生存例では,軟便は4日目,緩徐呼吸は8日目,自発運動の低下は10日目までに回復した.体重では,すべての被験物質投与群の雌雄で増加抑制または減少がみられたが,6ないし8日目からは順調な増加がみられた.病理学検査において,死亡例では,肺に肉眼的に暗赤色化および収縮不全が,組織学的にはうっ血および肺胞内水腫がみられ,肉眼的には気管内の泡沫状液体の貯留および胸水の貯留もみられた.腎臓では肉眼的に褪色が,組織学的には急性尿細管壊死,尿細管への鉱質沈着および尿細管の好塩基性化がみられた.胃では肉眼的に前胃粘膜の白色点および腺胃粘膜の白色点が,組織学的には前胃粘膜の潰瘍および腺胃粘膜のびらんがみられ,肉眼的には小腸ないし大腸に黒褐色内容物の貯留もみられた.胸腺では肉眼的に萎縮が,組織学的には萎縮および鉱質沈着がみられた.脾臓では肉眼的および組織学的に萎縮がみられた.一方,生存例では,腎臓で肉眼的に皮髄境界部の灰白色化が,組織学的には尿細管の好塩基性化および拡張,間質の線維化ならびに当該部位へのリンパ球性細胞浸潤がみられた.前胃では肉眼的に粘膜の白色点が,組織学的には粘膜に扁平上皮の過形成がみられた.胸腺では肉眼的および組織学的に萎縮がみられた.
投与経路は経口とし,16〜17時間絶食させた動物に胃管を用いて1回強制投与した.投与容量は10 mL/kgとし,各動物の投与液量は投与日の体重を基に算出した.
1280 mg/kg群の雌2例,1600 mg/kg群の雄3例および雌2例ならびに2000 mg/kg群の雄5例および雌4例が3日目から13日目に死亡した.LD50値(95 %信頼限界)は,雄で1565 mg/kg(1406〜1742 mg/kg),雌で1496 mg/kg(1256〜1782 mg/kg)であった.

生存例では,腎臓の皮髄境界部の灰白色化が1280 mg/kgおよび1600 mg/kg群の雌各1例にみられ,前胃粘膜の白色点が1024 mg/kg群の雄1例,1280 mg/kg群の雄2例,1600 mg/kg群の雄1例および2000 mg/kg群の雌1例にみられた.また,1600 mg/kg群の雌1例で胸腺の萎縮,1600 mg/kg群の雄1例で両側性の精巣および精巣上体の萎縮がみられた.
生存例では,腎臓に剖検での皮髄境界部の灰白色化に対応して皮髄境界部を主体とした尿細管の好塩基性化および拡張,間質の線維化ならびに当該部へのリンパ球性細胞浸潤がみられ,剖検での前胃粘膜の白色点に対応して前胃粘膜の扁平上皮の過形成がみられた.胸腺では肉眼的および組織学的に萎縮がみられた.また,精巣および精巣上体では剖検での萎縮に対応して精巣の萎縮および精巣上体管腔内の生殖上皮細胞の残屑がみられた.
死亡は,1600 mg/kg以上の群の雄および1280 mg/kg以上の群の雌で3日目から13日目までにみられた.LD50値(95 %信頼限界)は,雄で1565 mg/kg(1406〜1742 mg/kg),雌で1496 mg/kg(1256〜1782 mg/kg)であった.
死亡例では,症状として軟便,自発運動の低下,緩徐呼吸,チアノーゼ,皮膚蒼白,眼球蒼白,体温低下および痩削などがみられた.また,剖検では肺に暗赤色化および収縮不全,腎臓に褪色ならびに胃に腺胃粘膜の白色点などがみられ,病理組織学検査では肺にうっ血および肺胞内水腫,腎臓に急性尿細管壊死,胃に腺胃粘膜のびらんなどがみられたことから,本被験物質は呼吸器,腎臓および消化管に影響を及ぼすことが考えられた.同様の結果は,Damskeらによって実施された本被験物質のラットにおける単回経口毒性試験1)でもみられている.そのほか,胸腺および脾臓では萎縮がみられたが,これらの所見を示した例では3ないし13日目の死亡に至るまでの間,前述した症状がほぼ継続してみられていることから,衰弱に伴った変化であろうと思われた.
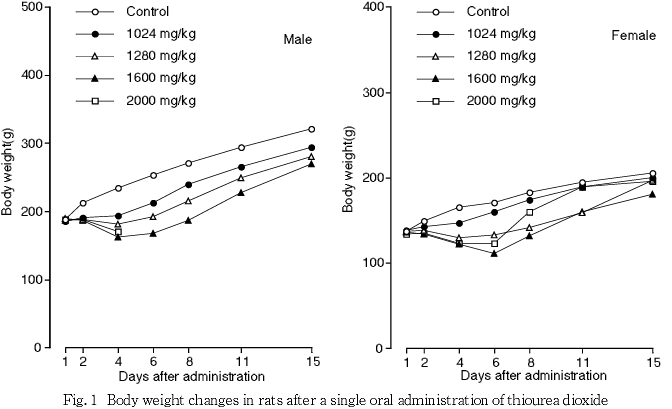
生存例では,症状として軟便がすべての被験物質投与群で,緩徐呼吸および自発運動の低下が1600 mg/kg以上の群でみられたが,これらの症状は10日目までにすべて回復した.体重では,すべての被験物質投与群で増加抑制または減少がみられたが,8日目からは順調な増加がみられた.病理学検査では,1280 mg/kg以上の群で肉眼的に腎臓の皮髄境界部の灰白色化がみられ,組織学的には尿細管の好塩基性化および間質の線維化などがみられた.また,1024 mg/kg以上の群では肉眼的に前胃粘膜の白色点がみられ,組織学的には前胃粘膜の扁平上皮の過形成がみられた.これらの変化は,前述の死亡例にみられた腎臓および消化管に対する障害の修復像と考えられた.また,1600 mg/kg群の1例では胸腺の萎縮がみられたが,死亡例と同様に衰弱に伴った変化と考えられた.そのほか,生存例では1600 mg/kg群の1例で精巣および精巣上体に萎縮がみられた.同様な変化は2000 mg/kg群ではみられておらず,SD系ラットでは時折みられる変化であることから,自然発生性のものと考えられた.
| 1) | D. R. Damske, F. J. Mecler, R. P. Beliles., Litton Bionetics Inc. LBI Project No.21048, 1979. |
| 連絡先 | |||
| 試験責任者: | 緒方英博 | ||
| 試験担当者: | 木村栄介,浜村政夫,幸 邦憲,和泉宏幸,鍬先恵美子 | ||
| (株)パナファーム・ラボラトリーズ 安全性研究所 | |||
| 〒869-0425 熊本県宇土市栗崎町1285 | |||
| Tel 0964-23-5111 | Fax 0964-23-2282 | ||
| Correspondence | ||||
| Authors: | Hidehiro Ogata(Study director) Eisuke Kimura, Masao Hamamura, Kuninori Yuki, Hiroyuki Izumi, Emiko Kuwasaki | |||
| Safety Assessment Laboratory, Panapharm Laboratories Co., Ltd. | ||||
| 1285 Kurisaki-machi, Uto-shi, Kumamoto, 869-0425, Japan | ||||
| Tel +81-964-23-5111 | Fax +81-964-23-2282 | |||