3a,4,7,7a-テトラヒドロ-1H-インデンのラットを用いる
反復経口投与毒性・生殖発生毒性併合試験
Combined Repeat Dose and Reproductive/Developmental Toxicity Screening Test of
3a,4,7,7a-Tetrahydro-1H-indene by Oral Administration in Rats
要約
OECD既存化学物質の安全性点検事業の一環として,3a,4,7,7a-テトラヒドロ-1H-インデン(CAS No. 3048-65-5)の67,200および600 mg/kgを雄ラットに対しては交配前,交配期間および交配後の計46日間,雌ラットに対しては交配前,交配および妊娠期間,ならびに哺育3日までの期間経口投与し,雌雄動物への反復投与による影響,雌雄動物の生殖および次世代の発生に及ぼす影響について反復投与毒性・生殖発生毒性併合試験を実施した.
雌雄動物への反復投与により,体重増加抑制が雌雄の200および600 mg/kg群で認められた.血液学検査では,赤血球数,ヘマトクリット値および血色素量の軽度の減少が雄の600 mg/kg群で認められた.器官重量では,肝臓重量の増加ないし増加傾向ならびに体重重量比の増加が雄の600 mg/kg群および雌の200 mg/kg以上の群で認められ,さらに左右の腎臓重量の増加ないし増加傾向ならびに体重重量比の増加が雄の67 mg/kg以上の群および雌の600 mg/kg群で認められた.また,病理組織学検査では,肝臓に軽度の小葉中心性肝細胞肥大が雌雄の600 mg/kg群で,腎臓において近位尿細管上皮の硝子滴沈着および好酸性小体の発現数の増加が雄の67 mg/kg以上の群に,さらに軽度の尿細管上皮の再生が雄の200および 600 mg/kg群で認められた.
以上より,雄の67 mg/kg以上の群の腎臓の重量および体重重量比の増加(増加傾向を含む),雌の200 mg/kg以上の群の体重増加抑制ならびに肝臓の重量および体重重量比の増加(増加傾向を含む)から,本試験における3a,4,7,7a-テトラヒドロ-1H-インデンの反復投与による無影響量は雄で67 mg/kg/day未満,雌で67 mg/kg/dayと判断した.
雌雄動物の生殖能に対しては,雄動物での影響はみられなかったが,雌の母動物の剖検および分娩観察で,妊娠期間の延長,ならびに妊娠黄体数および着床数の減少が600 mg/kg群で認められた.また,雌雄動物の次世代に対する影響として出産児数および出産生児数の減少が600 mg/kg群で認められたことから,本試験における3a,4,7,7a-テトラヒドロ-1H-インデンの雄動物の生殖に対する無影響量は600 mg/kg/day,雌動物および次世代に対する無影響量は200 mg/kg/dayと判断した.
方法
1.被験物質
被験物質は3a,4,7,7a-テトラヒドロ-1H-インデン(CAS No.3048-65-5)で,不快臭のある無色透明液体であり,遮光気密容器に入れ,冷蔵庫内に保存した.本試験では,日本石油化学(株)製造のロット番号D1G02(純度:99.0%)を使用した.なお,被験物質は投与期間中安定であったことが製造業者の分析により確認された.
投与には,被験物質を1.34,4および 12 w/v% の濃度となるようにオリーブ油(日本薬局方,ヤクハン製薬(株))に溶解して調製した.調製頻度は7日間に1回以上とし,投与に用いるまで遮光気密容器に入れ,冷蔵庫内に保存した.各濃度の調製液は規定の濃度であり,かつ均一であることが(財)日本食品分析センターにより確認された.
2.試験動物および飼育条件
生後8週齢のCrj:CD(SD)系のSPFラットを日本チャールス・リバー(株)から受け入れ,15日間の検疫・馴化飼育を行い,順調な発育を示した動物を試験に用いた.雌については10日間の性周期検査を併せて行い,性周期に異常の認められない動物を用いた.
動物は,温度23±3℃,湿度55±10%,換気回数10〜15回/時間および照明時間12時間に設定されたバリアシステムの飼育室において,ブラケット式金属製金網床ケージを用いて飼育した.雌は,妊娠17日から金網床のかわりに実験動物用床敷(ホワイトフレーク,日本チャ-ルス・リバー(株))を敷いたステンレス製受皿を使用した.ケージ当たりの収容匹数は,群分け前は2匹以内,群分け後は1匹,交配中は雌雄各1匹,妊娠期間中は1母動物,哺育期間中は1腹とした.飼料は固型飼料(CRF-1,オリエンタル酵母工業(株))を金属製給餌器を用いて,飲料水は水道水(札幌市水道水)を自動給水装置あるいは給水器を用いて,それぞれ自由に摂取させた.
3.投与量の設定,試験群の構成および群分け
試験群は,3a,4,7,7a-テトラヒドロ-1H-インデンの100,300および1000 mg/kgを雌雄各5例に14日間反復経口投与した用量設定試験の結果を参考に設定した.すなわち,1000 mg/kg群では衰弱による屠殺例が雄5例中1例にみられたほか,同群の雌雄でよろめき歩行,呼吸緩除,自発運動の減少,体重増加抑制,摂餌量の低値,肝臓の重量および体重重量比の増加,肝臓の暗褐色化,前胃粘膜の肥厚が認められ,300 mg/kg群の雄では肝臓の重量および体重重量比の増加が認められた.本試験では投与期間が用量設定試験の約3倍になることから,高用量は明らかな毒性徴候がみられる用量として,1000 mg/kg群と300 mg/kg群のほぼ等比中項である600 mg/kgとし,以下公比3で200および67 mg/kgを設定した.さらに,媒体であるオリーブ油を投与する対照群を加えて計4群とし,動物数は1群当たり雌雄各12匹を用いた.群分けは,投与開始前日に投与開始前々日の体重値をもとに各群の体重が均一になるように体重別層化無作為抽出法を用いて行った.
4.投与方法
投与経路は経口投与とし,胃ゾンデを用いて強制的に胃内に行った.
投与期間は,雄については交配前14日間,交配期間および交配後の計46日間,雌については交配前14日間および交尾までの交配期間,さらに交尾例は妊娠期間および哺育3日までの期間とした.
投与容量は,体重1 kg当たり5 mlとして投与日に最も近い日に測定した体重に基づいて算出し,体重測定当日の投与容量はその日の体重に基づいて算出した.投与は10週齢から開始し,投与開始時の平均体重(体重範囲)は雄で416.4 g(392〜447g),雌で240.0 g(222〜270 g)であった.
5.観察,測定および検査項目
(1) 一般状態観察
雌雄全例について,試験期間中1日1回以上の頻度で,視診および触診により行動,外観などを観察した.
(2) 体重測定
体重は投与1日(投与前),投与2,5,7,10および14日,その後は雄については7日毎(投与終了日)および剖検日に,雌については妊娠0,1,3,5,7,10,14,17および20日,哺育0,1および4日に,また交配期間中(雄と同居中)は相手雄の測定日と同じ日に電子天秤を用いて体重を測定した.また,雄については投与1から46日の,雌については投与1日から14日,妊娠0から20日および哺育0日から4日の体重増加量および体重増加率を算出した.
(3) 摂餌量測定
摂餌量は,雄については交配期間および剖検日を除き,雌については妊娠0日および哺育0日を除き体重測定日と同じ日(投与終了日を含む)に,電子天秤を用いて測定した.測定前日に適当量の飼料をケージ毎にセットし,翌日(測定日)に残量を測定して1匹当たりの1日分の摂餌量を算出した.
(4) 尿検査
投与期間の最終週(投与43〜44日)に雄の各群6例について,ラット用代謝ケージ(KN-646 B-1型,夏目製作所)に収容して非絶食下で採尿を行った.約3時間の蓄尿の一部を用いて,pH,蛋白,糖,ケトン体,ウロビリノーゲン,ビリルビン,潜血反応(以上,試験紙マルチスティックス;バイエル・三共)および沈渣(鏡検)を検査し,21時間蓄尿を用いて比重(アタゴ製屈折計ユリコン)および尿量(容量)を測定した.また,採尿中の飲水量測定も併せて実施した.
(5) 血液学検査
投与46日の翌日の剖検時に約16時間絶食した雄の全例について,エーテル麻酔下で大腿静脈から採血した.EDTA・2Kで処理した血液を用いて,赤血球数,平均赤血球容積,血小板数,白血球数(以上,電気抵抗法;コールターカウンター T660型),血色素量(シアンメトヘモグロビン法;コールターカウンター T660型),ヘマトクリット値(赤血球数,平均赤血球容積より算出),平均赤血球ヘモグロビン量(赤血球数,血色素量より算出),平均赤血球ヘモグロビン濃度(ヘマトクリット値,血色素量より算出),網赤血球率(Brecher法)および白血球百分比(メイ・ギムザ染色法)を鏡検により測定した.また,大腿静脈から採取した無処理血液を用いて凝固時間(流体粘度変化による空気圧測定法;グライナー社製マイクロコアグロメーター)を測定した.さらに,腹部大動脈から採取した血液をクエン酸ナトリウムで処理した後,3000 r.p.m.で10分間遠心し,得られた血漿を用いてプロトロンビン時間(トロンボプラスチン法)および活性化部分トロンボプラスチン時間(エラジン酸法)(以上,AMELUNG KC-10A,バクスターKK)を測定した.
(6) 血液生化学検査
投与46日の翌日の剖検時に約16時間絶食した雄の全例について,血液学検査のための採血後,腹部大動脈から採取した血液を3000 r.p.m.で10分間遠心分離し,得られた血清を用いて,GOT,GPT(以上,IFCC法),γ-GTP(包接L-γ-グルタミル-ρ-ニトロアニリド基質法),コリンエステラーゼ(ヨウ化ブチリルチオコリン基質法),血糖(ヘキソキナーゼ法),総コレステロール(酵素法),トリグリセリド(遊離グリセロール消去法),リン脂質(酵素法),総ビリルビン(アゾビリルビン法),尿素窒素(ウレアーゼ・インドフェノール法),クレアチニン(ヤッフェ法),カルシウム(OCPC法),無機リン(フィスケ・サバロー法),総蛋白(ビウレット法)およびアルブミン(BCG法)(以上,日立7150形自動分析装置),ナトリウムおよびカリウム(以上,炎光法;コーニング 480型炎光光度計),クロール(電量滴定法;平沼 CL-6M型クロライドカウンター),A/G比(総蛋白,アルブミンより算出)および蛋白分画(セルロースアセテート膜電気泳動法)を測定した.
(7) 剖検および器官重量測定
雄については投与46日の翌日にエーテル麻酔下で採血後放血致死させ,全身の器官および組織を肉眼的に観察した.雌は全哺育児死亡例は発見後直ちに,哺育3日まで生存児のみられた例は哺育4日に,妊娠25日まで分娩の認められない例は妊娠26日に,エーテル麻酔下で放血致死させ,全身の器官および組織を肉眼的に観察し,子宮の着床痕および卵巣の妊娠黄体を計数した.さらに,雌雄の全例について肝臓,腎臓(左右),胸腺,副腎(左右),精巣,精巣上体(左右)および卵巣の重量を電子天秤を用いて測定するとともに,器官体重重量比を算出した.
(8) 病理組織学検査
雌雄の全例について,肝臓,腎臓,脾臓,心臓,肺,脳,下垂体,胸腺,副腎,甲状腺,胃(前胃・腺胃),十二指腸,空腸,回腸,盲腸,結腸,直腸,前立腺および卵巣を10%中性緩衝ホルマリン液,精巣および精巣上体をブアン液で固定後,パラフィン切片を作製し,ヘマトキシリン・エオジン染色標本ならびに必要に応じて特殊染色(PAS染色,PTAH染色)標本を作製して病理組織検査を行った.
(9) 生殖能検査
雌全例について,投与開始日の10日前から交尾までの連日,ギムザ染色による腟垢塗抹標本を作製し,光学顕微鏡下で性周期段階(発情前期,発情期前期,発情期後期,発情後期および発情休止期)の判定を行い,性周期の異常の有無を検索した.投与14日の雌雄について,同試験群内で夕方から1対1(無作為組合わせ)で14日間を限度として同居させ,雌の腟垢中に精子が確認された日を妊娠0日とした.妊娠の成立は雌の子宮に着床痕が確認された場合とし,交尾率〔(交尾動物数/同居動物数)×100〕および受胎率〔(受胎動物数/交尾動物数)×100〕を算出した.
(10) 分娩および母性行動観察
交尾した雌全例について,妊娠21日から分娩終了日まで分娩状態を観察し,午前9時に分娩が終了していた動物を当該日分娩とし,その日を哺育0日とした.分娩終了が確認された母動物について母性行動,総出産児数,生存児数および死亡児数,出産児の性別および外表を観察した.また,妊娠期間〔妊娠0日から哺育0日までの日数〕,出産率〔(生児出産雌数/妊娠雌数)×100〕,分娩率〔(総出産児数/着床痕数)×100〕,出生率〔(出産生児数/総出産児数)×100〕,哺育4日時哺育率〔(哺育4日時に哺育児の認められる雌動物数/正常に分娩した雌動物数)×100〕および性比〔雄生児数/雌生児数〕を算出した.また,剖検時の計測結果から着床率〔(着床痕数/妊娠黄体数)× 100〕を算出した.
(11) 新生児の一般状態観察および生存性
全例について,哺育0日から哺育4日まで1日1回生存および死亡を確認し,一般状態および外表について観察した.観察結果から新生児の哺育4日の生存率〔(哺育4日生存児数/出産生児数)×100〕を1腹を単位として算出した.なお,喰殺を受け死亡あるいは不明例となった新生児は死亡例として扱った.
(12) 新生児の体重測定
測定対象となる全例について,哺育0,1および4日に電子天秤を用いて測定し,体重値は1腹毎に雌雄別に1匹あたりの平均値で示した.得られた測定値から体重増加量(哺育4日体重-哺育0日体重)および体重増加率〔(体重増加量/哺育0日体重)×100〕を算出した.
(13) 新生児の剖検
死亡例は直ちに剖検し,その他の例については哺育4日に二酸化炭素吸入法を用いて安楽致死させた後,体外表(口腔内を含む)および全身の器官および組織を肉眼的に観察した.死亡例および異常所見部位の認められた例については,whole bodyを10%中性緩衝ホルマリン液で固定し,保存した.
6.統計解析
性周期,交尾率,受胎率,出産率および哺育率,ならびに病理組織学検査結果のうち1段階の陽性グレードがみられた所見については,多試料χ^2-検定を行い,有意な場合,2試料χ^2-検定をおこなった.また,これらの検定に不適合な場合はFisherの直接確率検定法を用いた.その他の項目ならびに病理組織学検査結果のうち2段階以上の陽性グレードがみられた所見については,Bartlettの等分散検定後,一元配置分散分析法あるいはKruskal-Wallis法により解析し,有意な場合,Dunnett の検定法あるいはMann-WhitneyのU-検定法により,対照群と3a,4,7,7a-テトラヒドロ-1H-インデン各投与群との比較を行った.対照群との検定に際しては,有意水準を5および1%とした.
結果
1.反復投与毒性
(1) 一般状態観察
雄では,流涎が600 mg/kg群の10例で投与15日以降,投与46日までのほぼ毎日,投与直後あるいは投与前から投与後3時間までの間に観察された.600 mg/kg群の他の1例では投与24日にのみ流涎が認められたが,残り1例では流涎は認められなかった.
雌においては,妊娠前投与期間で流涎が600 mg/kg群の7例で投与15日以降,投与前ないし投与直後より1時間程度の間に認められた.妊娠期間では600 mg/kg群の11例で妊娠1日以降,妊娠期間のほぼ毎日,投与前ないし投与直後より2時間程度の間に断続的に認められた.哺育期間では哺育0日より3日の間に,600 mg/kg群の8例で投与直後より1時間程度の間に散発的に認められた.
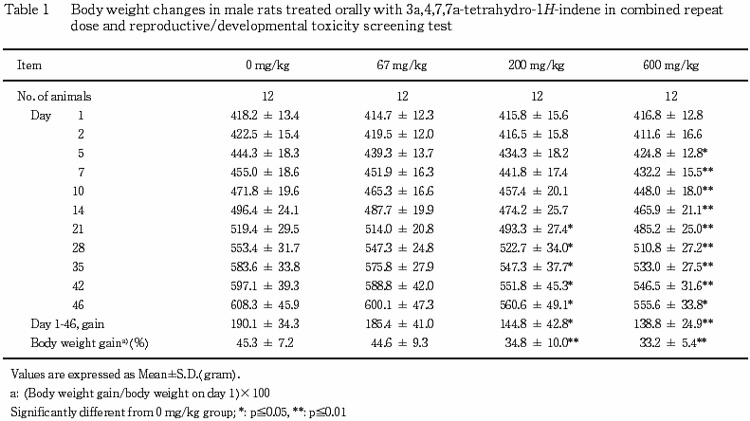
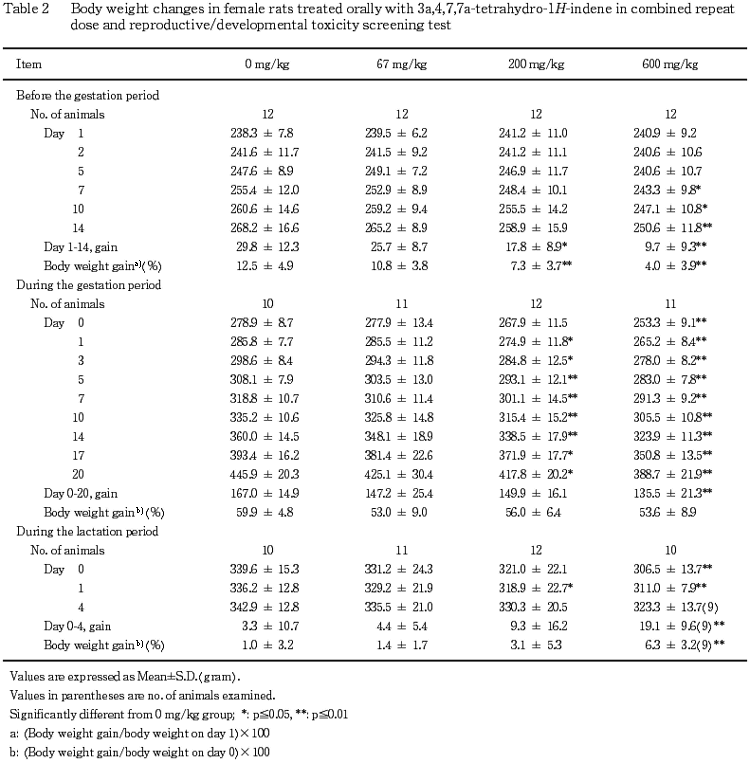
(2) 体重推移(Table 1,2)
雄では,体重の低値が200 mg/kg群の投与21〜46日,600 mg/kg群の投与5〜46日に認められ,これらの群では体重増加量および体重増加率の低値も認められた.
雌の妊娠前投与期間では,体重の低値が600 mg/kg群で投与7日以降にみられ,体重増加量および体重増加率の低値も200および 600 mg/kg群で認められた.妊娠期間でも,体重の低値が200 mg/kg群で妊娠1〜20日に,600 mg/kg群で妊娠0〜20日にみられ,600 mg/kg群では体重増加量の低値も認められた.哺育期間では,体重の低値が200 mg/kg群で哺育1日に,600 mg/kg群で哺育0および1日にみられたが,哺育期間の体重増加量および体重増加率は対照群を上回り,600 mg/kg群ではいずれも統計学的に有意な高値を示した.
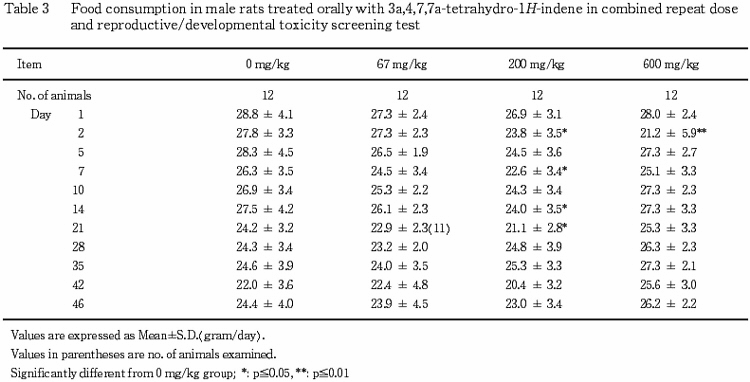
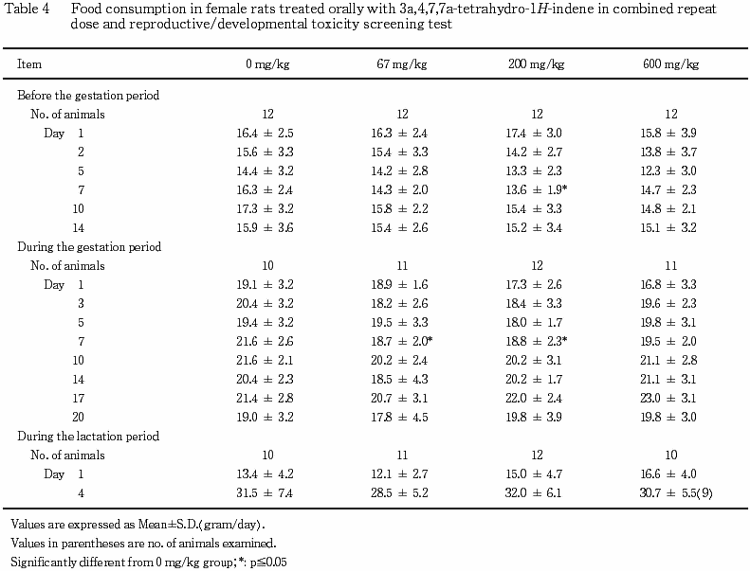
(3) 摂餌量(Table 3,4)
摂餌量の低値が雄の200 mg/kg群の投与2,7,14および21日,ならびに600 mg/kg群の投与2日に認められた.
雌においては,妊娠前投与期間で200 mg/kg群の投与7日,妊娠期間では67および200mg/kg群の妊娠7日に低値が認められた.哺育期間に異常は認められなかった.
(4) 尿検査
いずれの検査項目にも対照群と比較して雄に異常は認められなかった.
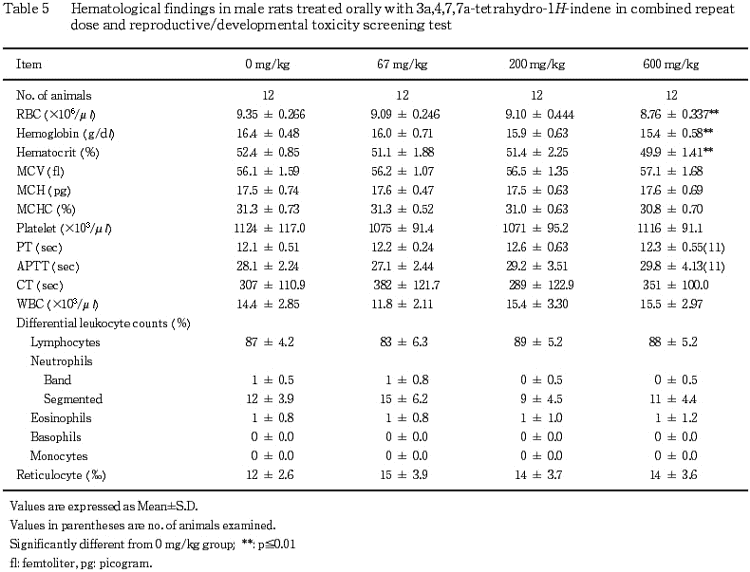
(5) 血液学検査(Table 5)
赤血球数,ヘマトクリット値および血色素量の軽度の減少が雄の600 mg/kg群で認められた.
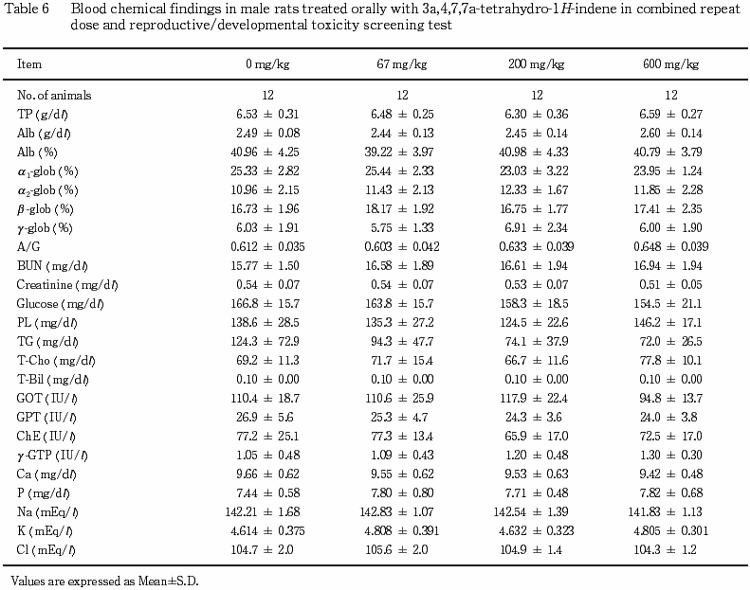
(6) 血液生化学検査(Table 6)
いずれの検査項目にも対照群と比較して雄に異常は認められなかった.
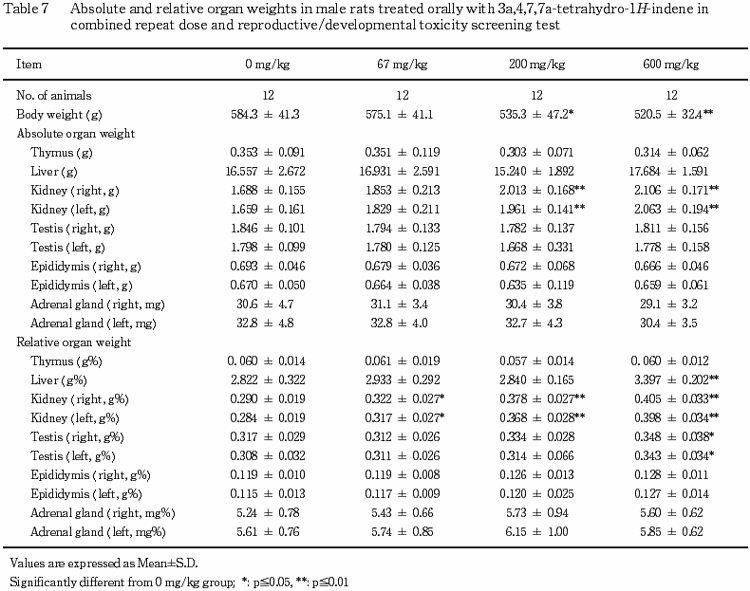
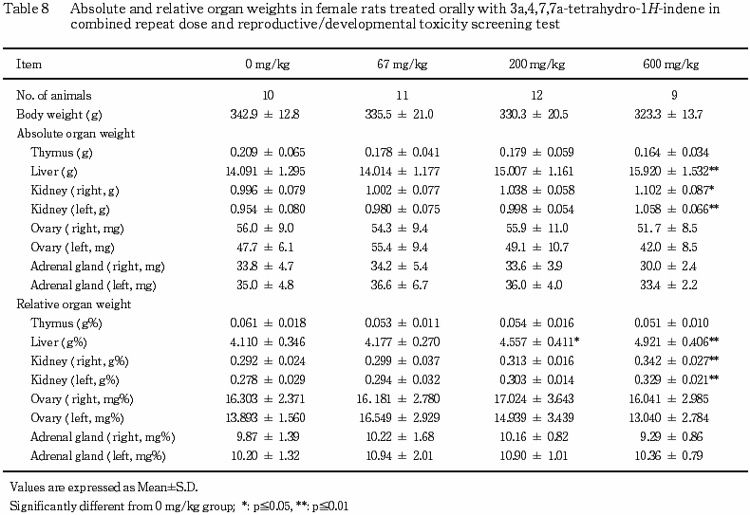
(7) 器官重量(Table 7,8)
雄では,剖検時体重の減少が200および600 mg/kg群で,肝臓の体重重量比の増加が600 mg/kg群で,左右の腎臓の重量の増加が200および600 mg/kg群で,左右の腎臓の体重重量比の増加が67,200および600 mg/kg群で,左右の精巣の体重重量比の増加が600 mg/kg群で認められた.なお,600 mg/kg群の肝臓重量および67 mg/kg群の左右の腎臓重量に統計学的有意差はないが,対照群と比較して高値が認められた.
一方,600 mg/kg群の左右の精巣重量には対照群との差は認められなかった.
雌では,肝臓の重量の増加が600 mg/kg群で,肝臓の体重重量比の増加が200および600 mg/kg群で,左右の腎臓の重量および体重重量比の増加が600 mg/kg群で認められた.なお,200 mg/kg群の肝臓重量にも統計学的な有意差はないが,対照群と比較して高値が認められた.
(8) 剖検
雄で,回腸に憩室が600 mg/kg群で1例に認められた.雌では,いずれの例にも異常は認められなかった.なお,流涎を示した例では唾液腺に異常は認められなかった.
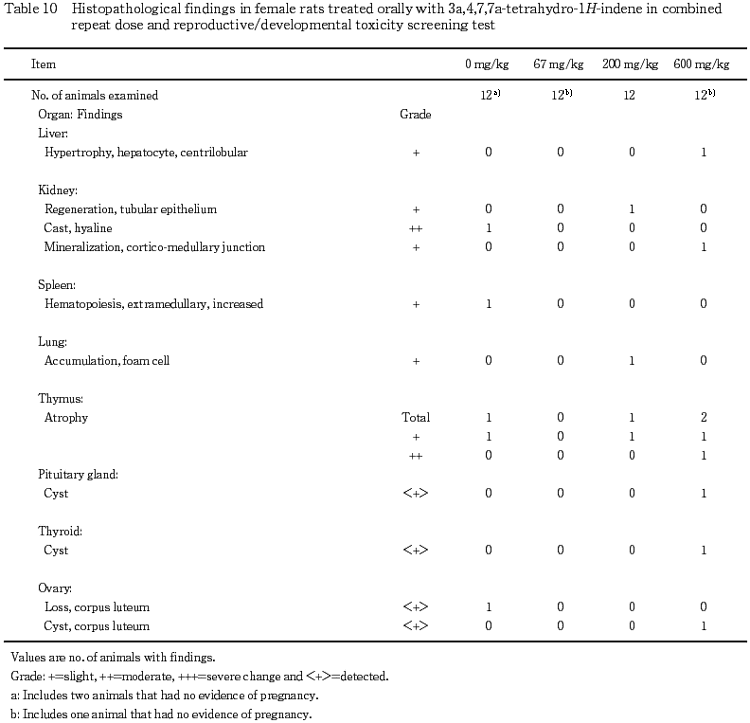
(9) 病理組織学検査(Table 9,10)
3a,4,7,7a-テトラヒドロ-1H-インデン投与による影響と考えられる所見として,雄では,肝臓で軽度の小葉中心性肝細胞肥大が600 mg/kg群で9例に,腎臓で軽度の近位尿細管上皮の硝子滴沈着が67および200 mg/kg群で各1例,中等度の硝子滴沈着が67および200 mg/kg群で各11例,600 mg/kg群で12例全例に,軽度の近位尿細管上皮の好酸性小体が67および200 mg/kg群で各8例,600 mg/kg群で9例に認められ,統計学的にも有意な変化であった.また,統計学的有意差は認められないものの,高用量群でより多くの例に認められ,3a,4,7,7a-テトラヒドロ-1H-インデン投与との関連が考えられる所見として,腎臓の尿細管上皮の再生が200 mg/kg群で4例,600 mg/kg群で3例に認められた.
雌では,600 mg/kg群の1例に,肝臓で軽度の小葉中心性肝細胞肥大が認められた.その他に被験物質投与と関連する変化は認められなかった.

2.生殖発生毒性
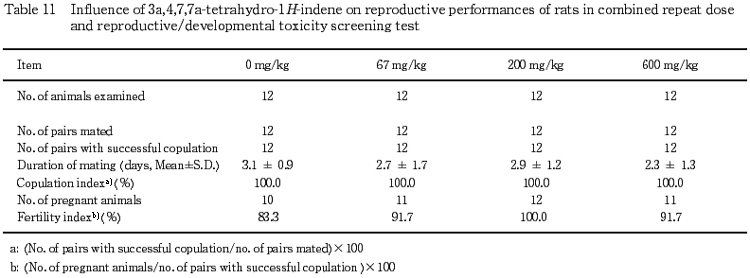
(1) 生殖能検査(Table 11)
雌の性周期検査では全例に異常は認められなかった.また,雌雄の交尾までに要した日数,交尾率および受胎率にも3a,4,7,7a-テトラヒドロ-1H-インデン投与の影響は認められなかった.
(2) 分娩および母性行動観察(Table 12)
妊娠期間の延長ならびに妊娠黄体数,着床数,出産児数および出産生児数の減少が600 mg/kg群で認められた.
分娩異常として,分娩中から分娩終了時まで生児のみられない例が600 mg/kg群で1例,また哺育異常として,全哺育児死亡例が600 mg/kg群で1例みられた.分娩異常例は着床数15,出産児数が5例であったが,分娩終了時に5例全例が死亡し,喰殺を受けた例もみられた.母動物の病理組織学検査では胸腺の萎縮が認められた.全哺育児死亡例では,着床数2,出産児数が1例であり,その1例が哺育2日に死亡した.母動物の病理組織学検査では下垂体に嚢胞が認められたのみであった.
分娩終了時の死亡児が67および200 mg/kg群で各雌3例,600 mg/kg群で雄3例,雌5例および性別不明例2例が認められ,67 mg/kg群の雌1例に腰椎の欠損,痕跡尾および鎖肛が認められた.
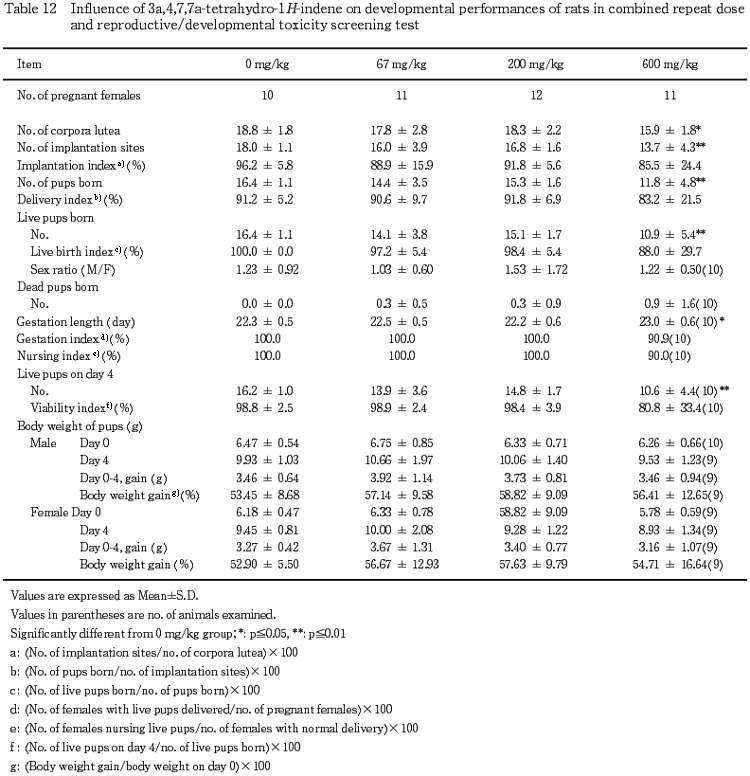
(3) 新生児の生存性(Table 12)
600 mg/kg群で,哺育4日の生存児数の低値が認められた.
(4) 新生児の一般状態観察
死亡あるいは不明例が対照群で雄2例,67 mg/kg群で雌雄各1例,200 mg/kg群で雄3例,600 mg/kg群で雄9例および雌5例に認められた.これらのうち,痕跡尾および鎖肛が600 mg/kg群で雄1例に認められた.
生存例では痕跡尾およびその痕跡尾の脱落が200 mg/kg群で雄1例に認められ,外傷が200 mg/kg群の他の1例に認められた.
(5) 新生児の体重推移(Table 12)
いずれの3a,4,7,7a-テトラヒドロ-1H-インデン投与群にも,対照群と比較して体重推移に異常は認められなかった.
(6) 新生児の剖検
一般状態観察でみられた600 mg/kg群の痕跡尾および鎖肛の1例,哺育4日に屠殺した200 mg/kg群の痕跡尾の欠損の1例および外傷の1例の他に,異常は認められなかった.
考察
1.反復投与毒性
一般状態観察では,流涎が雄においては600 mg/kg群の12例中10例で投与15日以降のほぼ毎日,また他1例では一過性に認められた.雌でも,雄と同様に,流涎が600 mg/kg群で妊娠前,投与期間および哺育期間を通して投与15日以降に計11例にみられた.剖検ではいずれの例にも唾液腺に異常は認められず,投与前から流涎がみられた例もいたことから,投与された3a,4,7,7a-テトラヒドロ-1H-インデンによる影響ではなく,投与薬物の臭いや口腔内への刺激による条件づけが成立したことによると考えられた.
体重推移では,体重増加抑制が雄の投与期間,雌の妊娠前交配期間および妊娠期間を通して200および600 mg/kg群で認められ,3a,4,7,7a-テトラヒドロ-1H-インデン投与の影響と考えられた.雌の600 mg/kg群では他に,哺育期間の体重増加量および増加率の高値が認められたが,それまでの体重増加抑制に対する哺育期間中の代償的反応と考えられた.
摂餌量では,雄の200 mg/kg群で投与2,7,14および21日に低値が認められた.しかし,高用量である雄の600 mg/kg群では投与2日に一過性の低値を示したのみであり,雌で67あるいは200 mg/kg群の哺育期間を除いた期間にみられた低値も一過性であったことから,3a,4,7,7a-テトラヒドロ-1H-インデン投与による摂餌量への影響はないと考えられた.
血液に及ぼす影響として,赤血球数,ヘマトクリット値および血色素量の減少が雄の600 mg/kg群で認められたが,いずれも軽度であり,尿検査,血液生化学検査ならびに脾臓を含む病理組織学検査においても異常は認められなかった.
肝臓に対する3a,4,7,7a-テトラヒドロ-1H-インデン投与の影響として,雄の600 mg/kg群で重量の増加傾向および体重重量比の増加がみられ,同群の病理組織学検査では軽度の小葉中心性肝細胞肥大が認められた.雌でも肝臓の重量の増加ないし増加傾向および体重重量比の増加が200 mg/kg以上の群で認められ,病理組織学検査でも,1例のみの発現であったが600 mg/kg群で肝臓に軽度の小葉中心性肝細胞肥大が認められた.
腎臓では,雄の67 mg/kg群で重量の増加傾向および体重重量比の増加,200および600 mg/kg群で重量および体重重量比の増加が認められ,雌でも腎臓の重量および体重重量比の増加が600 mg/kg群で認められた.病理組織学検査では,雄の3a,4,7,7a-テトラヒドロ-1H-インデン投与群全群で,近位尿細管上皮の硝子滴沈着および好酸性小体の発現に有意差が認められた.尿細管上皮の再生についても雄の200および600 mg/kg群で出現頻度の増加傾向が認められ,いずれも3a,4,7,7a-テトラヒドロ-1H-インデン投与による影響と考えられた.炭化水素化合物をラットに投与した場合,特に雄では腎臓の近位尿細管に硝子滴が沈着することが知られており,それ自体に毒性学的意義はないと考えられるが,硝子滴の沈着の程度が強い場合には尿細管上皮の障害および再生を引き起こすと考えられている1).また,好酸性小体についても硝子滴と同一物質であるという報告がある2).したがって,本試験では近位尿細管上皮への硝子滴あるいは好酸性小体の出現数の増加を認めたものの,毒性病理学的影響は200および600 mg/kg群でみられた尿細管上皮の再生の出現頻度の増加と考えるのが妥当と判断した.
また,雄の腎臓重量および体重重量比の増加は,硝子滴および好酸性小体の増加と関連していると思われるが,雌の600 mg/kg群ではこのような病理組織学的変化を伴わずに重量および体重重量比の増加が生じており,一元的には説明できなかった.
以上のことから,雄の67 mg/kg以上の群の腎臓の重量および体重重量比の増加(増加傾向を含む),雌の200 mg/kg以上の群の体重増加抑制ならびに肝臓の重量および体重重量比の増加(増加傾向を含む)から,本試験における3a,4,7,7a-テトラヒドロ-1H-インデンの反復投与による無影響量は雄で67 mg/kg/day未満,雌で67 mg/kg/dayと判断した.
2.生殖発生毒性
生殖能検査では雌の性周期,雌雄の交尾および受胎,雌雄の生殖器および内分泌器官の重量,あるいは剖検および病理組織学検査において3a,4,7,7a-テトラヒドロ-1H-インデン投与による影響は認められなかった.なお,600 mg/kg群で認められた精巣の体重重量比の増加は重量に影響が認められないことから,同群の体重低値に基づくものと判断された.3a,4,7,7a-テトラヒドロ-1H-インデン投与群の不妊例の生殖器では,その原因を示唆する病理組織学所見は認められなかった.
分娩異常として分娩終了時に生児のみられない例,ならびに哺育異常として全哺育児死亡例が600 mg/kg群でそれぞれ1例認められた.しかし,後述のように,3a,4,7,7a-テトラヒドロ-1H-インデン投与による妊娠黄体数の減少はみられるものの,着床率および胎児の生存性に及ぼす影響はみられず,またこれら2例の母動物では共通した所見がみられないことから,偶発的なものと考えられた.
母動物の剖検および分娩観察では,妊娠期間の延長ならびに妊娠黄体数,着床数,出産児数および出産生児数の減少が600 mg/kg群で認められた.着床数,出産児数,生存児数の減少については,それぞれ着床率,出産率および新生児の哺育4日の生存率に3a,4,7,7a-テトラヒドロ-1H-インデン投与の影響は認められないことから,これらは妊娠黄体数(排卵数)の減少に起因した変化であると考えられ,3a,4,7,7a-テトラヒドロ-1H-インデンが着床および胎児の生存性に直接影響を及ぼしたとは考えられなかった.妊娠期間の延長については,ウサギで産児数の少ない場合に妊娠期間が長くなることが知られており3),本試験の場合も出産児数の減少との関連が考えられた.
新生児では,一般状態観察および剖検で痕跡尾,鎖肛および腰椎の欠損が67 mg/kg群で1例,痕跡尾が200 mg/kg群で1例,痕跡尾および鎖肛が600 mg/kg群で1例にみられたが,各群1例のみの出現であり,3a,4,7,7a-テトラヒドロ-1H-インデン投与との関連はないものと考えられた.また,哺育4日の生存児数の低値が600 mg/kg群で認められたが,前述した全哺育児死亡例および妊娠黄体数の減少に起因するものであり,体重推移にも異常はみられないことから,新生児の生存性に対する3a,4,7,7a-テトラヒドロ-1H-インデン投与の影響はないと考えられた.
以上のことから,雄動物の生殖能に対する影響は600 mg/kg群でも認められず,一方,雌動物では600 mg/kg群で妊娠黄体数の減少ならびにそれに起因すると考えられる着床数の減少および妊娠期間の延長が,次世代に対しては出産児数および出産生児数の減少が認められたことから,本試験における3a,4,7,7a-テトラヒドロ-1H-インデンの親世代の生殖に対する無影響量は,雄動物では600 mg/kg/day,雌動物では200 mg/kg/dayであり,また,次世代に対する無影響量は200 mg/kg/dayと判断した.
文献
| 1) | P.Greaves, "Histopathology of Preclinical Toxicity Studies:Interpretation and Relevance in Drug Safety Evaluation," Elsevier, Amsterdam, Netherlands, 1990, pp. 532-538. |
| 2) | 海平充代ら,ラット慢性腎症の病理組織学的解析
-硝子滴変性について-,第8回日本毒性病理学会講演要旨集,76(1992). |
| 3) | 佐久間勇次 監,“ウサギ-生殖生理と実験手技-,”近代出版,東京,1988,p.24. |
| 連絡先 |
| 試験責任者: | 吉村浩幸 |
| 試験担当者: | 茂野 均,長谷淳一,古川正敏 |
| (株)化合物安全性研究所 |
| 〒229 北海道札幌市清田区真栄363番24号 |
| Tel 011-885-5031 | Fax 011-885-5313 | |
| Correspondence |
| Authors: | Hiroyuki Yoshimura(Study director)
Hitoshi Shigeno,Jyunichi Nagaya,Masatoshi Furukawa |
| Safety Research Institute for Chemical Compounds Co., Ltd. |
| 363-24 Shin-ei, Kiyota-ku, Sapporo, Hokkaido, 004, Japan |
| Tel +81-11-885-5031 | Fax +81-11-885-5313 | |












