2-(ジメチルアミノ)エチルメタクリラートのラットを用いる
反復経口投与毒性・生殖発生毒性併合試験
Combined Repeat Dose and Reproductive/Developmental Toxicity Screening Test of
2-(Dimethylamino)ethyl methacrylate by Oral Administration in Rats
要約
2-(ジメチルアミノ)エチルメタクリラートは,共重合による合成樹脂の接着性,染色性などの改善に用いられる他,凝集材,制電剤イオン交換樹脂,塗料用樹脂などのカチオン性コモノマー,潤滑油および燃料油添加剤の原料として使用されている.毒性に関する情報としては,ラットの経口投与による最小致死量は2000 mg/kg以上で,前胃に刺激性を示唆する病理変化を起こすことが報告されている1).今回,OECDによる既存化学物質の安全性点検に係わる毒性調査事業の一環として,SDラット(1群雌雄各12匹)に40,200および1000 mg/kgの用量を交配前14日から交配を経て雄は計43日間,雌は妊娠,分娩を経て哺育3日まで経口投与し,反復投与毒性および生殖発生毒性について検討した.
1. 反復投与毒性
1000 mg/kg群において,雄で投与開始後36日以降,雌で31日以降に攣縮,挙尾,間代性痙攣が散見された.また,雌雄で体重増加抑制,雌で3例の死亡および授乳期間の摂餌量減少が認められた.病理学検査では,雌雄で脳および脊髄の神経線維の変性,前胃壁の肥厚,粘膜上皮の増生,水腫および炎症性細胞浸潤,雌で胸腺の萎縮が認められた.この他,雌雄の腎臓および雄の肝臓,雌の副腎の重量が増加を示したが,組織変化は認められなかった.また,雄の血液生化学検査では,尿素窒素の上昇,血液学検査では赤血球数,ヘモグロビン濃度およびヘマトクリット値の減少,網状赤血球比の増加などの貧血性変化,白血球数および分葉核球数の増加が認められた.
200 mg/kg群においても雄でヘモグロビン濃度およびヘマトクリット値の減少が認められた.
2. 生殖発生毒性
親動物の交尾率,受胎率,黄体数,着床数,着床率,分娩率,出産率,妊娠期間および分娩には被験物質に起因する変化は認められなかった.哺育期間の観察では,1000 mg/kg群の母動物3例で全新生児死亡が認められた.新生児の検査では,1000 mg/kg群で低体重および4日生存率の低下が認められた.出産児数,出産生児数,性比,出生率,外表,一般状態および剖検では被験物質に起因する変化は認められなかった.
以上の結果から,2-(ジメチルアミノ)エチルメタクリラートの反復投与毒性に関する無影響量は雄が40 mg/kg/day,雌が200 mg/kg/day,生殖発生毒性に関する無影響量は,親動物に対して雄が1000 mg/kg/day,雌が200 mg/kg/day,児動物に対しては200 mg/kg/dayと考えられる.
方法
1. 被験物質
2-(ジメチルアミノ)エチルメタクリラート(三洋化成工業 ,Lot No. K609415,純度99.9 %)は,融点-30℃,沸点182〜192℃,比重0.936,水,アセトンおよびDMSOに溶けやすい,アミン臭のある無色透明の液体である.被験物質は室温・暗所・密閉で保管した.また,試験期間中安定であったことが確認された.
,Lot No. K609415,純度99.9 %)は,融点-30℃,沸点182〜192℃,比重0.936,水,アセトンおよびDMSOに溶けやすい,アミン臭のある無色透明の液体である.被験物質は室温・暗所・密閉で保管した.また,試験期間中安定であったことが確認された.
2. 試験動物および飼育条件
日本チャールス・リバー から入手した雌雄のSDラット〔Crj:CD(SD)IGS〕を6日間検疫・馴化後,試験に供した.投与開始前日に体重別層化無作為抽出法により,1群につき雌雄各12匹を振り分けた.投与開始時の週齢は雌雄とも9週齢,体重範囲は雄が325〜360 g,雌が191〜242 gであった.
から入手した雌雄のSDラット〔Crj:CD(SD)IGS〕を6日間検疫・馴化後,試験に供した.投与開始前日に体重別層化無作為抽出法により,1群につき雌雄各12匹を振り分けた.投与開始時の週齢は雌雄とも9週齢,体重範囲は雄が325〜360 g,雌が191〜242 gであった.
検疫・馴化期間を含めた全飼育期間中,温度22±2℃,湿度55±15 %,換気約12回/時,照明12時間/日(7:00〜19:00)に設定した飼育室を使用した.動物は実験動物用床敷(ベータチップ:日本チャールス・リバー )を敷いたポリカーボネート製ケージに,群分け後は1匹,交配期間は雌雄各1匹,哺育期間は1腹で収容し,飼育した.
)を敷いたポリカーボネート製ケージに,群分け後は1匹,交配期間は雌雄各1匹,哺育期間は1腹で収容し,飼育した.
動物には,オートクレーブ滅菌した実験動物用固型飼料(CRF-1:オリエンタル酵母工業 )および5 μmのフィルターで濾過後,紫外線照射した水道水をそれぞれ自由摂取させた.
)および5 μmのフィルターで濾過後,紫外線照射した水道水をそれぞれ自由摂取させた.
3. 投与量および投与方法
SDラットの雌雄を用いて,被験物質を30,100,300および1000 mg/kgの用量で14日間経口投与した結果,1000 mg/kg群の雄で体重減少,雌で体重増加抑制,雌雄で前胃粘膜の肥厚が認められた.以上の結果から,本試験では高用量を1000 mg/kgとし,以下公比5で中用量を200 mg/kg,低用量を40 mg/kgとした.また,媒体(コーン油)のみを投与する対照群を設けた.
投与期間は,雌雄とも交配前14日間,交配期間,および雄は剖検前日までの計43日間,雌は交尾成立後,妊娠,分娩を経て哺育3日まで(41〜52日間)とし,プラスチック製胃ゾンデを用いて1日1回,午前中に強制経口投与した.投与液量は5 mL/kgとし,至近測定日の体重を基に算出した.
被験物質はコーン油に溶解させ,投与に供するまで冷蔵保存し,調製後8日以内に使用した.投与開始前に投与液中の被験物質の安定性および濃度を確認した.
4. 反復投与毒性に関する観察・検査
1) 一般状態
全例について生死,外観,行動等を投与前および投与後に毎日観察した.死亡動物は発見後速やかに剖検した.
2) 体重および摂餌量
体重は,雌雄とも投与開始日,投与開始後3,7,14日,およびその後週1回,交尾した雌は妊娠0,7,14,20日および哺育0,4日に測定した(交尾確認日を妊娠0日,分娩確認日を哺育0日とする).また,雄では投与開始日の体重を基準に,雌では交配前期間,妊娠期間,哺育期間をそれぞれ投与開始日,妊娠0日,哺育0日の体重を基準に体重増加量を算出した.摂餌量は,交配期間を除き体重測定日に測定した.
3) 雄の尿検査
解剖日の2日前に各群6匹の新鮮尿を採取し,pH ,蛋白,グルコース,ケトン体,ビリルビン,潜血,ウロビリノーゲン(試験紙法,マルティスティックス:マイルス・三共 )を尿分析器(クリニテック100:マイルス・三共
)を尿分析器(クリニテック100:マイルス・三共 )により測定し,尿沈渣(Sternheimer-Malbin染色標本)を検査した.また,約21時間蓄尿について,尿量を計量し,比重(屈折法)を尿比重計(ユリコン-S:
)により測定し,尿沈渣(Sternheimer-Malbin染色標本)を検査した.また,約21時間蓄尿について,尿量を計量し,比重(屈折法)を尿比重計(ユリコン-S: アタゴ)により測定した.
アタゴ)により測定した.
4) 雄の血液学検査
雄の全生存動物について,解剖日の前日から約21時間絶食させ,チオペンタールナトリウム(ラボナール:田辺製薬 )の腹腔内投与による麻酔下で後大静脈より採取した血液の一部をEDTA-2Kにより凝固阻止し,赤血球数(シースフローDCインピーダンス検出法),白血球数(RF/DCインピーダンス検出法),血小板数(シースフローDCインピーダンス検出法),ヘモグロビン濃度(SLSヘモグロビン法),ヘマトクリット値(赤血球パルス波高値検出法)を多項目自動血球分析装置(NE-4500:東亞医用電子
)の腹腔内投与による麻酔下で後大静脈より採取した血液の一部をEDTA-2Kにより凝固阻止し,赤血球数(シースフローDCインピーダンス検出法),白血球数(RF/DCインピーダンス検出法),血小板数(シースフローDCインピーダンス検出法),ヘモグロビン濃度(SLSヘモグロビン法),ヘマトクリット値(赤血球パルス波高値検出法)を多項目自動血球分析装置(NE-4500:東亞医用電子 ),白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROX HEG-70A:オムロン
),白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROX HEG-70A:オムロン ),網状赤血球数(アルゴンレーザーを用いたフローサイトメトリー法)を自動網赤血球測定装置(R-2000:東亞医用電子
),網状赤血球数(アルゴンレーザーを用いたフローサイトメトリー法)を自動網赤血球測定装置(R-2000:東亞医用電子 )により測定した. また,検査結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.
)により測定した. また,検査結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.
5) 雄の血液生化学検査
雄の全生存動物について,解剖日に採取した血液を室温で約30分間静置後遠心分離し,得られた血清についてGOT(SSCC改良法),GPT(SSCC改良法),γ-GTP(SSCC改良法),ALP(GSCC改良法),総ビリルビン(Jendrassik改良法),尿素窒素(Urease-GLDH法),クレアチニン(Jaff 法),グルコース(GK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(UV法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形:
法),グルコース(GK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(UV法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形: 日立製作所)により測定した.また,採取した血液の一部をヘパリン(リチウム塩)処理後遠心分離し,得られた血漿についてLDH(SSCC改良法)を自動分析装置(COBAS FARA
日立製作所)により測定した.また,採取した血液の一部をヘパリン(リチウム塩)処理後遠心分離し,得られた血漿についてLDH(SSCC改良法)を自動分析装置(COBAS FARA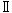 :F. Hoffmann La Roche & Co.)により測定した.
:F. Hoffmann La Roche & Co.)により測定した.
6) 病理学検査
雌雄とも最終投与日の翌日に,全生存動物についてチオペンタールナトリウムの腹腔内投与による麻酔下で腹大動脈の切断・放血により安楽死させて剖検し,脳,下垂体,甲状腺,胸腺,心臓,肝臓,腎臓,脾臓,副腎,精巣および精巣上体の重量を測定した.また,解剖日の体重を基に相対重量(対体重比)を算出した.さらに,これらの器官に加えて,眼球およびハーダー腺,唾液腺(下顎・舌下),リンパ節(下顎・腸間膜),上皮小体,気管,肺,食道,胃,腸管(十二指腸〜直腸),膵臓,膀胱,前立腺腹葉,精のう,卵巣,子宮,膣,骨髄(胸骨・大腿骨),坐骨神経,脊髄,乳腺および肉眼的異常部位を採取し,10 %中性リン酸緩衝ホルマリン液で固定後保存した.ただし,死亡例以外の眼球およびハーダー腺はダビドソン液,精巣および精巣上体はブアン液で固定した.
病理組織学検査は雌雄の対照群および1000 mg/kg群の脳,下垂体,甲状腺,胸腺,気管,肺,胃,腸管,心臓,肝臓,腎臓,脾臓,副腎,膵臓,膀胱,骨(胸骨・大腿骨),骨髄(胸骨・大腿骨),リンパ節(下顎・腸間膜),坐骨神経,脊髄,精巣,精巣上体,前立腺腹葉,精のう,卵巣,子宮,膣,雌の乳腺ならびに全動物の肉眼的異常部位について,常法に従いヘマトキシリン・エオジン染色標本を作製して鏡検した.その結果,雌雄とも脳,脊髄,胃および胸腺で被験物質に起因する変化が認められたので,40および200 mg/kg群のこれらの器官についても検査した.なお,この他に雄の40および200 mg/kg群の前立腺および精のうも検査した.
5. 生殖発生毒性に関する観察・検査
1) 生殖機能
交配前の投与期間終了後,各群内で雄1雌1の交配対を設け,最長14日間昼夜同居させ,毎日午前中に雌の膣垢を採取し,ギムザ染色して鏡検した.膣栓形成あるいは膣垢標本中に精子が認められた場合を交尾成立とし,その日を妊娠0日とした.交尾した対は雌雄を分離し,以後の検査に供した.これらの結果から,交尾所要日数(交配開始後,交尾成立までに要した日数),交尾成立までに逸した発情期の回数,交尾率〔(交尾動物数/同居動物数)×100〕,受胎率〔(受胎動物数/交尾動物数)×100〕を算出した.
2) 分娩・哺育状態
交尾が確認された雌は全例を自然分娩させ,分娩状態を観察した.午前9時の時点で分娩が完了している動物を当該日分娩とし,その日を哺育0日とした.その後,新生児を生後4日(哺育4日)まで哺育させ,授乳,営巣,食殺の有無等の哺育状態を毎日観察した.
母動物は,哺育4日の剖検時に卵巣,子宮を摘出し,黄体数および着床数を検査した.分娩しない雌は交尾確認後26日に剖検し,肉眼的に着床が認められない動物の子宮は10 %硫化アンモニウム水溶液に浸漬して着床の有無を確認した.また,全新生児が死亡した母動物はその時点で剖検した.これらの結果から,妊娠期間(妊娠0日から出産が確認された日までの期間),出産率〔(生児出産雌数/受胎雌数)×100〕,着床率〔(着床数/黄体数)×100〕,分娩率〔(総出産児数/着床数)×100〕を算出した.
3) 新生児の観察・検査
(1) 新生児の観察
哺育0日に出産児数(出産生児数,死産児数),性別および外表異常の有無を検査した.その後,一般状態,死亡の有無を哺育4日まで毎日観察した.哺育0および4日の生存児数から出生率〔(出産生児数/総出産児数)×100〕,新生児の4日生存率〔(哺育4日生児数/出産生児数)×100〕を算出した.
(2) 体重
哺育0および4日に全生存児を個体ごとに測定した.また,哺育0日の体重を基準に体重増加量を算出した.
(3) 剖検
哺育4日に全生存児の口腔を含む外表を検査した後,親動物と同様にして安楽死させ,剖検した.死亡動物は食殺等で検査に耐えないものを除き,10 %中性リン酸緩衝ホルマリン液に浸漬・固定後,実体顕微鏡下で剖検した.
6. 統計解析
計量データについては,パラメトリックデータはBartlett法による等分散性の検定を行い,分散が一様の場合は一元配置分散分析を行った.分散が一様でない場合およびノンパラメトリックデータはKruskal-Wallisの検定を行った.群間に有意な差が認められた場合はDunnett法またはDunnett型の多重比較を行った.計数データのうち,尿検査の定性所見および病理組織所見はa×bのc 2 検定を行い,有意差が認められた場合はArmitageのc 2 検定により対照群と各被験物質投与群間の比較を行った.その他の計数データはFisherの直接確率法により検定した.有意水準は5 %とし,新生児に関するデータは各母動物ごとに算出した平均値を標本単位とした.なお,1000 mg/kg群の雄1例は投与開始後25日に上切歯を破損し,体重増加不良を示したため,生殖機能検査以外の以後のデータを集計から除外した.
結果
1. 反復投与毒性
1) 死亡動物
1000 mg/kg群の雌で,投与開始後2,6および38日(妊娠23日)にそれぞれ1例が死亡した.投与初期の死亡例には,死亡1〜2日前にラッセル音,自発運動低下,呼吸困難あるいは不整呼吸などが認められた.また,妊娠後期の死亡例には投与開始後31日(妊娠16日)から攣縮および挙尾が死亡前日まで観察された.
この他,対照群の雌1例が妊娠23日に分娩を開始したが,体温低下および蒼白を示して翌日に死亡した.
2) 一般状態
1000 mg/kg群で,攣縮および挙尾が,雄で投与開始後36日,雌で31日からそれぞれ4および3例で認められ,さらに一部の動物には間代性痙攣あるいは不整呼吸が観察された.これらの症状は,投与時の保定などの刺激により発症し,数分間持続した後消失した.また,投与直後の流涎が雌雄で投与開始後7日から認められた.一部には投与前から発症する動物もみられ,投与終了時までには雌雄ともほぼ全例で観察された.
200 mg/kg群では,雌で同様の流涎が投与開始後14日に4例で観察された.
その他,軟便,紅涙,脱毛が各群で散見されたが,1000 mg/kg群で多発する傾向がみられなかったことから,被験物質との関連はないと判断した.
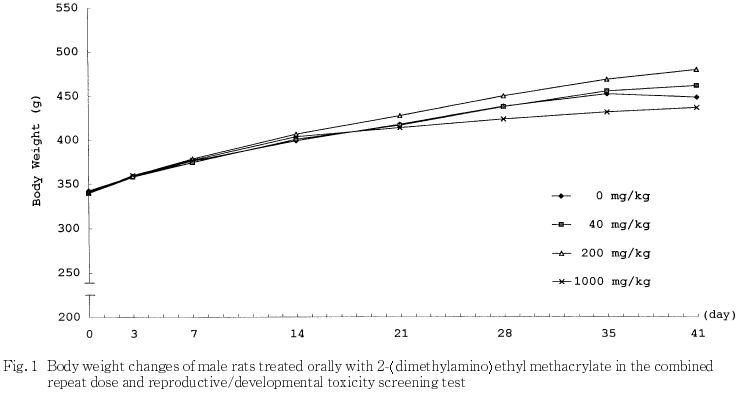
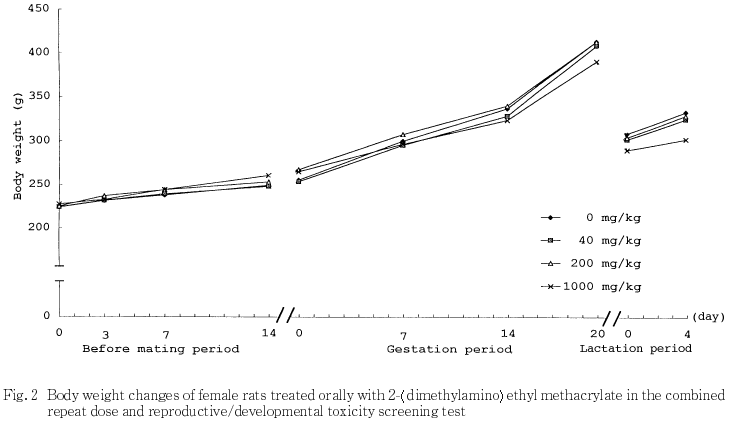
3) 体重(Fig.1,2)
1000 mg/kg群の雌で,体重増加量が妊娠7および14日に有意な低値を示し,その後も哺育4日まで体重および増加量とも低値で推移した.また,雄でも有意差は認められなかったものの,交配以後の体重は低値傾向を示した.
その他,200 mg/kg群の雄の体重増加量が投与開始後41日に有意な高値を示したが,1000 mg/kg群では増加傾向はなく,偶発変化と判断した.
4) 摂餌量
1000 mg/kg群の雌で,投与開始後7および14日に有意な高値を,哺育4日に有意な低値を示した.
雄では対照群と被験物質投与群との間に有意な変化は認められなかった.
5) 雄の尿検査
1000 mg/kg群で尿量が有意な高値を示したが,生理的変動範囲内の値であったことから,偶発的な変化と判断した.その他の検査項目には有意な変化は認められなかった.
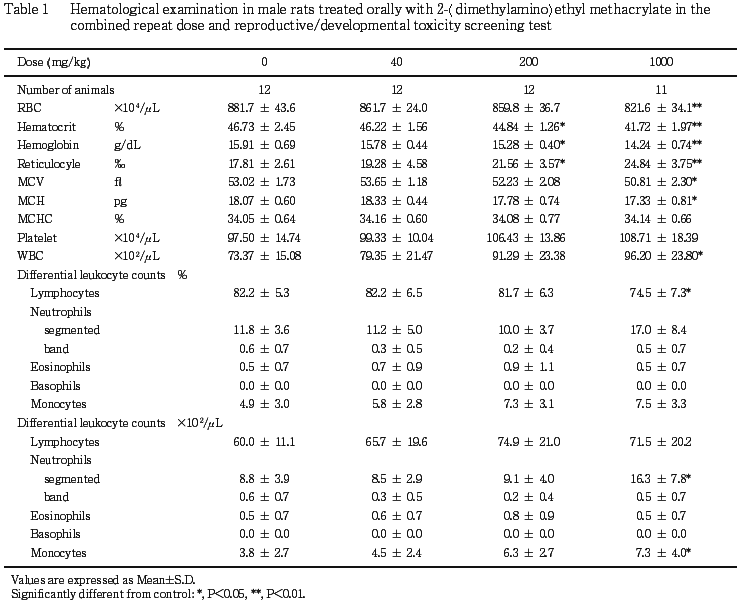
6) 雄の血液学検査(Table 1)
200 mg/kg以上の群でヘモグロビン濃度およびヘマトクリット値が有意な低値を,網状赤血球比が有意な高値を,1000 mg/kg群で赤血球数,平均赤血球容積および平均赤血球血色素量が有意な低値を示した.また,1000 mg/kg群で白血球数が有意な高値を,白血球百分率ではリンパ球が有意な低値を示し,実数換算値で分葉核球数の有意な増加が認められた.なお,同群の単球数も有意な高値を示したが,百分率では有意差は認められず,生理的変動範囲内の値であった.
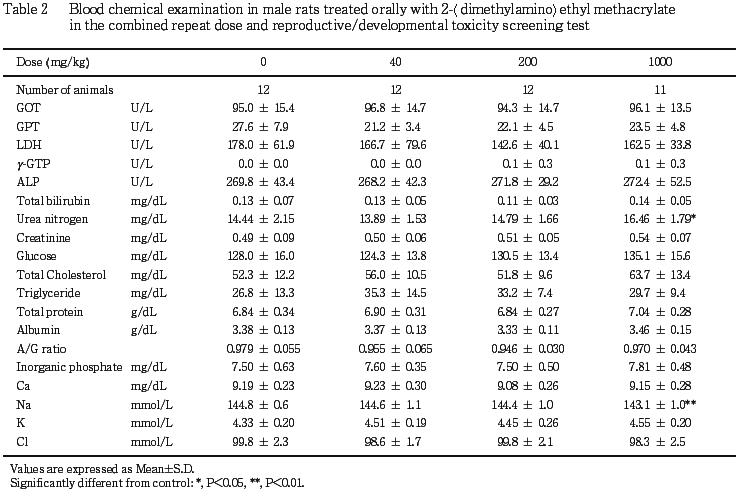
7) 雄の血液生化学検査(Table 2)
1000 mg/kg群で尿素窒素が有意な高値を示した.その他,ナトリウムが有意な低値を示したが,生理的変動範囲内の値であったことから,偶発的な変化と判断した.その他の検査項目には有意な変化は認められなかった.
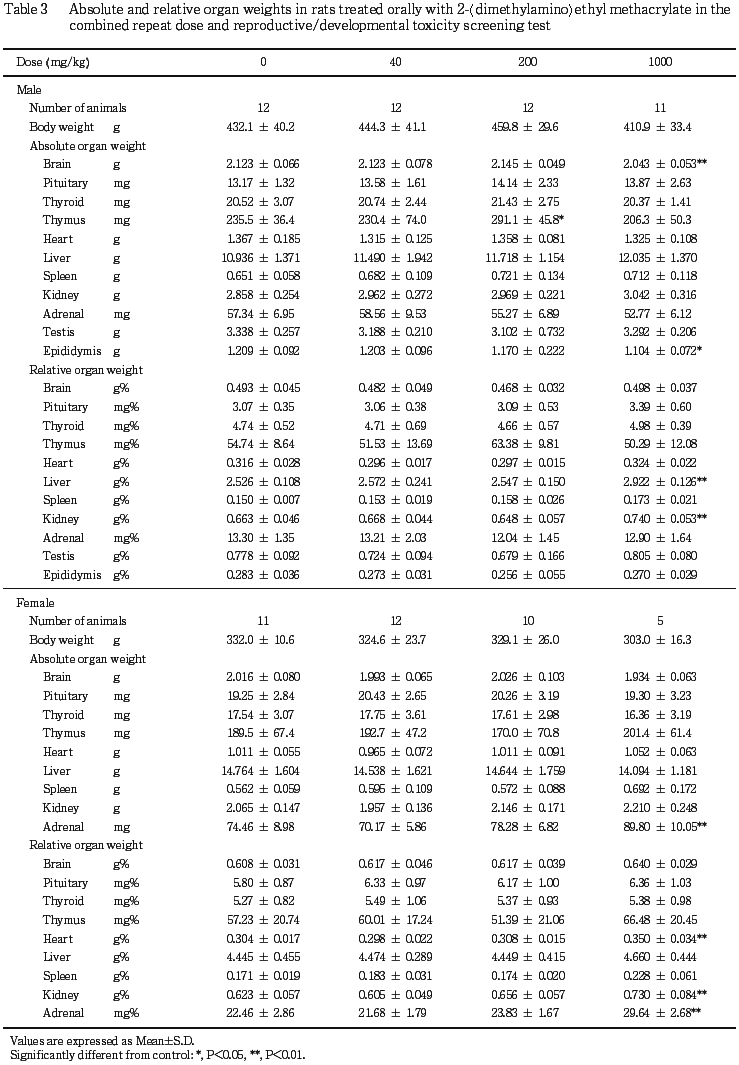
8) 器官重量(Table 3)
雄では,1000 mg/kg群で肝臓および腎臓の相対重量が有意な高値を示し,絶対重量でも高値の傾向がみられた.また雌では,1000 mg/kg群で副腎の絶対重量および相対重量,腎臓の相対重量が有意な高値を示した.
この他,1000 mg/kg群で雄の脳および精巣上体の絶対重量が有意な低値を,雌の心臓の相対重量が有意な高値を示したが,相対重量あるいは絶対重量では明確な変化はみられなかったことから,体重増加抑制が反映したものと考えられた.また,200 mg/kg群で雄の胸腺の絶対重量が有意な高値を示したが,1000 mg/kg群では同様の変化は認められなかったことから,偶発変化と判断した.
9) 剖検所見
前胃壁の肥厚が1000 mg/kg群の雄の全例,雌では死亡例を含めて10例に認められた.肥厚した前胃粘膜の表面は粗造であった.この他,1000 mg/kg群の雌の死亡例では全例に肺水腫が認められた他,脾臓の小型化,心房拡張,肝臓のうっ血,腺胃の潰瘍,腺胃粘膜の充血,副腎の腫大および胃腸管の鼓張などが観察された.
対照群の雌の死亡例では子宮および胸腺の出血が認められた.また,全新生児が死亡した母動物では,1000 mg/kg群の1例で胸腺の小型化,子宮および膣の出血,200 mg/kg群の1例で腎臓の褪色,脾臓の褐色化および腫大が認められた.
この他,対照群を含む各群で種々の変化が認められたが,いずれも1例のみであったことから偶発所見と判断した.
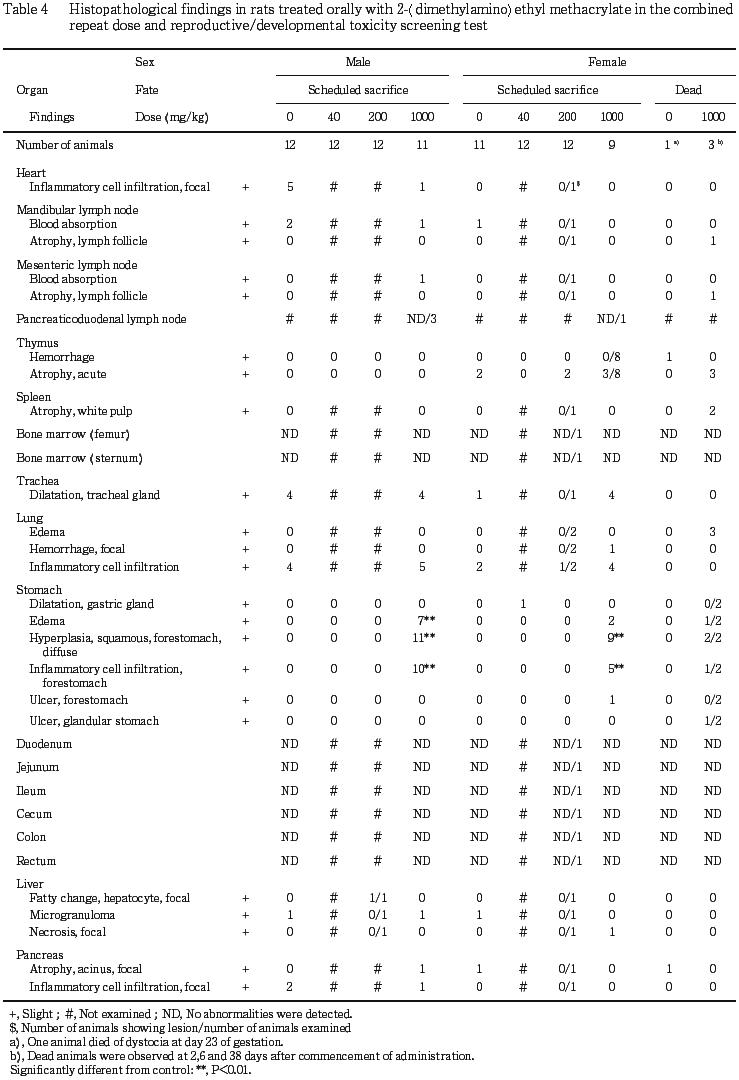
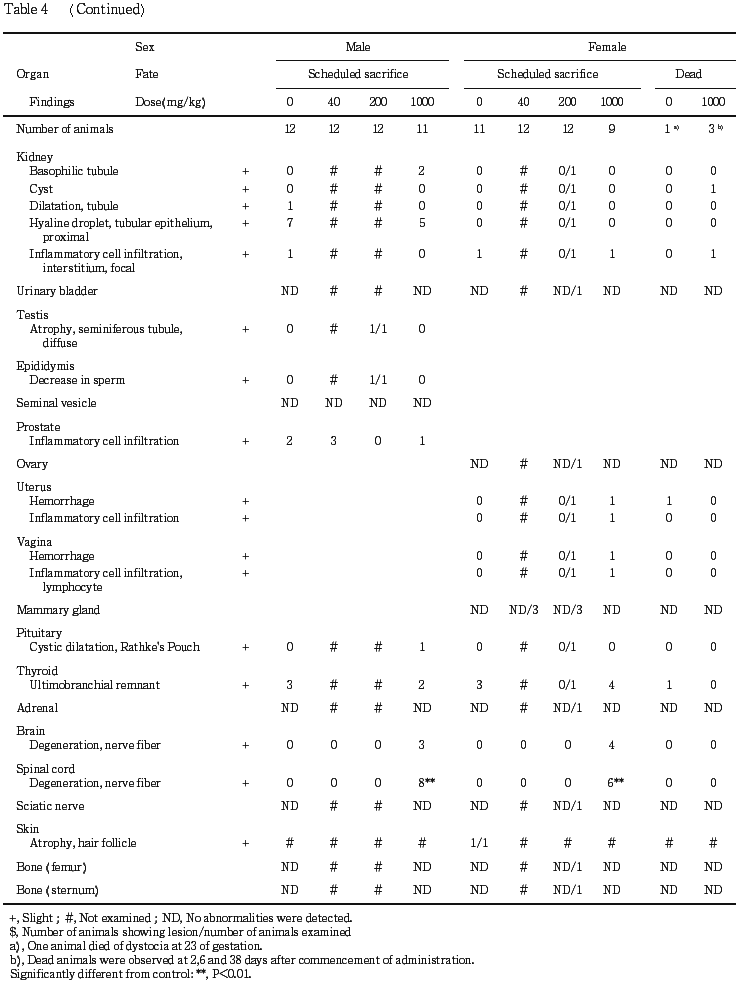
10) 組織所見(Table 4)
被験物質に起因する変化が雌雄の脳,脊髄,前胃および雌の胸腺で認められた.脳では,橋の赤核脊髄路領域の神経線維の変性が1000 mg/kg群の雄3例,雌4例で左右対称性に観察された.脊髄でも,背側後脊髄小脳路の神経線維の変性が1000 mg/kg群の雄8例,雌6例で左右対称性に観察され,雌雄とも発現頻度に有意差が認められた.前胃では,粘膜上皮の増生が1000 mg/kg群で死亡例も含めて雌雄全例(死後変化の著しい投与開始後2日の死亡例を除く)で認められた.多くの例ではさらに増生した粘膜の下織に水腫と炎症性細胞浸潤を伴っており,発現頻度に有意差も認められた.雌の胸腺では,萎縮が対照群,40,200および1000 mg/kg群でそれぞれ2,0,2および6例に認められ,有意差は認められなかったものの,1000 mg/kg群で高頻度に発現した.これらのうち,1000 mg/kg群の6例中5例は死亡動物あるいは全新生児が死亡した母動物であった.
1000 mg/kg群の雌の死亡例では,肺の水腫が全例,脾臓の白脾髄の萎縮が2例,下顎および腸間膜リンパ節のリンパ小節の萎縮が1例に認められた.
対照群の死亡例では子宮と胸腺に出血が認められ,子宮の大量出血が原因で衰弱し,死亡したものと考えられた.
この他,対照群を含む各群で種々の変化が認められたが,自然発生性に認められる変化であり,1000 mg/kg群で多発する傾向はみられなかったことから,偶発所見と判断した.
2. 生殖発生毒性
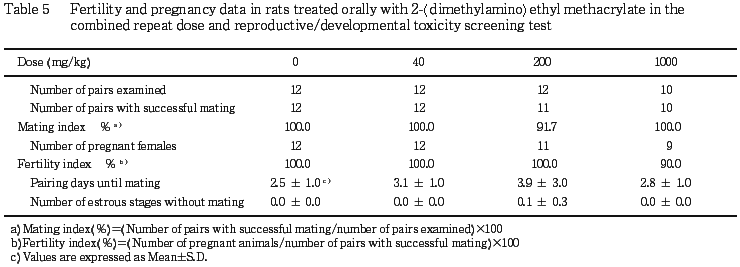
1) 生殖機能(Table 5)
未交尾動物は200 mg/kg群で1対観察されただけで,ほとんどの交配対は交配開始後5日以内に雌が発情期を示して交尾し,交尾率,交尾所要日数および交尾成立までに逸した発情期の回数ともに対照群と被験物質投与群との間に有意な差は認められなかった.また,非妊娠動物は1000 mg/kg群で1例観察されただけであり,受胎率にも有意な差は認められなかった.なお,200 mg/kg群の未交尾動物の雄には,剖検で精巣の小型化,病理組織学検査では精細管のび漫性萎縮などが認められ,交尾不成立の原因と思われた.
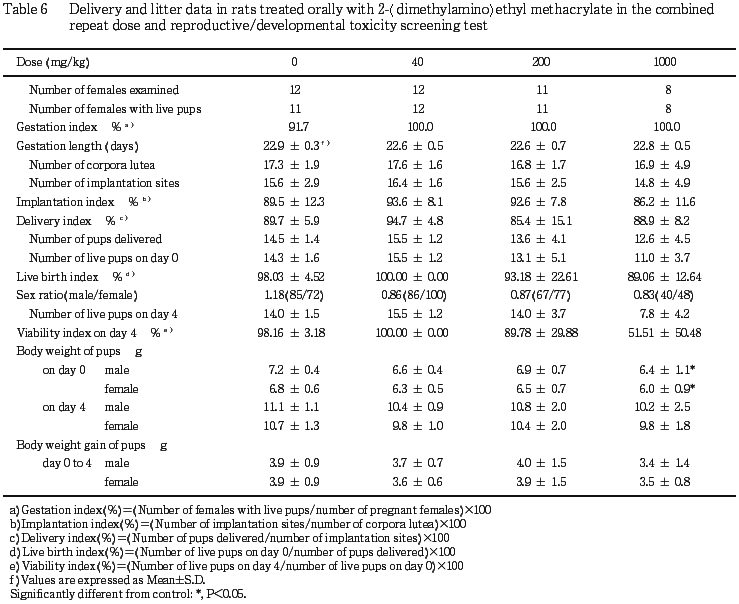
2) 分娩・哺育状態(Table 6)
分娩の観察において,対照群の1例が妊娠23日に分娩を開始したが,新生児1例を娩出したのみで,分娩が完了しないまま翌日に死亡した.また,200 mg/kg群の1例が妊娠24日に分娩し,授乳,児なめ,胎盤摂食,回集行動などの母性行動を示さず,全ての新生児が哺育1日までに死亡した.その他の母動物は各群とも妊娠22または23日に正常な分娩を示し,妊娠期間,黄体数,着床数,着床率,分娩率および出産率ともに対照群と被験物質投与群との間に有意な差は認められなかった.
哺育期間の観察において,全新生児死亡が,分娩遅延を示した200 mg/kg群の1腹の他に,1000 mg/kg群の3腹で観察された.これらの母動物には母性行動がみられたが,新生児のほとんどは受乳状態が不良で,哺育2日までに全例が死亡した.また,同群の他の1腹でも分娩日に未受乳の新生児が多数観察され,それらのほとんどは死亡した.その他の母動物の哺育状態には異常は認められなかった.
3) 新生児に及ぼす影響
(1) 生存率(Table 6)
1000 mg/kg群で,有意差は認められなかったものの,哺育4日の新生児数および新生児の4日生存率が低値を示した.本変化は母動物が哺育異常を示した4腹で新生児死亡が多発したことに起因しており,同群のその他の腹では新生児死亡はほとんど観察されなかった.出産児数,出産生児数,性比および出生率には対照群と被験物質投与群との間に有意な差は認められなかった.なお,1000 mg/kg群の出産児数が他の群に比べて低値を示したが,着床数が8および6と少なかった母動物2例の出産児数が反映していた.対照群でも着床数8を示す母動物が1例観察されており,これらを除外した場合の対照群および1000 mg/kg群の出産児数は14.5および14.7とほぼ同様の値であった.さらに,黄体数,着床率,分娩率にも被験物質の影響は認められなかったことから,偶発変化と考えられる.
(2) 外表および一般状態
皮下出血が対照群で出生日に1例観察された.その他には,1000 mg/kg群で未受乳の新生児が多発した以外は一般状態に変化はみられず,外表異常も認められなかった.
(3) 体重(Table 6)
1000 mg/kg群で雌雄とも哺育0日の体重が有意な低値を示した.200 mg/kg以下の群では雌雄とも対照群と被験物質投与群との間に有意な変化は認められなかった.なお,1000 mg/kg群の体重について,全新生児死亡および死亡児が多発した腹を除いた場合,哺育0日の平均体重は雄7.1 g,雌6.5 g,また平均体重増加量は雄4.0 g,雌3.8 gと対照群とほぼ同様の値であった.
(4) 剖検
生存動物ではいずれの群にも異常は認められなかった.また,死亡動物では胸腺頸部残留が対照群の1腹で1例,1000 mg/kg群の2腹で2例観察されただけであったことから,被験物質に起因する変化ではないと判断した.
考察
1. 反復投与毒性
反復投与による影響として,1000 mg/kg群の雌雄で攣縮,挙尾および間代性痙攣が,投与開始後30日以上経過した後,投与時の保定などの刺激により発現した.また,同群では雌雄で体重増加抑制,雌で授乳期間の摂餌量減少が認められた他,雌では3例が死亡し,病理学検査で肺水腫が認められた.化学構造が類似する物質では,中毒症状として呼吸器刺激による呼吸困難が起こり,肺水腫により死亡することが知られており2),同様な原因により死亡した可能性が考えられる.
病理学検査において,1000 mg/kg群の雌雄で脳,脊髄および前胃,雌で胸腺に被験物質に起因する変化が認められた.すなわち,脳および脊髄では,橋の赤核脊髄路領域と背側後脊髄小脳路で神経線維の変性が左右対称性に認められた.これらは筋の運動あるいは筋緊張の調節に関与する神経連絡路であり,同群で投与後期に観察された攣縮,挙尾などの行動異常と関連する変化と推察される.化学構造が類似するメタクリル酸2-ヒドロエチルエステルおよび2-エチルヘキシルメタクリラートでも反復投与により行動異常の発現および脳の組織変化が起こることが報告されている3,4).また,メチルメタクリラートは行動異常を誘発することが知られ5),脳内アミンあるいは神経伝達に影響を及ぼすことが明らかにされている5-7).発現機序は不明であるが,被験物質も中枢神経系への影響が示唆される.前胃では,剖検で肥厚が観察され,組織学的には粘膜上皮の増生と粘膜下織の水腫および炎症性細胞浸潤が認められた.化学構造が類似するアクリル酸のエステル化合物は,ラットの前胃に対し刺激性を有することが知られており8-10),被験物質も同様の刺激性を有するものと考えられる.また,胸腺の萎縮が1000 mg/kg群の雌で高頻度に認められたが,死亡あるいは全新生児死亡を示した母動物がほとんどであり,死亡例の一部では脾臓の白脾髄およびリンパ節のリンパ小節の萎縮も観察された.これらの変化はストレス状態の動物に非特異的にみられる変化でもあることから11),被験物質に直接起因したものではなく,二次的に生じた変化である可能性が考えられる.
器官重量では雌雄の腎臓重量が増加の傾向を示し,雄では血清尿素窒素の上昇が認められたことから,被験物質による腎機能への影響の可能性が示唆される.また,雄の肝臓および雌の副腎にも重量増加が認められ,これらの器官にも影響している可能性が考えられた.しかし,いずれも病理組織学検査では変化は認められなかったことから,影響としては軽度のものと推察される.
雄の血液学検査では,1000 mg/kg群で赤血球数,ヘモグロビン濃度およびヘマトクリット値の減少,網状赤血球比の増加などの貧血性変化と白血球数および分葉核球数の増加が認められた.これらの変化は前胃の病変部の炎症との関連が考えられるが,貧血性変化については,前胃に病変が認められなかった200 mg/kg群でも観察されており,被験物質による造血機能への影響が示唆される.しかし,脾臓および骨髄には組織変化は認められなかったことから,影響としては軽度なものと考えられる.
投与直後の流涎が1000 mg/kg群の雌雄および200 mg/kg群の雌で観察されたが,一部には投与直前から反射的に発現する例もみられたことから,被験物質の局所刺激性に起因したものであり,反復投与毒性を示すものではないと考えられる.
2. 生殖発生毒性
親動物の検査において,交尾率,受胎率,黄体数,着床数,着床率,分娩率,出産率,妊娠期間には被験物質の影響を示唆する変化は認められなかった.また,分娩にも異常は認められなかった.したがって,被験物質による親動物の生殖機能および分娩への影響はないと考えられる.一方,哺育期間の観察では,全新生児死亡が1000 mg/kg群の母動物3例で観察された他にも,1例で新生児死亡が多発したことから,被験物質により哺育機能に何らかの障害を来した可能性が考えられる.なお,200 mg/kg群でも全新生児死亡が1例観察されたが,分娩が遅延した母動物であり,対照群でも難産が1例で観察されていること,200 mg/kg群では本動物以外に新生児死亡が多発した例がなかったことなどから,被験物質との関連はない偶発的なものと考えられる.
新生児の検査において,出産児数,出産生児数,性比および出生率に被験物質の影響はみられなかったが,1000 mg/kg群で低体重および新生児の4日生存率の低下が認められた.全新生児死亡あるいは死亡が多発した腹以外の新生児の体重および4日生存率は対照群とほぼ同様な値を示していたことから,低体重および4日生存率の低下は母動物の哺育機能障害に起因したものである可能性が考えられる.外表検査,一般状態および剖検では被験物質に起因する変化は認められなかった.
以上のように,本試験では反復投与による一般毒性学的影響として,200 mg/kg以上の群の雄で貧血性変化が認められ,1000 mg/kg群では雌雄で行動異常,体重増加抑制,脳,脊髄および前胃の組織変化,雌で死亡,摂餌量減少,胸腺の萎縮が認められた.生殖・発生に及ぼす影響として,親動物の生殖機能および分娩には異常は認められなかったが,1000 mg/kg群で母動物の哺育機能および新生児の発育への影響を示唆する変化が認められた.したがって,本試験条件下における反復投与毒性に関する無影響量は雄が40 mg/kg/day,雌が200 mg/kg/day,生殖発生毒性に関する無影響量は親動物に対して雄が1000 mg/kg/day,雌が200 mg/kg/day,児動物に対しては200 mg/kg/dayと考えられる.
文献
| 1) | 山下弘太郎ら,化学物質毒性試験報告,6,545(1998). |
| 2) | 後藤 稠, 池田正之, 原 一郎編,"産業中毒便覧(増補版)," 医歯薬出版 , 東京, 1984, pp. 889-993. , 東京, 1984, pp. 889-993. |
| 3) | 古橋忠和ら,化学物質毒性試験報告,5,583(1997). |
| 4) | 古橋忠和ら,化学物質毒性試験報告,6,405(1998). |
| 5) | R. Husain, S.P. Srivastava, P.K. Seth, Arch. Toxicol., 58, 33(1985). |
| 6) | D.L. Innes, M.F. Tansy, Neurotoxicology, 2, 515(1981). |
| 7) | E. Verkkala, R. Rajaniemi, H. Savolainen, Toxicol. Lett., 18, 111(1983). |
| 8) | B.I. Ghanayem, R.R. Maronpot, H.B. Matthews, Toxicol. Appl. Pharmacol., 80, 323(1985). |
| 9) | B.I. Ghanayem, R.R. Maronpot, H.B. Matthews, Toxicol. Appl. Pharmacol., 80, 336(1985). |
| 10) | B.I. Ghanayem, R.R. Maronpot, H.B. Matthews, Toxicol. Appl. Pharmacol., 83, 576(1986). |
| 11) | P. Greaves, "Histopathology of Preclinical Toxicity Studies," Elsevier, Amsterdam, 1990, pp. 77-142. |
| 連絡先 |
| 試験責任者: | 松浦郁夫 |
| 試験担当者: | 星野信人, 土居卓也,豊田直人, 高野克代,鈴木美江 |
|  三菱化学安全科学研究所鹿島研究所 三菱化学安全科学研究所鹿島研究所 |
| 〒314-0255 茨城県鹿島郡波崎町砂山14 |
| Tel 0479-46-2871 | Fax 0479-46-2874 | |
| Correspondence |
| Authors: | Ikuo Matsuura(Study director)
Nobuhito Hoshino, Takuya Doi,
Naoto Toyota, Katsuyo Takano,
Yoshie Suzuki |
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory |
| 14 Sunayama, Hasaki-machi, Kashima-gun, Ibaraki, 314-0255, Japan |
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | |
 )を敷いたポリカーボネート製ケージに,群分け後は1匹,交配期間は雌雄各1匹,哺育期間は1腹で収容し,飼育した.
)を敷いたポリカーボネート製ケージに,群分け後は1匹,交配期間は雌雄各1匹,哺育期間は1腹で収容し,飼育した. ,Lot No. K609415,純度99.9 %)は,融点-30℃,沸点182〜192℃,比重0.936,水,アセトンおよびDMSOに溶けやすい,アミン臭のある無色透明の液体である.被験物質は室温・暗所・密閉で保管した.また,試験期間中安定であったことが確認された.
,Lot No. K609415,純度99.9 %)は,融点-30℃,沸点182〜192℃,比重0.936,水,アセトンおよびDMSOに溶けやすい,アミン臭のある無色透明の液体である.被験物質は室温・暗所・密閉で保管した.また,試験期間中安定であったことが確認された. から入手した雌雄のSDラット〔Crj:CD(SD)IGS〕を6日間検疫・馴化後,試験に供した.投与開始前日に体重別層化無作為抽出法により,1群につき雌雄各12匹を振り分けた.投与開始時の週齢は雌雄とも9週齢,体重範囲は雄が325〜360 g,雌が191〜242 gであった.
から入手した雌雄のSDラット〔Crj:CD(SD)IGS〕を6日間検疫・馴化後,試験に供した.投与開始前日に体重別層化無作為抽出法により,1群につき雌雄各12匹を振り分けた.投与開始時の週齢は雌雄とも9週齢,体重範囲は雄が325〜360 g,雌が191〜242 gであった. )を敷いたポリカーボネート製ケージに,群分け後は1匹,交配期間は雌雄各1匹,哺育期間は1腹で収容し,飼育した.
)を敷いたポリカーボネート製ケージに,群分け後は1匹,交配期間は雌雄各1匹,哺育期間は1腹で収容し,飼育した. )および5 μmのフィルターで濾過後,紫外線照射した水道水をそれぞれ自由摂取させた.
)および5 μmのフィルターで濾過後,紫外線照射した水道水をそれぞれ自由摂取させた. )を尿分析器(クリニテック100:マイルス・三共
)を尿分析器(クリニテック100:マイルス・三共 )により測定し,尿沈渣(Sternheimer-Malbin染色標本)を検査した.また,約21時間蓄尿について,尿量を計量し,比重(屈折法)を尿比重計(ユリコン-S:
)により測定し,尿沈渣(Sternheimer-Malbin染色標本)を検査した.また,約21時間蓄尿について,尿量を計量し,比重(屈折法)を尿比重計(ユリコン-S: アタゴ)により測定した.
アタゴ)により測定した. )の腹腔内投与による麻酔下で後大静脈より採取した血液の一部をEDTA-2Kにより凝固阻止し,赤血球数(シースフローDCインピーダンス検出法),白血球数(RF/DCインピーダンス検出法),血小板数(シースフローDCインピーダンス検出法),ヘモグロビン濃度(SLSヘモグロビン法),ヘマトクリット値(赤血球パルス波高値検出法)を多項目自動血球分析装置(NE-4500:東亞医用電子
)の腹腔内投与による麻酔下で後大静脈より採取した血液の一部をEDTA-2Kにより凝固阻止し,赤血球数(シースフローDCインピーダンス検出法),白血球数(RF/DCインピーダンス検出法),血小板数(シースフローDCインピーダンス検出法),ヘモグロビン濃度(SLSヘモグロビン法),ヘマトクリット値(赤血球パルス波高値検出法)を多項目自動血球分析装置(NE-4500:東亞医用電子 ),白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROX HEG-70A:オムロン
),白血球百分率(Wright染色塗抹標本)を血液細胞自動分析装置(MICROX HEG-70A:オムロン ),網状赤血球数(アルゴンレーザーを用いたフローサイトメトリー法)を自動網赤血球測定装置(R-2000:東亞医用電子
),網状赤血球数(アルゴンレーザーを用いたフローサイトメトリー法)を自動網赤血球測定装置(R-2000:東亞医用電子 )により測定した. また,検査結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.
)により測定した. また,検査結果から平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した. 法),グルコース(GK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(UV法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形:
法),グルコース(GK-G6PDH法),総コレステロール(CES-CO-POD法),トリグリセライド(LPL-GK-G3PO-POD法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(UV法),ナトリウム,カリウム,クロール(イオン選択電極法)を自動分析装置(日立736-10形: 日立製作所)により測定した.また,採取した血液の一部をヘパリン(リチウム塩)処理後遠心分離し,得られた血漿についてLDH(SSCC改良法)を自動分析装置(COBAS FARA
日立製作所)により測定した.また,採取した血液の一部をヘパリン(リチウム塩)処理後遠心分離し,得られた血漿についてLDH(SSCC改良法)を自動分析装置(COBAS FARA :F. Hoffmann La Roche & Co.)により測定した.
:F. Hoffmann La Roche & Co.)により測定した.








 , 東京, 1984, pp. 889-993.
, 東京, 1984, pp. 889-993. 三菱化学安全科学研究所鹿島研究所
三菱化学安全科学研究所鹿島研究所