エテニルトリメトキシシランの培養細胞に及ぼす細胞遺伝学的影響について,チャイニーズ・ハムスター培養細胞(CHL/IU細胞)を用いて染色体異常試験を実施した.
細胞増殖抑制試験を行った結果,短時間処理法及び連続処理法とも1500 μg/mL(10 mM相当)において細胞毒性は認められず,被験物質の析出も認められなかった.このことから,染色体異常試験における試験濃度は,短時間処理法及び連続処理法とも1500 μg/mLを最高濃度とし,以下公比2で計5段階設定した.すなわち,93.8,187.5,375,750,1500 μg/mLとした.
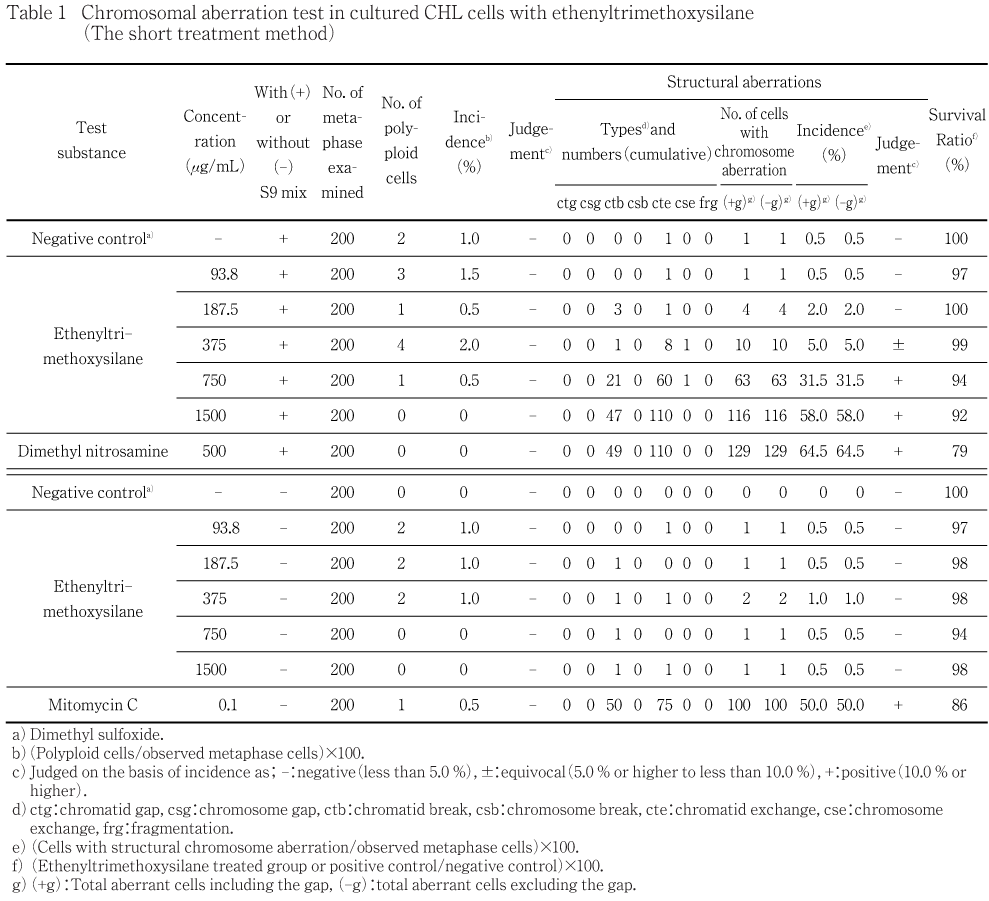
試験の結果,短時間処理法のS9 mix添加の375,750,1500 μg/mLにおいてそれぞれ5.0 %,31.5 %,58.0 %と用量に伴う構造異常の増加が認められた.倍数性細胞の誘発作用は,短時間処理法および連続処理法のいずれの処理群においても認められなかった.
以上の結果より,エテニルトリメトキシシランは,上記の試験条件下で染色体異常誘発性を有する(陽性)と結論する.
エテニルトリメトキシシランは,無色透明の液体で微臭があり,水に難溶(加水分解性あり)である[Lot No. 308595,含量:100 %,沸点:123℃,蒸気圧:2.7 kPa以下/25℃,揮発性:なし,融点:0℃以下,比重又は嵩比重:0.97(25℃),信越化学工業(東京)].入手後は,冷蔵・遮光の条件下で保管した.実験終了後に被験物質を分析し,使用期間中安定であったことを確認した.
被験物質はジメチルスルホキシド(以下DMSO,同仁化学研究所)に用時溶解して最高濃度原液を調製し,その後,DMSOで順次希釈して所定の濃度の被験物質調製液を調製した.
大日本製薬から入手したチャイニーズ・ハムスター由来のCHL/IU細胞を,解凍後継代10代以内で試験に用いた.
Eagle-MEM粉末(GIBCO)を処方に従って調製し,非働化(56℃,30分)した仔牛血清(GIBCO)を最終濃度で10 vol%になるように加えた培養液を用いた.
2×10^4個/5 mL培養液のCHL/IU細胞をディッシュ(径6 cm,CORNING)に播き,37℃のCO2インキュベーター(5 % CO2)内で培養した.
短時間処理法では,細胞播種3日後に被験物質を加え,S9 mix添加および無添加で6時間処理し,処理終了後,新鮮な培養液でさらに18時間培養した.また,連続処理法では,細胞播種3日後に被験物質を加え,24時間処理した.
S9(オリエンタル酵母工業)は,誘導剤としてフェノバルビタールおよび5,6-ベンゾフラボンを投与したSprague-Dawley系雄ラットの肝臓から調製されたものを購入し,製造後6ヵ月以内に使用した.添加量は培養液に対して5 vol%とした.
染色体異常試験における被験物質の処理濃度を決定するため,被験物質の細胞増殖に及ぼす影響を調べた.被験物質のCHL/IU細胞に対する増殖抑制作用は,血球計測盤を用いて各群の細胞数を計測し,陰性(溶媒)対照群に対する割合をもって指標とした.
その結果,短時間処理法及び連続処理法とも最高濃度の1500 μg/mLにおいて細胞毒性は認められなかった(Fig. 1).

細胞増殖抑制試験の結果により,短時間処理法のS9 mix添加及びS9 mix無添加,連続処理法の24時間処理とも最高濃度の1500 μg/mLにおいて細胞毒性は認められず,被験物質の析出も認められなかったことから,試験濃度は,1500 μg/mLを最高濃度とし,以下公比2で計5段階設定した.対照として,陰性(溶媒)対照および陽性対照を設けた.
陽性対照として,短時間処理法のS9 mix添加には,ジメチルニトロサミン(DMN,和光純薬工業)を500 μg/mL,S9 mix無添加には,マイトマイシンC(MMC,協和醗酵工業)を0.1 μg/mL,連続処理法には,MMCを0.05 μg/mLの濃度で用いた.
いずれの処理群も,各濃度3枚のディッシュに処理し,2枚を染色体標本作製,1枚を細胞増殖計測用に用いた.
培養終了2時間前にコルセミド(GIBCO)を最終濃度として約0.2 μg/mLとなるように添加した.染色体標本の作製は常法に従って行った.スライド標本は各ディッシュにつき3枚作製した.作製した標本を2 vol%ギムザ染色液で15分間染色した.
各ディッシュ当たり100個,すなわち1濃度当たり200個の分裂中期像を顕微鏡下で観察した.標本はすべてコード化し,盲検法で観察を行った.染色体の分析は,日本環境変異原学会・哺乳動物試験分科会による分類法1)に基づいて行い,染色体型あるいは染色分体型の切断,交換などの構造異常と倍数性細胞の有無について観察した.
構造異常を有する細胞あるいは倍数性細胞の出現頻度を,石館ら2)の基準に従って判定した.染色体異常を有する細胞の出現頻度が5 %未満を陰性(-),5 %以上10 %未満を疑陽性(±),10 %以上を陽性(+)とした.
なお,構造異常はギャップのみを有する細胞を含めない(-gap)場合について判定した.
また,統計学的手法を用いた検定は実施しなかった.
短時間処理法による試験結果をTable 1に示した.染色体構造異常の出現頻度は,S9 mix添加の375,750,1500 μg/mLにおいてそれぞれ5.0 %,31.5 %,58.0 %と用量に伴う増加が認められた.S9 mix無添加では,誘発作用は認められなかった.陽性対照として用いたDMN(S9 mix添加)およびMMC(S9 mix無添加)では,染色体構造異常の顕著な誘発が認められた.
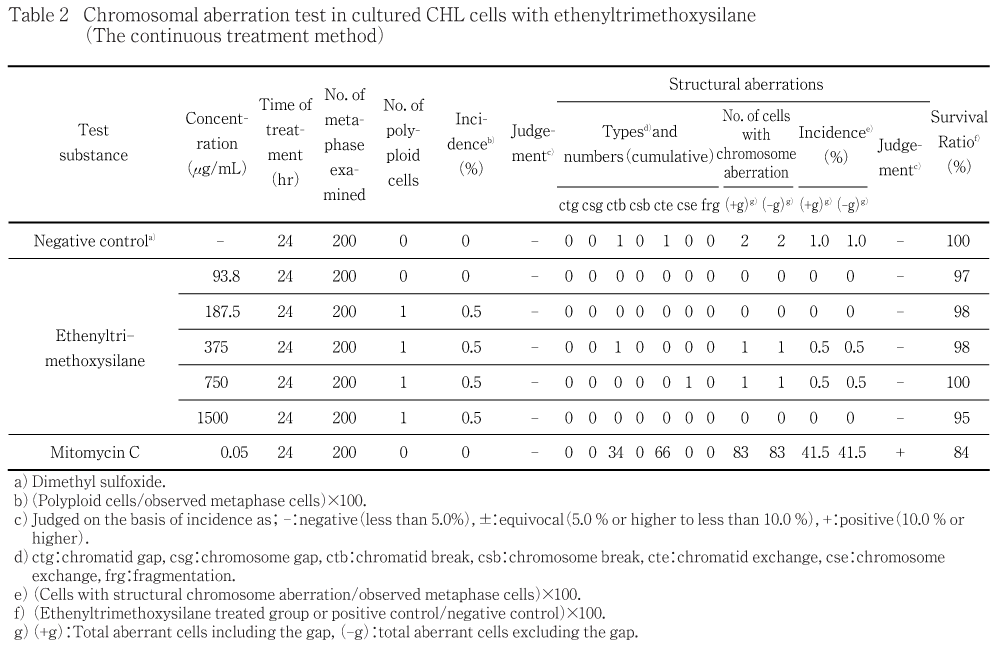
連続処理法による試験結果をTable 2に示した.エテニルトリメトキシシランを24時間連続処理した処理群では,染色体の構造異常および数的異常の誘発性は認められなかった.陽性対照として用いたMMCでは,染色体構造異常の顕著な誘発が認められた.
陽性結果が得られたことからD20値を算出したところ0.35 mg/mLであった.
以上の結果から,本試験条件下においてエテニルトリメトキシシランは染色体異常誘発性を有する(陽性)と結論する.
なお,エテニルトリメトキシシランは当試験施設で同時期に実施した細菌を用いる復帰突然変異試験で陰性の結果が得られている3).
| 1) | 日本環境変異原学会・哺乳動物試験分科会(編):「化学物質による染色体異常アトラス」朝倉書店,東京(1988)pp.16-37. |
| 2) | 祖父尼俊雄(監修):「〈改定〉染色体異常試験データー集」エル・アイ・シー,東京(1987)p.23. |
| 3) | 三輪芳久ら:エテニルトリメトキシシランの細菌を用いる復帰変異試験.化学物質毒性試験報告,13: 177-181(2006). |
| 連絡先 | |||
| 試験責任者: | 三輪芳久 | ||
| 試験担当者: | 小林梨沙 | ||
| (株)日本バイオリサーチセンター 羽島研究所 | |||
| 〒501-6251 岐阜県羽島市福寿町間島6-104 | |||
| Tel 058-392-6222 | Fax 058-392-1284 | ||
| Correspondence | |||
| Authors: | Yoshihisa Miwa(Study director) Risa Kobayashi |
||
| Hashima Laboratory, Nihon Bioresearch Inc. | |||
| 104, 6-chome, Majima, Fukuju-cho, Hashima, Gifu, 501-6251, Japan. | |||
| Tel +81-58-392-6222 | Fax +81-58-392-1284 | ||