ジベンジルトルエンを0,20,100および500 mg/kgの用量で雌雄のCrj:CD(SD)IGSラットに28日間反復経口投与し,その毒性について検討した.0 mg/kg(対照群)および500 mg/kg群については14日間回復群を設けた.
被験物質に起因すると思われる変化が血液学検査,器官重量,剖検および病理組織学検査に認められた.
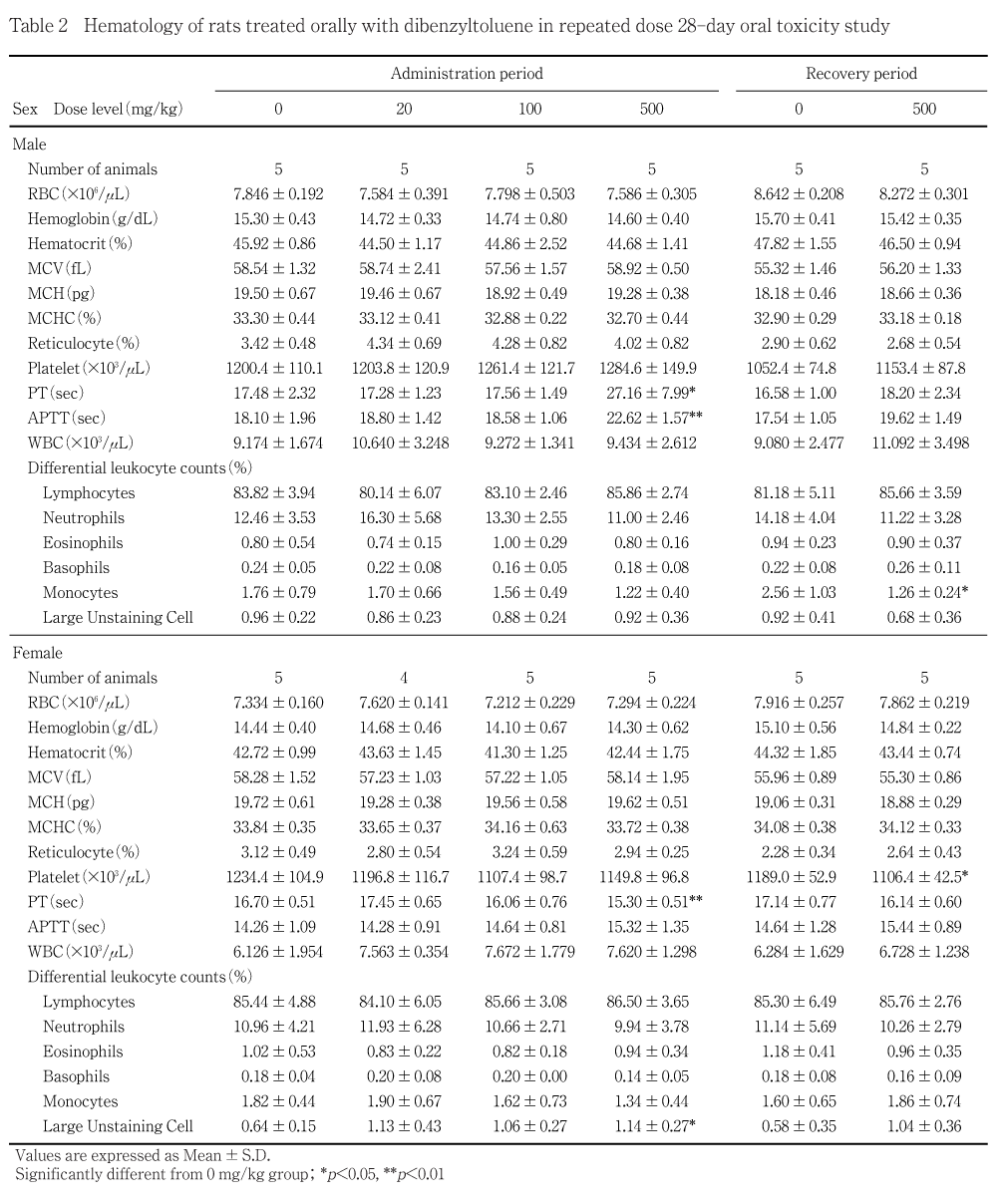
血液学検査では,プロトロンビン時間および活性化部分トロンボプラスチン時間の延長が500 mg/kg群の雄に認められた.
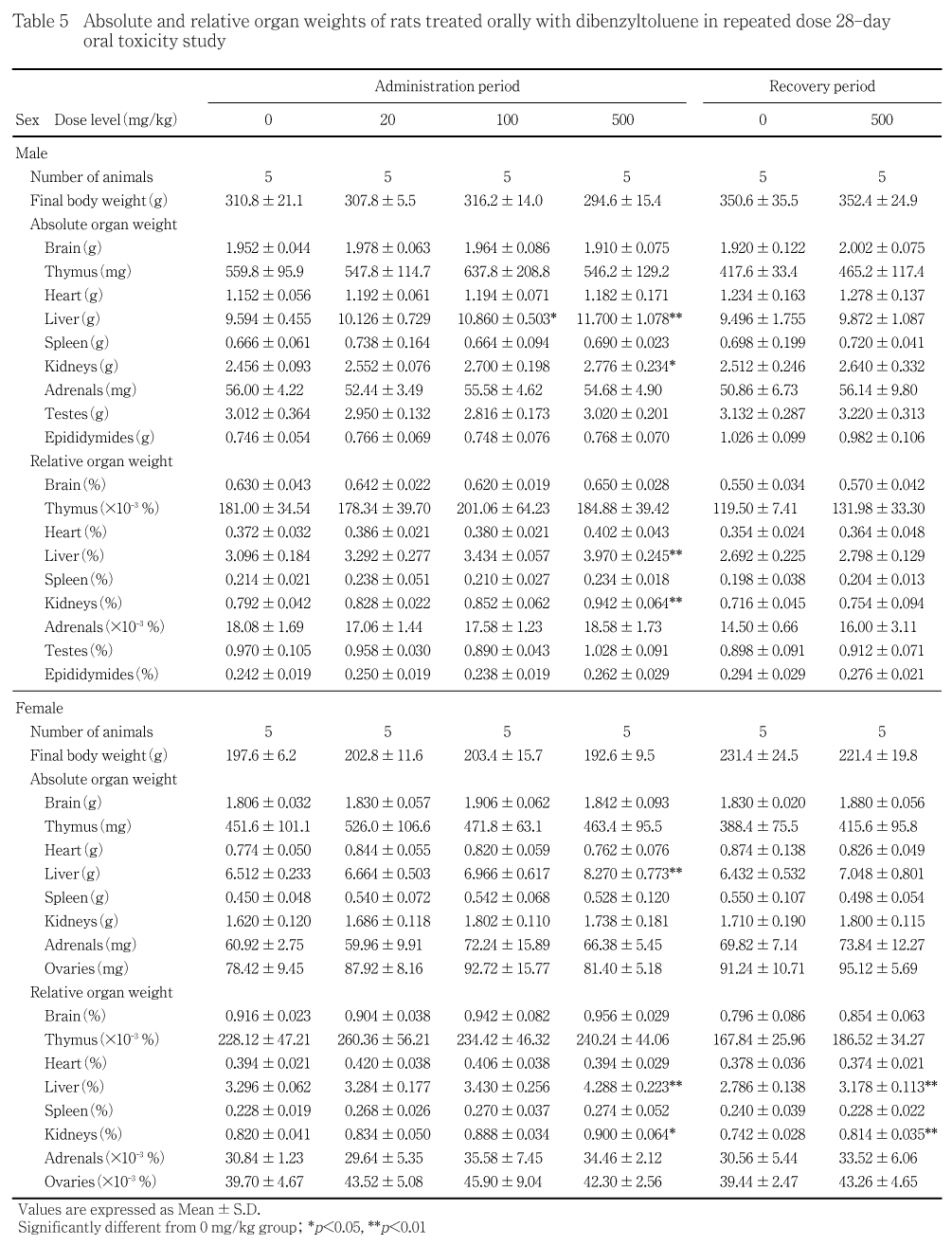
器官重量では,肝臓および腎臓重量の高値が500 mg/kg群の雌雄に認められた.また,肝臓重量の高値については100 mg/kg群の雄にも認められた.
剖検では,肝臓の腫大が500 mg/kg群の雌雄に認められた.
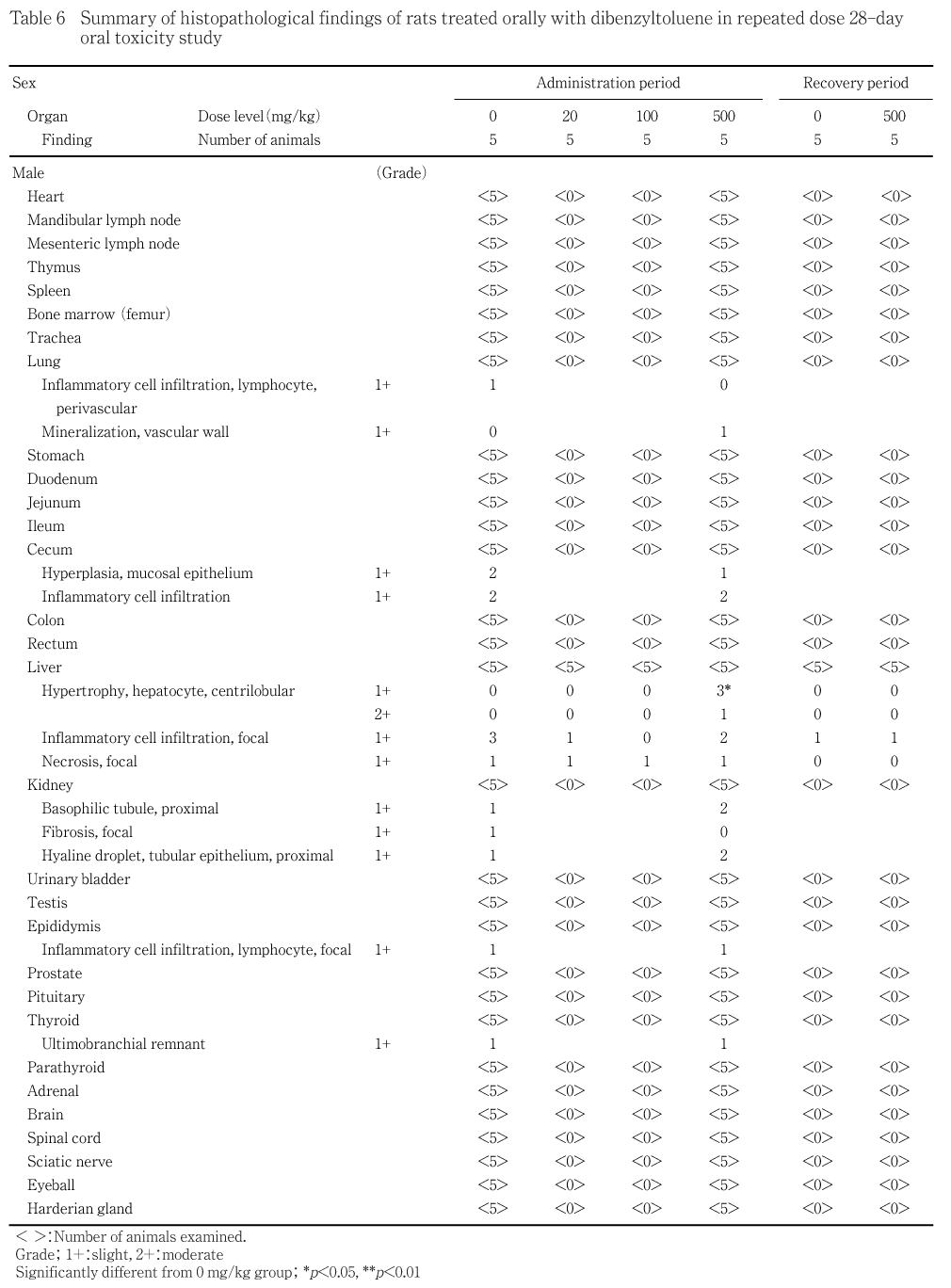
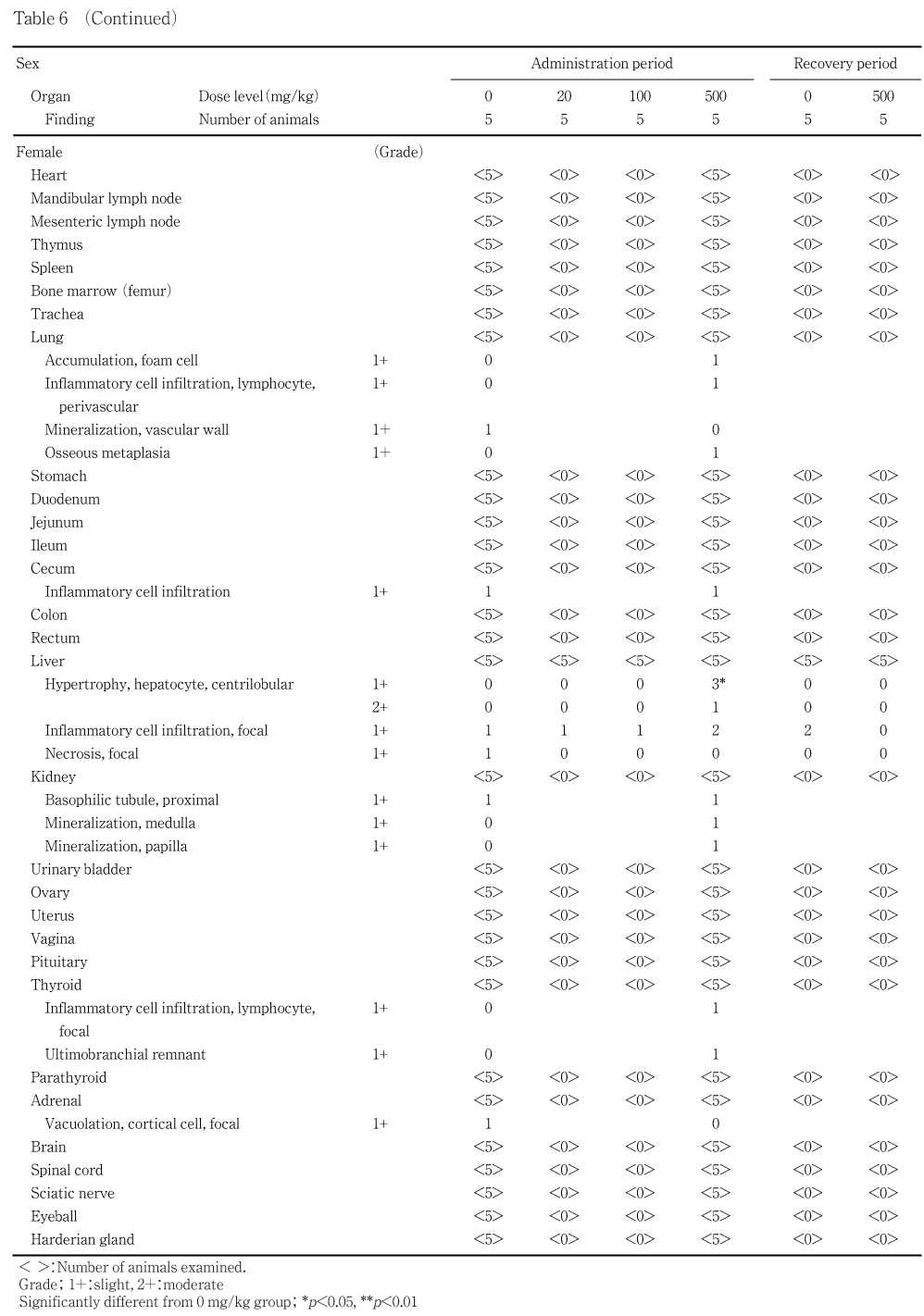
病理組織学検査では,肝臓の小葉中心性肝細胞肥大が500 mg/kg群の雌雄に認められた.
一般状態,行動検査,体重,摂餌量,血液生化学検査および尿検査では,被験物質投与に起因した影響は認められなかった.
以上,被験物質投与に起因すると考えられる変化が,雄の100 mg/kg以上の群,雌の500 mg/kg群で認められたことから,本試験条件下におけるジベンジルトルエンの無影響量(NOEL)は,雄が20 mg/kg/day,雌が100 mg/kg/dayと判断した.
ジベンジルトルエン(略称:DBT,新日鐵化学,ロット番号3-MYR,純度99.62 %)を使用した.被験物質は不快臭のする沸点387℃の淡黄色透明液体である.被験物質原体は冷蔵・遮光・気密条件下で保存し,試験に供した.試験に使用したロットは赤外吸収スペクトルを比較して試験期間中安定であることを確認した.
投与液の調製はイエローランプ照明下の調剤室にて実施した.用量毎に所定重量の被験物質をビーカーに秤量し,これに媒体(1 %Tween 80水溶液)を加え,ディスポーザブルシリンジおよび三方活栓を用いて乳化させた後,2,10および50 mg/mLの投与液を懸濁調製した.
投与液は冷蔵・暗所保存条件下で8日間安定であることを確認した.また,初回調製時の投与液を用量群ごとに分析し,設定濃度±10 %以内であることを確認した.
日本チャールス・リバー厚木生産所からCrj:CD (SD) IGSラット(SPF)雌雄各33匹を入手し,そのうち雌雄各30匹を使用した.
動物入荷後,雌雄とも5日間の検疫期間後,投与開始日まで馴化した.投与開始2日前に体重層別無作為抽出法によって群分けした.投与開始時の週齢は5週齢,体重範囲は雄が139〜155 g,雌が107〜123 gであった.
検疫・馴化期間を含む全飼育期間を通じて,温度21.3〜24.7℃(許容範囲19.0〜25.0℃),相対湿度37.0〜57.4 %(許容範囲35.0〜75.0 %),換気6〜20回/時(オールフレッシュエアー供給),照明12時間/日(7:00〜19:00)に自動調節した飼育室を使用した.
動物を滅菌済のステンレス製つり下げ型金網ケージ(トキワ科学器械)に群分け前は1ケージあたり1〜2匹(同性),群分け後は,個別に収容し飼育した.
動物には,実験動物用固型飼料(CR-LPF,オリエンタル酵母工業)と,5 μmのフィルター濾過後,紫外線照射した水道水をそれぞれ自由に摂取させた.
投与経路は,OECDガイドラインに準じて経口投与とした.投与期間は28日間とし,ディスポーザブルシリンジに装着したテフロン製胃ゾンデを用いて1日1回,午前中に強制経口投与した.
7日間経口投与予備試験(用量:0,100,500,1000 mg/kg,動物数:各群雌雄5匹)の結果,以下のような被験物質投与に起因する変化が認められた.
100 mg/kg群の雌でALPの低値が認められた.500 mg/kg以上の群の雌雄でALPの低値,肝臓重量の高値,肝臓の腫大,GOTの低値傾向およびトリグリセライドの低値あるいは低値傾向が,雄で血小板数の高値,胸腺の絶対および相対重量の低値あるいは低値傾向,プロトロンビン時間および活性化部分トロンボプラスチン時間の延長あるいは延長傾向が,雌でヘモグロビン濃度の低値あるいは低値傾向,ヘマトクリットの低値,プロトロンビン時間の短縮および活性化部分トロンボプラスチン時間の延長傾向がそれぞれ認められた.1000 mg/kg群の雌雄でg GTの高値,体重,摂餌量の低値傾向,雄でヘモグロビン濃度の低値および白血球百分率好酸球比の低値傾向,雌で白血球百分率好酸球比の低値およびGPTの高値がそれぞれ認められた.従って,本試験では確実に毒性変化が発現すると考えられる500 mg/kgを高用量とし,以下公比5で100および20 mg/kgの計3用量群を設定した.また,媒体(1 %Tween 80水溶液)のみを投与する対照群(0 mg/kg)を設定した.
投与液量は10 mL/kgとし,至近日に測定した体重に基づいて各動物の投与液量を算出した.また,対照群と500 mg/kg群の雌雄各5匹に,投与期間終了後14日間の回復期間を設けた.
下記の項目を検査した.なお,日と週の表記は投与開始日を第1日,第1〜7日を第1週とした.また,第29日以降を回復期間とした.
全例について,投与期間のうち第1〜20日は1日2回(投与前,投与後約30分),第21〜28日は1日3回(投与前,投与直後,投与後約1時間)観察した.その他の期間は1日1回午前中に観察した.
体重は第1,8,15,22,28,29,36,42および43日に測定した.ただし,第29日および43日の絶食後体重は体重データとしては利用せず,それぞれ解剖時の器官相対重量の算出のみに用いた.
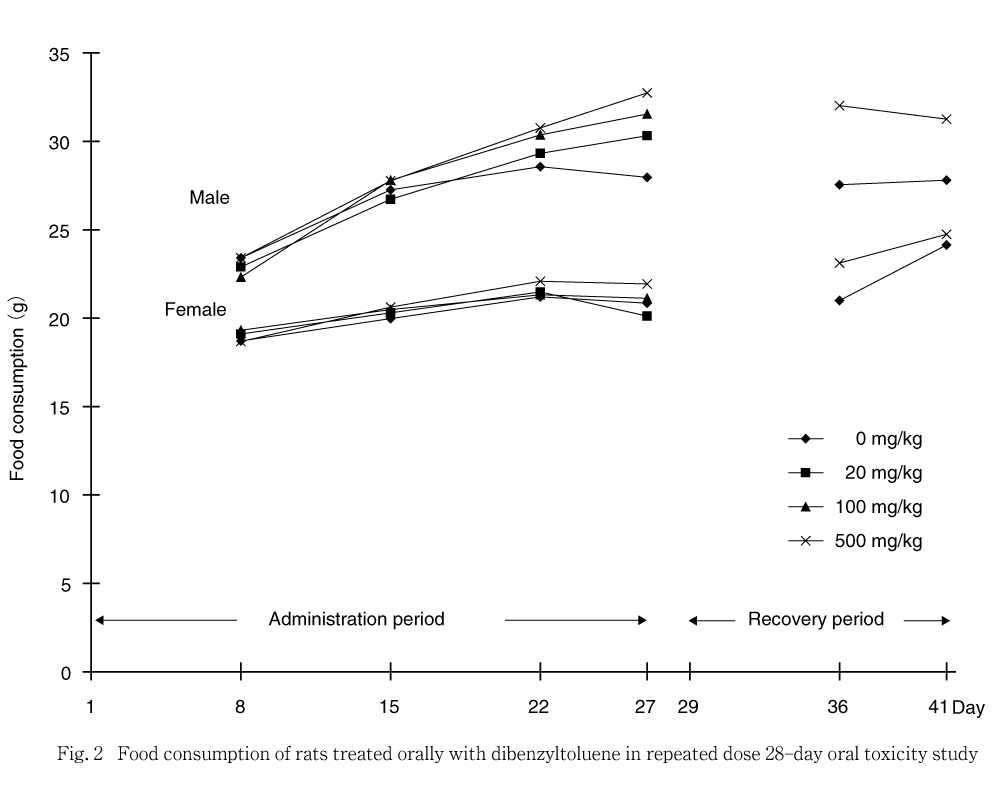
摂餌量は第1〜8日,第8〜15日,第15〜22日,第24〜27日,第29〜36日および第38〜41日の測定日間における,1日平均摂餌量を算出した.
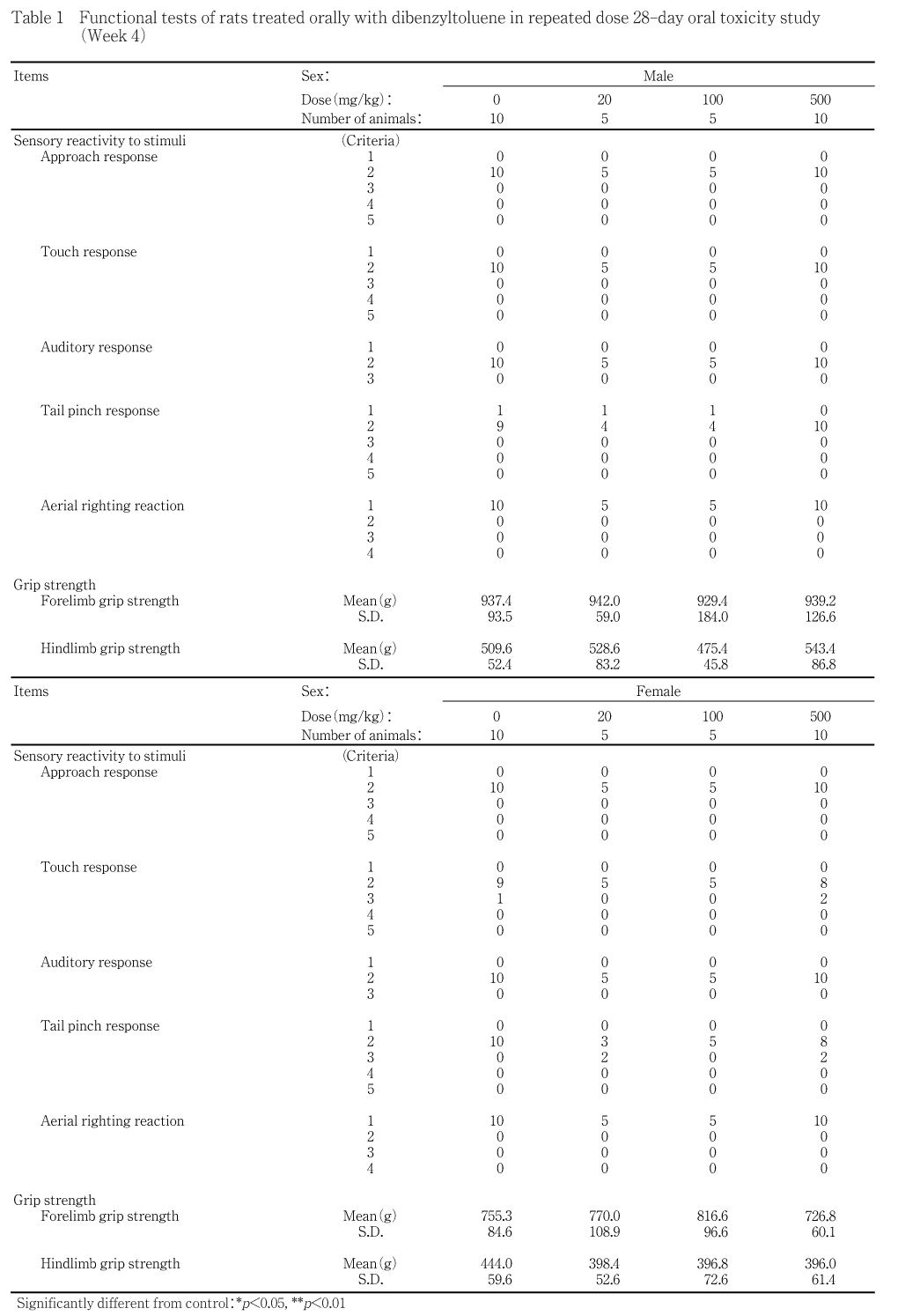
詳細な症状観察(ホームケージ内,ハンドリング時,オープンフィールドでの観察)は,投与開始前日に1回,投与期間中に毎週1回,いずれも午後に行った.機能検査(刺激に対する反応性,握力)および自発運動量の測定は,第4週に1回午後に実施した.握力はデジタルフォースゲージ(DPS-5),自発運動量はSUPERMEX(室町機械)を用いて測定した.投与期間中の検査で被験物質の影響が疑われる変化が認められなかったため,回復期間中の検査は実施しなかった.
投与および回復期間終了時の計画解剖日(第29および43日)に,全対象動物を前日夕方より絶食し,チオペンタールナトリウムを腹腔内投与して麻酔し,後大静脈より採血した.採取した血液を用いて以下に示す項目を測定した.
赤血球数(球状化処理二次元レーザーFCM法),ヘモグロビン濃度(シアンメトヘモグロビン法),ヘマトクリット値(球状化処理二次元レーザーFCM法),網赤血球数(RNA染色によるレーザーFCM法),血小板数(球状化処理二次元レーザーFCM法),白血球数(酸性界面活性剤によるレーザーFCM法)を多項目自動血球分析装置(ADVIA120:バイエルメディカル)を用いて測定した.さらに,平均赤血球容積(MCV),平均赤血球血色素量(MCH),平均赤血球血色素濃度(MCHC)を算出した.白血球百分率(ペルオキシダーゼ染色によるFCM法および酸性界面活性剤によるレーザーFCM法)を自動血球分析装置(ADVIA120:バイエルメディカル)を用いて測定した.プロトロンビン時間(PT,光散乱検出方式),活性化部分トロンボプラスチン時間(APTT,光散乱検出方式)を自動血液凝固測定装置(CA-510:シスメックス)で測定した.
凝固阻止剤としてプロトロンビン時間および活性化部分トロンボプラスチン時間の測定には,3.2 w/v%クエン酸三ナトリウム水溶液を,その他の項目の測定には,EDTA-2Kを用いた.
採取した血液の一部を室温で約30分間以上静置後遠心分離し,得られた血清を用いて下記の項目を測定した.
ASAT(GOT,UV-rate法(JSCC改良法)),ALAT (GPT,UV-rate法(JSCC改良法)),g GT(g-グルタミル-p-ニトロアニリド基質法(SSCC改良法)),ALP(p-ニトロフェニルリン酸基質法(JSCC改良法)),総ビリルビン(酵素法(BOD法)),尿素窒素(酵素-UV法(Urease- LEDH法)),クレアチニン(酵素法(Creatininase-POD法)),グルコース(酵素法(HK-G6PDH法)),総コレステロール(酵素法(CO-HDAOS法)),トリグリセライド(酵素法(GPO-HDAOS法),グリセリン消去法),総蛋白(Biuret法),アルブミン(BCG法),A/G比(総蛋白およびアルブミンより算出),カルシウム(OCPC法),無機リン(酵素法(PNP-XOD-POD法)),ナトリウム(イオン選択電極法),カリウム(イオン選択電極法),クロール(イオン選択電極法)を自動生化学分析装置(TBA- 200FR:東芝)により測定した.
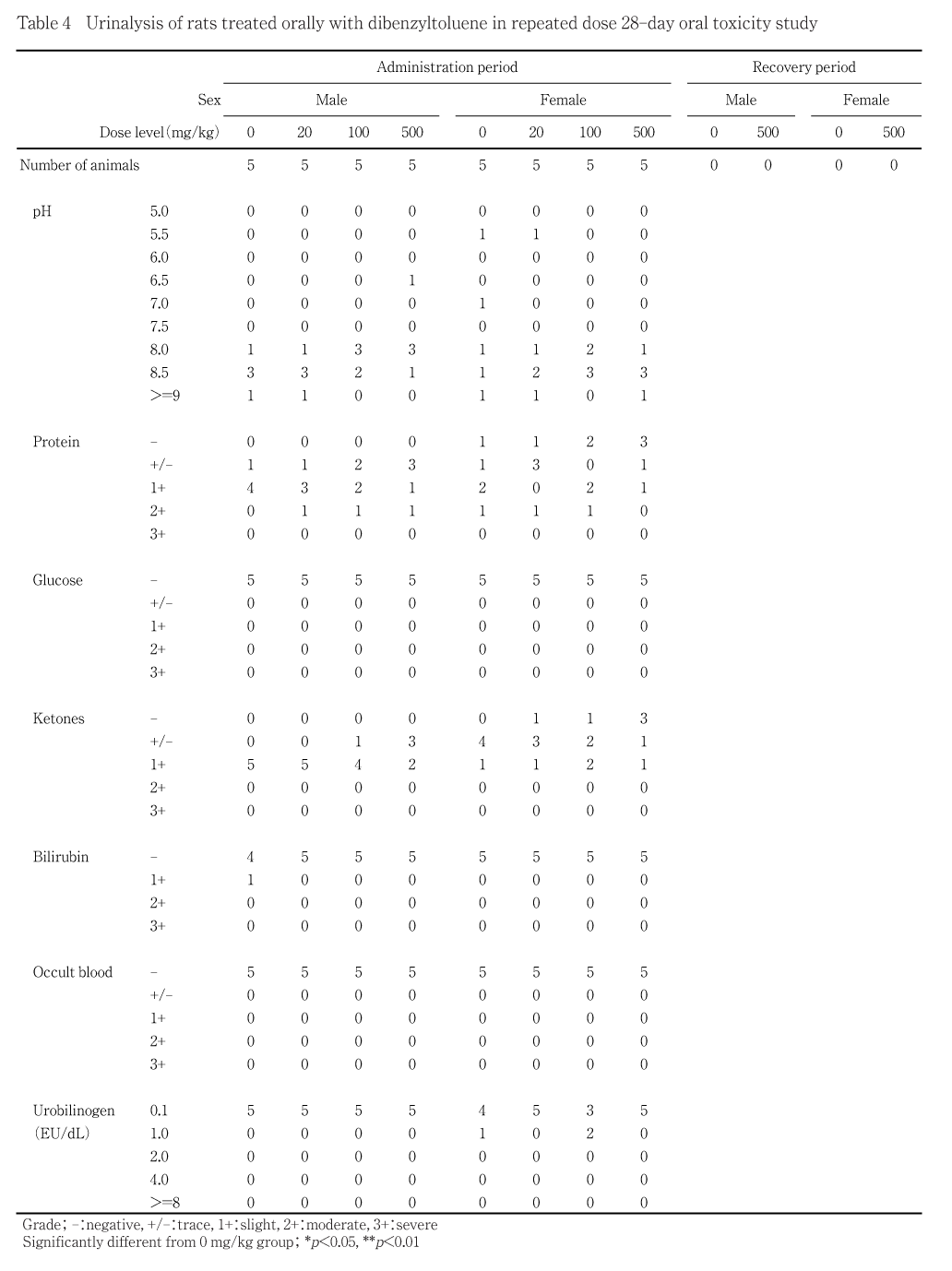
第23日に各群の雌雄各5匹の新鮮尿を採取して,pH,蛋白,グルコース,ケトン体,ビリルビン,潜血,ウロビリノーゲン(試験紙法;マルチスティックス,バイエルメディカル)を自動尿分析器(クリニテック100,バイエルメディカル)を用いて測定した.その結果,被験物質投与の影響を疑わせる変化が認められなかったため,その他の尿検査項目(尿沈渣,尿定量検査)および回復期間中の全項目の検査は実施しなかった.
第29日および第43日に計画解剖した動物について,採血後に腹大動脈を切断して放血,安楽死させ剖検した.全動物の下記の器官重量を測定した.また,解剖日の体重に基づいて相対重量(対体重比)を算出した.
[肝臓,腎臓,副腎,精巣,精巣上体,卵巣,胸腺,脾臓,脳,心臓]
全動物の下記の器官・組織を採取し,10 %中性リン酸緩衝ホルマリン液で固定し,保存した.ただし,精巣および精巣上体はブアン液(Bouin液)で,眼球とハーダー腺はダビドソン液(Davidson液)でそれぞれ固定後,10 %中性リン酸緩衝ホルマリン液で保存した.
[脳(大脳,小脳および橋を含む部位),脊髄,胃,十二指腸,空腸,回腸(パイエル板を含む),盲腸,結腸,直腸,肝臓,腎臓,副腎,脾臓,心臓,胸腺,眼球・ハーダー腺,下垂体,甲状腺(上皮小体含む),気管および肺,精巣,卵巣,精巣上体,前立腺,子宮,膣,膀胱,下顎リンパ節,腸間膜リンパ節,坐骨神経(大腿筋に付けて採材),骨髄(大腿骨)]
投与期間終了後解剖動物の対照群および500 mg/kg群の雌雄全例の上記器官・組織について常法に従ってヘマトキシリン・エオジン染色標本を作製し,鏡検した.(眼球・ハーダー腺は片側のみ標本作製し,鏡検した.)その結果,被験物質の影響が疑われる変化が500 mg/kg群の雌雄の肝臓に認められたため,投与期間終了後解剖動物の20および100 mg/kg群の雌雄,ならびに回復期間終了後解剖動物の雌雄の肝臓についても同様に検査した.
計量データは,Bartlett法による等分散性の検定を行い,分散が等しい場合は一元配置分散分析,分散が等しくない場合は,Kruskal-Wallisの検定を行った.群間に有意な差が認められた場合はDunnett法またはDunnett型の多重比較検定を行った.計数データは,a×bのχ2検定を行い,有意差が認められた場合はArmitageのχ2検定で対照群と各用量群を比較した.有意水準はいずれも5 %とした.
投与期間中に流涎が100 mg/kg群の雄1例,500 mg/kg群の雄7例,雌9例で認められた.本変化は投与直後から投与後約30分に発現したが,投与後1時間にはほぼ消失しており,投与後一過性に発現する変化であった.流涎は100 mg/kg群の雄では第19日,500 mg/kg群の雌雄では第15日より発現し,投与期間中散見された.その他の群では,異常症状は認められなかった.回復期間中には,何ら異常症状は認められなかった.
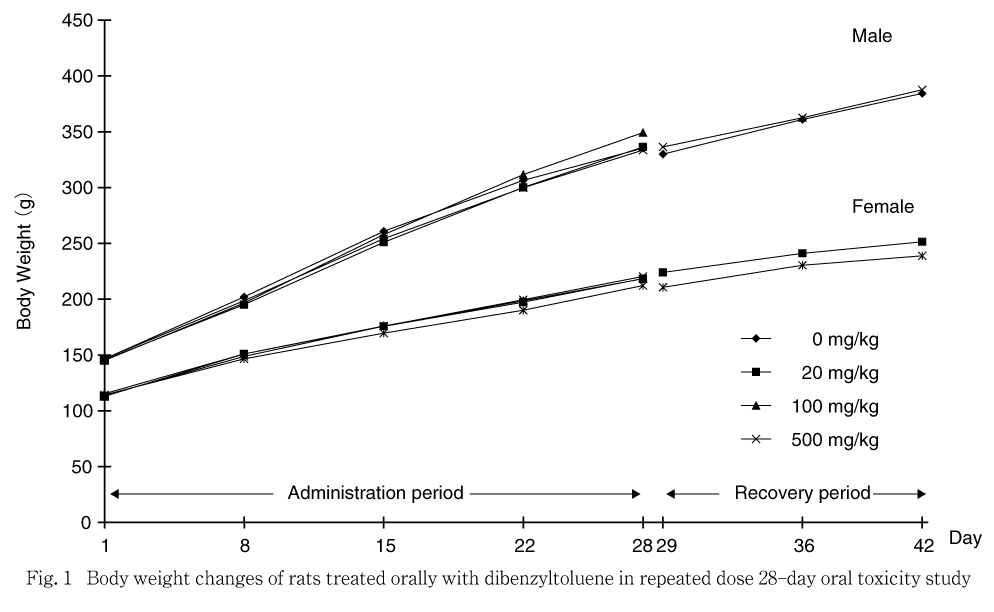
投与および回復期間中ともに,対照群と被験物質投与群との間に有意な差は認められなかった.

投与期間中に,摂餌量の高値が500 mg/kg群の雄で第27日に認められた.本変化は一過性に認められたことから,被験物質投与とは関連のない変化と判断した.
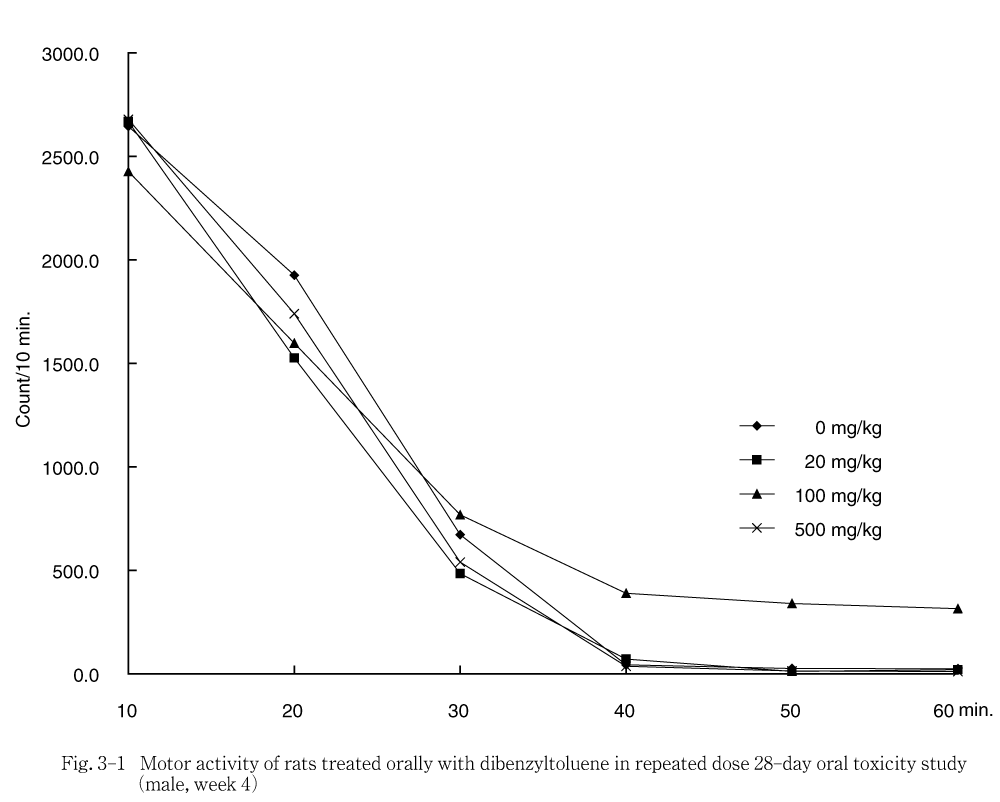
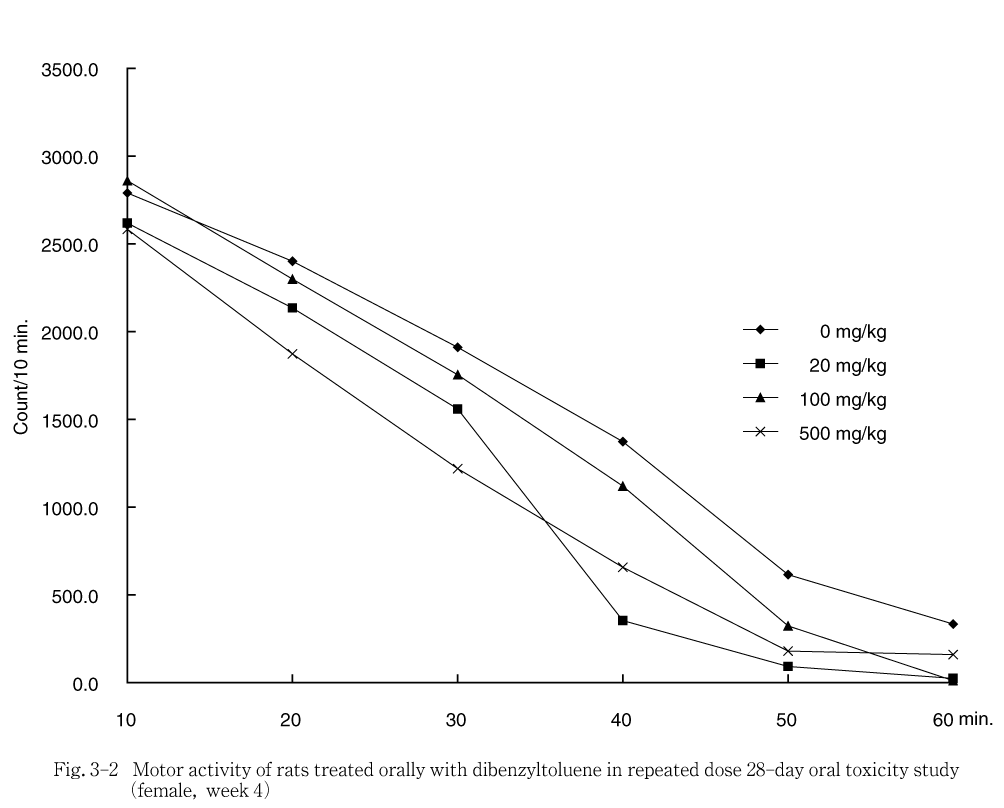
自発運動量の経時的推移をFig. 3,第4週の機能検査結果(刺激に対する反応性,握力)をTable 1に示した.
投与期間中の詳細な症状観察,機能検査および自発運動量測定の結果,いずれの検査においても,被験物質投与に起因すると思われる変化は認められなかった.
投与期間終了時の検査では,プロトロンビン時間および活性化部分トロンボプラスチン時間の延長が500 mg/kg群の雄に認められた.その他,プロトロンビン時間の短縮および白血球分類における非染色性巨細胞比の高値が500 mg/kg群の雌に認められたが,いずれも軽微な変化であり,被験物質投与とは関連のない変化と判断した.
回復期間終了時の検査では,白血球分類における単球比の低値が500 mg/kg群の雄にみられ,血小板数の低値が500 mg/kg群の雌に認められたが,いずれも投与期間終了時の検査では認められておらず,被験物質投与とは関連のない変化と判断した.
被験物質投与に起因すると思われる変化は認められなかった.
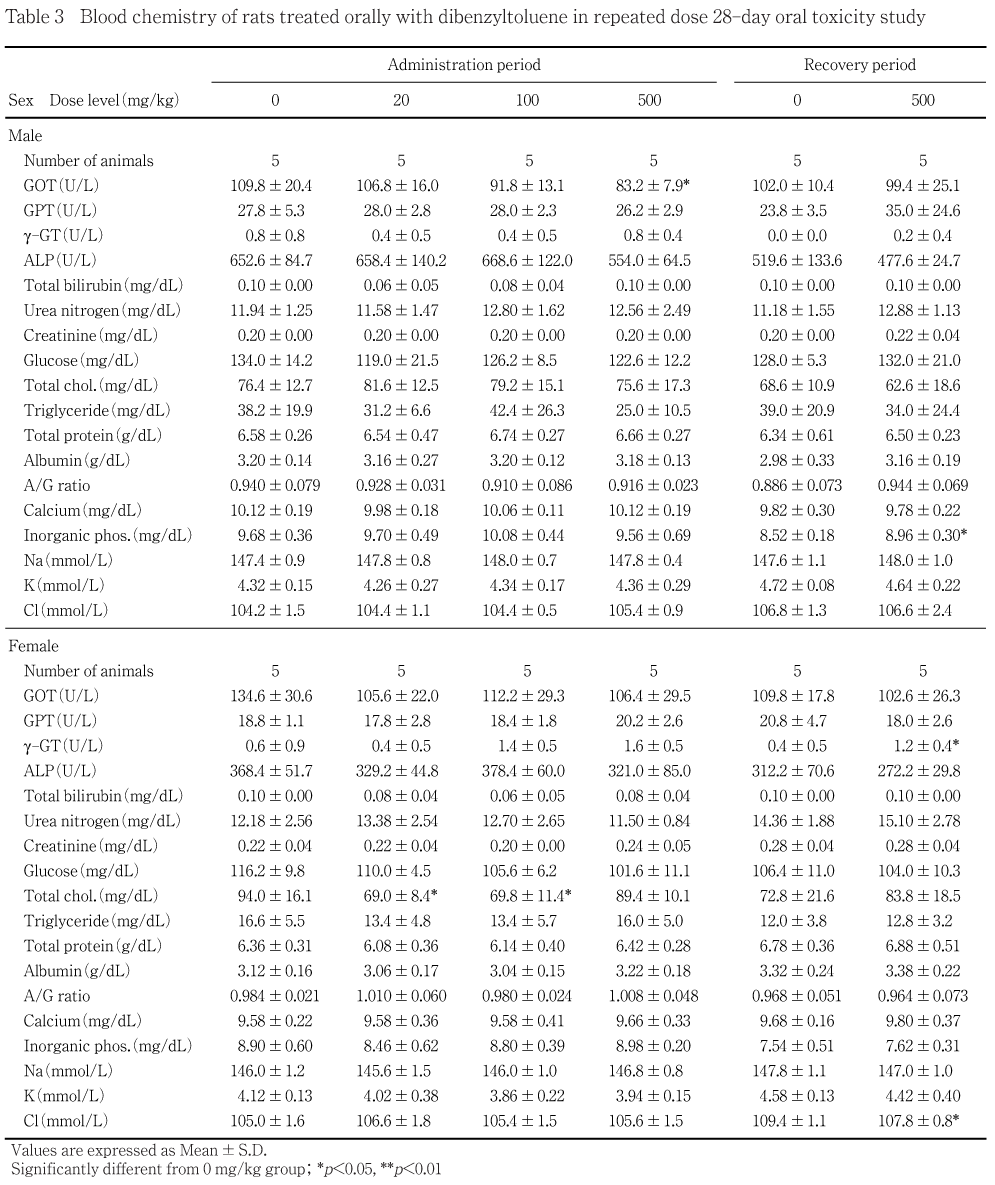
投与期間終了時の検査では,ASAT(GOT)の低値が500 mg/kg群の雄にみられ,また総コレステロールの低値が20および100 mg/kg群の雌に認められた.毒性学的意義の乏しい変化か,用量との関連性のない変化であり,いずれも被験物質投与とは関連のない変化と判断した.
回復期間終了時の検査では,無機リンの高値が500 mg/kg群の雄にみられ,g GTの高値およびクロールの低値が500 mg/kg群の雌に認められたが,いずれも投与期間終了時の検査では認められておらず,被験物質投与とは関連のない変化と判断した.
雌雄とも有意な変化は認められなかった.
投与期間終了時には,肝臓の絶対重量および相対重量の高値が500 mg/kg群の雌雄に認められた.肝臓の絶対重量の高値は100 mg/kg群の雄にも認められた.また,腎臓の絶対重量および相対重量の高値が500 mg/kg群の雄,腎臓の相対重量の高値が500 mg/kg群の雌に認められた.
回復期間終了時には,投与期間終了時に認められた肝臓および腎臓の相対重量の高値が500 mg/kg群の雌に認められたが,その程度は明らかに軽減していた.
被験物質投与に起因した変化が雌雄の肝臓に認められた.
投与期間終了時の解剖動物では,肝臓の腫大が500 mg/kg群の雌雄全例に認められた.
回復期間終了時の解剖動物では,何ら異常所見は認められなかった.
被験物質に起因すると思われる変化が,雌雄の肝臓に認められた.
投与期間終了時の解剖動物では,肝臓の小葉中心性肝細胞肥大が500 mg/kg群の雌雄各4例に認められた.
回復期間終了時の解剖動物では,この変化は認められなかった.
その他,種々の組織変化が投与期間終了時および回復期間終了時の解剖動物に認められたが,いずれもラットでは非特異的に発現する変化であり,またその発現状況に明らかな群差も認められなかったことから,被験物質投与とは関連のない変化と判断した.
ジベンジルトルエンを0,20,100および500 mg/kgの用量で雌雄のCrj:CD(SD)IGSラット(SPF)に28日間反復経口投与し,現れる生体の機能および形態の変化を観察し,その毒性と回復性を評価した.
一般状態では,流涎が100 mg/kg群の雄,500 mg/kg群の雌雄に認められた.本変化は投与後一過性に発現しており,また縮瞳や流涙などの自律神経系への作用を疑わせるような変化は認められなかった.したがって,本試験で認められた流涎は被験物質を含有する投与液の苦味によって惹起されたものと考えられ,毒性学的意義はないものと判断した.
血液学検査では,プロトロンビン時間および活性化部分トロンボプラスチン時間の延長が500 mg/kg群の雄に認められ,被験物質投与に起因した変化と判断した.
肝臓重量の高値が100 mg/kg群の雄および500 mg/kg群の雌雄にみられ,剖検では肝臓の腫大が500 mg/kg群の雌雄に認められた.病理組織学検査の結果,肝臓の小葉中心性肝細胞肥大が500 mg/kg群の雌雄に認められた.肝臓の小葉中心性肝細胞肥大は種々の化学物質投与によりしばしば惹起され,一般的に薬物代謝酵素誘導による生体の適応性反応と考えられている1).本試験においても同様の原因により肝臓の小葉中心性肝細胞肥大が発現したものと判断した.また,種々の化学物質投与により惹起された小葉中心性肝細胞肥大は,投与休止により速やかに回復することが知られており1),本試験においても2週間の投与休止により消失した.また,腎臓の絶対重量および相対重量の高値が500 mg/kg群の雄,相対重量の高値が500 mg/kg群の雌に認められ,被験物質投与に起因した変化と判断した.
上述した変化は,回復期間終了時には回復または回復傾向を示し,回復性は良好と判断した.
以上,被験物質投与に起因すると考えられる変化が,雄の100 mg/kg以上の群,雌の500 mg/kg群で認められたことから,本試験条件下におけるジベンジルトルエンの無影響量(NOEL)は,雄が20 mg/kg/day,雌が100 mg/kg/dayと判断した.
| 1) | Greaves P:Digestive system 2. Liver, hepatocellular hypertrophy and hyperplasia. In “Histopathology of preclinical toxicity studies”, 2nd ed., Greaves P (ed.), Elsevier, Amsterdam(2000)pp.445-452. |
| 連絡先 | |||
| 試験責任者: | 平塚秀明 | ||
| 試験担当者: | 黒崎智晴,二木力夫,豊田直人, 小山 隆 | ||
| (株)三菱化学安全科学研究所 鹿島研究所 | |||
| 〒314-0255 茨城県神栖市砂山14 | |||
| Tel 0479-46-2871 | Fax 0479-46-2874 | ||
| Correspondence | |||
| Authors: | Hideaki Hiratsuka (Study director) Tomoharu Kurosaki, Rikio Niki, Naoto Toyota, Takashi Koyama |
||
| Mitsubishi Chemical Safety Institute Ltd., Kashima Laboratory | |||
| 14 Sunayama, Kamisu-shi, Ibaraki 314-0255, Japan | |||
| Tel +81-479-46-2871 | Fax +81-479-46-2874 | ||